基于光热ICD诱导联合多糖的抗肿瘤疫苗的制备方法
文献发布时间:2024-04-18 20:00:50
技术领域
本发明属于医药技术领域,尤其涉及基于光热ICD诱导联合多糖的抗肿瘤疫苗的制备方法。
背景技术
由于肿瘤的复杂性、多样性和异质性,单一的治疗方法无法达到理想的抑瘤效果,通过联合多种抗肿瘤策略对肿瘤进行协同治疗引起了越来越多的关注。已有研究使用化疗-光热联合疗法进行抗肿瘤研究,该研究通过纳米平台实现多模式协同治疗,同时装载化药阿霉素和光热材料介孔二氧化硅纳米粒子(MSNs)。实验结果显示,纳米平台对肿瘤生长有较好的抑制作用,实现了化疗与光热治疗的协同结合。但此协同疗法只针对原位瘤有较好的抑制效果,而肿瘤的转移及其相关并发症是造成多种癌症病人死亡的主要原因,有效的癌症治疗不仅需要移除原发肿瘤,更重要的是防止肿瘤转移与复发。
癌症免疫疗法通过激活人体免疫系统并识别和杀死特定的肿瘤细胞,使免疫记忆效应的产生具有持久的疗效。光热疗法(PTT)、化疗和免疫疗法相结合已显示出增强的肿瘤抑制潜力。中药多糖属于天然高分子化合物,广泛存在于各种中药材中,一般由多个单糖组成,其具有抗肿瘤、调节肠道菌群、免疫调控等药理作用,并具有毒副作用小、生物活性广泛等特点。有研究将云芝中提取的多糖-K(PSK)与多西他赛联用治疗前列腺癌,化疗药多西他赛作为ICD诱导剂具有肿瘤杀伤作用。PSK具有免疫调控作用,可被用作癌症免疫疗法,其与多西他赛联用显著增加肿瘤浸润CD4
免疫原性细胞死亡(ICD)是由某些化疗药物、光热光动力疗法、物理化学疗法、溶瘤病毒和放射治疗等引起的一种新兴的肿瘤细胞死亡类型。经ICD治疗的濒死肿瘤细胞经过皮下注射可在体内激发抗肿瘤免疫应答,起到类似疫苗样的效应。ICD的成功触发总共需要五个步骤。1)细胞死亡;2)濒死细胞释放DAMPs;3)DAMPs介导吞噬细胞吞噬并处理死亡细胞,使其抗原呈递到抗原提呈细胞的表面(如:DC等);4)活化的DCs迁移到引流的淋巴器官,在那里它们成熟,并遇到原始T细胞,由DC将MHCⅠ或MHCⅡ分子上的肿瘤抗原分别递呈给CD8
发明内容
本发明的目的在于提供基于光热ICD诱导联合多糖的抗肿瘤疫苗的制备方法,旨在解决上述背景技术中提出的问题。
为实现上述目的,本发明提供如下技术方案:
基于光热ICD诱导联合多糖的抗肿瘤疫苗的制备方法,包括以下步骤:
将肿瘤细胞与纳米制剂共孵育并进行光热,将共孵育体系收集后作为抗肿瘤疫苗。
进一步的,所述纳米制剂的制备方法包括以下步骤:
步骤S1、将70mg/mL Zein溶解于DMSO,取Zein溶液75μL,在超声状态下逐次加入到1mL纯净水中,即得Zein NPs;
步骤S2、将Zein NPs在超声状态下逐次加入到1mL纯净水或1mL中药多糖溶液中,再依次加入50μL GTP溶液及50μL Fecl
步骤S3、离心纳米制剂,除去未包裹药物,沉淀用450μL纯净水重悬。
进一步的,所述步骤S2中,中药多糖溶液包括CSP、AP、ASP和PCP。
进一步的,所述步骤S2的具体操作为:
将Zein NPs在超声状态下逐次加入到1mL纯净水或1mLCSP、AP、ASP和PCP溶液中,再依次加入50μL GTP溶液及50μL Fecl
进一步的,所述步骤S3中,将纳米制剂以12000rpm的速度离心15min。
根据制备方法制得的抗肿瘤疫苗。
抗肿瘤疫苗在制备治疗癌症的药物中的应用。
与现有技术相比,本发明的有益效果是:
1、本发明利用光热-免疫联合疗法进行抗肿瘤免疫,癌症免疫疗法通过训练或刺激宿主固有的免疫系统来识别并攻击肿瘤细胞,促进宿主的免疫监视和防御,帮助宿主产生抗肿瘤免疫反应,抗肿瘤疫苗可抑制肿瘤生长,预防肿瘤转移与复发。
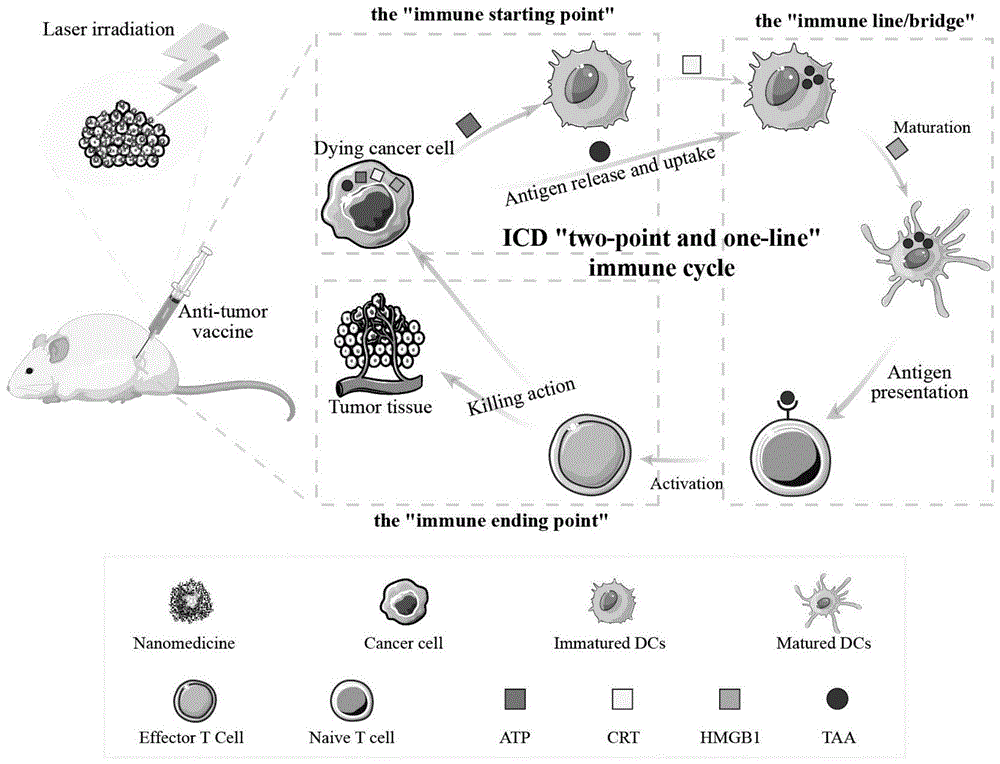
2、本发明基于ICD诱导与中药多糖免疫增强联合抗肿瘤的理念设计了抗肿瘤疫苗。通过体外构建“纳米药物→肿瘤细胞→DC→T细胞→肿瘤细胞”共孵育体系模拟体内ICD免疫循环过程进行理念验证,选择ICD的三个重要节点为研究对象,即“起点”—肿瘤抗原的暴露、“桥/线”—DC参与的抗原呈递、“终点”—T细胞活化后杀伤肿瘤细胞。ICD诱导过程即为暴露肿瘤抗原,增强“起点”的过程,中药多糖则全过程增强ICD“两点一线”免疫循环。
3、本发明将中药多糖与基于光热的ICD诱导结合,并实现纳米化。肿瘤细胞与纳米制剂共孵育并进行光热,暴露肿瘤相关抗原,将共孵育体系收集后作为抗肿瘤疫苗。抗肿瘤疫苗注射入小鼠体内后将诱导机体产生ICD效应,纳米药物中包含的中药多糖作为免疫调节剂通过增强ICD“两点一线”免疫循环动态过程放大机体产生的免疫应答,帮助机体建立强大的抗肿瘤免疫应答,对抗肿瘤的进展。本发明的纳米化设计中,中药多糖可替换,四种多糖与光热联用均有显著的抗肿瘤作用。
附图说明
图1为本发明的结构示意图。
具体实施方式
为了使本发明的目的、技术方案及优点更加清楚明白,以下结合附图及实施例,对本发明进行进一步详细说明。应当理解,此处所描述的具体实施例仅用以解释本发明,并不用于限定本发明。
以下结合具体实施例对本发明的具体实现进行详细描述。
本发明一个实施例提供的基于光热ICD诱导联合多糖的抗肿瘤疫苗的制备方法,包括以下步骤:
将肿瘤细胞与纳米制剂共孵育并进行光热,将共孵育体系收集后作为抗肿瘤疫苗。
在本发明实施例中,优选的,光热可被其他ICD诱导方式如化疗、放疗等代替。本发明将光热作为ICD诱导方式,诱导肿瘤细胞发生免疫原性死亡,释放肿瘤相关分子模式(DAMPs),作为免疫治疗起点;中药多糖通过全过程免疫调节作用放大抗肿瘤免疫,以达到抑制原位瘤,抑制肿瘤转移复发的作用。
作为本发明的一种优选实施例,所述纳米制剂的制备方法包括以下步骤:
步骤S1、将70mg/mL玉米醇溶蛋白(Zein)溶解于DMSO,取Zein溶液75μL,在超声状态(90W)下逐次(25μL/次)加入到1mL纯净水中,即得Zein NPs;
步骤S2、将Zein NPs在超声状态下逐次(530μL/次)加入到1mL纯净水或1mL锁阳多糖(CSP)、黄芪多糖(AP)、当归多糖(ASP)和茯苓多糖(PCP)溶液(15mg)中,再依次加入50μLGTP(30mg/mL,DMSO溶)溶液及50μL Fecl
步骤S3、将步骤S2得到的四种纳米制剂以12000rpm的速度离心15min,除去未包裹药物,沉淀用450μL纯净水重悬。
在本发明实施例中,我们研究了四种中药多糖(锁阳多糖、黄芪多糖、当归多糖、茯苓多糖)的免疫调节作用,发现中药多糖可以进行免疫全过程调节,即具备调控ICD的两点一线(免疫起点、免疫桥/线、免疫终点)的作用,具有多个靶点。首先促进肿瘤细胞ICD效应物的表达释放,其次促进DC细胞增殖、成熟、迁移,使其发挥强大的抗原呈递作用,最后促进T细胞增殖、分化,表现出增强的肿瘤细胞毒性,有助于帮助机体建立起强大、长效的抗肿瘤免疫应答。
本发明一个实施例提供的根据制备方法制得的抗肿瘤疫苗。
本发明一个实施例提供的抗肿瘤疫苗在制备治疗癌症的药物中的应用。
在本发明实施例中,本发明进行以下研究:
1、体外ICD标志物表达释放检测
首先研究四种不同多糖介导的“免疫-光热”联合疗法对ICD标志物表达释放影响,ATP、CRT和HMGB1是主要的ICD标志物,通过检测给药处理后4T1乳腺癌细胞表达释放ICD标志物的水平,可以初步判断ICD效应的强弱。
取对数生长期4T1细胞配制成2.5×10
ATP及HMGB1检测:取对数生长期4T1细胞配制成2.5×10
2、对抗原呈递细胞(DCs)的影响(免疫线或免疫桥)
2.1DC细胞的提取分离与体外培养
分离出8周龄雌性Balb/c荷瘤小鼠后腿股骨与胫骨,1mL PBS冲洗骨髓三次,将所得细胞混悬液350g离心5min,细胞沉淀加入3mL红细胞裂解液裂红处理5min,加入5mLRPMI-1640完全培养基停止反应,350g离心5min,细胞沉淀用5mL完全培养基洗涤两次,即得BMDC细胞,将细胞均匀铺于12孔板(2.5×10
2.2DC表型检测
取对数生长期4T1细胞配制成1×10
2.3DC细胞的增殖检测
取对数生长期4T1细胞配制成1×10
2.4DC细胞的迁移募集检测
采用Transwell实验来研究药物处理后肿瘤细胞培养液对DC细胞的募集能力。取对数生长期4T1细胞配制成1×10
3、对T细胞的影响(免疫终点)
3.1T细胞的分离提取及体外培养
分离出8周龄雌性Balb/c荷瘤小鼠脾脏,于5mL 1640培养基中研磨成细胞混悬液,过70μm细胞筛得到单细胞混悬液,取2mL单细胞混悬液于15mL离心管中,350g离心5min,细胞沉淀加入5mL红细胞裂解液裂红处理5min,加入10mL RPMI-1640完全培养基停止反应,350g离心5min,细胞沉淀用5mL完全培养基洗涤两次,用5mL 1640完培重悬后计数,备用。将CD3e抗体铺于24孔板(每孔5μg)中,于二氧化碳培养箱中包被2-4h,然后弃掉包被液,每孔加入1mL脾脏细胞混悬液(1×10
3.2T细胞的表型、增殖及细胞因子检测
通过细胞共培养技术,在体外模拟ICD效应的抗原传递过程。首先应用药物处理肿瘤细胞,使肿瘤抗原暴露,然后加入DC细胞共孵育,最后加入T细胞共培养,检测T细胞的表型变化。
取对数生长期4T1细胞配制成1×10
3.3T细胞的迁移募集检测
采用Transwell实验来研究药物处理后肿瘤细胞培养液对T细胞的募集能力。取对数生长期4T1细胞配制成1×10
3.4经过ICD效应激活后的T细胞毒性考察
取对数生长期4T1细胞配制成1×10
提前1d将小鼠乳腺癌细胞(4T1)及小鼠正常乳腺上皮细胞(HC11)接种于96孔板中,二氧化碳培养箱中孵育过夜。将收集所得T细胞以1∶10、1∶30、1∶60的靶效细胞比(4T1/HC11∶Activated T cells)接种于96孔板,最终每孔培养液体积为200μL。二氧化碳培养箱中继续孵育72h后,轻轻吹打使T细胞悬浮,并移除培养基,此时4T1及HC11吸附于板底,加入100μL PBS轻轻吹打洗涤一次,弃掉PBS,加入100μL含有10%cck-8的1640完培,于培养箱中孵育1h后,用酶标仪检测450nm处吸光度,并计算细胞毒性。
4、小鼠淋巴结中DC表型检测
取对数生长期4T1细胞配制成2.5×10
5、小鼠脾脏T细胞分群检测
取对数生长期4T1细胞配制成2.5×10
首先,加入100μL cell staining buffer,室温下封闭30min,防止非特异性结合,然后加入1μg CD45RO兔抗,室温孵育30min,随后加入0.75μg山羊抗兔IgG(H+L)-Alexa
6、治疗性抗肿瘤研究
建立并使用LLC荷瘤小鼠模型。将2×10
7、预防性抗肿瘤研究
将8周龄balb/c雌性小鼠随机分为6组。取对数生长期4T1细胞配制成2.5×10
复发:将对数生长期4T1细胞消化后配置成4×10
转移:将对数生长期4T1细胞消化后配置成3×10
治疗期间每2d记录小鼠肿瘤体积、体重。18d后,处死实验动物,分离肿瘤组织及其他主要器官组织(包括心、肝、脾、肺、肾),浸泡于4%多聚甲醛固定液中。
以上仅是本发明的优选实施方式,应当指出,对于本领域的技术人员来说,在不脱离本发明构思的前提下,还可以作出若干变形和改进,这些也应该视为本发明的保护范围,这些均不会影响本发明实施的效果和专利的实用性。
- 一种型面约束超声振动辅助旋转磨料流光整加工装置
- 一种纵扭复合超声振动辅助铣削加工装置
- 一种难加工复合材料TiB2/7050Al的超声振动辅助铣削加工方法
