一种粒状铝盐基提锂吸附剂及其制备方法和应用
文献发布时间:2024-04-18 19:58:26
技术领域
本发明属于吸附分离材料制备的技术领域,具体涉及一种粒状铝盐基提锂吸附剂的制备方法和应用。
背景技术
锂是一种稀有的轻金属元素。锂及其化合物已被广泛应用于多种工业领域,其中,主要用于生产各种类型的锂电池,此外,还在航空航天、核反应堆、陶瓷、玻璃及制药等领域中有重要用途。2021年全球锂的消费量估计为93000吨,比2020年的70000吨增加33%。
根据美国地质调查局统计,全世界已确定的锂资源储量约为8900万吨。中国已确定的锂资源储量约为510万吨,其中,青海、西藏的盐湖卤水中的锂约占我国总储量的85%以上,而从盐湖卤水中提取锂的成本通常比从花岗伟晶岩矿床中提取锂的成本低30%~50%。但是,盐湖卤水的组成成分复杂,尤其是高的镁/锂比对从卤水中高选择性地提取锂带来了很大的挑战。
从盐湖卤水中提取锂的方法有:溶剂萃取法、吸附法、电渗析法及膜分离法等。与其它方法相比,吸附法具有选择性高,环境友好,成本低,回收效率高,操作方便等优点。锰基和钛基锂离子筛以及锂铝层状双氢氧化物(即铝盐基提锂吸附剂)在盐湖卤水提锂中均表现出优异的选择性。与锂离子筛吸附剂相比,铝系锂吸附剂具有制备方法简单,解吸条件温和以及重复使用性能良好等优点,在盐湖卤水提锂中具有很高的应用价值。但是,粒径很小的粉末状铝盐基提锂吸附剂直接填充进入固定床柱中使用时,吸附柱的水力传导力非常低,使其在大规模连续工业化生产中的应用受到限制。
发明内容
针对现有技术的以上缺陷或改进需求,本发明的目的是在于提供了一种粒状铝盐基提锂吸附剂的制备方法,该制备方法具体为:首先制备得到锂铝层状双氢氧化物前驱体与壳聚糖的复合凝胶产物,再经过筛挤压造粒得到复合凝胶颗粒,然后再经干燥、漂洗、脱水等处理步骤,可根据需要制备得到不同粒径大小的粒状铝盐基提锂吸附剂。制备得到的粒状吸附剂对锂的吸附容量大,使用过程中溶损率低,作为造粒粘结剂的壳聚糖能够被生物降解,吸附剂制备过程全程使用水做溶剂,不需要使用有机溶剂,具有绿色、低碳、环保、成本低的优势。制备得到的粒状吸附剂能够填充至固定床中用于连续大规模从盐湖卤水等多种含锂水溶液中提取锂资源,避免了粉末状铝盐基吸附剂在固定床中存在水力传导力低,固液分离困难等问题。
为实现上述目的,在本发明的第一方面,提供了一种粒状铝盐基提锂吸附剂的制备方法,包括:
(1)将锂铝层状双氢氧化物前驱体分散至壳聚糖水溶液中,形成壳聚糖与锂铝层状双氢氧化物前驱体的均匀混合浆液;其中所述壳聚糖水溶液的pH值控制在3.5~7.5的范围内;
(2)在步骤(1)中所述混合浆液中加入交联剂混合,经交联反应及老化处理得到壳聚糖与锂铝层状双氢氧化物前驱体的复合凝胶产物;
(3)将步骤(2)中的所述复合凝胶产物经过筛挤压造粒,得到复合凝胶颗粒,再经干燥、漂洗、脱水处理得到粒状铝盐基提锂吸附剂。
作为本发明的优选,在步骤(1)中,所述壳聚糖水溶液由酸性水溶液溶解壳聚糖配制得到;所述壳聚糖水溶液中壳聚糖的质量分数为0.5%~5%。
作为本发明的优选,在步骤(1)中,所述壳聚糖与所述锂铝层状双氢氧化物前驱体的质量比为1:(1~8);所述壳聚糖水溶液与所述锂铝层状双氢氧化物前驱体混合时的温度为5~40℃。
作为本发明的优选,在步骤(2)中,所述交联剂包括乙二醛、丙二醛、丁二醛、戊二醛中的至少一种,且所述交联剂的用量为所述壳聚糖质量的0.1%~35%。
作为本发明的优选,在步骤(2)中,所述交联反应的温度为5℃~70℃,交联反应的时间为5min~24h。
作为本发明的优选,在步骤(2)中,所述老化的温度为20℃~60℃,老化处理的时间为1h~24h。
作为本发明的优选,将所述复合凝胶产物经5~50目的筛网挤压造粒后,所得复合凝胶颗粒在40℃~60℃下干燥1h~24h后,漂洗,脱水,制得所述粒状铝盐基提锂吸附剂。
作为本发明的优选,所述锂铝层状双氢氧化物前驱体通过共沉淀法或水热法制备得到。
在本发明的另一方面,提供了一种基于本发明第一方面的方法制得的粒状铝盐基提锂吸附剂。
在本发明的又一方面,提供了一种如本发明第一方面提供的粒状铝盐基提锂吸附剂在在提取锂中应用,优选在盐湖卤水、地下水、海水或工业含锂废水中提取锂的应用。
总体而言,通过本发明所构思的以上技术方案与现有技术相比,主要具备以下的技术优点:
(1)本发明通过先形成壳聚糖与锂铝层状双氢氧化物前驱体的复合凝胶,再将该复合凝胶经过筛网挤压造粒,制备得到复合凝胶颗粒,再经干燥、漂洗及脱水处理,最后得到粒状吸附剂。由于本发明的复合凝胶是在弱酸性及中性条件下形成的,能够避免现有技术需要在强碱性接收液中滴制凝胶小球导致的锂铝层状双氢氧化物前驱体结构的坍塌及破坏,因此,能进一步避免吸附剂提锂性能的显著降低。因为锂铝层状双氢氧化物前驱体中的主要成分是氢氧化铝,它在弱酸性及中性条件下能保持其结构的稳定,但它在强碱性溶液中会溶解。凝胶小球在强碱性接收液中浸泡的时间越长,凝胶小球中嵌锂铝盐前驱体结构的溶损程度越大,因此凝胶小球的吸附量会受到较大的影响。
(2)本发明所制备的复合凝胶颗粒其内部及外部的交联剂分布均匀,因此,复合凝胶颗粒内部及外部的交联程度均匀可控,能得到机械强度更好的粒状吸附剂。这是因为本发明制备复合凝胶时,是先将交联剂在壳聚糖与锂铝层状双氢氧化物前驱体的混合浆液中分散均匀后,再引发交联反应的,这样才能得到内外交联程度均匀的复合凝胶;但是,现有的滴球技术则是在强碱性接收液中滴制成凝胶小球后,再将凝胶小球放入含交联剂的水溶液中发生交联反应,然而这些交联剂的亲水性一般很差,因此不易从凝胶小球的外部扩散至其内部,可能会导致其内部交联程度较小,导致整个凝胶小球的机械强度不高。
(3)本发明的制备方法是通过将复合凝胶经过筛网挤压造粒的,而通过过筛等处理步骤,可使得制备的吸附剂的颗粒粒径可控。一般来说,吸附剂的粒径越小,比表面积越大,吸附量越大。因此,可以通过选用“目数”更大的筛网,制得粒径较小的铝盐基提锂吸附剂,提高其吸附量。因此,本发明的制备方法不仅能够通过选择不同目数的筛网,得到不同粒径大小的颗粒,而且还能够制备得到比现有滴球造粒技术粒径更小的颗粒。这是因为滴制粒径越小的凝胶小球,需要造粒机的滴球孔道也要越细小。当胶液中固体纳米粒子的含量较高时或胶液的浓度较高时,极易堵塞造粒机的滴球孔道,使得粒径较小的凝胶小球难以通过滴球工艺制备得到。
(4)本发明的过筛造粒成型过程可在常温下进行,操作方便,设备投资小,造粒效率高,成本低。相比于现有技术中的滴球造粒法,一台机器单位时间内只能滴一颗球,而本发明通过选用恰当的筛网,单位时间内可以让复合凝胶同时通过多个筛网孔造出更多的凝胶颗粒。此外,在滴球造粒过程中,当胶液中固体纳米粒子的含量较高时或胶液的浓度较高时,极易堵塞造粒机的滴球孔道,常需要停车检修。
(5)本发明的造粒粘结剂组成简单,价格低廉且绿色环保。本发明使用壳聚糖作为造粒粘结剂,壳聚糖是甲壳素的脱乙酰产物,来源广泛且价格低廉,能降低造粒成本。壳聚糖无毒且具有良好的生物相容性及生物可降解性,由壳聚糖做造粒的粘结剂,符合绿色低碳环保要求。在使用壳聚糖做粘结剂制备粒状吸附剂过程中,全部用水做溶剂,不需要使用有机溶剂,粒状吸附剂制备过程绿色环保。
(6)由于壳聚糖具有良好的亲水性,与亲水性的锂铝层状双氢氧化物有良好的相容性及结合性,因此,锂铝层状双氢氧化物与壳聚糖的复合吸附剂有利于水分子在吸附剂颗粒内的扩散,提高粒状吸附剂的吸附性能,同时还能减小卤水中油性污染物对吸附剂的污染。
附图说明
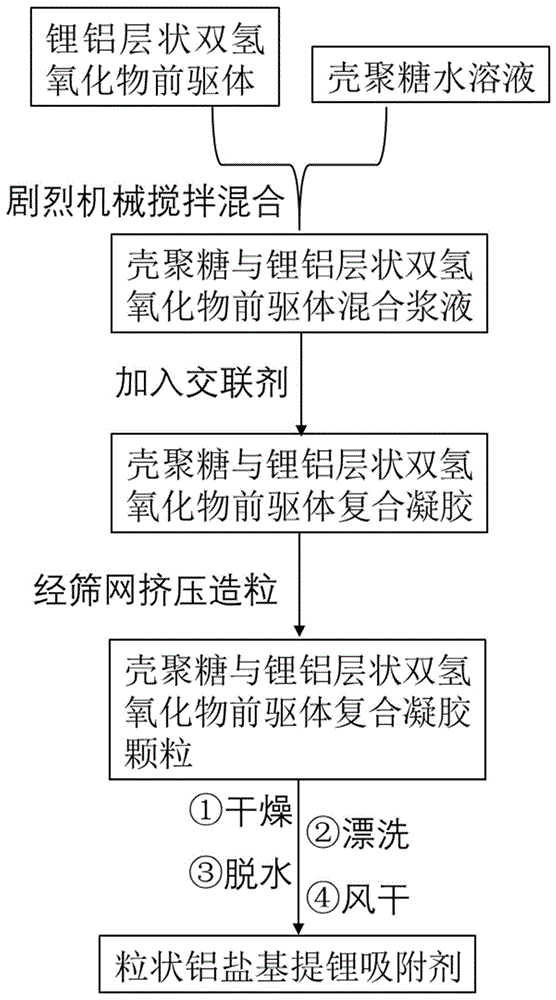
图1为本发明的粒状铝盐基提锂吸附剂的制备工艺流程图;
图2为本发明实施例2中示例的粒状铝盐基提锂吸附剂样品的照片图;
图3为本发明实施例2中示例的粒状铝盐基提锂吸附剂在显微镜下观察得到的形貌图;
图4为本发明实施例2中示例的粒状铝盐基提锂吸附剂的扫描电镜图;
图5为本发明实施例2中示例的粒状铝盐基提锂吸附剂的XRD谱图;
图6为本发明实施例2-3中示例的粒状铝盐基提锂吸附剂、对比例1中示例的铝盐基提锂吸附剂以及单纯壳聚糖的XRD谱图比较;
图7为本发明实施例2中示例的粒状铝盐基提锂吸附剂的重复利用图。
具体实施方式
为了使本发明的目的、技术方案及优点更加清楚明白,以下结合附图及实施例,对本发明进行进一步详细说明。应当理解,此处所描述的具体实施例仅仅用以解释本发明,并不用于限定本发明。此外,下面所描述的本发明各个实施方式中所涉及到的技术特征只要彼此之间未构成冲突就可以相互组合。
在本发明的实施例中,粒状铝盐基提锂吸附剂的制备方法,如图1所示,具体如下:
步骤1,通过共沉淀法或水热法制备锂铝层状双氢氧化物前驱体,所述锂铝层状双氢氧化物前驱体不需要进一步的洗涤及干燥等后续处理,可直接分散于壳聚糖水溶液中。
步骤2,使用酸性水溶液如醋酸水溶液、盐酸水溶液或硫酸水溶液中的一种溶解壳聚糖,得到均匀的壳聚糖水溶液。同时,根据需要应用盐酸或氢氧化钠将壳聚糖水溶液的pH值调节至3.5~7.5,其中壳聚糖水溶液中壳聚糖的质量分数为0.5%~5%。
在5~40℃的温度下,将步骤1中的锂铝层状双氢氧化物前驱体分散至所述壳聚糖水溶液中,并剧烈搅拌充分混合得到均匀的混合浆液,浆液中的壳聚糖与锂铝层状双氢氧化物前驱体的质量比为1:(1~8)。
步骤3,在步骤2所制得的壳聚糖与锂铝层状双氢氧化物前驱体的混合浆液中加入一定质量的交联剂,搅拌均匀后,在一定温度下反应一段时间并老化一段时间,最后得到壳聚糖与锂铝层状双氢氧化物前驱体复合凝胶产物。
壳聚糖的交联剂为乙二醛、丙二醛、丁二醛、戊二醛中的至少一种,且交联剂的用量为壳聚糖质量的0.1%~35%;壳聚糖的交联反应的温度控制在5~70℃的范围内,并且交联反应的时间控制在5min~24h的范围内,以及凝胶老化时间控制在1h~24h范围内。
步骤4,将步骤3所述复合凝胶产物经5~50目(国家标准筛规格)的筛网挤压造粒后得到复合凝胶颗粒,将复合凝胶颗粒在40℃~60℃下真空干燥后,经漂洗、脱水后得到粒状铝盐基提锂吸附剂。
例如,该粒状铝盐基提锂吸附剂还可进一步采用真空干燥或常温风干等处理步骤得到具有一定水含量的粒状吸附剂或完全干燥的粒状吸附剂,备用。粒状吸附剂在使用前需要再经过12~24h的漂洗脱锂后,可直接填充进入固定床柱用于各种含锂水溶液包括盐湖卤水、地下水、海水及工业含锂废水中锂的提取。
在本发明的实施例中所采用的模拟盐湖老卤水的化学组成如表1所示:
表1模拟的盐湖老卤水中的主要离子及其浓度(pH为5.6):
具体实施例如下:
实施例1
将氯化锂和氯化铝按摩尔比为Li
将湿的Li-Al-LDH(其湿重为8.10g,其干重为2.4g)分散到40mL的3%壳聚糖水溶液中(壳聚糖用醋酸水溶液溶解,并将壳聚糖水溶液的pH调节至4.4),在15℃水浴中剧烈机械搅拌混合浆液20min,然后继续在剧烈机械搅拌的条件下,缓慢将4mL戊二醛的水溶液(该水溶液中戊二醛的质量分数为4.5%,且戊二醛交联剂的总质量为壳聚糖质量的15%)滴加至混合浆液中,并将交联剂在混合浆液中分散均匀。然后将水浴温度升高在40℃,在此温度下继续反应20min至复合凝胶生成,并使此复合凝胶在常温下老化4.5h。
将复合凝胶压碎后过20目筛网得到复合凝胶颗粒,在55℃真空干燥12h。将干燥的凝胶颗粒用去离子漂洗三次,抽滤脱水,在常温下表面风干后,得到粒状铝盐基提锂吸附剂1号。
粒状吸附剂1号使用前按固液比为1g:100mL的比例用去离子水振荡漂洗脱锂12h。然后,再按固液比为1g(吸附剂干重):30mL的比例,将脱锂的粒状吸附剂1号加入到模拟盐湖老卤水中,在30℃的恒温水浴摇床中以200rpm的转速振荡吸附48h,测得吸附剂对锂的平衡吸附量为8.33mg/g。
实施例2
粒状铝盐基提锂吸附剂的制备方法同实施例1,区别仅在于将实施例1中分散至壳聚糖水溶液中的湿的Li-Al-LDH的用量进行了调整:在本实施例中的壳聚糖与Li-Al-LDH的混合浆液中,加入的Li-Al-LDH的湿重为12.2g,其干重为3.6g,壳聚糖与Li-Al-LDH的质量比为1:3,这样制备得到粒状铝盐基提锂吸附剂2号。
在与实施例1中测定吸附剂对锂的静态吸附量的相同吸附条件下,测得粒状吸附剂2号对锂的平衡吸附量为9.71mg/g。
图2为本发明实施例2中的粒状铝盐基提锂吸附剂的光学照片图,相比于现有滴球造粒技术制备的凝胶小球,本发明的吸附剂颗粒尺寸从外观上看起来要小得多;图3为本发明实施例2中的粒状铝盐基提锂吸附剂在显微镜下观察得到的形貌图,由图可见粒状吸附剂的形状不规则,其粒径大小主要介于600~1000微米范围内;图4为本发明实施例2中示例的粒状铝盐基提锂吸附剂的扫描电镜图,即使在放大倍数达到4万倍的情况下,仍然观察不到明显的以纳米颗粒形式存在的锂铝层状双氢氧化物,说明锂铝层状双氢氧化物在壳聚糖凝胶网络中分布均匀。如图5所示,实施例2中的粒状铝盐基提锂吸附剂的XRD谱图中有很强的锂铝层状双氢氧化物的特征衍射峰信号出现,说明壳聚糖凝胶网络中分布着大量能够提取锂的锂铝层状双氢氧化物。
实施例3
粒状铝盐基提锂吸附剂的制备方法同实施例1,区别仅在于将实施例1中分散至壳聚糖水溶液中的湿的Li-Al-LDH的用量进行了调整:在本实施例中的壳聚糖与Li-Al-LDH的混合浆液中,加入的Li-Al-LDH的湿重为32.4g,其干重为9.6g,壳聚糖与Li-Al-LDH的质量比为1:8,这样制备得到粒状铝盐基提锂吸附剂3号。
在与实施例1中测定吸附剂对锂的静态吸附量的相同吸附条件下,测得粒状吸附剂3号对锂的平衡吸附量为11.86mg/g。
对比例1
按实施例1中制备锂铝层状双氢氧化物前驱体的方法离心得到Li-Al-LDH湿的沉淀,在55℃真空干燥12h。将干燥的Li-Al-LDH用去离子水振荡漂洗脱锂12h,再在55℃真空干燥12h,得到脱锂的锂铝层状双氢氧化物吸附剂,经研磨过200目筛后备用。
在与实施例1中测定吸附剂对锂的静态吸附量的相同吸附条件下,测得脱锂的锂铝层状双氢氧化物吸附剂对锂的平衡吸附量为6.50mg/g。
图6为单纯壳聚糖、对比例1和实施例2-3中对应的铝盐基提锂吸附剂的XRD谱图的比较,除单纯壳聚糖外,对比例1和实施例2-3中对应的铝盐基提锂吸附剂均出现了锂铝层状双氢氧化物的特征衍射峰(与锂铝层状双氢氧化物LiAl
实施例4
粒状铝盐基提锂吸附剂的制备方法同实施例1,区别仅在于将实施例1中处理复合凝胶的筛网进行了调整:本实施例中制得的复合凝胶压碎后过30目筛网以获到粒径更小的凝胶颗粒,这样制备得到粒状铝盐基提锂吸附剂4号。
在与实施例1中测定吸附剂对锂的静态吸附量的相同吸附条件下,测得粒状吸附剂4号对锂的平衡吸附量为8.86mg/g。
实施例5
粒状铝盐基提锂吸附剂的制备方法同实施例1,区别仅在于将实施例1中处理复合凝胶产物的筛网进行了调整:本实施例中制得的复合凝胶压碎后过10目筛网以获到粒径更大的凝胶颗粒,这样制备得到粒状铝盐基提锂吸附剂5号。
在与实施例1中测定吸附剂对锂的静态吸附量的相同吸附条件下,测得粒状吸附剂5号对锂的平衡吸附量为7.79mg/g。
实施例6
粒状铝盐基提锂吸附剂的制备方法同实施例1,区别仅在于将实施例1中制备复合凝胶时所加的交联剂戊二醛的用量改为壳聚糖质量的30%,这样制备得到粒状铝盐基提锂吸附剂6号。
在与实施例1中测定吸附剂对锂的静态吸附量的相同吸附条件下,测得粒状吸附剂6号对锂的平衡吸附量为8.25mg/g。
实施例7
粒状铝盐基提锂吸附剂的制备方法同实施例1,区别仅在于将实施例1中制备复合凝胶时所加的交联剂调整为乙二醛,这样制备得到粒状铝盐基提锂吸附剂7号。
按实施例1中测定吸附剂对锂的静态吸附量的相同吸附条件,测得粒状吸附剂7号对锂的平衡吸附量为7.45mg/g。
实施例8
基于实施例2制备得到的粒状吸附剂2号在静态吸附条件下的重复使用性能。按固液比为1g(吸附剂干重):30mL的比例,将脱锂粒状吸附2号加入到模拟盐湖老卤水中,在30℃的恒温水浴摇床中,以200rpm的转速振荡吸附48h。吸附过程结束后,过滤得到吸附锂的粒状吸附剂2号,滤液中残留的锂浓度用ICP-OES测定。按固液比为1g:30mL的比例,用冰的去离子水淋洗去除吸附剂2号表面附着的杂质离子。然后,再按固液比为1g:100mL的比例,将吸附锂的粒状吸附剂2号分散在去离子水中,在30℃的恒温水浴摇床中,以200rpm的转速振荡脱锂4h,过滤得到经脱锂处理的粒状吸附剂2号,这样就完成了第一个吸附-脱附循环过程。
如图7所示,粒状吸附剂2号在15次的吸附-脱附循环过程中,对锂的吸附量基本没有发生明显的改变,说明粒状吸附剂2号具有良好的重复使用性能。
本领域的技术人员容易理解,以上所述仅为本发明的较佳实施例而已,并不用以限制本发明,凡在本发明的精神和原则之内所作的任何修改、等同替换和改进等,均应包含在本发明的保护范围之内。
- 一种高吸附容量颗粒型铝盐提锂吸附剂的制备方法
- 一种铝盐型锂吸附剂及其制备方法与应用
