由四氯硅烷和氢硅烷合成三氯硅烷
文献发布时间:2023-06-19 11:05:16
背景技术
三氯硅烷常规地是通过将粉末状的冶金级硅在300℃下在鼓吹氯化氢的情况下处理而生产的:
Si+3 HCl→HSiCl
可实现80-90%的产率。其是太阳能硅(solar silicon)的生产中的重要中间体,在所述生产中将三氯硅烷以复杂工艺蒸馏并且在加热的超纯硅棒上分解为硅、四氯化硅和氯化氢:
2 HSiCl
三氯硅烷还由四氯化硅在T=500℃的温度下生产:
3 SiCl
(热力学限制产率为20%)。
在拜耳工艺(Bayer Process)中,使SiCl
对于反应SiCl
非工业程序例如描述于以下科学文献中:
a)Preparation of Trichlorosilane from Hydrogenation ofSilicontetrachloride in Thermal Plasma:W.Qingyou,C.Hanbin,L.Yuliang,T.Xumei,H.Zhijun,S.Shuyong,Y.Yongxiang,D.Xiaoyan:Inorganic Materials 2010,46(3),251-254.(HSiCl
b)Gas-Dynamic and Thermal Process in the Synthesis of Trichlorosilaneby Hydrogen Reduction of Silicon Tetrachloride in a High-Frequency Discharge:R.A.Kornev,V.A.Shaposhnikov,A.M.Kuz’min:Russian Journal of Applied Chemistry2014,87(9),1246-1250。
c)Mechanism of the silicide-catalyzed hydrodehalogenation of silicontetrachloride to trichlorosilane:H.Walter,G.Roewer,K.Bohmhammel:J.Chem.Soc.Faraday Trans.1996,92(22),4605-4608(转化率~15%,T=600℃)。
d)Hydrodehalogenation of Chlorosilanes in the Presence of MetalSilicides:Experimental Studies of Gas and Solid Phase Composition related toThermodynamic Calculations:K.Bohmhammel,G.Roewer,H.Walter:J.Chem.Soc.FaradayTrans.1995,91(21),3879-3882。
e)Catalytic conversion of silicon tetrachloride to trichlorosilanefor a poly-Si process:J.Y.Lee,W.H.Lee,Y.-Ki Park,H.Y.Kim,N.Y.Kang,K.B.Yoon,W.C.Choi,O-Bong Yang:Solar Energy Materials and Solar cells 105(2012)142-147(使用碳基催化剂(在连续流固定床反应器中的金属-碳复合催化剂)T~650℃,HSiCl
f)Base-Catalyzed Hydrogenation of Chlorosilanes by OrganotinHydrides:U.
涉及三氯硅烷生产的专利公布包括例如US7442824 B2、US2008/0112875 A1、US2013/0216464 A1、US2016/0002052 A1、US2017/0369325 A1。
在制备上将SiCl
在制造HSiCl
由该直接合成,HSiCl
因此,一直强烈需要从可容易获得的起始材料以高的产率选择性地制备三氯硅烷的经济上可行的工艺,该工艺是节能的,在低温下进行,并且其容许三氯硅烷与副产物的简单分离。
发明内容
本发明人发现,可从四氯硅烷和氢硅烷以高产率制备三氯硅烷,该工艺是节能的,在低温下进行,并且容许三氯硅烷与副产物的简单分离。
根据本发明,提供了制备三氯硅烷(HSiCl
在本发明的一种优选实施方式中,氢硅烷选自下式:
R
R
其中
R为有机基团,
X为卤素或烷氧基,
n为0-3、优选l-3、更优选2,
m为0-2、优选0,和
n+m=0-3、优选1-3、更优选2,
o为0-5、优选1-5,
p为0-5、优选0,和
o+p=1-5。
在上式(1)和(2)中,R优选地选自芳族或优选地具有最高达6个碳原子的脂族烃基团,优选地选自C1-C6烷基基团或C2-C6烯基基团,更优选地选自C1-C4烷基基团。
有机或有机基基团R可为相同或不同的,并且优选地R包括芳族基团例如苯基、甲苯基,和/或脂族烃基团;更优选地R为烷基基团例如甲基,乙基,正或异丙基,正丁基,仲丁基,异丁基,叔丁基,正戊基,叔戊基,新戊基,异戊基,仲戊基,正、异或仲己基,正、异或仲庚基,正、异或仲辛基等,甚至更优选地R为正烷基基团,或者R为烯基基团。
更优选的基团R选自Me=甲基、Et=乙基、Vi=乙烯基、n-Pr=正丙基、i-Pr=异丙基、烯丙基、t-Bu=叔丁基、n-Bu=正丁基、Hex=正己基、Ph=苯基、p-Tol=对甲苯基、Bz=苄基、和Mes=莱基、或其混合物。最优选的R为甲基基团。
X为卤素原子、优选氯或溴、更优选氯,或烷氧基基团例如C1-C6烷氧基、优选甲氧基或乙氧基。
优选地氢硅烷选自SiH
根据本发明的工艺在促进SiCl
-R
-式R
-式R
-N-杂环胺、优选非N取代的甲基咪唑例如2-甲基咪唑和4-甲基咪唑,
-碱金属卤化物例如LiCl,和
-碱土金属卤化物。
在本发明的一种优选实施方式中,该制备三氯硅烷的工艺在式R
优选的催化剂选自:
-季铵或鏻化合物,例如
-R
-R
-式R
-式R
-N-杂环胺,优选非N取代的甲基咪唑例如2-甲基咪唑和4-甲基咪唑,优选的是在氮原子处具有自由亲核电子对的N-杂环胺,这意味着此类N-杂环胺中的氮原子处的亲核性未被诱导或者中介(mesomeric)相互作用所降低。特别地,环状酰胺通常不适合作为再分配(重分布,redistribution)催化剂,
-碱金属卤化物,例如NaCl、KCl、LiCl,
-碱土金属卤化物,例如MgCl
而且可使用两种或更多种类型催化剂的组合。
最优选的再分配催化剂选自通式R
进一步优选的催化剂选自三有机基膦PR
关于催化剂相对于四氯硅烷的摩尔比,其优选地在约0.0001摩尔%-约600摩尔%、更优选地约0.01摩尔%-约20摩尔%、甚至更优选地约0.05摩尔%-约2摩尔%、和最优选地约0.05摩尔%-约1摩尔%的范围内。
此处,以%计的摩尔比定义为
[n(催化剂的摩尔量)/n(四氯硅烷的摩尔量)]×100。
在根据本发明的另一优选实施方式中,式R
根据本发明,R
在本发明中,发现n-Bu
在一种特别优选的实施方式中,本发明涉及通过使四氯硅烷与二甲基硅烷反应而制备三氯硅烷的工艺。
在一种特别的优选实施方式中,本发明涉及制备三氯硅烷的工艺,其包括使四氯硅烷与二甲基硅烷根据反应方程式(I)或(II)反应:
Me
Me
因此,取决于优选形成Me
本发明的另一特别优选的实施方式涉及如下反应工艺:Me
根据本发明的制备三氯硅烷的工艺可在存在或不存在溶剂的情况下进行。如果使用溶剂,则本发明的工艺在一种或多种溶剂存在下进行,所述溶剂优选地选自醚溶剂。根据本发明,所述醚溶剂可选自醚化合物,其优选地选自线型和环状脂族醚化合物。在本发明中,术语“醚化合物”应意指含有醚基团-O-、特别是具有式R
优选地,R
根据本发明的制备三氯硅烷的工艺优选地于在约-40℃至约250℃范围内、更优选地在约0℃至约200℃范围内、还更优选地在约25℃至约150℃范围内的温度下进行。
根据本发明的制备三氯硅烷的工艺优选地在约0.1-约10巴的压力下进行,优选地反应在大约常压(约1013毫巴)下进行。
本发明的工艺优选地在惰性条件下进行。根据本发明,术语“惰性条件”意指,所述工艺部分地或完全地在排除周围空气、特别是水分和氧气的情况下进行。为了从反应混合物和反应产物排除环境空气,可使用密闭反应容器,减压和/或惰性气体、特别是氮气或氩气,或此类手段的组合。
本发明的工艺可连续地或不连续地例如间歇进行。
在根据本发明的工艺的一种优选实施方式中,通过蒸馏将所得三氯硅烷和由氢硅烷形成的氯硅烷从反应混合物分离。本发明意义上的术语“蒸馏”涉及通过选择性蒸发和冷凝从液体混合物分离组分或物质的任何工艺。其中,蒸馏可导致实际上完全分离,从而致使几乎纯组分的离析,或者其可为使混合物的所选组分的浓度提高的部分分离。可构成分离步骤B)的蒸馏过程可为简单蒸馏、分馏、真空蒸馏、短程蒸馏或者技术人员已知的任何其它种类的蒸馏。将三氯硅烷以及由氢硅烷形成的氯硅烷分离的步骤可包括一个或多个间歇蒸馏步骤,或者可包括连续蒸馏过程。
本发明的一种特别的优选工艺进一步包括如下步骤:将所得氯硅烷氢化为式(1)或(2)的氢硅烷,并且将所述氢硅烷再循环到与四氯硅烷的反应中。
例如在包括使四氯硅烷与二甲基硅烷优选地根据反应方程式(I)或(II)反应的特别的制备三氯硅烷的工艺中:
Me
Me
将所得Me
优选地,将所述氯硅烷氢化的步骤用氢化剂进行,所述氢化剂选自金属氢化物,优选地选自碱金属氢化物例如LiH、NaH、KH,碱土金属氢化物例如氢化钙,或复合金属氢化物例如LiAlH
合适的氢化剂通常包括金属氢化物,其中优选地选自二元金属氢化物例如LiH、NaH、KH、CaH
最优选的氢化剂为氢化锂。
在根据本发明的工艺的一种优选实施方式中,在氢化反应中,氢化剂、特别是金属氢化物、优选地LiH相对于氯硅烷化合物的量在约1摩尔%-约600摩尔%、优选地约1-约400摩尔%、更优选地约1-约200摩尔%、最优选地约25-约150摩尔%的范围内,基于氯硅烷化合物中存在的氯原子的总摩尔量。
如上所述,最优选的氢化源为LiH,其在该反应中被转化为氯化锂(LiCl)。在使用氢化锂的此类工艺的一种特别的优选实施方式中,将所形成的LiCl分离并且使其经历如下步骤:纯化,任选地与KCl混合以制备LiCl-KCl低共熔组合物,将该低共熔或熔融LiCl电解以获得金属Li并且从如此制备的Li再生LiH。
该实施方式的特别的优点是,通过将产生的LiCl再循环和增值并且将其转化回LiH,其使本发明的工艺是经济的并且高效的,包括特别是在转化反应
(完全化学计量:
2 LiCl→2 Li+Cl
2 Li+H
氢化反应优选地在一种或多种溶剂的存在下进行,所述溶剂优选地选自醚溶剂例如以上描述的那些。
因此,本发明的一种特别优选的实施方式涉及制备三氯硅烷的工艺,其包括:
A)使四氯硅烷与二甲基硅烷在式R
Me
Me
在式R
B)从反应混合物分离HSiCl
C)将Me
D)将Me
本发明的工艺容许以高的选择性制备三氯硅烷。特别地,形成HSiCl
形成的HSiCl
即,根据本发明的工艺,四氯硅烷被选择性地反应为三氯硅烷,而不形成更高的氢化物例如H
而且,本发明的工艺中的转化率优选为至少90%、优选至少95%和还更优选至少99%。本发明中的术语转化率意指,如果例如使Me
实例1)Me
实例2)10 Me
实例3)10 Me
因此,对于100%转化率,所使用的氢硅烷必须被完全氯化以形成HSiCl
(形成的HSiCl
在根据本发明的制备三氯硅烷的工艺中,优选地氢硅烷对四氯硅烷(SiCl
在本发明的一种优选实施方式中,在制备三氯硅烷的工艺中,氢硅烷是由氯硅烷和LiH原位形成的。在该原位工艺的一种优选实施方式中,使SiCl
将理解,本文中叙述的任何数值范围包括在该范围内的所有子范围以及此类范围或子范围的各种端点的任意组合,不论其是在说明书的实施例中还是任何其它地方描述的。
还将理解,本文中叙述的各数值可存在一定误差,使得各数值应当与“约”相联系。
本文中还将理解,本文中本发明的任意组分在它们通过任何具体的属(genus)或者在说明书的实施例部分中详述的物种(species)描述时,可在一个实施方式中用于限定说明书中其它地方关于该组分所描述的范围的任意端点的替代的相应定义,并且可因此在一个非限制性实施方式中用于代替其它地方描述的此类范围端点。
将进一步理解,明确地或者隐含地在说明书中公开和/或在权利要求中叙述为属于在结构、组成和/或功能上相关的化合物、材料或物质的集合的任何化合物、材料或物质包括该集合的单独代表以及其全部组合。
虽然以上描述包含了许多细节,但是这些细节不应被解释为对本发明范围的限制,而是仅作为其优选实施方式的示例。本领域技术人员可展望在如由所附权利要求所定义的本发明的范围和精神内的许多其它可能的变型。
实施例
本发明通过以下实施例进行进一步说明,而不限于其。
为获得作为起始材料的有机基氢硅烷,通过用常规还原剂例如金属氢化物MH或MH
作为有机基硅烷的反应伙伴(reaction partner)使用以获得三氯硅烷和有机基氯硅烷的四氯硅烷是包括由硅金属和HCl生产三氯硅烷的西门子工艺的主要副产物,并且在市场上是可过多获得的。在NMR管中混合反应伙伴即氢硅烷(0.1ml)和以化学计量所需的约20-50摩尔%过量的SiCl
在优化和完成氢化反应SiCl
所形成产物的量可通过由NMR光谱法测量的摩尔比率以及所应用起始材料的量而估算。
由NMR实验评价最佳反应条件,并且将所述最佳反应条件示例性地转用到由四氯硅烷与作为氢转移剂的有机基硅烷Me
所述玻璃安瓿具有150mm的长度、50mm的外径和2mm的壁厚(内部容积~200ml)。对于高沸点有机基硅烷例如PhSiH
产物通过
起始材料和所形成反应产物的
表1:单-和二硅烷的
如从表2断定的,四氯硅烷单氢化以选择性地产生三氯硅烷的程度主要受两个因素支配:首先,在作为转移剂的带有氢的单硅烷的硅中心处的有机基取代基的空间要求;然后,所调查催化剂的氢化活性。甲基取代的氢硅烷MeSiH
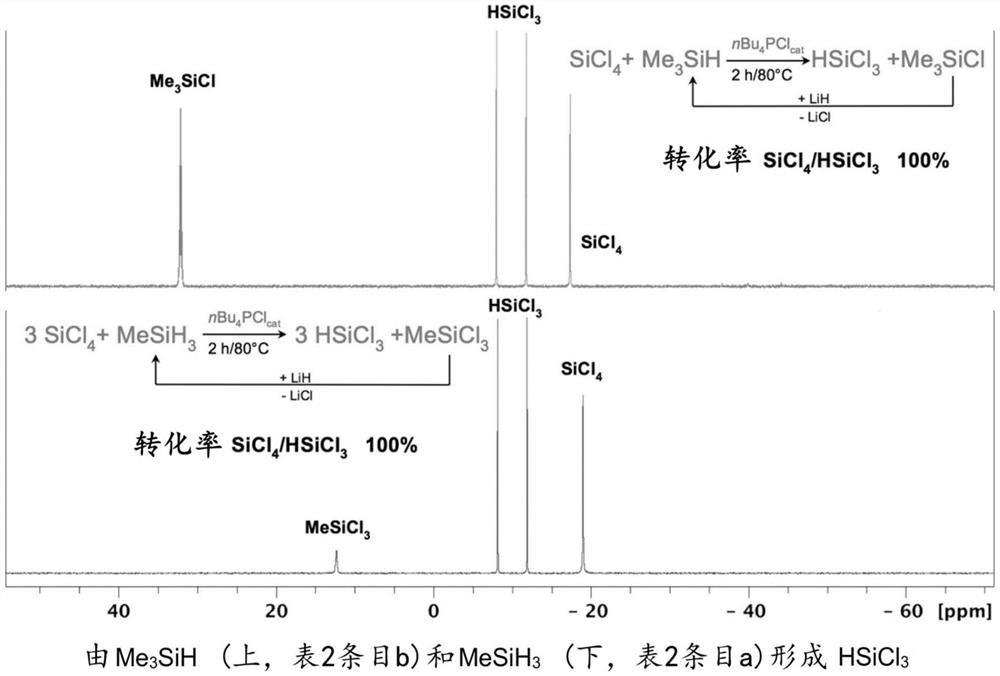
A)在制备规模上由Me
在惰性的氮气气氛下,在装备有滴液漏斗、回流冷凝器和磁力搅拌器的250ml三颈烧瓶中放置7.22g(0.88mol,97%)氢化锂(LiH),将其悬浮在100ml彻底干燥的四氢呋喃(THF)中。通过在真空中脱气和用气态氮再填充以建立惰性条件,将该THF/LiH悬浮液仔细地剥除氧气/空气。向该经剧烈搅拌的悬浮液,用滴液漏斗缓慢地添加56.84g(53.6ml,0.44mol)二甲基二氯硅烷(Me
将玻璃安瓿(长度:15cm,内径:5cm,壁厚:2mm)在真空中抽真空并且随后用气态氮填充以产生惰性气氛。然后,将96.6g(0.57mol)SiCl
B)在制备规模上由Me
如对于Me
类似于使用Me
C)在制备规模上、开放系统中由PhSiH
在开放系统中进行PhSiH
表3:收集在玻璃安瓿中的冷凝的产物混合物(59.44g)。
PhSiH
D)在制备规模上HSiCl
类似于B)中使用Me
表4:使用Me
将产物混合物随后在80℃下加热另外的2小时以完成Me
表5:收集在冷阱中的挥发物的产物分布。
转化率SiCl
E)在LiCl和KCl催化下由Et
在NMR管中将0.08ml(0.62mmol)Et
表6:LiCl和KCl催化的Et
在LiCl催化的情况下,在120℃下54h的反应时间之后没有Et
在相当的条件下,通过将LiCl用KCl代替,HSiCl
F)由甲基氢二硅烷和SiCl
F1)在NMR管中将0.1ml(0.61mmol)Me
表7:四甲基二硅烷与SiCl
该实施例清楚地证明,作为氢穿梭剂(shuttle)的四甲基二硅烷将四氯硅烷选择性地单脱卤而产生纯三氯硅烷(转化率SiCl
F2 a)在NMR管中将0.05m1(0.4mmol)MeH
表8:在室温下二甲基二硅烷与SiCl
如从表8(其包含包括过量SiCl
F2 b)将与F2 b)相当的样品[0.05ml(0.4mmol)MeH
表9:在80℃下二甲基二硅烷与SiCl
将样品在80℃下加热12h导致形成39摩尔%
F3)在NMR管中将0.07ml甲基氢二硅烷混合物(二硅烷分布如表10中描绘)、0.21mlSiCl
表10:起始二硅烷混合物的二硅烷分布。
表11:二硅烷混合物与SiCl
在F3)下面描述的实验明确地将用于甲基氯硅烷生产的Müller-Rochow-直接工艺(Si+MeCl/Cu催化剂/350℃→Me
所进行并且在表2中列出的所有实验以及在制备规模上三氯硅烷的合成是根据对于限定的产物形成而言的化学计量要求而运行的。如早先提及的,四氯硅烷向三氯硅烷的转变是以关于SiCl
G)在n-Bu
在惰性条件下将四氯硅烷(0.4ml)、二甘醇二甲醚(0.3ml)、C
H)使用不同催化剂由SiCl
在惰性条件下,在NMR管中将四氯硅烷(0.2ml)、五氯二硅烷(0.2ml)、二甘醇二甲醚(0.2ml)以及C
表12:使用PCDS的SiCl
在所有实验中SiCl
I)在nBu
为了详细研究化学计量在四氯硅烷的单还原中的作用,进行一组实验。示例性地,在作为溶剂的C
原料溶液的制备:将1.00ml(7.7mmol)Et
在三个竞争实验的第一个中,将0.6ml的原料溶液和催化量的nBu
表12:使用Et
如预期的,使等摩尔量的Et
J)由SiCl
在NMR管中将0.6ml(5.2mmol)SiCl
将样品在80℃下进一步加热(另外的7h)得到42.0%HSiCl
1)考虑到沸点,所形成的产物可通过在常压下蒸馏而分离:
HSiCl
2)反应物例如Me
3)SiCl
4)对于运行Müller Rochow直接工艺(Si+MeCl(Cu催化剂,ΔT)→Me
5)Me
6)氢硅烷RSiH
Me
具有高的经济价值。该工艺是高度经济的并且可用于有机硅工业中以及用于硅沉积。由于大多数的消耗硅的公司运行两种直接工艺(Müller Rochow和西门子),因此可将该工艺容易地包括到主要产品物流中。另外,所有的囊括的消费者都良好地装备有用以对起始材料进行预先纯化的高度发达的蒸馏装备以生产高纯产物例如HSiCl
- 由四氯硅烷和氢硅烷合成三氯硅烷
- 连续分离四氯化硅、丙基三氯硅烷及3-氯丙基三氯硅烷的装置及方法
