用于表征表面活性剂蛋白D(SP-D)寡聚物的系统和方法
文献发布时间:2023-06-19 09:30:39
相关申请的交叉引用
本申请要求2018年3月29日提交的标题为“用于表征表面活性剂蛋白D(SP-D)寡聚物的方法(METHODS FOR CHARACTERIZING SURFACTANT PROTEIN D(SP-D)OLIGOMERS)”的美国临时申请第62/650138号的优先权,所述美国临时申请通过引用以其整体并入本文。
关于序列表
本申请与电子格式的序列表一起提交。序列表提供为2019年3月20日创建的名称为AIRWY013WOSEQLIST的文件,其大小为约7Kb。电子格式的序列表的信息通过引用以其整体并入本文。
发明领域
本文提供的方法和组合物的一些实施方案包括鉴定和/或定量表面活性剂蛋白-D(SP-D)的寡聚物质。一些实施方案包括对SP-D进行非对称流场流分离和多角度激光光散射(AF4-MALLS)分析。
发明背景
哺乳动物肺表面活性剂是蛋白质(10%)和脂质(90%)(包括主要脂质组分二棕榈酰基磷脂酰胆碱)的混合物(Zuo YY,等人,Biochim Biophys Acta(2008)1778:1947–77)。肺表面活性剂的主要功能是确保肺内的最小表面张力,以避免呼吸过程中的塌陷。此外,通过与吸入的病原体相互作用,肺表面活性剂也参与宿主防御(Clements JA.Am Rev RespirDis(1977)115:67–71)。因此,肺表面活性剂缺乏与肺部疾病如哮喘、细支气管炎、呼吸窘迫综合征(RDS)、囊性纤维化和肺炎有关(Griese M.Eur Respir J(1999)13:1455–76)。表面活性剂制剂可用于治疗RDS,RDS每年在全球影响约150万名早产婴儿。呼吸窘迫综合征是一种由早产儿的肺结构不成熟引起的主要肺表面活性剂缺乏疾病,其使呼吸困难、抑制气体交换并促进肺泡塌陷(Notter RH.2000Lung Surfactants.Basic Science and ClinicalApplications.New York,NY:Marcel Dekker Inc.)。然而,如果肺部受到感染或如果存在炎性或氧化并发症,治疗将变得更加困难,因为当前的表面活性剂制剂缺乏表面活性剂蛋白D(SP-D)。因此,成功治疗复杂的肺部疾病需要产生表面活性剂制剂,其组分应尽可能接近地匹配天然的肺表面活性剂(Robertson B,等人,Biochim Biophys Acta(1998)1408:346–61)。
SP-D通过提供抗炎和抗微生物活性解决慢性肺部疾病(如哮喘、囊性纤维化和吸烟诱导的肺气肿)而在肺部先天免疫系统中发挥作用(Clark H,等人,Immunobiology(2002)205:619–31)。基于早产新生羔羊的数据表明,与100mg/kg
传统上,SP-D已从支气管肺泡灌洗液或羊水的上清液中分离出来,但大多数SP-D在纯化过程中会丢失,部分原因是SP-D的亲水性特性(Dodagatta-Marri E,等人,MethodsMol Biol(2014)100:273–90)。因为当前的肺表面活性剂制剂缺乏在不存在亲水性表面活性剂蛋白的情况下有效调节宿主免疫应答的能力,所以使用重组人表面活性剂蛋白D(rhSP-D)补充肺表面活性剂制剂可以确保治疗功效。必须在任何药物组合物中维持的天然SP-D的特征是适当的寡聚化状态,因为内源性表面活性剂蛋白中的高阶多聚化增加了病原体表面上碳水化合物配体的SP-D-结合位点的数量,从而达到有效的细菌和病毒凝集作用(White M,等人,J Immunol(2008)181:7936–43)。也需要适当的寡聚化状态进行受体识别和受体介导的信号转导以调节宿主免疫应答(Yamoze M等人,J Biol Chem(2008)283:35878-35888)以及维持表面活性剂内稳态(Zhang L等人,J Biol Chem(2001)276:19214-19219)。低的SP-D产量和可变的寡聚化状态使得难以使用天然来源产生药物SP-D(StrongP,等人,J Immunol Methods(1998)220:139–49)。为了克服这些局限性中的一些,可以在微生物或哺乳动物细胞系中产生重组的SP-D,从而潜在地提供产生同质重组SP-D制剂提供大规模平台。然而,重组的SP-D可具有可变的寡聚化状态和/或非活性聚集形式,因此降低了此类制剂的潜在功效。因此,需要有一种方法可用于将活性寡聚形式与非活性聚集形式区分开,并对寡聚形式进行定量以确保生产过程中可重现的质量。
发明概述
本文提供的方法和组合物的一些实施方案包括确定包含表面活性剂蛋白-D(SP-D)的药物组合物的活性的方法。一些此类实施方案包括方法,所述方法包括:测量所述药物组合物中SP-D的寡聚物质的相对比例;和计算所述药物组合物中SP-D十二聚体的相对比例,从而确定所述药物组合物的活性。一些实施方案还包括计算所述药物组合物中平均半径大于70nm或均方根(RMS)半径大于70nm的SP-D聚集物的相对比例。在一些实施方案中,测量包括进行非对称流场流分离和多角度激光光散射(AF4-MALLS)分析。在一些实施方案中,计算包括提供包含棒状几何形状和球状几何形状的SP-D的寡聚物质的模型。在一些实施方案中,模型包括SP-D的寡聚物质的Zimm模型和二阶德拜模型(second order Debyemodel)。一些实施方案还包括测量SP-D样品中至少一种SP-D寡聚物质的相对比例,其中SP-D寡聚物质选自:SP-D三聚体、SP-D六聚体、SP-D十二聚体、平均半径为70nm或RMS半径为70nm的SP-D星状寡聚物和平均半径大于70nm或RMS半径大于70nm的SP-D聚集物。
本文提供的方法和组合物的一些实施方案包括确定样品中表面活性剂蛋白-D(SP-D)的寡聚物质的相对比例,其包括:对SP-D样品进行非对称流场流分离和多角度激光光散射(AF4-MALLS)分析;和由AF4-MALLS分析的结果确定SP-D寡聚物质的相对比例,其中SP-D寡聚物质选自:SP-D三聚体、SP-D六聚体、SP-D十二聚体、平均半径为70nm或RMS半径为70nm的SP-D星状寡聚物和平均半径大于70nm或RMS半径大于70nm的SP-D聚集物。一些实施方案还包括测量样品中SP-D十二聚体的相对比例。一些实施方案还包括测量样品中平均半径大于70nm或RMS半径大于70nm的SP-D聚集物的相对比例。
本文提供的方法和组合物的一些实施方案包括确定样品中表面活性剂蛋白-D(SP-D)的活性寡聚物质的相对比例的方法,其包括:对SP-D样品进行非对称流场流分离和多角度激光光散射(AF4-MALLS)分析;测量SP-D样品中SP-D十二聚体的相对比例;测量SP-D样品中至少一种SP-D寡聚物质的相对比例,所述SP-D寡聚物质选自:SP-D三聚体、SP-D六聚体、平均半径为70nm或RMS半径为70nm的SP-D星状寡聚物和平均半径大于70nm或RMS半径大于70nm的SP-D聚集物;以及计算每个测量的相对比例之间的比率。在一些实施方案中,至少一种SP-D寡聚物质包括平均半径大于70nm或RMS半径大于70nm的SP-D聚集物。一些实施方案还包括将来自AF4-MALLS分析的级分图级分成峰。一些实施方案还包括测量指示SP-D寡聚物质的至少一个峰的级分图的相对峰面积(RPA),所述SP-D寡聚物质选自SP-D三聚体、SP-D六聚体、SP-D十二聚体、平均半径为70nm或RMS半径为70nm的SP-D星状寡聚物和平均半径大于70nm或RMS半径大于70nm的SP-D聚集物。在一些实施方案中,SP-D星状寡聚物的摩尔质量小于或等于约6MDa。在一些实施方案中,SP-D聚集物的摩尔质量大于6MDa。
一些实施方案还包括测量样品中平均半径为70nm或RMS半径为70nm的样品中的SP-D星状寡聚物质的相对比例。一些实施方案还包括测量样品中平均半径大于70nm或RMS半径大于70nm的SP-D聚集物的相对比例。
在一些实施方案中,预测SP-D样品在脂多糖-Toll样受体4(LPS-TLR4)测定或细菌聚集测定中具有活性。在一些实施方案中,SP-D样品中SP-D十二聚体的相对比例大于或等于所述样品中SP-D寡聚物质的35%指示SP-D样品具有活性。在一些实施方案中,SP-D样品中平均半径大于70nm或RMS半径大于70nm的SP-D聚集物的相对比例小于所述样品中总SP-D寡聚物质的5%指示SP-D样品具有活性。
在一些实施方案中,AF4-MALLS在螯合剂不存在下进行,所述螯合剂选自EDTA和EGTA。
在一些实施方案中,SP-D是重组人SP-D(rhSP-D)。在一些实施方案中,rhSP-D来源于表达来自转基因的rhSP-D的人髓系白血病细胞系。在一些实施方案中,rhSP-D包含SEQID NO:02的氨基酸序列。在一些实施方案中,rhSP-D在多态性位置处包含对应于选自Met11、Thr160、Ser 270和Ala 286的残基的残基。
在一些实施方案中,寡聚物质的相对比例是就质量而言。在一些实施方案中,SP-D的寡聚物质的相对比例是就分子数而言。在一些实施方案中,寡聚物质的相对比例是就在AF4-MALLS分析中的相对峰面积(RPA)或调整的RPA而言。在一些实施方案中,SP-D十二聚体的分子量为约520kDa。
本文提供的方法和组合物的一些实施方案包括用于确定包含表面活性剂蛋白-D(SP-D)的药物组合物的活性的电子系统。一些此类实施方案可包括系统,所述系统包括具有经配置以执行以下步骤的指令的处理器:测量药物组合物中SP-D的寡聚物质的相对比例;计算药物组合物中SP-D十二聚体的相对比例;和基于SP-D十二聚体的相对比例确定药物组合物的活性,其中SP-D十二聚体的较高相对比例指示与具有较低相对比例的SP-D十二聚体的组合物的活性相比,组合物具有更高水平的活性。在一些实施方案中,活性包括在toll样受体4(TLR4)测定、或在细菌聚集测定中的活性。一些实施方案还包括计算药物组合物中平均半径大于70nm或RMS半径大于70nm的SP-D聚集物的相对比例。在一些实施方案中,测量包括进行非对称流场流分离和多角度激光光散射(AF4-MALLS)分析。在一些实施方案中,计算包括提供包含棒状几何形状和球状几何形状的SP-D的寡聚物质的模型。在一些实施方案中,模型包括SP-D的寡聚物质的Zimm模型和二阶德拜模型。一些实施方案还包括测量SP-D样品中至少一种SP-D寡聚物质的相对比例,其中SP-D寡聚物质选自:SP-D三聚体、SP-D六聚体、SP-D十二聚体、平均半径为70nm或RMS半径为70nm的SP-D星状寡聚物和平均半径大于70nm或RMS半径大于70nm的SP-D聚集物。
本文提供的方法和组合物的一些实施方案包括用于确定样品中表面活性剂蛋白-D(SP-D)的寡聚物质的相对比例的电子系统。一些此类实施方案可包括系统,所述系统包括具有经配置以执行以下步骤的指令的处理器:对SP-D样品进行非对称流场流分离和多角度激光光散射(AF4-MALLS)分析;和由AF4-MALLS分析的结果确定SP-D寡聚物质的相对比例,其中SP-D寡聚物质选自:SP-D三聚体、SP-D六聚体、SP-D十二聚体、平均半径为70nm或RMS半径为70nm的SP-D星状寡聚物和平均半径大于70nm或RMS半径大于70nm的SP-D聚集物。一些实施方案还包括测量样品中的SP-D十二聚体的相对比例。一些实施方案还包括测量样品中平均半径大于70nm或RMS半径大于70nm的SP-D聚集物的相对比例。
本文提供的方法和组合物的一些实施方案包括用于确定样品中表面活性剂蛋白-D(SP-D)的活性寡聚物质的相对比例的电子系统。一些此类实施方案包括系统,所述系统包括具有经配置以执行以下步骤的指令的处理器:对SP-D样品进行非对称流场流分离和多角度激光光散射(AF4-MALLS)分析;测量SP-D样品中SP-D十二聚体的相对比例;测量SP-D样品中至少一种SP-D寡聚物质的相对比例,所述SP-D寡聚物质选自SP-D三聚体、SP-D六聚体、平均半径为70nm或RMS半径为70nm的SP-D星状寡聚物和平均半径大于70nm或RMS半径大于70nm的SP-D聚集物;以及计算每个测量的相对比例之间的比率。在一些实施方案中,至少一种SP-D寡聚物质包括平均半径大于70nm或RMS半径大于70nm的SP-D聚集物。一些实施方案还包括将来自AF4-MALLS分析的级分图积分成峰。一些实施方案还包括测量指示SP-D寡聚物质的至少一个峰的级分图的相对峰面积(RPA),所述SP-D寡聚物质选自SP-D三聚体、SP-D六聚体、SP-D十二聚体、平均半径为70nm或RMS半径为70nm的SP-D星状寡聚物和平均半径大于70nm或RMS半径大于70nm的SP-D聚集物。在一些实施方案中,SP-D星状寡聚物的摩尔质量小于或等于约6MDa。在一些实施方案中,SP-D聚集物的摩尔质量大于6MDa。一些实施方案还包括测量样品中平均半径为70nm或RMS半径为70nm的所述样品中的SP-D星状寡聚物质的相对比例。一些实施方案还包括测量样品中平均半径大于70nm或RMS半径大于70nm的SP-D聚集物的相对比例。
在一些实施方案中,预测SP-D样品在脂多糖-Toll样受体4(LPS-TLR4)测定、或在细菌聚集测定中具有活性。
在一些实施方案中,SP-D样品中SP-D十二聚体的相对比例大于或等于所述样品中SP-D寡聚物质的35%指示SP-D样品具有活性。
在一些实施方案中,SP-D样品中平均半径大于70nm或RMS半径大于70nm的SP-D聚集物的相对比例小于所述样品中总SP-D寡聚物质的5%指示SP-D样品具有活性。
在一些实施方案中,AF4-MALLS在螯合剂不存在下进行,所述螯合剂选自EDTA和EGTA。
在一些实施方案中,SP-D是重组人SP-D(rhSP-D)。在一些实施方案中,rhSP-D来源于表达来自转基因的rhSP-D的人髓系白血病细胞系。在一些实施方案中,rhSP-D包含SEQID NO:02的氨基酸序列。在一些实施方案中,rhSP-D在多态性位置处包含对应于选自Met11、Thr160、Ser 270和Ala 286的残基的残基。
在一些实施方案中,寡聚物质的相对比例是就质量而言。在一些实施方案中,寡聚物质的相对比例是就AF4-MALLS分析中相对峰面积(RPA)或调整的RPA而言。在一些实施方案中,SP-D十二聚体的分子量为约520kDa。
附图简述
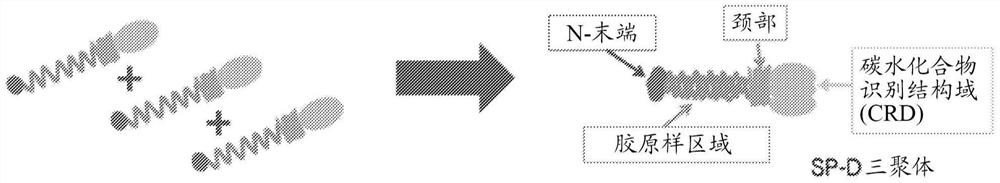
图1是描绘SP-D三聚体的形成和SP-D三聚体的结构特征的示意图。
发明详述
表面活性剂蛋白D(SP-D)是C型(Ca
一些实施方案包括使用非对称流场流分离(AF4)技术的变型解析SP-D的寡聚物质的系统和方法。开发了一些此类实施方案以从较高阶SP-D物质(十二聚体和更大)中拆分较低阶SP-D物质(六聚体和更小)。这些实施方案允许使用多角度激光光散射(MALLS)在复杂的级分图包络内清晰地描绘SP-D的十二聚体形式。使用掺入了MALLS的AF4技术的这种变型允许在众多(n=102)样品的分析中十二聚体的摩尔质量一致地确定为521.8±3.6kD。如本文所用,术语“AF4-MALLS”意指进行非对称流场流分离,然后使用多角度激光光散射鉴定分析的混合物中寡聚物质的方法。AF4-MALLS方法的精度计算为约5%。SP-D的级分图还显示了与比十二聚体大的物质有关的峰,所述峰以由十二聚体和/或六聚体组装产生的星状物质(通过原子力显微术(AFM))以及半径大于70nm的聚集物出现。因此,发现使用AF4-MALLS技术的实施方案提供了SP-D的多种高阶寡聚缔合状态的详细概况,发现其是精确和准确地确定的。
SP-D的样品可以包括SP-D蛋白的几种寡聚物质,包括:三聚体、六聚体、十二聚体以及更高阶的寡聚物,如平均均方根(RMS)半径为约70nm的星状寡聚物质和半径可以大于70nm的聚集物。如本文所述,SP-D的某些寡聚物质已经与某些有用的活性相关。例如,在Toll样受体4(TLR4)测定中,SP-D十二聚体已经与拮抗活性相关。TLR4测定可通过阻止LPS结合/激活TLR4复合物来测量rhSP-D抑制脂多糖(LPS)-诱导的炎性细胞应答的活性。SP-D在测定(如TLR4测定)中的活性可能是某些治疗方法中SP-D预测功效的有用指标。另外,SP-D的不同样品可以含有SP-D寡聚物质的不同相对分布。
样品中重组人SP-D(rhSP-D)的寡聚形式的分布可通过多种技术来确定。一些实施方案可包括通过进行AFM来鉴定rhSP-D的寡聚物质。一些实施方案可包括通过进行尺寸排除色谱如高效液相色谱(HPLC)来鉴定rhSP-D的寡聚物质。一些实施方案可包括通过进行聚丙烯酰胺凝胶电泳来鉴定rhSP-D的寡聚物质。在一些此类方法中,rhSP-D的样品可以与阴离子去污剂(如SDS)接触,然后使该样品与交联剂(如1%戊二醛)接触。交联的蛋白然后可通过尺寸使用诸如聚丙烯酰胺凝胶电泳的技术解析。一些方法还可以包括鉴定rhSP-D的不同寡聚物质,如进行蛋白质印迹。
一些实施方案包括对SP-D样品进行AF4-MALLS分析。AF4是一种类型的非对称流场流分离,其能够快速分离和高分辨率表征包括生物分子在内的各种颗粒。参见如Giddings,J.C.等人,Science 193:1244-1245(1976);Giddings,J.C.等人,Anal.Chem.48:1126-1132(1976);和Wagner等人,(2014)Anal Chem 86:5201-5210,将其各自通过引用以其整体并入。AF4可以分离范围从几纳米到几微米的颗粒。场流分离分离发生在与色谱分离柱相当的薄流道中。水性或有机溶剂通过该通道携带样品。由于通道高度低,因此通过通道的流动是层流的,并且是施加在样品上的第一力。垂直于通道流产生第二力。在AF4中,流道的一侧是膜,并且第二力是通过膜穿过通道的流体流动。由于这两个力,在该系统中发生了颗粒分离。首先,由于通道内的层流引起的速度梯度导致通道中心的颗粒沿通道移动得更快,并与更靠近通道侧面的那些颗粒分离。其次,第二力将样品推向膜。发生尺寸分离的原因是,较小的分子比较大的颗粒更快地向通道中心扩散回去,并且由于溶剂流向通道的中心更快,因此与较大的颗粒分离。在一些实施方案中,AF4-MALLS在螯合剂(如EDTA和EGTA)不存在下进行。
一些实施方案包括确定SP-D样品中活性寡聚物质的相对比例,其中SP-D寡聚物质选自:SP-D三聚体、SP-D十二聚体、平均半径为70nm或RMS半径为70nm的SP-D星状寡聚物和平均半径或RMS半径大于70nm的SP-D聚集物。在一些实施方案中,SP-D星状寡聚物可具有小于或等于约6MDa的摩尔质量。在一些实施方案中,SP-D聚集物的摩尔质量大于6MDa。
一些实施方案还包括将来自AF4-MALLS分析的级分图积分成峰。级分图中的第一峰(峰1)可包括SP-D三聚体和六聚体。级分图中的第二峰(峰2)可包括SP-D十二聚体。级分图中的第三峰(峰3)可包括SP-D十二聚体与SP-D星状寡聚物之间的中间物质。级分图中的第四峰(峰4)可包括与通过AFM测量对星状寡聚物质观察一致的恒定RMS半径为约70nm的rhSP-D寡聚物和半径大于70nm的更大SP-D聚集物质的异质团块。
一些实施方案还包括确定或测量峰的相对峰面积(RPA)占测量的峰(如以上鉴定的四个峰)的总峰面积的百分比。一些此类实施方案包括测量指示SP-D寡聚物质(如SP-D三聚体、SP-D十二聚体、平均半径为70nm或RMS半径为70nm的SP-D星状寡聚物和平均半径大于70nm或RMS半径大于70nm的SP-D聚集物)的至少一个峰的级分图的相对峰面积(RPA)。
在一些实施方案中,SP-D样品中SP-D十二聚体的相对比例大于或等于所述样品中SP-D寡聚物质的某一百分比指示SP-D样品具有活性,百分比可以是20%、25%、30%、35%、40%、45%、50%、55%、60%、65%、70%、75%、80%、85%、90%、95%以及前述百分比的任两个之间的任何百分比。
在一些实施方案中,在SP-D样品中SP-D聚集物的相对比例SP-D寡聚物质的某一百分比的样品指示SP-D样品具有活性,百分比可以是40%、35%、30%、25%、20%、15%、10%、5%、3%、2%、1%以及前述百分比的任两个之间的任何百分比。
在一些实施方案中,SP-D寡聚物质的相对比例可以是就质量、SP-D不同寡聚物质群体中的分子数/聚集物数、或AF4-MALLS分析中的相对峰面积(RPA)而言。
在一些实施方案中,SP-D包含野生型人SP-D多肽。在一些实施方案中,SP-D包括人SP-D多肽的多态性。示例性SP-D多肽序列提供于表1中。人SP-D多肽中的多态性可包括:残基11,ATG(Met)->ACG(Thr);残基25,AGT(Ser)->AGC(Ser);残基160,ACA(Thr)->GCA(Ala);残基270,TCT(Ser)->ACT(Thr);和残基286,GCT(Ala)->GCC(Ala),其中位置涉及成熟SP-D多肽中的位置,如SEQ ID NO:02的示例性多肽。在一些实施方案中,rhSP-D在多态性位置处包含某些残基,其中残基选自Met11/31、Thr160/180、Ser 270/290和Ala286/306,其中残基位置涉及成熟SP-D多肽(诸如例如SEQ ID NO:02)中的位置和具有前导多肽的SP-D多肽(如示例性SEQ ID NO:01)中的位置。在一些实施方案中,SP-D包含Met11/31。在一些实施方案中,rhSP-D包含Met11/31、Thr160/180、Ser 270/290和Ala 286/306。在一些实施方案中,SP-D多肽在整个长度的多核苷酸上与SEQ ID NO:02的多肽具有至少80%、90%、95%、99%和100%、或在任一个前述百分比之间的范围内任何百分比的同一性。
表1
在一些实施方案中,SP-D是重组人SP-D(rhSP-D)。在一些实施方案中,rhSP-D来源于表达来自整合的转基因的rhSP-D的人髓系白血病细胞系。从此类细胞纯化rhSP-D的示例性表达载体、rhSP-D多肽、细胞系和方法提供于U.S.2019/0071693和U.S.2019/0071694中,其各自通过引用以其整体明确并入本文。
本文提供的方法和组合物的一些实施方案包括用于确定包含表面活性剂蛋白-D(SP-D)的药物组合物的活性的电子系统。一些此类实施方案可包括系统,所述系统包括具有经配置以执行以下步骤的指令的处理器:测量药物组合物中SP-D的寡聚物质的相对比例;计算药物组合物中SP-D十二聚体的相对比例;和基于SP-D十二聚体的相对比例,确定药物组合物的活性,其中SP-D十二聚体的较高相对比例指示与具有较低相对比例的SP-D十二聚体的组合物的活性相比,组合物具有更高水平的活性。在一些实施方案中,活性包括toll样受体4(TLR4)测定中的拮抗活性。一些实施方案还包括计算药物组合物中平均半径大于70nm或RMS半径大于70nm的SP-D聚集物的相对比例。在一些实施方案中,测量包括进行非对称流场流分离和多角度激光光散射(AF4-MALLS)分析。在一些实施方案中,计算包括提供包含棒状几何形状和球状几何形状的SP-D的寡聚物质的模型。在一些实施方案中,模型包括SP-D的寡聚物质的Zimm模型和二阶德拜模型。一些实施方案还包括测量SP-D样品中至少一种SP-D寡聚物质的相对比例,其中SP-D寡聚物质选自:SP-D三聚体、SP-D六聚体、SP-D十二聚体、平均半径为70nm或RMS半径为70nm的SP-D星状寡聚物和平均半径大于70nm或RMS半径大于70nm的SP-D聚集物。
本文提供的方法和组合物的一些实施方案包括用于确定样品中表面活性剂蛋白-D(SP-D)的寡聚物质的相对比例的电子系统。一些此类实施方案可包括系统,所述系统包括具有经配置以执行以下步骤的指令的处理器:对SP-D样品进行非对称流场流分离和多角度激光光散射(AF4-MALLS)分析;和由AF4-MALLS分析的结果确定SP-D寡聚物质的相对比例,其中SP-D寡聚物质选自:SP-D三聚体、SP-D六聚体、SP-D十二聚体、平均半径为70nm或RMS半径为70nm的SP-D星状寡聚物和平均半径大于70nm或RMS半径大于70nm的SP-D聚集物。一些实施方案还包括测量样品中SP-D十二聚体的相对比例。一些实施方案还包括测量样品中平均半径大于70nm或RMS半径大于70nm的SP-D十二聚体的相对比例。
本文提供的方法和组合物的一些实施方案包括用于确定样品中表面活性剂蛋白-D(SP-D)的活性寡聚物质的相对比例的电子系统。一些此类实施方案包括系统,所述系统包括具有经配置以执行以下步骤的指令的处理器:对SP-D样品进行非对称流场流分离和多角度激光光散射(AF4-MALLS)分析;测量SP-D样品中SP-D十二聚体的相对比例;测量SP-D样品中至少一种SP-D寡聚物质的相对比例,所述SP-D寡聚物质选自:SP-D三聚体、SP-D六聚体、平均半径为70nm或RMS半径为70nm的SP-D星状寡聚物;和平均半径大于70nm或RMS半径大于70nm的SP-D聚集物;以及计算每个测量的相对比例之间的比率。在一些实施方案中,至少一种SP-D寡聚物质包括平均半径大于70nm或RMS半径大于70nm的SP-D聚集物。一些实施方案还包括将来自AF4-MALLS分析的级分图积分成峰。一些实施方案还包括测量指示SP-D寡聚物质的至少一个峰的级分图的相对峰面积(RPA),所述SP-D寡聚物质选自:SP-D三聚体、SP-D六聚体、SP-D十二聚体、平均半径为70nm或RMS半径为70nm的SP-D星状寡聚物和平均半径大于70nm或RMS半径大于70nm的SP-D聚集物。在一些实施方案中,SP-D星状寡聚物的摩尔质量小于或等于约6MDa。在一些实施方案中,SP-D聚集物的摩尔质量大于6MDa。一些实施方案还包括测量样品中平均半径为70nm或RMS半径为70nm的样品中SP-D星状寡聚物质的相对比例。一些实施方案还包括测量样品中平均半径大于70nm或RMS半径大于70nm的SP-D聚集物的相对比例。
在一些实施方案中,预测SP-D样品在脂多糖-Toll样受体4(LPS-TLR4)测定中具有拮抗活性。
在一些实施方案中,SP-D样品中SP-D十二聚体的相对比例大于或等于所述样品中SP-D寡聚物质的35%指示SP-D样品具有活性。在一些实施方案中,SP-D样品中SP-D十二聚体的相对比例大于或等于所述样品中SP-D寡聚物质的一定百分比指示SP-D样品具有活性,百分比可以是20%、25%、30%、35%、40%、45%、50%、55%、60%、65%、70%、75%、80%、85%、90%、95%、和前述百分比的任两个之间的任何百分比。
在一些实施方案中,SP-D样品中平均半径大于70nm或RMS半径大于70nm的SP-D聚集物的相对比例小于所述样品中总SP-D寡聚物质的5%指示SP-D样品具有活性。在一些实施方案中,SP-D样品中SP-D聚集物的相对比例小于所述样品中SP-D寡聚物质的一定百分比指示SP-D样品具有活性,百分比可以是40%、35%、30%、25%、20%、15%、10%、5%、3%、2%、1%、和前述百分比的任两个之间的任何百分比。
在一些实施方案中,AF4-MALLS在螯合剂不存在下进行,所述螯合剂选自EDTA和EGTA。
在一些实施方案中,SP-D是重组人SP-D(rhSP-D)。在一些实施方案中,rhSP-D来源于表达来自转基因的rhSP-D的人髓系白血病细胞系。在一些实施方案中,rhSP-D包含SEQID NO:02的氨基酸序列。在一些实施方案中,rhSP-D在多态性位置处包含对应于选自Met11、Thr160、Ser 270和Ala 286的残基的残基。
在一些实施方案中,寡聚物质的相对比例是就质量而言。在一些实施方案中,寡聚物质的相对比例是就AF4-MALLS分析中相对峰面积(RPA)或调整的RPA而言。
实施例
通过原子力显微镜(AFM)表征重组人SP-D(rhSP-D)的寡聚物质。参见,如ArroyoR,等人(2017)Biophysical Journal 112(3):503a,将其通过引用以其整体并入。将包含于稀释缓冲液(200mM NaCl,20mM Tris(pH 7.4),1mM EDTA)中的0.85ng/μL rhSP-D的溶液置于新鲜切割的云母基板上。将样品用来自Nanotec(Nanotec Electrónica,Madrid,Spain)和PointProbePlus尖端,PPP-NCH型(Nanosensors,
获得的图像中鉴定的寡聚物质包括三聚体、六聚体、十二聚体和星状寡聚物。三聚体具有棒状外观,并且一些三聚体经测量具有约65nm(±8.6nm)的平均长度。十二聚体具有X形外观,并且一些十二聚体经测量具有约136nm(±8.1nm)的尖端至相对尖端的长度。星状物质包括具有由6-20个三聚体组成的星形外观的成员,每个三聚体通过中心枢纽连结至该物质的特定成员。星状物质包括具有由6-20个三聚体组成的星形外观的成员,每个三聚体都通过中央枢纽与该物质的特定成员相连。一些星状物质经测量具有约140nm的直径,其类似于测量的十二聚体的直径。表2总结了观察到的寡聚物质的分布和频率。
表2
通过AF4-MALLS分析确定了rhSP-D的不同寡聚物质的分布。对于AF4-MALLS分析,通过AF4系统(Eclipse Dual Tec,Wyatt Technology Corp.,Santa Barbara,CA),然后通过UV(Ultimate 3000可变波长检测器,Dionex Corporation,Sunnyvale,CA)和MALS分析(Dawn Heleos II检测器,Wyatt Technology Corp.,Santa Barbara,CA)分离rhSP-D样品。Dionex Ultimate 3000HPLC系统(Dionex Corporation,Sunnyvale,CA)用于注射样品并将流动相递送至AF4系统。AF4配置使用具有350μm厚的垫片(Wyatt Technology Corp.,SantaBarbara,CA)的短通道。使用Chromeleon(DionexCorporation,Sunnyvale,CA)和ASTRA(Wyatt Technology Corp.,Santa Barbara,CA)软件进行数据的分析和计算。AF4-MALLS分析的结果包括具有几个峰的级分图。
ASTRA软件(版本6.1.1.17)计算出以下:每个选定峰的摩尔质量和均方根(RMS)半径力矩。力矩是指整个样品内的平均值,其可包括许多峰。等式(1)涉及数均摩尔质量:
ASTRA测量通常需要独立的浓度测定。由于浓度(mg/mL)与数密度(数量/ml)之间的关系为nM=c,因此可以确定等式(2)的结果。等式(2)涉及重均摩尔质量:
多分散性指数值为:ρ=M
为了确定摩尔质量,选择混合数学模型以使用光散射数据在rhSP-D分析中计算分子的大小和MW。如本文所指示,AFM图像显示了rhSP-D寡聚物质包括单体、二聚体、三聚体、六聚体、十二聚体和更高阶的寡聚结构。AFM图像显示了棒形、X形和星状的结构。星状结构通过AFM测量并经计算具有约70nm的半径,其通过二阶德拜模型最佳表征(P.Debye,“Molecular-weight determination by light scattering,”J.Phys.Coll.Chem.,第51卷,pp.18-32(1947),将其通过引用以其整体并入)。德拜模型使用Rθ/K*c形式体系并在较大的摩尔质量(包括非常大的质量(大于~10
其中u=[(2πno/λo)L sin(θ/2)],以及L是杆长
度,假定其比其可忽略的直径大得多。
单个模型无法适应SP-D结构的多样性。通常,Zimm模型可以足够灵活以适应多种几何形状,但在SP-D的情况下,使用了混合模态分析,其结合使用了二阶德拜模型和棒模型。将二阶德拜模型应用于SP-D寡聚物质,其包括半径大于70nm的聚集物(峰4)。将棒模型应用于棒状SP-D结构,其包括单体、二聚体、三聚体、六聚体和十二聚体(峰1和2)。在十二聚体和星状结构(峰3)的形成之间存在过渡,为此应用了棒模型来最好地表征MW。混合模型更好地拟合了AF4-MALLS数据,并且与通过AFM获得的几何测量结果一致。
通过使用对UV信号的分析和摩尔质量的分析(如通过光散射测定)的组合,将样品积分成四个峰部分,即峰1-4。所有相对面积均使用选定点的下拉积分(drop-downintegration)计算。峰2对应于rhSP-D十二聚体峰,其界线通过分析摩尔质量和多分散性指数来测定。将中心点(通常是UV迹线(UV trace)的最高点)和边界设置为与该点等距。如本文所述,该部分的多分散性通过Mw/Mn测量。通常,将大于1.2的值视为多分散性,而将小于1.1的值指定为具有低多分散性。移动边界直到多分散性指数为约1.05。指数在1.008至1.090变化。观察到峰边界的轻微移动可能导致指数变化。从峰2的后边界设置峰3边界,直到36.5分钟处发现UV迹线下降。峰4的外边界设定为45分钟。在45分钟时,关闭错流。那时残留在通道中的任何材料开始洗脱,并且没有有效地发生分离。峰1包括小于rhSP-D十二聚体的所有物质。在一些情况下,解析了较低分子量的物质,并进行了单独的积分。可以将MW迹线叠加在UV迹线上,并且发现六聚体(258kDa)、三聚体(129kDa)、二聚体(86kDa)和单体(42kDa)的积分点。峰相当窄,并且可以可靠地确定。
在最初的一系列研究中,使用原始流动相组成(20mM Tris缓冲液,pH 7.4,200mMNaCl,1mM EDTA)研究了错流参数。一旦建立了错流程序,一系列实验就研究了流动相组成的影响,导致了从包含20mM Tris,200mM NaCl,pH 7.4的流动相中去除EDTA。对聚焦步骤进行最终调整,导致了最终方法的运行时间为59.2分钟。表3列出了用于AF4的参数。
表3
在另一系列研究中,分析了从表达来自整合的转基因的rhSP-D的17种不同细胞系获得的102个rhSP-D冻干制剂。这些包括细胞系:S888、S990、S991、S1010、S2099及十二个细胞系(编号为2428至2439)。AF4方法的重现性使用四个不同的度量标准进行了测量:(i)级分图下的总面积,其表明精度,(ii)十二聚体的相对面积,(iii)根据MALLS数据计算的十二聚体的摩尔质量,以及(iv)十二聚体峰包络内摩尔质量的多分散性。计算所有样品中每个度量标准的相对标准偏差(rsd)。平均而言,表明精度的级分图下的总面积显示范围为4.3%至5.3%的rsd值。换句话说,对于给定的样品,这些复杂的级分图的总面积在运行间约5%内可重现。然而,这些样品中rhSP-D十二聚体的相对面积变化很大,从约25%至65%,并且这些相对量是可重现的,rsd值范围为约5%至6.5%。根据MALLS数据计算的摩尔质量的平均rsd非常低,为0.86%。最后,根据MALLS数据计算的多分散性指数(PDI)值表现出约1.5%的平均rsd值。
分析使用AF4-MALLS的数据,以确定洗脱期间某个时间的rhSP-D的绝对摩尔质量和尺寸。尺寸与质量之比指示rhSP-D的形状。根据尺寸与质量之比,确定了在洗脱的早期(0-34分钟),rhSP-D分子具有线性或棒状形状。对于棒模型计算,软件假定棒状颗粒的厚度与其长度相比不显著(0.0nm)。确定棒长度与136±8.1nm(N=50个单独分子)的AFM测量值一致。rhSP-D洗脱的后期(34-45分钟)表明观察到了更紧凑的结构。二阶德拜模型用以分析洗脱的这些阶段。二阶德拜模型在较大的摩尔质量(包括非常大的(大于~10
基于根据棒模型的质量计算,级分图中的第一峰(峰1)含有rhSP-D三聚体和六聚体。级分图中的第二峰(峰2)含有rhSP-D十二聚体。基于如由棒模型测定的中间分子量,级分图中的第三峰(峰3)含有rhSP-D十二聚体至rhSP-D星状寡聚物之间的中间物质。级分图中的第四峰(峰4)含有与通过AFM测量对星状寡聚物质观察一致的恒定RMS半径为约70nm的rhSP-D寡聚物和半径大于70nm的更大物质的异质团块。在级分图中超过36分钟后,RMS半径进一步增加,表明存在更多的聚集物质。将每个峰的相对峰面积(RPA)确定为四个峰的总峰面积的百分比。
为了使用更高分辨率的AF4-MALLS分析来确定溶液中寡聚物质的分布,对峰4的物质进行了进一步分析。基于来自AFM分析的图像,假定星状rhSP-D寡聚物的最大分子量为约6MDa。最大分子量用作标称截止值,以区分星状rhSP-D寡聚物与更大聚集物。然而,当将6MDa用作分析中的截止值时,与峰3相关的rhSP-D寡聚物质被包括在聚集测定中。这与在34分钟附近新峰明显开始洗脱不一致。在分析中使用了70nm的基于尺寸的截止值。如通过UV迹线或整体LS迹线看到的,70nm截止值几乎与峰4的开始完全一致。因此,使用70nm截止值是区分rhSP-D寡聚聚集物存在的更准确测量。
确定了峰3和4中每一个的调整的RPA。具体地,确定了峰4中对应于恒定RMS半径为约70nm的星状寡聚物质的RPA的相位(aspects),将这些相位从峰4的RPA中去除,并添加至峰3的RPA中,以提供峰4和峰3的调整的RPA。因此,峰1的RPA、峰2的RPA、峰3的调整的RPA和峰4的调整的RPA分别对应于AF4-MALLS分析中以下rhSP-D寡聚物质的相对分布:(1)三聚体和六聚体;(2)十二聚体;(3)RMS半径为约70nm的星状寡聚物质;和(4)RMS半径大于70nm的聚集物。
对从表达来自整合的转基因的rhSP-D的不同人髓系白血病细胞系获得的三种rhSP-D样品进行了AF4-MALLS分析。表4总结了结果。
表4
如表4所示,rhSP-D样品8B11的峰2的RPA为44.37%,这表明该样品具有三种测试样品中最高相对量的十二聚体。rhSP-D样品8B11的峰4的调整的RPA为1.04%,这表明该样品具有三种测试样品中最低相对量的RMS半径大于70nm的聚集物。
Toll样受体(TLR)在先天免疫系统和适应性免疫系统中均起作用,并且SP-D具有通过TLR(如Toll样受体2(TLR2)和Toll样受体4(TLR4))调节信号传导的活性。参见,如Haagsman HP等人,(2008)Neonatology 93:288-294;Yamazoe M.等人,(2008)J.BiolChem.283:35878-35888;和Vieira F.等人,(2017)Ann Anat 211:184-201,将其各自通过引用以其整体并入。TLR4活性还可调节病况(如支气管肺发育不良(BPD))的严重程度(Malash AH等人,(2016)Gene 592:23-28,将其通过引用以其整体并入)。因此,测量了rhSP-D调节TLR4活性的活性,作为rhSP-D对宿主免疫应答的作用的指示。在LPS-TLR4测定中,测试了含有rhSP-D的复溶制剂的活性。在LPS-TLR4测定中,复溶的rhSP-D可通过阻止LPS结合/激活Toll样受体4(TLR4)来抑制脂多糖(LPS)诱导的炎性细胞应答。参见,如,Yamazoe M.等人,(2008)J.Biol Chem.283:35878-35888。
在LPS-TLR4测定中复溶的rhSP-D的活性以与以下方法基本相似的方法进行测试。将HEK-Blue
表5
如表5所示,rhSP-D样品8B11是唯一在TLR4测定中具有活性的测试细胞克隆样品。值得注意的是,rhSP-D样品8B11是唯一测试的峰2的RPA大于35%的样品。
在细菌聚集测定中测试rhSP-D样品的活性。在细菌聚集测定中,活性rhSP-D聚集细菌细胞,并降低吸光度/增加通过细菌悬液的透射。细菌聚集测定通过与以下方法基本相似的方法进行。简而言之,制备指数大肠杆菌(ATCC:Y1088)培养物,取等分试样,重悬于1mL缓冲液(150mM HEPES,20mM NaCl pH 7.4)中。在光谱仪中于700nm处测量细菌悬液的吸光度,并调节细菌悬液以获得范围为1.0000至1.1000的吸光度。将1M CaCl
(1-abs)*100=%的聚集
其中1=没有rhSP-D的大肠杆菌悬液的测量的吸光度。
Abs=60分钟时大肠杆菌悬液+rhSP-D的吸光度值。
从3个重复中取聚集百分比(%)值的平均,并将其与标准偏差一起导入GraphPadPrism v7.0c,(GraphPad,La Jolla,CA 92037)中。使用四参数逻辑斯谛曲线拟合平均值。测定每个复溶的rhSP-D样品的EC50和跨度的所得值。pEC50是EC50的–Log10。
rhSP-D样品7H8、1C4和8B11各自在细菌聚集测定中具有活性。
进行了多变量统计分析,以确定各种rhSP-D制剂的AF4-MALLS分析中的级分图中观察到的峰与细菌聚集测定或TLR4测定中rhSP-D样品的活性之间的任何相关性。从40多个不同样品中获得的数字化级分图用作数据矩阵,并使用PLS确定与来自TLR4测定的测量的pIC
使用标准技术对所有校准模型进行了完整的交叉验证。参见,如Katz,M.H.“Multivariate Analysis:A Practice Guide for Clinicians.”Cambridge UniversityPress,New York,pp.158-162(1999);Stahle,L.等人,(1988)“Multivariate dataanalysis and experimental design in biomedical research.Prog.Med.Chem.25:291-338;Wold S.(2001)“PLS-regression:a basic tool of chemometrics.”Chemom.Intell.Lab.Syst.58:109-130,将其各自通过引用以其整体并入。简而言之,一次取出一个样品,重新校准数据集,并构建一个新模型。重复该过程,直到所有校准样品均被取出一次并量化为验证模型为止。因此,将含有所有样品的第一集合称为校准集合,并将交叉验证后的一个集合称为验证集合。使用刀切算法(jack-knife algorithm)来确定用于构建偏最小二乘法(PLS)模型的任何因素的统计显著性(Martens,H.等人,(2001)“Multivariate Analysis of Quality:An Introduction”Wiley and Sons,Chichester,UK)。
对于各种rhSP-D制剂,关于在AF4-MALLS分析中观察到的特定峰与细菌聚集测定中的活性之间的相关性,发现大部分活性存在于峰1和2中,一些在整个峰3中持续存在。发现峰4与细菌聚集测定中的活性之间呈负相关。对于各种rhSP-D制剂,关于在AF4-MALLS分析中观察到的特定峰与TLR4测定中的活性之间的相关性,发现该活性几乎完全位于峰2中。因此,TLR4测定中rhSP-D的活性与rhSP-D的十二聚体物质直接相关。因此,AF4-MALLS提供了确定样品比例的方法,所述样品包括在TLR4测定中有活性的十二聚体。值得注意的是,在校正的峰4中发现的半径>70nm的聚集物质与细菌聚集测定或TLR4测定中的活性均无关,证实了这些物质代表了rhSP-D的非活性形式。
本文中所用的术语“包含(comprising)”与“包括(including)”、“含有(containing)”或“特征在于”同义,并且是包括性的或开放性的,并且不排除另外的未叙述的要素或方法步骤。
以上描述公开了本发明的一些方法和材料。本发明容易对方法和材料进行修改,以及改变制造方法和设备。通过考虑本公开内容或本文公开的本发明的实践,此类修改对于本领域技术人员将变得显而易见。因此,无意将本发明限制于本文公开的特定实施方案,而是其涵盖了落入本发明的真实范围和精神内的所有修改和替代。
本文引用的所有参考文献(包括但不限于公开和未公开的申请、专利和文献资料)均通过引用以其整体并入本文,并且在此构成本说明书的一部分。在通过引用并入的出版物和专利或专利申请与说明书中包含的公开内容相矛盾的程度上,本说明书旨在取代和/或优先于任何此类矛盾的材料。
序列表
<110> 简·苏珊·罗森鲍姆(Jan Susan Rosenbaum)
马克·康奈尔·曼宁(Mark Cornell Manning)
瑞恩·R·曼宁(Ryan R. Manning)
<120> 用于表征表面活性剂蛋白D(SP-D)寡聚物的系统和方法
<130> AIRWY.013WO
<150> 62/650138
<151> 2018-03-29
<160> 2
<170> FastSEQ for Windows Version 4.0
<210> 1
<211> 376
<212> PRT
<213> 智人(homo sapiens)
<220>
<223> 人SP-D多肽,其包含前导序列。
在Met 31、Thr 180、Ser 290、Ala 306具有多态性。
<400> 1
Met Leu Leu Phe Leu Leu Ser Ala Leu Val Leu Leu Thr Gln Pro Leu
1 5 10 15
Leu Gly Tyr Leu Glu Ala Glu Met Lys Thr Tyr Ser His Arg Thr Met
20 25 30
Pro Ser Ala Cys Thr Leu Val Met Cys Ser Ser Val Glu Ser Gly Leu
35 40 45
Pro Gly Arg Asp Gly Arg Asp Gly Arg Glu Gly Pro Arg Gly Glu Lys
50 55 60
Gly Asp Pro Gly Leu Pro Gly Ala Ala Gly Gln Ala Gly Met Pro Gly
65 70 75 80
Gln Ala Gly Pro Val Gly Pro Lys Gly Asp Asn Gly Ser Val Gly Glu
85 90 95
Pro Gly Pro Lys Gly Asp Thr Gly Pro Ser Gly Pro Pro Gly Pro Pro
100 105 110
Gly Val Pro Gly Pro Ala Gly Arg Glu Gly Pro Leu Gly Lys Gln Gly
115 120 125
Asn Ile Gly Pro Gln Gly Lys Pro Gly Pro Lys Gly Glu Ala Gly Pro
130 135 140
Lys Gly Glu Val Gly Ala Pro Gly Met Gln Gly Ser Ala Gly Ala Arg
145 150 155 160
Gly Leu Ala Gly Pro Lys Gly Glu Arg Gly Val Pro Gly Glu Arg Gly
165 170 175
Val Pro Gly Asn Thr Gly Ala Ala Gly Ser Ala Gly Ala Met Gly Pro
180 185 190
Gln Gly Ser Pro Gly Ala Arg Gly Pro Pro Gly Leu Lys Gly Asp Lys
195 200 205
Gly Ile Pro Gly Asp Lys Gly Ala Lys Gly Glu Ser Gly Leu Pro Asp
210 215 220
Val Ala Ser Leu Arg Gln Gln Val Glu Ala Leu Gln Gly Gln Val Gln
225 230 235 240
His Leu Gln Ala Ala Phe Ser Gln Tyr Lys Lys Val Glu Leu Phe Pro
245 250 255
Asn Gly Gln Ser Val Gly Glu Lys Ile Phe Lys Thr Ala Gly Phe Val
260 265 270
Lys Pro Phe Thr Glu Ala Gln Leu Leu Cys Thr Gln Ala Gly Gly Gln
275 280 285
Leu Ala Ser Pro Arg Ser Ala Ala Glu Asn Ala Ala Leu Gln Gln Leu
290 295 300
Val Val Ala Lys Asn Glu Ala Ala Phe Leu Ser Met Thr Asp Ser Lys
305 310 315 320
Thr Glu Gly Lys Phe Thr Tyr Pro Thr Gly Glu Ser Leu Val Tyr Ser
325 330 335
Asn Trp Ala Pro Gly Glu Pro Asn Asp Asp Gly Gly Ser Glu Asp Cys
340 345 350
Val Glu Ile Phe Thr Asn Gly Lys Trp Asn Asp Arg Ala Cys Gly Glu
355 360 365
Lys Arg Leu Val Val Cys Glu Phe
370 375
<210> 2
<211> 355
<212> PRT
<213> 智人(homo sapiens)
<220>
<223> SEQ ID NO:01的SP-D多肽,其没有前导序列。
在Met 11、Thr 160、Ser 270、Ala 286具有多态性。
<400> 2
Ala Glu Met Lys Thr Tyr Ser His Arg Thr Met Pro Ser Ala Cys Thr
1 5 10 15
Leu Val Met Cys Ser Ser Val Glu Ser Gly Leu Pro Gly Arg Asp Gly
20 25 30
Arg Asp Gly Arg Glu Gly Pro Arg Gly Glu Lys Gly Asp Pro Gly Leu
35 40 45
Pro Gly Ala Ala Gly Gln Ala Gly Met Pro Gly Gln Ala Gly Pro Val
50 55 60
Gly Pro Lys Gly Asp Asn Gly Ser Val Gly Glu Pro Gly Pro Lys Gly
65 70 75 80
Asp Thr Gly Pro Ser Gly Pro Pro Gly Pro Pro Gly Val Pro Gly Pro
85 90 95
Ala Gly Arg Glu Gly Pro Leu Gly Lys Gln Gly Asn Ile Gly Pro Gln
100 105 110
Gly Lys Pro Gly Pro Lys Gly Glu Ala Gly Pro Lys Gly Glu Val Gly
115 120 125
Ala Pro Gly Met Gln Gly Ser Ala Gly Ala Arg Gly Leu Ala Gly Pro
130 135 140
Lys Gly Glu Arg Gly Val Pro Gly Glu Arg Gly Val Pro Gly Asn Thr
145 150 155 160
Gly Ala Ala Gly Ser Ala Gly Ala Met Gly Pro Gln Gly Ser Pro Gly
165 170 175
Ala Arg Gly Pro Pro Gly Leu Lys Gly Asp Lys Gly Ile Pro Gly Asp
180 185 190
Lys Gly Ala Lys Gly Glu Ser Gly Leu Pro Asp Val Ala Ser Leu Arg
195 200 205
Gln Gln Val Glu Ala Leu Gln Gly Gln Val Gln His Leu Gln Ala Ala
210 215 220
Phe Ser Gln Tyr Lys Lys Val Glu Leu Phe Pro Asn Gly Gln Ser Val
225 230 235 240
Gly Glu Lys Ile Phe Lys Thr Ala Gly Phe Val Lys Pro Phe Thr Glu
245 250 255
Ala Gln Leu Leu Cys Thr Gln Ala Gly Gly Gln Leu Ala Ser Pro Arg
260 265 270
Ser Ala Ala Glu Asn Ala Ala Leu Gln Gln Leu Val Val Ala Lys Asn
275 280 285
Glu Ala Ala Phe Leu Ser Met Thr Asp Ser Lys Thr Glu Gly Lys Phe
290 295 300
Thr Tyr Pro Thr Gly Glu Ser Leu Val Tyr Ser Asn Trp Ala Pro Gly
305 310 315 320
Glu Pro Asn Asp Asp Gly Gly Ser Glu Asp Cys Val Glu Ile Phe Thr
325 330 335
Asn Gly Lys Trp Asn Asp Arg Ala Cys Gly Glu Lys Arg Leu Val Val
340 345 350
Cys Glu Phe
355
- 用于表征表面活性剂蛋白D(SP-D)寡聚物的系统和方法
- 淀粉状蛋白β肽类似物,其寡聚物,用于制备的方法以及包括所述类似物或寡聚物的组合物,及其用途
