一种制备5-HT3受体调节剂的方法
文献发布时间:2024-04-18 19:58:21
技术领域
本发明属于药物合成领域,具体涉及一种制备5-HT
背景技术
肠易激综合征(irritable bowel syndrome,IBS)是一种持续或间歇发作,以腹痛、腹胀、排便习惯和(或)大便性状改变为临床表现,缺乏胃肠道结构和生化异常的肠道功能紊乱性疾病。罗马Ⅲ将其列为功能性肠病的一类,患者以中青年人为主,发病年龄多见于20~50岁,女性较男性多见,有家族聚集倾向,常与其他胃肠道功能紊乱性疾病如功能性消化不良并存伴发。在成人中肠易激综合征的患病率为10%~20%,目前能够有效治疗该疾病的药物还较少。
研究指出,5-羟色胺(5-HT)是胃肠道关键神经递质之一,5-羟色胺3(5-HT
开发出一种具有更高收率的合成(S)-7-(奎宁-3-基)-2,7,8,9-四氢-6H-氮杂环[5,4,3-cd]吲唑-6-酮的方法具有重要意义。
发明内容
本发明的目的在于提供一种制备(S)-7-(奎宁-3-基)-2,7,8,9-四氢-6H-氮杂环[5,4,3-cd]吲唑-6-酮的新方法。
本发明提供了一种合成式I所示化合物的方法,所述方法包括以下步骤:
(1)化合物5与酸反应,得到化合物6;
(2)化合物6与化合物7或其盐反应,得到化合物8;
(3)化合物8与氢氧化锂或其水合物反应,得到化合物9;
(4)化合物9在碱和脱水剂的存在下反应,得到化合物10;
(5)化合物10与脱保护试剂反应,得到式I所示化合物;
R
进一步地,步骤(1)中,所述酸为盐酸,所述化合物5与酸的摩尔比为1:(5-20),所述反应的溶剂为有机溶剂,反应的温度为40-60℃,反应的时间为2-6小时;
步骤(2)中,所述反应是在酸和还原剂的存在下进行的,化合物6、化合物7或其盐、酸、还原剂的摩尔比为1:(1-4):(1-4):(1-4),所述反应的溶剂为有机溶剂,反应的温度为20-40℃,反应的时间为12-22小时;
步骤(3)中,化合物8、氢氧化锂或其水合物的摩尔比为1:(1-4),所述反应的溶剂为水、有机溶剂中的一种或两种的混合,反应的温度为50-90℃,反应的时间为0.5-3小时;
步骤(4)中,化合物9与碱的质量比为1:(1-3),碱与脱水剂的摩尔比为(1-3):1,所述碱为有机碱,所述脱水剂为1-丙基磷酸酐,所述反应的溶剂为有机溶剂,反应的温度为20-40℃,反应的时间为6-20小时;
步骤(5)中,所述脱保护试剂为三氟乙酸,化合物10与三氟乙酸的质量体积比为50-70mg/mL,反应的溶剂为有机溶剂,反应的温度为60-100℃,反应的时间为6-20小时。
进一步地,步骤(1)中,所述盐酸的浓度为5-7mol/L,所述化合物5与酸的摩尔比为1:12,所述有机溶剂为四氢呋喃,所述反应的温度为50℃,反应的时间为4小时;
步骤(2)中,所述还原剂为三乙酰氧基硼氢化钠,化合物7的盐为化合物7的二盐酸盐,化合物6、化合物7或其盐、酸、还原剂的摩尔比为1:2:1:2,所述有机溶剂为乙腈,所述反应的温度为室温,反应的时间为16-18小时;
步骤(3)中,化合物8、氢氧化锂或其水合物的摩尔比为1:2,氢氧化锂的水合物为一水氢氧化锂,所述反应的溶剂为甲醇、水中的一种或两种的混合,所述反应的温度为70℃,反应的时间为1小时;
步骤(4)中,化合物9与碱的质量比为1:1.5,碱与脱水剂的摩尔比为1.6:1,所述有机碱为N,N-二异丙基乙胺,所述有机溶剂为四氢呋喃、乙酸乙酯中的一种或两种的混合,所述反应的温度为室温,反应的时间为8-12小时;
步骤(5)中,化合物10与三氟乙酸的质量体积比为62.5mg/mL,所述有机溶剂为苯甲醚,反应的温度为80℃,反应的时间为8-12小时。
进一步地,步骤(1)中,反应结束后还包括以下纯化步骤:将反应液加入冰水中,用饱和碳酸氢钠水溶液调节pH至9-11,乙酸乙酯萃取,保留有机相,干燥,得到化合物6;
步骤(2)中,反应结束后还包括以下纯化步骤:将反应液加入冰水中,二氯甲烷萃取,取水相用饱和碳酸氢钠水溶液调节pH至9-11,用二氯甲烷萃取,保留有机相,干燥,得到化合物8;
步骤(4)中,反应结束后还包括以下纯化步骤:将反应液加入水中,二氯甲烷萃取,保留有机相,干燥,得到化合物10;
步骤(5)中,反应结束后还包括以下纯化步骤:在反应液中加入盐酸,用甲基叔丁基醚萃取,取水相调节pH至9-11,用二氯甲烷溶液萃取,保留有机相,干燥,得到式I所示化合物。
进一步地,所述化合物5的制备方法包括以下步骤:化合物3与化合物4反应,得到化合物5;
R
进一步地,所述反应是在钯催化剂和相转移催化剂的存在下进行的,化合物3、化合物4、钯催化剂和相转移催化剂的摩尔比为1:(1-3):(0.01-0.1):(1-3),反应的溶剂为水、有机溶剂中的一种或两种的混合,反应的温度40-60℃,反应的时间为12-20h。
进一步地,所述钯催化剂为二氯二叔丁基-(4-二甲基氨基苯基)磷钯(II),相转移催化剂为碳酸铯,化合物3、化合物4、钯催化剂和相转移催化剂的摩尔比为1:1.5:0.05:2,反应的溶剂为水、1,4-二氧六环中的一种或两种的混合,反应的温度50℃,反应的时间为16h;
优选地,反应结束后还包括以下纯化步骤:将反应液浓缩后经过柱层析,得到化合物5;所述柱层析的洗脱剂为石油醚与乙酸乙酯的混合溶剂,石油醚与乙酸乙酯的体积比为6:1。
进一步地,所述化合物3的制备方法包括以下步骤:
(a)化合物1与卤代试剂反应,得到化合物2;
(b)化合物2与氨基保护剂反应,得到化合物3;
X为卤素,R
进一步地,步骤(a)中,所述卤代试剂为溴代试剂,所述反应是在碱的存在下进行的;化合物1、溴代试剂、碱的摩尔比为1:(0.8-1.2):(2-6),反应的溶剂为有机溶剂,反应的温度为20-40℃,反应的时间为0.5-3小时;
步骤(b)中,所述氨基保护试剂为对甲氧基苄氯,化合物2与对甲氧基苄氯的质量体积比为0.1-0.5g/mL,反应的温度为40-60℃,反应的时间为5-9小时;
X为溴,R
进一步地,步骤(a)中,所述溴代试剂为N-溴代丁二酰亚胺,所述碱为无机碱,优选为氢氧化钾;化合物1、溴代试剂、碱的摩尔比为1:1:4,所述有机溶剂为N,N-二甲基甲酰胺,反应的温度为室温,反应的时间为1小时;
优选地,步骤(a)反应结束后还包括以下纯化步骤:将反应液浓缩过滤,滤液加入冰水中,乙酸乙酯萃取,保留有机相用饱和食盐水洗涤,干燥,得到化合物2;
步骤(b)中,化合物2与对甲氧基苄氯的质量体积比为0.2g/mL,反应的温度为50℃,反应的时间为7小时;
优选地,步骤(b)反应结束后还包括以下纯化步骤:将反应液加入石油醚,搅拌后过滤,滤饼用石油醚洗涤,干燥,得到化合物3。
本发明中,室温指25±5℃。
本发明提供了一种制备(S)-7-(奎宁-3-基)-2,7,8,9-四氢-6H-氮杂环[5,4,3-cd]吲唑-6-酮的新方法。本发明的方法原料易得,反应条件温和,总收率高达45.1%,产物纯度高达97%,适合工业化生产。
显然,根据本发明的上述内容,按照本领域的普通技术知识和惯用手段,在不脱离本发明上述基本技术思想前提下,还可以做出其它多种形式的修改、替换或变更。
以下通过实施例形式的具体实施方式,对本发明的上述内容再作进一步的详细说明。但不应将此理解为本发明上述主题的范围仅限于以下的实例。凡基于本发明上述内容所实现的技术均属于本发明的范围。
附图说明
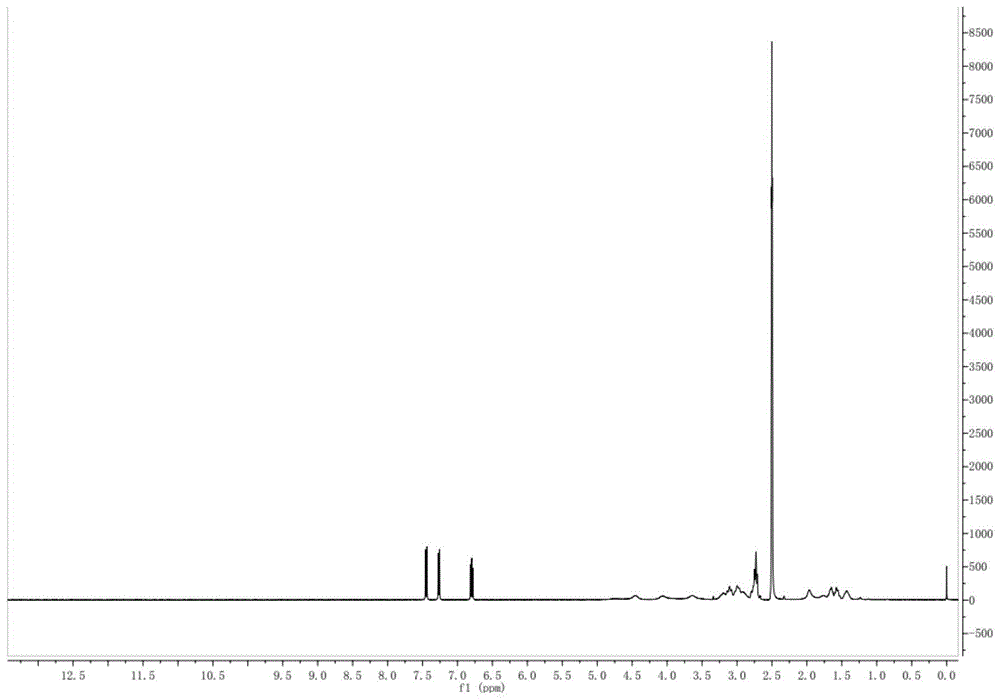
图1:实施例1所得(S)-7-(奎宁-3-基)-2,7,8,9-四氢-6H-氮杂环[5,4,3-cd]吲唑-6-酮的核磁谱图。
具体实施方式
本发明所用原料与设备均为已知产品,通过购买市售产品所得。
实施例1、(S)-7-(奎宁-3-基)-2,7,8,9-四氢-6H-氮杂环[5,4,3-cd]吲唑-6-酮的制备
第一步:3-溴-1H-吲唑-4-羧酸甲酯的制备
将1H-吲唑-4-羧酸甲酯(45.0g,255.6mmol)溶于干燥的N,N-二甲基甲酰胺(0.9L)中,加入氢氧化钾(57.0g,1022.7mmol),搅拌下将N-溴代丁二酰亚胺(简称NBS,45.5g,255.7mmol)分批加入反应体系中,室温反应1h。反应结束后减压过滤除去残余的氢氧化钾,滤液倒入3L冰水中,乙酸乙酯萃取,合并有机相,有机相用饱和食盐水洗涤,无水硫酸钠干燥,减压浓缩得黄色固体3-溴-1H-吲唑-4-羧酸甲酯(59.8g,收率为92.4%)。
MS m/z(ESI):255.0,257.0[M+H]
1
第二步:3-溴-2-(4-甲氧基苄基)-2H-吲唑-4-羧酸甲酯盐酸盐的制备
将3-溴-1H-吲唑-4-羧酸甲酯(30.0g,117.6mmol)加入到对甲氧基苄氯(简称PMB-Cl,150mL)中,50℃反应7h。反应结束后待冷却至室温,体系加入到1L石油醚,搅拌1h,减压过滤,滤饼用0.4L石油醚洗涤,烘干得白色固体3-溴-2-(4-甲氧基苄基)-2H-吲唑-4-羧酸甲酯盐酸盐(39.7g,收率为82%)。
MS m/z(ESI):374.0,376.0[M+H]
1
第三步:甲基(E)-3-(2-乙氧基乙烯基)-2-(4-甲氧基苄基)-2H-吲唑-4-羧酸酯的制备
将3-溴-2-(4-甲氧基苄基)-2H-吲唑-4-羧酸甲酯盐酸盐(5.5g,13.3mmol),(E)-2-(2-乙氧基乙烯基)-4,4,5,5-四甲基-1,3,2-二氧杂环戊烷(4.0g,20.0mmol),二氯二叔丁基-(4-二甲基氨基苯基)磷钯(II)(0.5g,0.7mmol),碳酸铯(简称Cs
MS m/z(ESI):367.2[M+H]
1
第四步:2-(4-甲氧基苄基)-3-(2-氧乙基)-2H-吲唑-4-羧酸甲酯的制备
将甲基(E)-3-(2-乙氧基乙烯基)-2-(4-甲氧基苄基)-2H-吲唑-4-羧酸酯(3.7g,10.1mmol),四氢呋喃(40mL),盐酸(20mL,6N)加入到100mL单瓶中,50℃反应4h。反应结束后待冷却至室温,体系倒入冰水中,用饱和碳酸氢钠水溶液调节pH=8,乙酸乙酯萃取三次,合并有机相,有机相用饱和食盐水洗涤,无水硫酸钠干燥,过滤,滤液减压浓缩得白色固体2-(4-甲氧基苄基)-3-(2-氧乙基)-2H-吲唑-4-羧酸甲酯(3.1g,收率为90.6%)。
MS m/z(ESI):339.1[M+H]
1
第五步:甲基(S)-2-(4-甲氧基苄基)-3-(2-(奎宁-3-基氨基)乙基)-2H-吲唑-4-羧酸酯的制备
向装有化合物2-(4-甲氧基苄基)-3-(2-氧乙基)-2H-吲唑-4-羧酸甲酯(310.0mg,0.92mmol)和S-3-氨基奎宁环二盐酸盐(360.0mg,1.84mmol)的乙腈(6mL)溶液中加入冰乙酸(60.0mg,1mmol),室温搅拌16小时。然后向反应液中加入三乙酰氧基硼氢化钠(390.0mg,1.84mmol),室温搅拌。反应结束后将反应液倒入水中,用二氯甲烷萃取一次,水相用饱和碳酸氢钠水溶液调节pH=8,用二氯甲烷萃取两次,合并有机相,有机相用无水硫酸钠干燥,过滤,减压浓缩得油状物甲基(S)-2-(4-甲氧基苄基)-3-(2-(奎宁-3-基氨基)乙基)-2H-吲唑-4-羧酸酯(374.0mg,收率为91.4%)。
MS m/z(ESI):449.2[M+H]
第六步:锂(S)-2-(4-甲氧基苄基)-3-(2-(奎宁-3-基氨基)乙基)-2H-吲唑-4-羧酸盐的制备
向装有化合物甲基(S)-2-(4-甲氧基苄基)-3-(2-(奎宁-3-基氨基)乙基)-2H-吲唑-4-羧酸酯(310.0mg,0.7mmol)的甲醇(5mL)溶液中加入一水氢氧化锂(58.0mg,1.4mmol)的水(1mL)溶液,70℃反应1h。反应结束后待冷却至室温,减压浓缩得锂(S)-2-(4-甲氧基苄基)-3-(2-(奎宁-3-基氨基)乙基)-2H-吲唑-4-羧酸盐(粗品),未进一步纯化直接用于下一步。
MS m/z(ESI):435.2[M+H]
第七步:(S)-2-(4-甲氧基苄基)-7-(奎宁-3-基)-2,7,8,9-四氢-6H-氮杂环[5,4,3-cd]吲唑-6-酮的制备
向装有化合物锂(S)-2-(4-甲氧基苄基)-3-(2-(奎宁-3-基氨基)乙基)-2H-吲唑-4-羧酸盐(320.0mg,粗品)和N,N-二异丙基乙胺(简称DIEA,469.0mg,3.6mmol)的四氢呋喃(6mL)溶液中加入1-丙基磷酸酐(浓度为50wt%的乙酸乙酯溶液)(简称T
MS m/z(ESI):417.2[M+H]
第八步:(S)-7-(奎宁-3-基)-2,7,8,9-四氢-6H-氮杂环[5,4,3-cd]吲唑-6-酮的制备
将化合物(S)-2-(4-甲氧基苄基)-7-(奎宁-3-基)-2,7,8,9-四氢-6H-氮杂环[5,4,3-cd]吲唑-6-酮(250mg,粗品),三氟乙酸(4mL),苯甲醚(1mL)混合,加热至80℃反应过夜。反应结束后待冷却至室温,加入50mL盐酸(1M),用甲基叔丁基醚萃取两次,水相用氢氧化钠(6M)水溶液调节至pH=10,用二氯甲烷溶液萃取两次。合并有机相,无水硫酸钠干燥,过滤,减压浓缩得(S)-7-(奎宁-3-基)-2,7,8,9-四氢-6H-氮杂环[5,4,3-cd]吲唑-6-酮(156.0mg,收率为87.6%,HPLC纯度为97%)。
MS m/z(ESI):297.2[M+H]
1
本发明实施例1制备(S)-7-(奎宁-3-基)-2,7,8,9-四氢-6H-氮杂环[5,4,3-cd]吲唑-6-酮的总收率高达45.1%。
综上,本发明提供了一种制备式I所述5-HT
- 一种酯醚交联型聚羧酸系和易性调节剂及其制备方法
- 一种含大量微矿元素的无菌土壤调节剂及其制备方法
- 一种农作物体内的碳氮比调节剂及其制备方法
- 一种适用于铁皮石斛培养再生的植物调节剂及其制备方法
- 一种混凝土增粘型粘度调节剂及其制备方法
- 一种含氮杂环类5-HT3受体调节剂及其制备方法和用途
- 一种含氮杂环类5-HT3受体调节剂及其制备方法和用途
