一种医用酵母重组Ⅲ型胶原蛋白敷料的制备方法
文献发布时间:2023-06-19 13:48:08
技术领域
本发明涉及医药技术领域,具体而言,涉及一种医用酵母重组Ⅲ型胶原蛋白敷料的制备方法。
背景技术
皮肤是人体重要的组织器官,完整的皮肤屏障可以保护人体面受外源性物质的侵害。当皮肤损伤时,机体会迅速启动愈合机制,减少次生危害的发生。伤口愈合是一个复杂的过程,完全愈合的时间与患者的年龄和健康状况有关,也受到伤口感染等外部因素的影响。皮肤创伤会导致患者生活质量下降,严重时会危害人体健康,所以伤口愈合问题是一个值得关注的社会问题。人们通常适用敷料来辅助伤口或创面的愈合,敷料的基本材料主要包括天然高分子材料和合成高分子材料。天然高分子材料主要有胶原、明胶、壳聚糖、淀粉、硫酸软骨素海藻酸等,合成高分子材料主要有聚乙二醇、聚氨酯、聚乙烯吡咯烷酮等。相对于合成高分子材料具有良好的机械性能、加工性能及化学稳
定性等特点,天然高分子材料则具有良好的生物相容性和可降解性,在组织工程与再生医学领域得到广泛的应用。胶原蛋白(也称胶原)是动物体中含量最丰富的一类蛋白质家族。胶原蛋白具有很强的生物活性及生物功能,能参与细胞的迁移、分化和繁殖,使结缔组织具有机械强度,同时胶原蛋白还能促进细胞生长,具有止血、生物相容性和生物降解性能。基于这些特性,胶原蛋白在烧伤、创伤、眼角膜疾病、保健、美容、矫形、硬组织修复、创面止血、药物传递、缓释技术等医药卫生领域有着广泛的应用。另外,胶原蛋白也可作为食品添加剂、饲料添加剂、絮凝剂、照相乳胶材料、表面活性剂和固定化酶载体材料等应用于各个工业和实验室领域。医用敷料的使用在促进创面愈合与皮肤修复必不可少;与传统敷料相比,新型生物敷料能够促进创面愈合,具有独特的功能优势,胶原蛋白敷料已经成为辅助伤口或创面愈合的首选产品之一,现有的医用胶原蛋白敷料仍然处于初始阶段,其在功能效用上还不够完善,仍具有较大的提升空间。
发明内容
本发明在于提供一种医用酵母重组Ⅲ型胶原蛋白敷料的制备方法,其能够缓解上述问题。
为了缓解上述的问题,本发明采取的技术方案如下:
本发明提供了一种医用酵母重组Ⅲ型胶原蛋白敷料的制备方法,所述酵母重组Ⅲ型胶原蛋白敷料按重量份数比计包括3份酵母重组Ⅲ型胶原蛋白、5份甘油、4份卡波姆以及88份纯化水;所述酵母重组Ⅲ型胶原蛋白敷料的制备方法包括:将酵母重组Ⅲ型胶原蛋白、甘油、卡波姆以及纯化水混合搅拌至完全溶解,调节PH至5~7.5,得到敷料原液;对敷料原液进行过滤处理,之后注入片状成型模具中,基于快速冷冻成型技术制备得到敷料冷冻品;将敷料冷冻品干燥、脱模后得到片状的医用酵母重组Ⅲ型胶原蛋白敷料。
在本发明的一较佳实施方式中,所述酵母重组Ⅲ型胶原蛋白、甘油、卡波姆以及纯化水混合搅拌时的温度保持在35~45℃。
在本发明的一较佳实施方式中,混合所述酵母重组Ⅲ型胶原蛋白、甘油、卡波姆以及纯化水的容器,为带有刻度线的透明容器。
在本发明的一较佳实施方式中,所述片状成型模具包括顶面缺失的长方形盒体,以及覆盖于所述长方形盒体内壁的塑料薄膜,所述塑料薄膜的边缘部延伸至所述长方形盒体外部。
在本发明的一较佳实施方式中,制备所述医用酵母重组Ⅲ型胶原蛋白敷料的整个过程均在无菌环境下进行。
在本发明的一较佳实施方式中,所述酵母重组Ⅲ型胶原蛋白由具有表达出重组III型胶原蛋白能力的重组酵母菌发酵得到。
与现有技术相比,本发明的有益效果是:方法简单,选用了酵母重组Ⅲ型胶原蛋白、甘油、卡波姆以及纯化水混合生产敷料,各组分所占比例合理,最终所得到的医用酵母重组Ⅲ型胶原蛋白敷料产品为片状,便于使用,基于快速冷冻成型技术进行生产,生产效率非常高,所得到的敷料产品能有效的抑制和缓解皮炎、敏感性肌肤、痤疮、激光治疗后等各种原因引起的皮肤炎症反应,促进创面愈合与皮肤修复,缩短病程,减轻炎症后色素沉着与瘢痕形成的风险,并对上述疾病具有一定的辅助治疗作用,产品安全,有效。
为使本发明的上述目的、特征和优点能更明显易懂,下文特举本发明实施例,并配合所附附图,作详细说明如下。
附图说明
为了更清楚地说明本发明实施例的技术方案,下面将对实施例中所需要使用的附图作简单地介绍,应当理解,以下附图仅示出了本发明的某些实施例,因此不应被看作是对范围的限定,对于本领域普通技术人员来讲,在不付出创造性劳动的前提下,还可以根据这些附图获得其他相关的附图。
图1是本发明实施例中片状成型模具的结构示意图;
图2是本发明实施例中不同时间点,肉眼观察大鼠皮损的恢复情况照片;
图3是本发明实施例中不同时间点大鼠皮损 HE 切片染色结果照片。
具体实施方式
为使本发明实施例的目的、技术方案和优点更加清楚,下面将结合本发明实施例中的附图,对本发明实施例中的技术方案进行清楚、完整地描述,显然,所描述的实施例是本发明一部分实施例,而不是全部的实施例。通常在此处附图中描述和示出的本发明实施例的组件可以以各种不同的配置来布置和设计。
因此,以下对在附图中提供的本发明的实施例的详细描述并非旨在限制要求保护的本发明的范围,而是仅仅表示本发明的选定实施例。基于本发明中的实施例,本领域普通技术人员在没有作出创造性劳动前提下所获得的所有其他实施例,都属于本发明保护的范围。
实施例
本发明实施例提供了一种医用酵母重组Ⅲ型胶原蛋白敷料的制备方法,该制备过程均无菌环境下进行,包括:
1)将3份酵母重组Ⅲ型胶原蛋白、5份甘油、4份卡波姆以及88份纯化水混合搅拌至完全溶解,调节PH至5~7.5,得到敷料原液。
其中,酵母重组Ⅲ型胶原蛋白、甘油、卡波姆以及纯化水混合搅拌时的温度保持在40℃。混合酵母重组Ⅲ型胶原蛋白、甘油、卡波姆以及纯化水的容器,为带有刻度线的透明容器,便于观察搅拌情况。
在本发明实施例中,敷料原液的PH调节至6.8。
在本发明实施例中,酵母重组Ⅲ型胶原蛋白由具有表达出重组III型胶原蛋白能力的重组酵母菌发酵得到。
2)对敷料原液进行过滤处理,之后注入片状成型模具中,基于快速冷冻成型技术制备得到敷料冷冻品。
其中,如图1所示,片状成型模具包括顶面缺失的长方形盒体,以及覆盖于长方形盒体内壁的塑料薄膜,塑料薄膜的边缘部延伸至长方形盒体外部,该结构的模块脱模操作非常方便,根据最终需制备的片状敷料厚度,可选用内深度匹配的长方形盒体。
3)将敷料冷冻品干燥、脱模后得到片状的医用酵母重组Ⅲ型胶原蛋白敷料。
其中,干燥过程可在一通风环境中进行,例如采用无菌风扇吹风。为了加速干燥过程中,可将吹向敷料冷冻品的风温保持在42°。
脱模过程中,只需要将夹住塑料薄膜边缘部将片状的医用酵母重组Ⅲ型胶原蛋白敷料从长方形盒体中撕出即可。塑料薄膜可与片状的医用酵母重组Ⅲ型胶原蛋白敷料分离,也可不分离。较佳的是,所采用的塑料薄膜可带有若干透气孔。
为了证明采用本制备方法制备得到的产品的有效性,将上述实施例制备得到的片状医用酵母重组Ⅲ型胶原蛋白敷料进行如下有效性实验;
1、皮肤刺激实验
取雌雄兔各1只,雌性无孕,皮肤健康无损伤,3~4个月龄,室温 17~25℃。在试验前 4~24 h,将兔背部脊柱两侧背毛去除约10.0 cm×15.0 cm 作为实验和观察部位。裁剪2.5 cm×2.5 cm 的医用酵母重组Ⅲ型胶原蛋白敷料覆盖操作部位,然后用绷带固定至少4h,取下医用酵母重组Ⅲ型胶原蛋白敷料后用持久性墨水对接触性部位进行标记,并用温水除去残留实验材料。取下医用酵母重组Ⅲ型胶原蛋白敷料后 1、24、48、72 h 各时间点记录贴敷部位红斑与水肿情况。根据 GB/T16886.10- 2005 进行计分,无红斑至严重红斑:0~4分;无水肿至重度水肿:0~4 分。
实验结果:实验部位观察数据包括红斑和水肿2个记分项目。当采用空白对照时,计算出对照组原发性刺激记分,将实验材料原发性刺激记分减去该记分,即得出原发性刺激记分。该值即为原发性刺激指数。本实验最终结果:实验组和对照组在除去医用酵母重组Ⅲ型胶原蛋白敷料后 1、24、48、72 h 时,均无水肿或红斑发生,计分为 0,证明产品对皮肤无刺激。
2、迟发性致敏试验
取白色健康豚鼠 20 只,雌雄各半,雌性无孕,体质量 300~500 g,7~8 周龄;取适量医用酵母重组Ⅲ型胶原蛋白敷料裁剪成 2.5 cm×2.5 cm 大小,备用。在实验前脱除豚鼠背部脊柱两侧被毛,作为试验和观察部位。将裁剪后的样品,局部贴敷于每只动物的左上背部。6 h 后除去固定器、封闭包扎带和医用酵母重组Ⅲ型胶原蛋白敷料。1 周中连续 3d 重复该步骤,同法操作3周。最后一次诱导贴敷后(14±1) d 用医用酵母重组Ⅲ型胶原蛋白敷料对全部动物进行激发,即将合适大小的敷料样品单独局部贴敷于每只动物去毛的未试部位。6 h 后除去固定器、封闭包扎带和敷料。首次激发后或再次激发接触后(24±2)h进行观察。观察前剃去激发部位及其周围部位的动物被毛,用温水彻底清洗脱毛区,并用毛巾擦干动物后放回笼中。脱毛后至少 2 h,对试验部位进行评分,并在去除激发敷贴片后(48±2)h 再进行评分。按 Magnusson 和Kligman分级标准(GB/T 16886.5- 2003)进行评分:0 级为无明显改变;1 级为散发性或斑点状红斑;2 级为中度融合性红斑;3 级为重度红斑和水肿。
实验结果:对照组动物评分等级<1,而实验组中等级≥1 时,一般提示致敏。如对照组动物等级≥1 时,实验动物反应超过对照动物中最严重的反应则认为致敏。实验组与对照组 Magnusson 和Kligman分级均为0级,说明该产品不会引起皮肤致敏反应,可安全使用。
3、动物实验有效性
取健康 SD 大鼠 8 只,雌雄各半,雌性无孕,体质量180~200 g,月龄 2~3 个月。在实验前脱除大鼠背部脊柱两侧被毛作为实验部位。用胶带对大鼠脱毛部位进行反复粘贴,待明显发红后,采用 0.5 mm 滚针进行循环穿刺,保证表皮深层的损伤,模拟皮损模型。分别采用医用酵母重组Ⅲ型胶原蛋白敷料(实验组)、生理盐水纱布(对照组)及未处理组(空白组)对 3 组动物皮损处进行贴敷,20 min/ 次,间隔 12 h 一次,连续 48 h;然后观察恢复效果,并观察1周后有无不良反应发生。
实验结果:
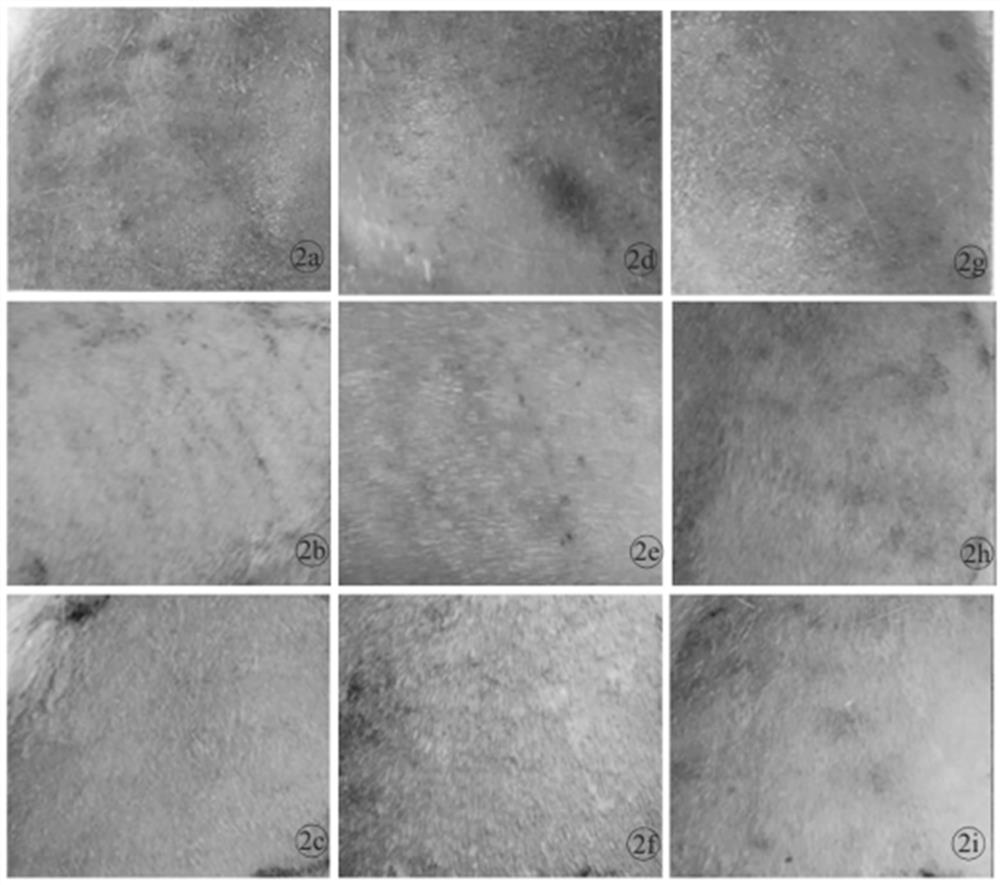
外观观察,建立模型后,3 组皮损部位均红肿明显,表皮及浅层真皮破损。24 h后,实验组和对照组皮损面改善明显,空白组略有自愈,红肿肉眼可见;48 h 后,实验组红肿基本消失,无皮损现象,对照组略有红肿及皮损现象,空白组红肿、皮损较为明显,如图2所示,其中,a.实验组即刻;b.实验组24 h; c.实验组48 h ;d.对照组即刻;e.对照组24 h;f.对照组48 h ;g.空白组即刻;h.空白组24 h ;i.空白组48 h。间隔1周后对实验组及对照组分别剃毛后进一步跟踪观察,皮损、伤口等均完全恢复,无炎症或其他不良反应。
组织学观察,模型建立后即刻进行HE取材切片观察,3组大鼠的皮肤表皮层损伤明显,真皮层无明显损伤;24 h 后,实验组与对照组表皮层有所修复,实验组效果较优,空白组缺损依然较为严重;48 h后,实验组HE结果显示,皮肤结构完整,而且较对照组相对完整,褶皱较为明显,空白组表皮结构未完全恢复,见图3所示,其中,a.实验组即刻;b.实验组24h; c.实验组48 h ;d.对照组即刻;e.对照组24 h;f.对照组48 h ;g.空白组即刻;h.空白组24 h ;i.空白组48 h。
从图2、图3中可以看出,实验组的皮损、伤口等恢复情况极好,即说明了医用酵母重组Ⅲ型胶原蛋白敷料对皮损、伤口的有效治愈性。
以上所述仅为本发明的优选实施例而已,并不用于限制本发明,对于本领域的技术人员来说,本发明可以有各种更改和变化。凡在本发明的精神和原则之内,所作的任何修改、等同替换、改进等,均应包含在本发明的保护范围之内。
- 一种医用酵母重组Ⅲ型胶原蛋白敷料的制备方法
- 一种含有重组人源胶原蛋白的医用敷料及制备方法
