格林森分级预测方法、装置、计算机设备和存储介质
文献发布时间:2024-04-18 19:59:31
技术领域
本申请涉及图像处理技术领域,特别是涉及一种格林森分级预测方法、装置、计算机设备、计算机可读存储介质和计算机程序产品。
背景技术
目前,前列腺癌已成为男性癌症死亡的第二大原因,分别占癌症发病率和死亡率的7.1%和3.8%。前列腺癌虽然常见,但往往不具备侵蚀性,因此医生很难确定癌症是否对患者构成足够大的风险。格林森分级是一种被广泛采用的前列腺癌组织学分级的方法,由于格林森分级与生物学行为和预后关联良好,逐渐得到承认,使用日渐广泛,成为制定前列腺癌治疗方案的重要参考指标。
现有技术中,由经验丰富的病理专家利用显微镜对比前列腺病理组织细胞的形态与正常细胞组织的形态的相似度,从而确定前列腺病理组织的格林森分级。然而前列腺病理组织的格林森分级工作量大,依靠病理专家人工进行观察耗时过长,导致现有技术中存在前列腺病理组织的格林森分级效率太低的问题。
发明内容
基于此,有必要针对上述技术问题,提供一种格林森分级预测方法、装置、计算机设备、计算机可读存储介质和计算机程序产品,以解决相关技术中存在的前列腺病理组织的格林森分级效率太低的问题。
第一个方面,本申请实施例了一种格林森分级预测方法,用于预测前列腺病理图像的格林森分级,所述方法包括以下步骤:
对待预测前列腺病理图像进行划分得到若干第一patch图像,组成待预测patch图像集;
对所述待预测前列腺病理图像进行缩放,得到与所述待预测patch图像集中的每个所述第一patch图像中心点相同、尺寸相同、且分辨率不同的图像,作为所述第一patch图像关联的第一图像对;
将所述待预测patch图像集中的每个所述第一patch图像及其关联的第一图像对,输入到训练完备的多分辨率分割网络模型,得到每个所述第一patch图像的格林森分级的预测结果;所述多分辨率分割网络模型用于对所述第一patch图像及其关联的所述第一图像对进行信息融合,得到所述第一patch图像的格林森分级;
将所述待预测patch图像集中的所有所述第一patch图像的格林森分级的预测结果进行拼接,得到所述待预测前列腺病理图像的格林森分级的预测结果。
在其中一个实施例中,在所述将所述待预测patch图像集中的每个所述第一patch图像及其关联的第一图像对,输入到训练完备的多分辨率分割网络模型之前,所述方法还包括:
从对待训练前列腺病理图像进行划分得到的若干第二patch图像中,筛选出标注区域大小满足预设要求的所述第二patch图像,并将标注区域大小满足所述预设要求的所述第二patch图像作为所述多分辨率分割网络模型的样本源;
遍历所有预设分辨率,按所述预设分辨率对所述待训练前列腺病理图像进行缩放,得到与所述样本源中的所述第二patch图像中心点相同、尺寸相同、且分辨率不同的图像,作为所述第二patch图像关联的第二图像对;
对所述样本源中的所述第二patch图像及其关联的所述第二图像对进行训练,生成所述多分辨率分割网络模型。
在其中一个实施例中,在所述从对待训练前列腺病理图像进行划分得到的若干第二patch图像中,筛选出标注区域大小满足预设要求的所述第二patch图像之前,所述方法还包括:
根据所述待训练前列腺病理图像的标签,确定所述待训练前列腺病理图像的标注区域所在位置以及所述标注区域的被标注等级。
在其中一个实施例中,所述对待预测前列腺病理图像进行划分得到若干第一patch图像,组成待预测patch图像集,包括以下步骤:
对所述待预测前列腺病理图像进行划分得到若干第一patch图像,从中筛选出存在组织区域的所述第一patch图像,组成所述待预测patch图像集。
在其中一个实施例中,在所述对待预测前列腺病理图像进行划分得到若干第一patch图像之前,所述方法还包括:
利用大津法对所述待预测前列腺病理图像进行组织区域检测,确定所述待预测前列腺病理图像的组织区域所在位置。
在其中一个实施例中,所述方法还包括:
采用混合损失函数训练所述多分辨率分割网络模型。
第二个方面,本申请实施例了一种格林森分级预测装置,所述装置包括划分模块、获取模块、计算模块和拼接模块;
所述划分模块,用于对待预测前列腺病理图像进行划分得到若干第一patch图像,组成待预测patch图像集;
所述获取模块,用于对所述待预测前列腺病理图像进行缩放,得到与所述待预测patch图像集中的每个所述第一patch图像中心点相同、尺寸相同、且分辨率不同的图像,作为所述第一patch图像关联的第一图像对;
所述计算模块,用于将所述待预测patch图像集中的每个所述第一patch图像及其关联的第一图像对,输入到训练完备的多分辨率分割网络模型,得到每个所述第一patch图像的格林森分级的预测结果;所述多分辨率分割网络模型用于对所述第一patch图像及其关联的所述第一图像对进行信息融合,得到所述第一patch图像的格林森分级;
所述拼接模块,用于将所述待预测patch图像集中的所有所述第一patch图像的格林森分级的预测结果进行拼接,得到所述待预测前列腺病理图像的格林森分级的预测结果。
第三个方面,在本实施例中提供了一种计算机设备,包括存储器、处理器及存储在存储器上并可在处理器上运行的计算机程序,所述处理器执行所述计算机程序时实现上述第一个方面所述方法的步骤。
第四个方面,在本实施例中提供了计算机可读存储介质,其上存储有计算机程序,所述计算机程序被处理器执行时实现上述第一个方面所述的方法的步骤。
第五个方面,本申请还提供了一种计算机程序产品。所述计算机程序产品,包括计算机程序,该计算机程序被处理器执行时实现上述第一个方面所述的方法的步骤。
上述格林森分级预测方法、装置、计算机设备、计算机可读存储介质和计算机程序产品,通过将待预测前列腺病理图像进行划分得到的若干第一patch图像及与第一patch图像存在上下文关联的第一图像对,输入到训练完备的多分辨率分割网络模型,实现对第一patch图像的格林森分级进行预测,之后将第一patch图像的格林森分级的预测结果进行拼接,得到待预测前列腺病理图像的格林森分级的预测结果,基于深度学习模型来预测前列腺病理图像的格林森分级,有效提高前列腺病理组织的格林森分级效率。
附图说明
此处所说明的附图用来提供对本申请的进一步理解,构成本申请的一部分,本申请的示意性实施例及其说明用于解释本申请,并不构成对本申请的不当限定。在附图中:
图1是根据本申请实施例提供的格林森分级预测方法的应用场景图;
图2是根据本申请实施例提供的格林森分级预测方法的流程图;
图3a是根据本申请实施例提供的格林森分级预测方法中第一patch图像的示意图;
图3b根据本申请实施例提供的格林森分级预测方法中与第一patch图像中心点相同、尺寸相同、且分辨率不同的图像的示意图一;
图3c根据本申请实施例提供的格林森分级预测方法中与第一patch图像中心点相同、尺寸相同、且分辨率不同的图像的示意图二;
图3d根据本申请实施例提供的格林森分级预测方法中与第一patch图像中心点相同、尺寸相同、且分辨率不同的图像的示意图三;
图4是根据本申请实施例提供的格林森分级预测方法中多分辨率分割网络模型的示意图;
图5根据本申请实施例提供的格林森分级预测装置的结构示意图;
图6根据本申请实施例提供的计算机设备的结构示意图。
具体实施方式
为了使本申请的目的、技术方案及优点更加清楚明白,以下结合附图及实施例,对本申请进行描述和说明。应当理解,此处所描述的具体实施例仅仅用以解释本申请,并不用于限定本申请。基于本申请提供的实施例,本领域普通技术人员在没有作出创造性劳动的前提下所获得的所有其他实施例,都属于本申请保护的范围。
显而易见地,下面描述中的附图仅仅是本申请的一些示例或实施例,对于本领域的普通技术人员而言,在不付出创造性劳动的前提下,还可以根据这些附图将本申请应用于其他类似情景。此外,还可以理解的是,虽然这种开发过程中所作出的努力可能是复杂并且冗长的,然而对于与本申请公开的内容相关的本领域的普通技术人员而言,在本申请揭露的技术内容的基础上进行的一些设计,制造或者生产等变更只是常规的技术手段,不应当理解为本申请公开的内容不充分。
在本申请中提及“实施例”意味着,结合实施例描述的特定特征、结构或特性可以包含在本申请的至少一个实施例中。在说明书中的各个位置出现该短语并不一定均是指相同的实施例,也不是与其它实施例互斥的独立的或备选的实施例。本领域普通技术人员显式地和隐式地理解的是,本申请所描述的实施例在不冲突的情况下,可以与其它实施例相结合。
除非另作定义,本申请所涉及的技术术语或者科学术语应当为本申请所属技术领域内具有一般技能的人士所理解的通常意义。本申请所涉及的“一”、“一个”、“一种”、“该”等类似词语并不表示数量限制,可表示单数或复数。本申请所涉及的术语“包括”、“包含”、“具有”以及它们任何变形,意图在于覆盖不排他的包含;例如包含了一系列步骤或模块(单元)的过程、方法、系统、产品或设备没有限定于已列出的步骤或单元,而是可以还包括没有列出的步骤或单元,或可以还包括对于这些过程、方法、产品或设备固有的其它步骤或单元。本申请所涉及的“连接”、“相连”、“耦接”等类似的词语并非限定于物理的或者机械的连接,而是可以包括电气的连接,不管是直接的还是间接的。本申请所涉及的“多个”是指两个或两个以上。“和/或”描述关联对象的关联关系,表示可以存在三种关系,例如,“A和/或B”可以表示:单独存在A,同时存在A和B,单独存在B这三种情况。字符“/”一般表示前后关联对象是一种“或”的关系。本申请所涉及的术语“第一”、“第二”、“第三”等仅仅是区别类似的对象,不代表针对对象的特定排序。
图1为本申请一个实施例提供的格林森分级预测方法的应用场景图。如图1所示,服务器101与移动终端102之间可以通过网络进行数据传输。其中,移动终端102用于采集待预测前列腺病理图像,并将采集到的待预测前列腺病理图像传输至服务器101中。在服务器101接收到待预测前列腺病理图像后,对待预测前列腺病理图像进行划分得到若干第一patch图像,组成待预测patch图像集;并对待预测前列腺病理图像进行缩放,得到与预测patch图像集中的每个第一patch图像中心点相同、尺寸相同、且分辨率不同的图像,作为第一patch图像关联的第一图像对;之后将待预测patch图像集中的每个第一patch图像及其关联的第一图像对,输入到训练完备的多分辨率分割网络模型,得到每个第一patch图像的格林森分级的预测结果;多分辨率分割网络模型用于对第一patch图像及其关联的第一图像对进行信息融合,得到第一patch图像的格林森分级;最后将待预测patch图像集中的所有第一patch图像的格林森分级的预测结果进行拼接,得到待预测前列腺病理图像的格林森分级的预测结果。其中,服务器101可以由独立的服务器或者是多个服务器组成的服务器集群来实现,移动终端102可以为任意一种图像扫描设备。
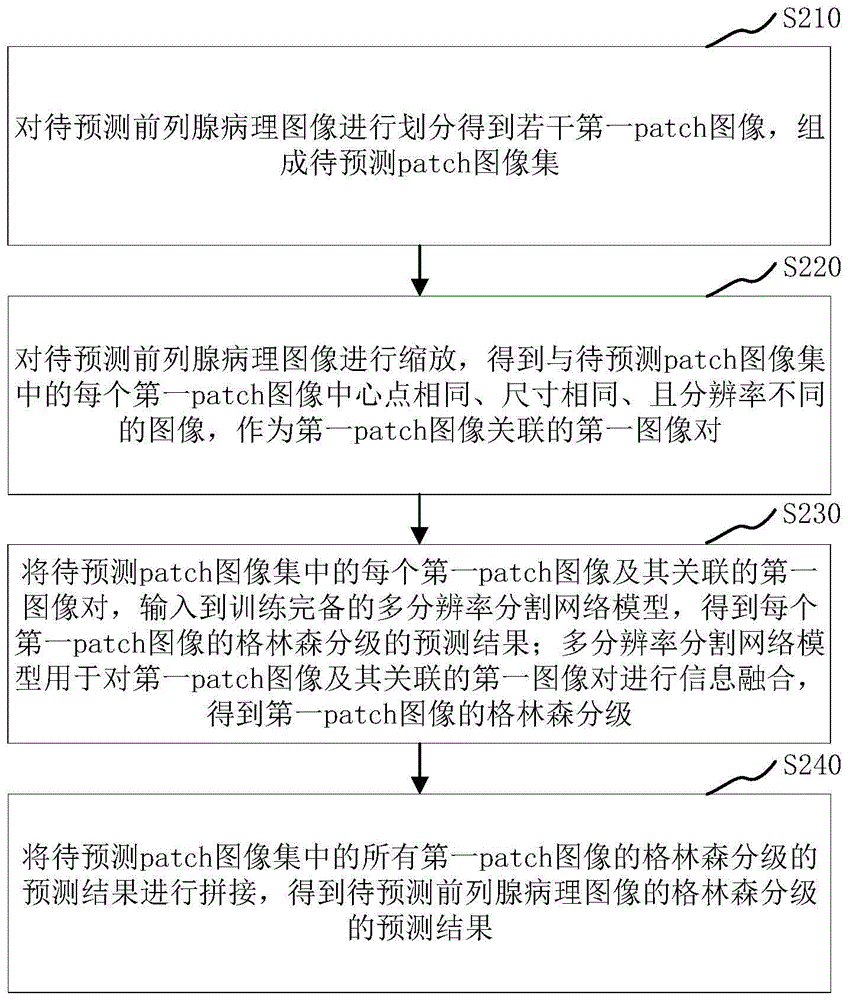
本实施例提供了一种格林森分级预测方法,用于预测前列腺病理图像的格林森分级,如图2所示,该方法包括以下步骤:
步骤S210,对待预测前列腺病理图像进行划分得到若干第一patch图像,组成待预测patch图像集。
具体地,待预测前列腺病理图像是对放置在载玻片上的待预测前列腺病例组织进行扫描得到的图像。由于前列腺病理图像尺寸很大,含有丰富信息,因此在进行分析和处理过程中需要将其进行划分,得到尺寸更小的第一patch图像以便后续进行读取和计算。其中,第一patch图像的尺寸可以依据实际的硬件和软件环境进行设置,例如可以是512*512或者256*256等,保证后续可对第一patch图像进行顺利地读取和计算即可。
步骤S220,对待预测前列腺病理图像进行缩放,得到与待预测patch图像集中的每个第一patch图像中心点相同、尺寸相同、且分辨率不同的图像,作为第一patch图像关联的第一图像对。
在获取到待预测patch图像集中的每个第一patch图像后,以图3a中的第一patch图像为例,假设图3a中的第一patch图像的尺寸是512*512,分辨率为mpp(micrometers perpixel,微米/像素)=0.5。通过将待预测前列腺病理图像进行缩放,可以得到与图3a中的第一patch图像中心点相同、尺寸相同、且分辨率不同的图像(分辨率分别为mpp=1,mpp=2,mpp=4),如图3b、图3c和图3d所示。可以看出,可以通过将待预测前列腺病理图像进行缩小,可以得到更多与第一patch图像相关的周边信息。可以通过将待预测前列腺病理图像进行放大,可以得到更多与第一patch图像相关的细节。具体地,与待预测patch图像集中的第一patch图像中心点相同、尺寸相同、且分辨率不同的图像的分辨率以及个数可以根据实际需求进行设置。
步骤S230,将待预测patch图像集中的每个第一patch图像及其关联的第一图像对,输入到训练完备的多分辨率分割网络模型,得到每个第一patch图像的格林森分级的预测结果;多分辨率分割网络模型用于对第一patch图像及其关联的第一图像对进行信息融合,得到第一patch图像的格林森分级。
具体地,本申请中的多分辨率分割网络模型的结构与U-Net模型类似,如图4所示,图4为多分辨率分割网络模型的示意图。多分辨率分割网络模型由多个编码器和一个解码器组成,多个编码器是共享权值参数的。将多个编码器划分为一个目标分支和若干个上下文分支,其中,目标分支用来输入待预测patch图像集中的每个第一patch图像,上下文分支用来输入第一patch图像关联的第一图像对中的图像。多个编码器实现对第一patch图像及其关联的第一图像对进行信息融合,得到第一patch图像的格林森分级。其中,多分辨率分割网络模型中的编码器个数可以根据需求进行扩展。
步骤S240,将待预测patch图像集中的所有第一patch图像的格林森分级的预测结果进行拼接,得到待预测前列腺病理图像的格林森分级的预测结果。
在得到待预测patch图像集中的所有第一patch图像的格林森分级的预测结果之后,将预测patch图像集中的所有第一patch图像的格林森分级的预测结果进行拼接,即可得到待预测前列腺病理图像的格林森分级的预测结果。作为其中一种实施方式,可以通过设置不同颜色来区分不同的格林森等级。
现有技术中,由经验丰富的病理专家利用显微镜对比前列腺病理组织细胞的形态与正常细胞组织的形态的相似度,从而确定前列腺病理组织的格林森分级。然而前列腺病理组织的格林森分级工作量大,依靠病理专家人工进行观察耗时过长,导致现有技术中存在的前列腺病理组织的格林森分级效率太低的问题。
为了解决上述问题,本申请提出一种格林森分级预测方法,通过将待预测前列腺病理图像进行划分得到的若干第一patch图像及与第一patch图像存在上下文关联的第一图像对,输入到训练完备的多分辨率分割网络模型,实现对第一patch图像的格林森分级进行预测,之后将第一patch图像的格林森分级的预测结果进行拼接,得到待预测前列腺病理图像的格林森分级的预测结果,基于深度学习模型来预测前列腺病理图像的格林森分级,有效提高前列腺病理组织的格林森分级效率。
在其中一个实施例中,在上述步骤S230将待预测patch图像集中的每个第一patch图像及其关联的第一图像对,输入到训练完备的多分辨率分割网络模型之前,格林森分级预测方法还包括以下步骤:
步骤S310,从对待训练前列腺病理图像进行划分得到的若干第二patch图像中,筛选出标注区域大小满足预设要求的第二patch图像,并将标注区域大小满足预设要求的第二patch图像作为多分辨率分割网络模型的样本源。
待训练前列腺病理图像即用来训练多分辨率分割网络模型的图像,通过对待训练前列腺病理图像进行划分,可以得到若干第二patch图像。其中上述第一patch图像和第二patch图像的大小需保持一致。由于第二patch图像是用来训练多分辨率分割网络模型,所以第二patch图像需要存在标注区域且标注区域大小需满足预设要求,例如标注区域需大于5%。预设要求可以根据实际需求进行设置。其中,标注区域即提前被标注了格林森等级的区域,是由病理专家标注过的典型的区域。作为其中一种实施方式,为了进一步提高分辨率分割网络模型计算的精度,可以从待训练前列腺病理图像进行划分得到的若干第二patch图像中,筛选出标注区域大小满足预设第一要求且组织区域大小满足第二设定要求的第二patch图像,作为多分辨率分割网络模型的样本源。其中,组织区域即存在病理组织的区域。
步骤S320,遍历所有预设分辨率,按预设分辨率对待训练前列腺病理图像进行缩放,得到与样本源中的第二patch图像中心点相同、尺寸相同、且分辨率不同的图像,作为第二patch图像关联的第二图像对。
在获取到样本源集中的每个第二patch图像后,遍历所有预设分辨率,通过按预设分辨率对待训练前列腺病理图像进行缩放,可以得到与样本源集中的每个第二patch图像中心点相同、尺寸相同、且分辨率不同的图像,将其作为与第二patch图像存在上下文关联的第二图像对。其中,第二patch图像关联的第二图像对中的图像的分辨率和图像个数与第一patch图像关联的第一图像对中的图像需保持一致。具体地,在样本源集中的第二patch图像的分辨率为mpp=0.5的情况下,所有预设分辨率可以是mpp=1,mpp=2和mpp=4。
步骤S330,对样本源中的第二patch图像及其关联的第二图像对进行训练,生成多分辨率分割网络模型。
通过对样本源中的第二patch图像及其关联的第二图像对进行训练,即可生成多分辨率分割网络模型。
作为其中一种实施方式,可以将待预测前列腺病理图像同时作为待训练前列腺病理图像,从待预测前列腺病理图像划分得到的若干第一patch图像中筛选出标注区域大小满足预设要求的第一patch图像作为多分辨率分割网络模型的样本源,实现对多分辨率分割网络模型进行进一步训练,从而进一步保证待预测前列腺病理图像的格林森分级预测的准确性。
在其中一个实施例中,在步骤S310从对待训练前列腺病理图像进行划分得到的若干第二patch图像中,筛选出标注区域大小满足预设要求的第二patch图像之前,格林森分级预测方法还包括以下步骤:
根据待训练前列腺病理图像的标签,确定待训练前列腺病理图像的标注区域所在位置以及标注区域的被标注等级。
具体地,每个前列腺病理图像一般都会由病理专家提前打过标签,标注过前列腺病理图像的典型区域以及该区域的格林森等级(Gleason 1级、Gleason 2级、Gleason 3级、Gleason 4级或Gleason 5级),那么根据待训练前列腺病理图像的标签,即可确定待训练前列腺病理图像的标注区域所在位置以及标注区域的被标注等级。
作为其中一种实施方式,上述步骤S210对待预测前列腺病理图像进行划分得到若干第一patch图像,组成待预测patch图像集,包括以下步骤:
步骤S211,对待预测前列腺病理图像进行划分得到若干第一patch图像,从中筛选出存在组织区域的第一patch图像,组成待预测patch图像集。
具体地,由于待预测前列腺病理图像的组织分布是分散的,那么对待预测前列腺病理图像进行划分得到的若干第一patch图像中,有不存在组织区域的第一patch图像。对于不存在组织区域的第一patch图像,若进行格林森分级预测流程,十分浪费格林森分级预测的资源及时间。故在本实施例中,从对待预测前列腺病理图像进行划分得到的若干第一patch图像中,筛选出存在组织区域的第一patch图像,组成待预测patch图像集,只对存在组织区域的第一patch图像进行格林森等级预测,可有效提高待预测前列腺病理图像的格林森分级预测效率。
在其中一个实施例中,在步骤S211对待预测前列腺病理图像进行划分得到若干第一patch图像之前,格林森分级预测方法还包括:
利用大津法对待预测前列腺病理图像进行组织区域检测,确定待预测前列腺病理图像的组织区域所在位置。
大津法(OTSU)是一种确定图像二值化分割阈值的算法,由日本学者大津于1979年提出。利用大津法对待预测前列腺病理图像进行组织区域检测,可有效区分待预测前列腺病理图像的背景区域和存在组织的区域,从而有效确定待预测前列腺病理图像的组织区域所在位置。
更进一步地,在其中一个实施例中,格林森分级预测方法还包括:
采用混合损失函数训练多分辨率分割网络模型。
混合损失函数由交叉熵损失、Dice损失、focal Tversky损失构成。混合损失相比单一的损失,能够为多分辨率分割网络模型提供更加丰富的监督信息。作为其中一种实施方式,训练多分辨率分割网络模型采用的混合损失函数如下:
其中,L
图5根据本发明实施例中格林森分级预测装置40的示意图,如图5示,格林森分级预测装置40包括划分模块41、获取模块42、计算模块43和拼接模块44;
划分模块41,用于对待预测前列腺病理图像进行划分得到若干第一patch图像,组成待预测patch图像集;
获取模块42,用于对待预测前列腺病理图像进行缩放,得到与待预测patch图像集中的每个第一patch图像中心点相同、尺寸相同、且分辨率不同的图像,作为第一patch图像关联的第一图像对;
计算模块43,用于将待预测patch图像集中的每个第一patch图像及其关联的第一图像对,输入到训练完备的多分辨率分割网络模型,得到每个第一patch图像的格林森分级的预测结果;多分辨率分割网络模型用于对第一patch图像及其关联的第一图像对进行信息融合,得到第一patch图像的格林森分级;
拼接模块44,用于将待预测patch图像集中的所有第一patch图像的格林森分级的预测结果进行拼接,得到待预测前列腺病理图像的格林森分级的预测结果。
上述格林森分级预测装置40,通过将待预测前列腺病理图像进行划分得到的若干第一patch图像及与第一patch图像存在上下文关联的第一图像对,输入到训练完备的多分辨率分割网络模型,实现对第一patch图像的格林森分级进行预测,之后将第一patch图像的格林森分级的预测结果进行拼接,得到待预测前列腺病理图像的格林森分级的预测结果,基于深度学习模型来预测前列腺病理图像的格林森分级,有效提高前列腺病理组织的格林森分级效率。
在其中一个实施例中,格林森分级预测装置40还包括训练模块,将待预测patch图像集中的每个第一patch图像及其关联的第一图像对,输入到训练完备的多分辨率分割网络模型之前,用于从对待训练前列腺病理图像进行划分得到的若干第二patch图像中,筛选出标注区域大小满足预设要求的第二patch图像,并将标注区域大小满足预设要求的第二patch图像作为多分辨率分割网络模型的样本源;遍历所有预设分辨率,按预设分辨率对待训练前列腺病理图像进行缩放,得到与样本源中的第二patch图像中心点相同、尺寸相同、且分辨率不同的图像,作为第二patch图像关联的第二图像对;对样本源中的第二patch图像及其关联的第二图像对进行训练,生成多分辨率分割网络模型。
在其中一个实施例中,在从对待训练前列腺病理图像进行划分得到的若干第二patch图像中,筛选出标注区域大小满足预设要求的第二patch图像之前,训练模块还用于根据待训练前列腺病理图像的标签,确定待训练前列腺病理图像的标注区域所在位置以及标注区域的被标注等级。
在其中一个实施例中,划分模块41还用于对待预测前列腺病理图像进行划分得到若干第一patch图像,从中筛选出存在组织区域的第一patch图像,组成待预测patch图像集。
在其中一个实施例中,在对待预测前列腺病理图像进行划分得到若干第一patch图像之前,划分模块41还用于利用大津法对待预测前列腺病理图像进行组织区域检测,确定待预测前列腺病理图像的组织区域所在位置。
在其中一个实施例中,格林森分级预测装置40还包括监督模块,用于采用混合损失函数训练多分辨率分割网络模型。
需要说明地是,上述各个模块可以是功能模块也可以是程序模块,既可以通过软件实现,也可以通过硬件来实现。上述各模块可以硬件形式内嵌于或独立于计算机设备中的处理器中,也可以以软件形式存储于计算机设备中的存储器中,以便于处理器调用执行以上各个模块对应的操作。
在一个实施例中,提供了一种计算机设备,该计算机设备可以是服务器,其内部结构图可以如图6所示。该计算机设备包括通过系统总线连接的处理器、存储器、网络接口和数据库。其中,该计算机设备的处理器用于提供计算和控制能力。该计算机设备的存储器包括非易失性存储介质、内存储器。该非易失性存储介质存储有操作系统、计算机程序和数据库。该存储器为非易失性存储介质中的操作系统和计算机程序的运行提供环境。该计算机设备的数据库用于存储预设配置信息集合。该计算机设备的网络接口用于与外部的终端通过网络连接通信。该计算机程序被处理器执行时以实现格林森分级预测方法。
在一个实施例中,提供了一种计算机设备,该计算机设备可以是终端。该计算机设备包括通过系统总线连接的处理器、存储器、网络接口、显示屏和输入装置。其中,该计算机设备的处理器用于提供计算和控制能力。该计算机设备的存储器包括非易失性存储介质、内存储器。该非易失性存储介质存储有操作系统和计算机程序。该存储器为非易失性存储介质中的操作系统和计算机程序的运行提供环境。该计算机设备的网络接口用于与外部的终端通过网络连接通信。该计算机程序被处理器执行时以实现一种格林森分级预测方法。该计算机设备的显示屏可以是液晶显示屏或者电子墨水显示屏,该计算机设备的输入装置可以是显示屏上覆盖的触摸层,也可以是计算机设备外壳上设置的按键、轨迹球或触控板,还可以是外接的键盘、触控板或鼠标等。
本领域技术人员可以理解,图6示出的结构,仅仅是与本申请方案相关的部分结构的框图,并不构成对本申请方案所应用于其上的计算机设备的限定,具体的计算机设备可以包括比图中所示更多或更少的部件,或者组合某些部件,或者具有不同的部件布置。
在一个实施例中,提供了一种计算机可读存储介质,其上存储有计算机程序,计算机程序被处理器执行时实现以下步骤:
对待预测前列腺病理图像进行划分得到若干第一patch图像,组成待预测patch图像集;
对待预测前列腺病理图像进行缩放,得到与待预测patch图像集中的每个第一patch图像中心点相同、尺寸相同、且分辨率不同的图像,作为第一patch图像关联的第一图像对;
将待预测patch图像集中的每个第一patch图像及其关联的第一图像对,输入到训练完备的多分辨率分割网络模型,得到每个第一patch图像的格林森分级的预测结果;多分辨率分割网络模型用于对第一patch图像及其关联的第一图像对进行信息融合,得到第一patch图像的格林森分级;
将待预测patch图像集中的所有第一patch图像的格林森分级的预测结果进行拼接,得到待预测前列腺病理图像的格林森分级的预测结果。
在一个实施例中,在将待预测patch图像集中的每个第一patch图像及其关联的第一图像对,输入到训练完备的多分辨率分割网络模型之前,处理器执行计算机程序时还实现以下步骤:
从对待训练前列腺病理图像进行划分得到的若干第二patch图像中,筛选出标注区域大小满足预设要求的第二patch图像,并将标注区域大小满足预设要求的第二patch图像作为多分辨率分割网络模型的样本源;
遍历所有预设分辨率,按预设分辨率对待训练前列腺病理图像进行缩放,得到与样本源中的第二patch图像中心点相同、尺寸相同、且分辨率不同的图像,作为第二patch图像关联的第二图像对;
对样本源中的第二patch图像及其关联的第二图像对进行训练,生成多分辨率分割网络模型。
在一个实施例中,在从对待训练前列腺病理图像进行划分得到的若干第二patch图像中,筛选出标注区域大小满足预设要求的第二patch图像之前,处理器执行计算机程序时还实现以下步骤:
根据待训练前列腺病理图像的标签,确定待训练前列腺病理图像的标注区域所在位置以及标注区域的被标注等级。
在一个实施例中,处理器执行计算机程序时还实现以下步骤:
对待预测前列腺病理图像进行划分得到若干第一patch图像,从中筛选出存在组织区域的第一patch图像,组成待预测patch图像集。
在一个实施例中,在对待预测前列腺病理图像进行划分得到若干第一patch图像之前,处理器执行计算机程序时还实现以下步骤:
利用大津法对待预测前列腺病理图像进行组织区域检测,确定待预测前列腺病理图像的组织区域所在位置。
在一个实施例中,处理器执行计算机程序时还实现以下步骤:
采用混合损失函数训练多分辨率分割网络模型。
上述存储介质,通过将待预测前列腺病理图像进行划分得到的若干第一patch图像及与第一patch图像存在上下文关联的第一图像对,输入到训练完备的多分辨率分割网络模型,实现对第一patch图像的格林森分级进行预测,之后将第一patch图像的格林森分级的预测结果进行拼接,得到待预测前列腺病理图像的格林森分级的预测结果,基于深度学习模型来预测前列腺病理图像的格林森分级,有效提高前列腺病理组织的格林森分级效率。
在一个实施例中,提供了一种计算机程序产品,包括计算机程序,该计算机程序被处理器执行时实现上述各方法实施例中的步骤。
需要说明的是,本申请所涉及的用户信息(包括但不限于用户设备信息、用户个人信息等)和数据(包括但不限于用于分析的数据、存储的数据、展示的数据等),均为经用户授权或者经过各方充分授权的信息和数据。
应该明白的是,这里描述的具体实施例只是用来解释这个应用,而不是用来对它进行限定。根据本申请提供的实施例,本领域普通技术人员在不进行创造性劳动的情况下得到的所有其它实施例,均属本申请保护范围。
显然,附图只是本申请的一些例子或实施例,对本领域的普通技术人员来说,也可以根据这些附图将本申请适用于其他类似情况,但无需付出创造性劳动。另外,可以理解的是,尽管在此开发过程中所做的工作可能是复杂和漫长的,但是,对于本领域的普通技术人员来说,根据本申请披露的技术内容进行的某些设计、制造或生产等更改仅是常规的技术手段,不应被视为本申请公开的内容不足。
“实施例”一词在本申请中指的是结合实施例描述的具体特征、结构或特性可以包括在本申请的至少一个实施例中。该短语出现在说明书中的各个位置并不一定意味着相同的实施例,也不意味着与其它实施例相互排斥而具有独立性或可供选择。本领域的普通技术人员能够清楚或隐含地理解的是,本申请中描述的实施例在没有冲突的情况下,可以与其它实施例结合。
以上实施例仅表达了本申请的几种实施方式,其描述较为具体和详细,但并不能因此而理解为对专利保护范围的限制。应当指出的是,对于本领域的普通技术人员来说,在不脱离本申请构思的前提下,还可以做出若干变形和改进,这些都属于本申请的保护范围。因此,本申请的保护范围应以所附权利要求为准。
- 一种双面交替TOPTIG冷丝增材制造系统及制造方法
- 一种基于激光光内同轴送丝增材制造系统及成型方法
- 用于增材制造物体的原料线和创建原料线的系统和方法
- 用于增材制造物体的系统和方法
- 热喷涂/激光复合增材再制造系统制备涂层的方法
- 增材制造系统、增材制造方法和计算机可读介质
- 增材制造系统、增材制造方法和计算机可读介质
