一种天然组合物作为雌激素受体降解剂的应用
文献发布时间:2023-06-19 19:30:30
技术领域
本发明涉及医药技术领域,尤其涉及一种天然组合物作为雌激素受体降解剂的应用。
背景技术
雌激素受体阳性乳腺癌是乳腺癌的一种类型,病情受到雌激素影响,通常内分泌治疗是有效的治疗手段。由于无法完全抑制雌激素受体(ER)信号传导,导致难以有效抑制癌细胞增殖,加上耐药问题,临床用药受限。因此ER阳性乳腺癌亟需新的治疗小分子药物。
现有代表治疗药物为他莫昔芬和氟维司群。临床上他莫昔芬耐药问题逐渐显现出来。氟维司群虽具有比他莫昔芬更高的的疗效及更低的副作用,可有效延长患者的生存期,但由于价格昂贵,加上肌肉注射、溶解性差和口服利用度缺乏等问题,限制了它的广泛应用。近年来,用于乳腺癌的雌激素受体降解剂的开发越来越多,更多集中于小分子合成化合物或药物组合物。例如以下中国专利中公开的化合物:CN110343101A,CN111646972A,CN112041307A,CN112424205A,CN112638916A,CN112912078A,CN113614076A,CN114302879A,CN114502539A,CN114656452A和CN114667147A。而天然来源的雌激素受体降解剂报道较少,寻找天然来源的雌激素受体降解剂具有重要意义。
多甲氧基黄酮是芸香科柑橘属植物果实和果皮所特有。多甲氧基黄酮具多种显著生物活性,如抗炎、抗氧化、抗病毒等,其代表物质包括川陈皮素(Nobiletin)、橘皮素(Tangeretin)、柚皮素等。多甲氧基黄酮作为天然化合物可有效预防和治疗疾病,如癌症。但并未有多甲氧基黄酮降解雌激素受体的报道。因此,进一步挖掘以多甲氧基黄酮为主要成分的橘醋发酵底泥提取物在乳腺癌的治疗和预防方面的应用,将具有重要的研究价值。
发明内容
本发明的目的在于克服现有天然来源的雌激素受体降解剂缺乏的问题,提供了一种从柑橘酿醋底泥中提取的天然雌激素受体降解剂,并提供了该天然组合物在降解雌激素受体中的用途。
为了实现上述发明目的,本发明提供以下技术方案:
本发明提供了一种天然组合物作为雌激素受体降解剂的应用,所述天然组合物的制备方法,包括如下步骤:工业橘醋发酵底泥水洗后,固液分离,取固体部分用有机溶剂浸提,得到有机相,所述有机相真空加压浓缩后得到所述天然组合物。
优选的,所述水洗时,所述工业橘醋发酵底泥与水的质量体积比1g:2~4ml。
优选的,所述固液分离的方法为离心,所述离心的转速为4000~6000rpm,时间为25~35min。
优选的,所述工业橘醋发酵底泥与有机溶剂的质量体积比为1g:2~4ml。
优选的,所述有机溶剂为甲醇或乙醇。
优选的,所述浸提的温度为20~30℃,所述浸提的时间为10~14h,所述浸提的次数为2~4次。
优选的,所述真空减压浓缩的温度为50~60℃。
优选的,按照所述制备方法得到的天然组合物包括:4',5,7-三羟基黄酮,4'-甲氧基-3',5,7-三羟基黄烷酮,3,5,7,4'-四羟基-8,3'-二甲氧基黄酮、5,7,8,4'-四甲氧基黄酮、5,6,7,8,3',4'-六甲氧基黄酮、3,5,6,7,8,3',4'-七甲氧基黄酮和5,6,7,8,4'-五甲氧基黄酮中的一种或几种。
本发明构建了雌激素受体阳性乳腺癌细胞株对本发明提取的天然雌激素降解剂进行验证,明确了所述雌激素受体降解剂对雌激素受体的降解作用和对雌激素受体阳性乳腺癌的疗效。
本发明提供的雌激素受体降解剂中的主要成分为多甲氧基黄酮,是来源于芸香科柑橘属植物的天然成分,通过降解雌激素受体进而治疗雌激素受体阳性乳腺癌,弥补了天然来源的雌激素受体降解剂的缺失。
附图说明
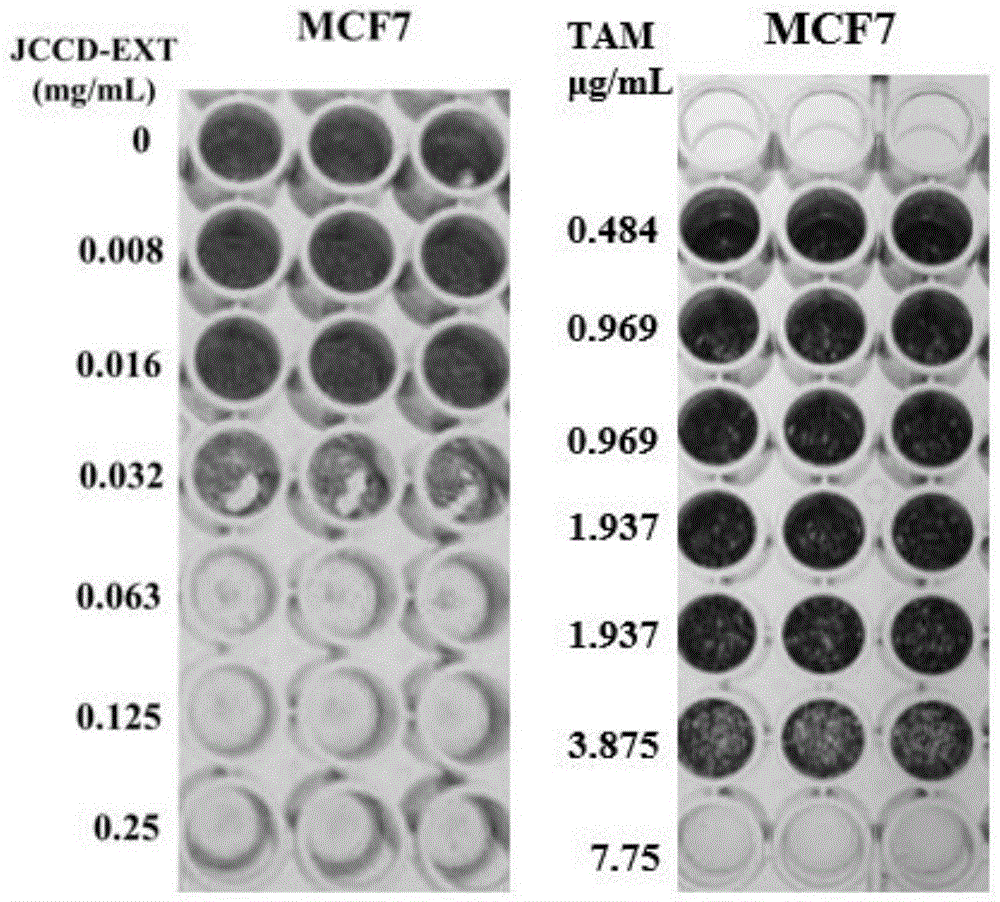
图1为实施例2中雌激素受体降解剂与人乳腺癌MCF7细胞共孵育后结晶紫活细胞染色结果;
图2为实施例2中雌激素受体降解剂对人乳腺癌MCF7细胞生长抑制曲线;
图3为实施例3中雌激素受体降解剂随着时间梯度及浓度梯度对人雌激素受体阳性乳腺癌细胞MCF7的雌激素受体蛋白水平的影响;
图4为实施例4的雌激素受体降解剂对人雌激素受体阳性乳腺癌细胞MCF7雌激素受体mRNA水平的影响;
图5为实施例5使用CHX抑制蛋白合成后,实施例1的雌激素受体降解剂在不同时间梯度对人雌激素受体阳性乳腺癌细胞MCF7的雌激素受体蛋白水平的影响;
图6为实施例6使用MG132(蛋白酶体途径抑制剂),BAF-A1(溶酶体途径抑制剂)分别抑制蛋白降解相关途径后,实施例1的雌激素受体降解剂在不同时间梯度对人雌激素受体阳性乳腺癌细胞MCF7的雌激素受体蛋白水平的影响。
具体实施方式
下面结合实施例对本发明提供的技术方案进行详细的说明,但是不能把它们理解为对本发明保护范围的限定。
实施例1
将55.0g橘醋发酵底泥利用165mL水洗涤后,于5000rpm离心30min,取固体部分用165mL分析纯的甲醇于25℃浸提12h,于5000rpm离心30min,收集有机相,将固相重复浸提3次,合并有机相,55℃减压浓缩得到雌激素受体降解剂10.9g。提取率为19.81%。
经NMR和UPLC-MS分析,鉴定主要成分包括4',5,7-三羟基黄酮,4'-甲氧基-3',5,7-三羟基黄烷酮,3,5,7,4'-四羟基-8,3'-二甲氧基黄酮、5,7,8,4'-四甲氧基黄酮、5,6,7,8,3',4'-六甲氧基黄酮、3,5,6,7,8,3',4'-七甲氧基黄酮和5,6,7,8,4'-五甲氧基黄酮等,结构式如下:
实施例2
本实施例以雌激素受体阳性乳腺癌细胞MCF7细胞为实验对象,验证实施例1制备的天然雌激素受体降解剂的作用。具体如下:
将雌激素受体阳性乳腺癌细胞MCF7细胞接种在于DMEM培养基中,DMEM培养基在加入10%胎牛血清的同时,加入100units/mL青霉素和100μg/mL链霉素,置于37℃、5%CO
由图1可知,经三次平行试验,雌激素受体降解剂与人雌激素受体阳性乳腺癌细胞MCF7共孵育72h后,阳性对照药他莫昔芬和雌激素受体降解剂对肿瘤细胞的生长抑制均可随给药的浓度梯度的增加而加强。
将上述不同浓度雌激素受体降解剂与人雌激素受体阳性乳腺癌细胞MCF7细胞共孵育后的结晶紫活细胞染色结果进行量化,采用柠檬酸三钠溶液置于室温摇床进行洗脱溶解一个小时,在570nm的吸收波长测定吸光度值。测定结果如图2所示。
由图2可知,雌激素受体降解剂与人雌激素受体阳性乳腺癌细胞MCF7细胞半数抑制浓度IC
实施例3
将实施例1中的雌激素受体降解剂与人雌激素受体阳性乳腺癌细胞MCF7细胞分别共孵育24、48、72小时后提取蛋白,通过Westernblot检测雌激素受体的蛋白水平,具体方法如下:
取处于对数生长期的雌激素受体阳性乳腺癌细胞MCF7细胞,使用0.125%胰蛋白酶消化后,将其接种在于含有DMEM培养基的6孔培养板中,DMEM培养基在加入10%胎牛血清的同时,加入100units/mL青霉素和100μg/mL链霉素,置于37℃、5%CO
Western blot具体方法如下:配10%分离胶和5%的浓缩胶,配置SDS-PAGE胶。将细胞样本提取蛋白,用BCA试剂盒(BCAProteinAssay Reagent Kit)蛋白定量后制备跑胶样品,蛋白经100℃高温金属浴10min变性。然后按照20μg蛋白总量上样,进行SDS-PAGE电泳(恒压120V),时间约为2h。电泳完毕后剥下凝胶,切去浓缩胶部分。将NC膜、滤纸和凝胶置于转膜液中进行组装。在电转板上由黑面(负极)至红面(正极)依次叠放:海绵垫、3张滤纸、凝胶、NC膜、3张滤纸、最后是海绵垫。按顺序安装好后插入电转槽,倒入新配制的转膜液,插上电极,在稳流200mA条件下转膜90min,由此将凝胶中的蛋白质转移至NC膜上。电转结束后,将NC膜取出,置于TBST溶液中进行短暂漂洗。用5%脱脂牛奶(TBST配制)于室温摇床上轻摇,封闭NC膜1h后用TBST洗3次,每次5min。在4℃层析柜摇床上一抗(兔源)孵育过夜。用TBST洗膜,5min/次,共洗3次。将TBST稀释的、HRP标记的羊抗兔IgG与NC膜共孵育,室温摇床孵育1h。用TBST洗膜,5min/次,共洗3次。将显影液A和B以1:1混合,取出NC膜,将混合液均匀滴加到膜上,凝胶成像系统拍照并保存结果。
Western blot显影结果如图3所示。由图3可知,雌激素受体降解剂随浓度升高而下调了人雌激素受体阳性乳腺癌细胞MCF7中雌激素受体的蛋白水平。
可见,本发明提供的雌激素降解剂能够下调雌激素受体阳性乳腺癌细胞株MCF7相关的雌激素受体的蛋白水平,且成浓度依赖性。此外,将雌激素受体降解剂与人雌激素受体阳性乳腺癌细胞SSM2、T47D共孵育,也能显著下调其雌激素受体的蛋白水平。
实施例4
将实施例1中的雌激素受体降解剂与人雌激素受体阳性乳腺癌细胞MCF7细胞共孵育24小时后提取mRNA进行反转录获得cDNA,再进行实时荧光定量PCR。探究雌激素受体降解剂对雌激素受体阳性乳腺癌细胞株MCF7、SSM2、T47D相关的雌激素受体的mRNA水平的影响。具体方法如下:
将对数生长期的细胞用胰蛋白酶消化后,进行细胞计数并以2×10
图4结果表明,雌激素受体降解剂与人雌激素受体阳性乳腺癌细胞MCF7共孵育24小时,随降解剂浓度递增均不能下调其雌激素受体的mRNA水平。将该雌激素受体降解剂与人雌激素受体阳性乳腺癌细胞SSM2、T47D共孵育结果和MCF7细胞相同。说明雌激素受体降解剂导致雌激素受体的蛋白水平下降,并非通过基因转录水平调控。
实施例5
本实施案例中,进行雌激素受体降解剂下调雌激素受体阳性乳腺癌细胞株MCF7、SSM2、T47D雌激素受体的蛋白水平的相关机制探索。现以典型人乳腺癌MCF7细胞及其中下调其雌激素受体的蛋白水平为例说明如下。
利用蛋白合成抑制剂放线菌酮(CHX)抑制蛋白合成。将对数生长期的细胞用胰蛋白酶消化后,进行细胞计数并以2×10
结果如图5所示,在使用CHX抑制蛋白合成后,雌激素受体降解剂仍然能在不同时间梯度下调雌激素受体蛋白水平。说明,雌激素受体降解剂对雌激素受体阳性乳腺癌细胞株MCF7的雌激素受体的下调水平并非通过抑制其蛋白合成。
实施例6
本实施案例中,进行雌激素受体降解剂下调雌激素受体阳性乳腺癌细胞株MCF7、SSM2、T47D雌激素受体的蛋白水平的相关机制进行进一步的探索。现以典型人乳腺癌MCF7细胞为例说明如下。
利用MG132(蛋白酶体途径抑制剂),BAF-A1(溶酶体途径抑制剂)分别抑制蛋白降解相关途径后,以此检测雌激素受体降解剂对雌激素受体蛋白水平的影响。将对数生长期的细胞用胰蛋白酶消化后,进行细胞计数并以2×10
结果如图6所示。利用BAF-A1(溶酶体途径抑制剂)抑制蛋白降解的溶酶体途径后,雌激素受体降解剂仍然能在不同时间梯度下调雌激素受体蛋白水平。而在利用MG132(蛋白酶体途径抑制剂)抑制蛋白降解的蛋白酶体途径后,雌激素受体降解剂对其雌激素受体蛋白水平的下调作用有了明显回升。表明,雌激素受体降解剂对雌激素受体阳性乳腺癌细胞株MCF7雌激素受体的下调水平是通过蛋白酶体途径促进其降解,并非通过溶酶体途径。
以上所述仅是本发明的优选实施方式,应当指出,对于本技术领域的普通技术人员来说,在不脱离本发明原理的前提下,还可以做出若干改进和润饰,这些改进和润饰也应视为本发明的保护范围。
