SEZ6L2作为生物标记物在多发性硬化症诊断的应用
文献发布时间:2024-04-18 19:58:26
技术领域
本发明涉及生物医药技术领域,具体涉及SEZ6L2作为生物标记物在多发性硬化症诊断的应用,以及一种能用于甄别多发性硬化症(MS)及视神经脊髓炎谱系疾病(NMOSD)的试剂盒。进一步的,本发明还涉及一种筛选能够用于检测受试者是否患有MS,和/或能够甄别NMOSD和MS试剂的方法。
背景技术
视神经脊髓炎谱系疾病(neuromyelitis optica speetrum disorders,NMOSD)是一种自身免疫介导的炎性脱髓鞘疾病,主要累及青壮年人群,女性居多,以视神经炎和急性横贯性脊髓炎为典型临床表现,复发率和致残率高。
NMOSD最早在19世纪由Devic描述记录并命名为德维克病(Devic disease),是一种自身免疫性疾病,多累及脊髓和视神经,是中枢神经系统脱髓鞘类疾病。早期研究者认为视神经脊髓炎(neuromyelitis optica,NMO)可能是多发性硬化(Multiple Sclerosis,MS)的一个亚型,最早也被称为视神经脊髓型MS,以视力损伤重和脊髓受损后预后差为特点。随着研究的深入,研究者证实高度聚集于脊髓灰质、中脑导水管脑室周围的星形胶质细胞足突中的水通道蛋白4-IgG(AQP4-IgG)抗体直接参与了NMOSD的发病。2015年,由国际视神经脊髓炎诊断小组,把视神经脊髓炎和更广义概念的NMOSD定义为不同于多发性硬化的一种独立疾病。NMOSD病变累及部位不仅包括视神经和脊髓,还包括脑实质。大约一半的NMOSD患者出现严重行走困难,60%~70%患者失明或单侧视力受影响,多数患者遗留有严重的尿便障碍、睡眠障碍等。NMOSD为高复发、高致残性疾病,90%以上患者为多时相病程,约60%的患者在1年内复发,90%的患者在3年内复发,严重影响患者生活质量同时,造成社会极大的经济负担。
NMOSD的诊断以病史和核心临床症候及影像特征为诊断基本依据,并参考其他亚临床及免疫学证据做出诊断,同时还需排除其他疾病可能。早期Wingerchuk等制定的NMO诊断标准以视神经炎和急性脊髓炎为必要条件,支持条件为1)脊髓MRI异常病变超过3个椎体节段以上;2)头颅MRI不符合MS诊断标准;3)血清NMO-IgG阳性。若具备全部必要条件和2条支持条件即可诊断NMO。2004年,一种靶向水通道蛋白4的IgG标记物AQP4-IgG的发现,改变了NMOSD发病机制的认识和诊断的发展。2015年国际NMO诊断小组制定的NMOSD诊断标准以AQP4-IgG作为分层,分为AQP4-IgG阳性与阴性组,列举了6大核心临床特征表现,强调影像学特征与临床特征的一致性,并对AQP4-IgG阴性NMOSD提出了更加严格的MRI附加条件。
在临床上,如何有效甄别MS和NMOSD是一直困扰临床医生的问题。AQP4-IgG作为NMOSD的血清生物标记物被发现后,研究者认为AQP4-IgG介导的异常免疫反应是NMOSD发生的关键因素,也是诊断为NMOSD的重要依据之一,但研究发现仍有近30%的NMOSD患者血清AQP4-IgG阴性,而大部分MS患者也是血清AQP4-IgG阴性,这便导致临床上诊断甄别NMOSD和MS出现了问题,而在临床诊断中,两种疾病的区分诊断十分关键,因为其对应的治疗方案完全不同:对MS治疗效果很好的药物(如IFN-β,natalizumab,oral fingolimod等)不仅对NMOSD治疗无效反而会加重NMOSD的病情,因此设法区分MS和NMOSD,对于疾病有效诊断和个体化治疗十分关键。
因此,需要开发一种新的检测MS的方法和试剂盒,以及区分MS和NMOSD的方法和试剂盒。
发明内容
针对上述现有技术的不足,本发明提供了癫痫相关蛋白6样蛋白2(简称SEZ6L2)作为生物标记物在制备多发性硬化症诊断产品的应用,主要解决现有MS诊断方法检测繁琐、代价较大,依赖相关专业人员的经验,无法客观量化同时,不能进行规模化筛查且无法区分MS和NMOSD等问题。
为解决上述提到的行业难题,本发明申请采用了以下技术方案:
本发明的第一目的是提供检测受试者生物样本中生物标记物表达水平的试剂在制备产品中的应用,所述产品用于预测或诊断多发性硬化症,所述的生物标记物为SEZ6L2。
在本发明中,生物标记物SEZ6L2,包括gene或其片段的mRNA或编码的蛋白及其同源物,突变,和同等型。该术语涵盖全长,未加工的生物标记物,以及源自细胞中加工的任何形式的生物标记物。该术语涵盖生物标记物的天然发生变体(例如剪接变体或等位变体)。
术语“受试者”包括任何人类或非人类动物。术语“非人类动物”包括所有脊椎动物,例如哺乳动物和非哺乳动物,例如非人类灵长类动物、马、羊、狗、牛、猪、鸡和其它兽医受试者。在一个典型的实施方案中,受试者是人。
术语“生物样本”包括但不限于,组织样本(例如肿瘤组织样本),原代或培养的细胞或细胞系,细胞上清,细胞裂解物,血液,体液,淋巴液,滑液,精液,羊水,乳,尿液,脑脊髓液,唾液,痰,泪,汗液,粘液,肿瘤裂解物,和组织培养液,组织提取物如匀浆化的组织,细胞提取物,及其组合。
进一步地,所述产品用于甄别多发性硬化症与视神经脊髓炎谱系疾病。
进一步地,所述试剂包括检测生物标记物SEZ6L2基因或其片段的mRNA表达水平的试剂,或检测生物标记物SEZ6L2的编码蛋白表达水平的试剂。
进一步地,所述检测生物标记物SEZ6L2基因或其片段的mRNA的表达水平使用选自聚合酶链反应、实时荧光定量逆转录多聚酶链反应、逆转录聚合酶链反应、竞争性聚合酶链反应、核酸酶保护分析、原位杂交法、核酸微阵列、RNA印迹或DNA芯片的方法中的任何一种或多种。此处所列方法有限,但只要是通过检测生物标记物基因或其片段的mRNA在预测或诊断多发性硬化症方面的应用方法,均在本专利的保护范围内。
进一步地,所述检测生物标记物SEZ6L2的编码蛋白的表达水平使用选自多重邻位延伸分析、酶联免疫吸附、放射免疫测定、夹心分析、蛋白质印迹、免疫沉淀、免疫组织化学染色、荧光免疫测定、酶底物显色、抗原抗体聚集、荧光激活细胞分选、质谱分析、采用一组多重胺特异性稳定同位素试剂的测定或蛋白质芯片测量中的任何一种或多种。
进一步地,所述试剂包括:
与所述生物标记物SEZ6L2基因或其片段的mRNA特异性结合的引物或探针;
和/或与所述生物标记物SEZ6L2蛋白特异性结合的抗体、肽、适配体或化合物。
术语“引物”是指具有短游离3'-羟基的核酸序列,是可以与互补模板形成碱基对并充当模板链复制的起点的短核酸。在适当的缓冲溶液和温度下,在存在用于聚合的试剂(即DNA聚合酶或逆转录酶)和四种不同的核苷三磷酸的情况下,引物可以引发DNA合成。可以根据本领域已知的技术适当地选择PCR条件以及正义和反义引物的长度。
术语“探针”是指对应于可以特异性结合mRNA的几个碱基至数百个碱基的核酸片段(例如RNA或DNA),并且可以通过标签来确认特定mRNA的存在与否以及表达水平。探针可以以寡核苷酸探针、单链DNA探针、双链DNA探针或RNA探针的形式制备。可以根据本领域已知的技术适当地选择合适的探针和杂交条件。
术语“抗体”是本领域众所周知的,是指针对抗原位点的特异性免疫球蛋白。本发明中的抗体是指与本发明的基因标记物蛋白特异性结合的抗体,可以根据本领域中的常规方法来制造抗体。抗体的形式包括多克隆抗体或单克隆抗体、抗体片段(诸如Fab、Fab'、F(ab')2和Fv片段)、单链Fv(scFv)抗体、多特异性抗体(诸如双特异性抗体)、单特异性抗体、单价抗体、嵌合抗体、人源化抗体、人抗体、包含抗体的抗原结合位点的融合蛋白,以及包含抗原结合位点的任何其他修饰的免疫球蛋白分子,只要该抗体表现出所需的生物结合活性。
术语“肽”具有与靶物质高度结合的能力,并且在热处理/化学处理期间不会发生变性。而且,由于其尺寸小,可以通过将其附接到其它蛋白上而用作融合蛋白。具体而言,可以特异性地附接到高分子蛋白链上,用作诊断试剂盒和药物递送物质。
术语“适配体”是指一种由特定类型的单链核酸(DNA、RNA或修饰的核酸)组成的多核苷酸,所述单链核酸自身具有稳定的三级结构,并且具有能够以高亲和力和特异性与靶分子结合的特性。如上所述,由于适配体可以像抗体那样特异性结合抗原性物质,但比蛋白更稳定并具有简单的结构,并且是由易于合成的多核苷酸组成,因此可以代替抗体来使用。
本发明的第二目的是提供一种用于诊断多发性硬化症的试剂盒,其特征在于,所述试剂盒用来在生物样本中检测生物标记物SEZ6L2的基因或其片段的mRNA或其编码蛋白中的一种或多种。
本发明的第三目的是提供一种用于诊断多发性硬化症的诊断试剂,所述诊断试剂用于检测生物标记物SEZ6L2,所述诊断试剂包含与所述生物标记物基因或其片段的mRNA特异性结合的引物或探针和/或与所述生物标记物的编码蛋白标记物特异性结合的抗体。
进一步地,所述抗体为多克隆抗体或单克隆抗体。
本发明的用于多发性硬化症的诊断试剂可通过抗原-抗体结合反应定量或定性分析所述抗体蛋白的抗原来诊断多发性硬化症。可通过利用常用的酶联免疫吸附分析法(ELISA)、放射免疫分析法(RIA)、夹心法、免疫印迹法、免疫沉淀法、免疫组织化学染色法、荧光免疫分析法、酶基质着色法、抗原抗体聚集法等来检测所述抗原-抗体结合反应。例如,提供所述诊断试剂盒来进行通过利用表面上包被有检体和对照物的96孔酶标板与重组单克隆抗体蛋白进行反应的ELISA。
根据本领域已知的常用方法向外部宿主注射作为抗原的蛋白标记物或其片段来制备所述多克隆抗体。这种外部宿主可以包括,例如哺乳动物,如小鼠、大鼠、羊和兔。所述抗原通常与用来增强抗原性的佐剂一起通过肌肉注射、腹腔注射或皮下注射进行给药,从而使外部宿主免疫化。从免疫外部宿主中定期收集血清。随后,可获取示出效价有提高且对抗原具有特异性的血清,或从所述血清中分离并提纯抗体,从而制备所述标记蛋白的特异性多克隆抗体。
所述单克隆抗体可通过本领域中已知的经融合的永生化细胞株的生产过程(Kohler G.et al.,Nature,256:495-497,1975)来进行制备。简单说明一下上述过程,首先用纯标记蛋白或其片段免疫小鼠。或者,通过合成所述标记蛋白的肽并使之与牛血清白蛋白结合来免疫小鼠。将从所述免疫小鼠中分离的能产生抗体的B淋巴细胞与人或小鼠的骨髓瘤细胞融合,以生成永生化杂交瘤细胞。随后,通过酶联免疫吸附分析法(ELISA)调查在所述杂交瘤细胞中单克隆抗体的形成,而选取阳性克隆。培养所选取的克隆,然后分离并提纯抗体。或者将所述克隆注射到大鼠的腹腔内而收集腹水,从而制备所述标记蛋白的特异性单克隆抗体。
在本发明的蛋白标记物的检测中使用的抗体包括具有两条全长轻链和两条全长重链的完整形式以及抗体分子的功能性片段。所述抗体分子的功能性片段是指至少具有抗原结合能力的片段。例如,Fab、F(ab’)、F(ab)2、Fv等。
到目前为止,业内开展了很多通过检测特定生物标记物水平来诊断MS或者甄别MS和NMOSD的研究,这些技术或者方法,一方面,或者工序复杂,或者操作复杂,或者对仪器设备配置有较高要求,同样不利于进行规模化筛查,不利于临床普及;另一方面,甄别效果不明显或者不理想,在临床上应用价值低。综合而言,目前还没有通过对某个生物标记物水平的简单有效检测便能达到诊断MS及有效区分MS及NMOSD目的的方法。
针对现行诊断方法的弊端,本发明提供一种工序简单、方便有效、利于进行规模化筛查,便于临床普及的MS诊断及更进一步的,能用于MS及NMOSD甄别的生物标记物及该生物标记物的应用办法。
本发明,通过大量的蛋白质组学分析工作,发现SEZ6L2靶标可能与脱髓鞘疾病相关,通过基因工程技术获得上述重组抗原,并进一步利用单克隆抗体技术开发了特异性识别上述靶标的单克隆抗体,对相关疾病的血液样本和脑脊液样本进一步分析后,证实了上述标记物在MS的诊断及进一步甄别MS及NMOSD疾病具有非常高的临床价值,利于开展规模化筛查。
本发明的优点和有益效果在于:
本发明提供一种通过检测人体生物样本中生物标记物SEZ6L2基因或其片段的mRNA或编码蛋白的表达水平诊断MS的方法,本发明方法可量化、操作更便捷,对操作人员专业性要求不高,比现有诊断方法更客观、更有利于开展规模化筛查工作,更有利于疾病的发现和确诊以及提供有针对性的个体化治疗方案。
附图说明
下面参照附图结合实施例对本发明作进一步的说明。
图1为多发性硬化症患者与正常人血样中生物标记物SEZ6L2编码蛋白水平对比图。
图2为多发性硬化症与视神经脊髓炎谱系疾病血样中生物标记物SEZ6L2编码蛋白水平对比图。
图3为正常人、多发性硬化症及视神经脊髓炎谱系疾病血样中生物标记物SEZ6L2编码蛋白水平对比图。
图4为多发性硬化症与非多发性硬化症患者脑脊液中生物标记物SEZ6L2编码蛋白水平对比图。
图5为非脱髓鞘疾病、多发性硬化症及视神经脊髓炎谱系疾病脑脊液中生物标记物SEZ6L2编码蛋白水平对比图。
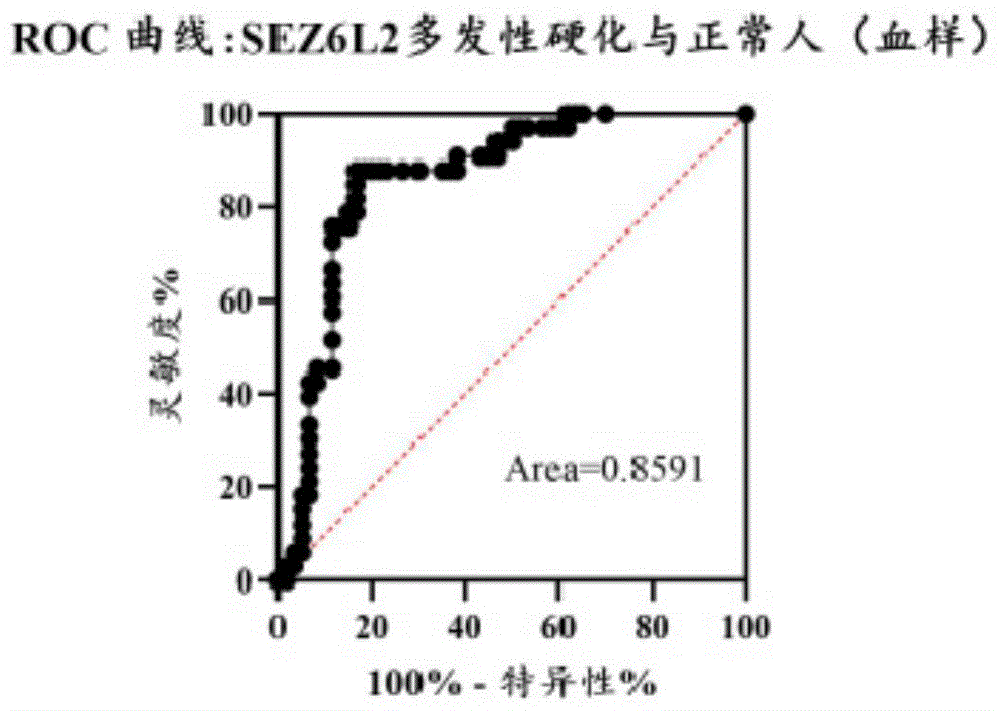
图6为多发性硬化症患者与正常人血样中生物标记物SEZ6L2编码蛋白水平的ROC曲线图。
图7为多发性硬化症与非多发性硬化症患者脑脊液中生物标记物SEZ6L2编码蛋白水平的ROC曲线图。
图8为多发性硬化症与视神经脊髓炎谱系疾病血样中生物标记物SEZ6L2编码蛋白水平的ROC曲线图。
图9为多发性硬化症与视神经脊髓炎谱系疾病脑脊液中生物标记物SEZ6L2编码蛋白水平的ROC曲线图。
具体实施方式
为了更好地理解本发明,下面结合实施例和附图对本发明做进一步的详细说明,但本领域技术人员了解,下述实施例不是对本发明保护范围的限制,任何在本发明基础上做出的改变和变化,都在本发明的保护范围之内。
下述实施例中所使用的实验方法如无特殊说明,均为常规方法。
下述实施例中所用的材料、试剂等,如无特殊说明,均可从商业途径得到。
实施例1多发性硬化症相关的基因标记物的筛选
采用下一代非标记定量蛋白质组学技术,分析正常人和脑部疾病患者的血样和脑脊液样本差异表达的蛋白,在其中选取SEZ6L2作为研究对象。
实施例2多发性硬化症检测单克隆抗体及效果评价
一、重组SEZ6L2相关蛋白制备
人源全长SEZ6L2(Gene Bank:NM_001114100.3)的氨基酸序列如SEQ ID NO:1所示,核苷酸序列全长如SEQ ID NO:2所示,人源SEZ6L2全长基因由通用生物公司合成并整合在pET-32a载体中,PCR引物由通用生物公司完成。利用大肠杆菌表达系统表达及纯化制备pET-32a-SEZ6L2全长抗原(后续简称为抗原S1)。
通过酶切回收抗原S1的目的片段,将该目标片段连接pCold-TF表达载体,进一步表达和制备pCold-TF-SEZ6L2全长抗原(后续简称为抗原S2);以上述质粒为模板,扩增1-395片段,克隆经pCold-TF载体中,进一步表达和制备pCold-TF-SEZ6L2 1-395片段抗原,(后续简称为抗原S3);将1-395片段克隆至pTT5载体,利用HEK293细胞进行真核表达获得含有真核抗原pTT5-SEZ6L2-1-395的细胞上清(后续简称抗原S4),对应氨基酸序列如SEQ IDNO:3所示,其核苷酸序列如SEQ ID NO:4所示。
SEQ ID NO:1
MGTPRAQHPPPPQLLFLILLSCPWIQGLPLKEEEILPEPGSETPTVASEALAELLHGALLRRGPEMGYLPGSDPDPTLATPPAGQTLAVPSLPRATEPGTGPLTTAVTPNGVRGAGPTAPELLTPPPGTTAPPPPSPASPGPPLGPEGGEEETTTTIITTTTVTTTVTSPAYLLSCGFPPRPAHGDVSVTDLHPGGTATFHCDSGYQLQGEETLICLNGTRPSWNGETPSCMASCGGTIHNATLGRIVSPEPGGAVGPNLTCRWVIEAAEGRRLHLHFERVSLDEDNDRLMVRSGGSPLSPVIYDSDMDDVPERGLISDAQSLYVELLSETPANPLLLSLRFEAFEEDRCFAPFLAHGNVTTTDPEYRPGALATFSCLPGYALEPPGPPNAIECVDPTEPHWNDTEPACKAMCGGELSEPAGVVLSPDWPQSYSPGQDCVWGVHVQEEKRILLQVEILNVREGDMLTLFDGDGPSARVLAQLRGPQPRRRLLSSGPDLTLQFQAPPGPPNPGLGQGFVLHFKEVPRNDTCPELPPPEWGWRTASHGDLIRGTVLTYQCEPGYELLGSDILTCQWDLSWSAAPPACQKIMTCADPGEIANGHRTASDAGFPVGSHVQYRCLPGYSLEGAAMLTCYSRDTGTPKWSDRVPKCALKYEPCLNPGVPENGYQTLYKHHYQAGESLRFFCYEGFELIGEVTITCVPGHPSQWTSQPPLCKVAYEELLDNRKLEVTQTTDPSRQLEGGNYYTKLQGKSLFGFSGSHSYSPITVESDFSNPLYEAGDTREYEVSISEQ ID NO:2
ATGGGTACACCGCGCGCACAGCATCCGCCGCCTCCTCAACTGCTGTTTCTGATTCTGCTGAGTTGTCCGTGGATTCAGGGTCTGCCGCTGAAAGAAGAAGAAATTCTGCCGGAACCGGGTAGTGAAACCCCGACCGTGGCAAGTGAAGCCCTGGCCGAACTGCTGCATGGCGCCCTGCTGCGTCGCGGTCCTGAAATGGGCTATCTGCCGGGCAGTGATCCGGACCCTACCCTGGCAACCCCGCCGGCAGGTCAGACCCTGGCAGTTCCGAGTCTGCCGCGCGCCACCGAACCGGGTACAGGTCCTCTGACCACCGCAGTGACCCCGAATGGTGTGCGCGGCGCAGGCCCTACCGCCCCTGAGTTACTGACCCCGCCGCCGGGTACAACCGCACCTCCTCCTCCGAGTCCGGCCAGTCCGGGTCCTCCTCTGGGCCCTGAAGGTGGCGAAGAAGAAACCACCACCACCATTATTACCACCACCACAGTTACCACCACCGTGACCAGCCCGGCCTATCTGCTGAGCTGTGGTTTTCCGCCGCGCCCGGCCCACGGTGACGTTAGCGTTACCGATCTGCATCCGGGCGGTACAGCCACCTTTCATTGTGATAGCGGCTATCAGCTGCAGGGCGAAGAAACCCTGATTTGCCTGAATGGTACACGTCCGAGCTGGAATGGTGAAACCCCGAGCTGTATGGCCAGTTGCGGCGGCACCATTCATAATGCAACCCTGGGCCGCATTGTGAGCCCGGAACCGGGCGGTGCCGTTGGTCCTAATCTGACCTGCCGTTGGGTTATTGAAGCCGCCGAAGGCCGCCGCCTGCATCTGCATTTTGAACGCGTTAGTCTGGATGAAGATAATGATCGTCTGATGGTTCGTAGTGGTGGTAGTCCGCTGAGTCCGGTTATCTATGATAGTGATATGGATGATGTTCCGGAACGCGGTCTGATTAGCGATGCCCAGAGCCTGTATGTTGAACTGCTGAGTGAAACCCCTGCCAATCCGCTGCTGCTGAGTCTGCGTTTTGAAGCATTTGAAGAAGATCGCTGTTTTGCACCGTTTCTGGCCCACGGTAATGTGACCACCACCGATCCGGAATATCGCCCGGGTGCACTGGCAACCTTTAGCTGTCTGCCGGGTTATGCCCTGGAACCGCCGGGCCCTCCGAATGCTATTGAATGCGTTGATCCGACCGAACCGCATTGGAATGATACCGAACCGGCATGTAAAGCCATGTGCGGTGGCGAACTGAGTGAACCGGCAGGCGTTGTTCTGAGCCCGGATTGGCCGCAGAGCTATAGTCCGGGCCAGGATTGCGTTTGGGGTGTTCATGTTCAGGAAGAAAAACGCATTCTGCTGCAGGTGGAAATTCTGAATGTTCGTGAAGGCGATATGCTGACCCTGTTTGATGGCGATGGTCCGAGTGCACGCGTGCTGGCCCAGCTGCGTGGTCCTCAGCCGCGTCGTCGCCTGCTGAGTAGTGGTCCGGATCTGACCCTGCAGTTTCAGGCCCCGCCGGGCCCACCTAATCCGGGTTTAGGCCAGGGTTTTGTTCTGCATTTTAAAGAAGTTCCGCGCAATGATACCTGTCCGGAACTGCCGCCGCCGGAATGGGGTTGGCGTACCGCAAGCCACGGTGACCTGATTCGCGGTACAGTGCTGACCTATCAGTGTGAACCGGGTTATGAACTGCTGGGTAGTGATATTCTGACCTGCCAGTGGGATCTGAGTTGGAGCGCAGCCCCGCCGGCATGTCAGAAAATTATGACCTGCGCCGATCCGGGCGAAATTGCCAATGGCCATCGCACCGCAAGTGATGCAGGTTTTCCGGTGGGCAGTCATGTTCAGTATCGCTGTCTGCCGGGCTATAGCCTGGAAGGCGCAGCAATGCTGACCTGCTATAGCCGTGATACCGGCACCCCGAAATGGAGCGATCGCGTGCCGAAATGTGCACTGAAATATGAACCGTGTCTGAATCCGGGTGTTCCGGAAAATGGCTATCAGACCCTGTATAAACATCATTATCAGGCAGGCGAAAGTCTGCGTTTCTTTTGCTATGAAGGTTTTGAACTGATTGGTGAAGTTACCATTACCTGTGTTCCGGGCCATCCGAGCCAGTGGACCAGTCAGCCGCCGCTGTGCAAAGTGGCCTATGAAGAACTGCTGGATAATCGCAAACTGGAAGTGACCCAGACCACCGATCCTAGTCGTCAGCTGGAAGGCGGTAATTATTATACCAAACTGCAGGGTAAAAGTCTGTTTGGCTTTAGTGGTAGCCATAGTTATAGTCCGATTACCGTGGAAAGTGATTTTAGCAATCCGCTGTATGAAGCCGGTGACACCCGCGAATATGAAGTGAGCATT
SEQ ID NO:3
MGTPRAQHPPPPQLLFLILLSCPWIQGLPLKEEEILPEPGSETPTVASEALAELLHGALLRRGPEMGYLPGSDPDPTLATPPAGQTLAVPSLPRATEPGTGPLTTAVTPNGVRGAGPTAPELLTPPPGTTAPPPPSPASPGPPLGPEGGEEETTTTIITTTTVTTTVTSPAYLLSCGFPPRPAHGDVSVTDLHPGGTATFHCDSGYQLQGEETLICLNGTRPSWNGETPSCMASCGGTIHNATLGRIVSPEPGGAVGPNLTCRWVIEAAEGRRLHLHFERVSLDEDNDRLMVRSGGSPLSPVIYDSDMDDVPERGLISDAQSLYVELLSETPANPLLLSLRFEAFEEDRCFAPFLAHGNVTTTDPEYRPGALATFSCLPGYALEPPGPPNAIECV
SEQ ID NO:4
ATGGGTACACCGCGCGCACAGCATCCGCCGCCTCCTCAACTGCTGTTTCTGATTCTGCTGAGTTGTCCGTGGATTCAGGGTCTGCCGCTGAAAGAAGAAGAAATTCTGCCGGAACCGGGTAGTGAAACCCCGACCGTGGCAAGTGAAGCCCTGGCCGAACTGCTGCATGGCGCCCTGCTGCGTCGCGGTCCTGAAATGGGCTATCTGCCGGGCAGTGATCCGGACCCTACCCTGGCAACCCCGCCGGCAGGTCAGACCCTGGCAGTTCCGAGTCTGCCGCGCGCCACCGAACCGGGTACAGGTCCTCTGACCACCGCAGTGACCCCGAATGGTGTGCGCGGCGCAGGCCCTACCGCCCCTGAGTTACTGACCCCGCCGCCGGGTACAACCGCACCTCCTCCTCCGAGTCCGGCCAGTCCGGGTCCTCCTCTGGGCCCTGAAGGTGGCGAAGAAGAAACCACCACCACCATTATTACCACCACCACAGTTACCACCACCGTGACCAGCCCGGCCTATCTGCTGAGCTGTGGTTTTCCGCCGCGCCCGGCCCACGGTGACGTTAGCGTTACCGATCTGCATCCGGGCGGTACAGCCACCTTTCATTGTGATAGCGGCTATCAGCTGCAGGGCGAAGAAACCCTGATTTGCCTGAATGGTACACGTCCGAGCTGGAATGGTGAAACCCCGAGCTGTATGGCCAGTTGCGGCGGCACCATTCATAATGCAACCCTGGGCCGCATTGTGAGCCCGGAACCGGGCGGTGCCGTTGGTCCTAATCTGACCTGCCGTTGGGTTATTGAAGCCGCCGAAGGCCGCCGCCTGCATCTGCATTTTGAACGCGTTAGTCTGGATGAAGATAATGATCGTCTGATGGTTCGTAGTGGTGGTAGTCCGCTGAGTCCGGTTATCTATGATAGTGATATGGATGATGTTCCGGAACGCGGTCTGATTAGCGATGCCCAGAGCCTGTATGTTGAACTGCTGAGTGAAACCCCTGCCAATCCGCTGCTGCTGAGTCTGCGTTTTGAAGCATTTGAAGAAGATCGCTGTTTTGCACCGTTTCTGGCCCACGGTAATGTGACCACCACCGATCCGGAATATCGCCCGGGTGCACTGGCAACCTTTAGCTGTCTGCCGGGTTATGCCCTGGAACCGCCGGGCCCTCCGAATGCTATTGAATGCGTT
二、抗SEZ6L2单克隆抗体制备
1、免疫原的准备:
免疫原抗原S1,将实施例1制备的抗原S3用10mmol/L PBS稀释至0.2mg/mL,按照终浓度为100ug/mL取相应抗原与弗氏佐剂等体积混合,使其成油包水状乳剂。初次免疫使用弗氏完全佐剂,加强免疫使用弗氏不完全佐剂。
2、基础免疫:选择6-8周龄BALB/c雌鼠进行皮下多点注射免疫,免疫原注射剂量为500μL/只/次,免疫间隔为2周,完整免疫程序为4针,在第2、4针免疫后2周用眼眶采血法采集分离血清用于间接ELISA测定免疫效价,确定小鼠血清效价达到平台期后,于细胞融合前72小时,将免疫原以100ug/只剂量进行脾脏免疫。
3、杂交瘤细胞筛选
3.1饲养细胞之巨噬细胞的制备:
(i)6周龄左右的BALB/c小鼠引颈处死,在75%酒精溶液中浸泡5min后;取出放入事先置于超净工作台的无菌平皿中,利用止血钳调整小鼠姿态,使其腹部朝上,整体更为舒展,将小鼠摆横,用止血钳夹近小鼠腹部偏下位置皮肤,骤然发力反方向撕拉开皮肤,充分暴露腹部。
(ii)无菌眼科弯镊提起腹膜,然后用5mL注射器向腹腔内注入适量培养基,以使其腹部充分鼓胀为准,放下注射器,双手持止血钳配合将小鼠对侧四肢提起轻柔摇晃,使腹腔中巨噬细胞充分浸润后用同一注射器吸出注入事先配制好的含20%胎牛血清的1640HT培养基中备用。
3.2饲养细胞之胸腺细胞的制备:
(i)三周龄BALB/c小鼠引颈处死,在75%酒精溶液中浸泡5min后;取出放入事先置于超净工作台的无菌平皿中,利用止血钳调整小鼠姿态,使其腹部朝上,整体更为舒展,将小鼠摆横,用止血钳夹近小鼠胸部偏下位置皮肤,骤然发力反方向撕拉开皮肤,充分暴露胸腹部。
(ii)左手用无菌弯镊隔胸腹部皮肤夹住胸骨尖,沿着胸骨体外沿剪开,充分暴露胸腔隔膜,并始终保持夹住胸骨尖,尽可能暴露胸腔的状态。
(iii)右手持干净的眼科剪剪开胸腔隔膜,充分暴露胸腔,用弯镊探入胸腔,夹住胸腺根部,完整取出胸腺,放入事先放置于平皿并用培养基浸润的200目筛网中进行研磨,得到胸腺饲养细胞液,全数转移进上述含20%胎牛血清的1640HT培养基中备用。
3.3小鼠骨髓瘤细胞的制备:融合前5天复苏小鼠骨髓瘤细胞,每次融合约需6瓶35cm
3.4脾细胞的制备:
(i)取待融合的BALB/C小鼠,眼眶采血,待血流停止,断颈处死小鼠,浸泡于75%酒精溶液中5min,随即放入超净台内无菌平皿上,右侧卧位。
(ii)用3.1所述方法暴露腹腔,无菌手术打开腹腔取出脾脏,放入事先放置于平皿并用培养基浸润的200目筛网中进行研磨,制备脾脏细胞悬液转移到50mL无菌离心管中。
(iii)补加适量RPMI-1640培养液30-35mL,用弯管清除明显的脂肪聚团及其他杂质后,1500rpm/min,5min/次,离心收集脾脏细胞,离心去上清,补加新的培养基30-35mL,重复上述过程2次清洗脾脏细胞。
(iv)用RPMI-1640培养液重悬细胞,计数。
3.5细胞融合:
(i)融合前先将1mL的PEG-1450和35mL的RPMI-1640无血清培养基和200mL事先配好的含20%胎牛血清的HAT完全培养基预温至37℃。
(ii)将制备的骨髓瘤细胞与脾细胞按比例1×10
(iii)1mL移液器管吸取1mL PEG加入离心管内,边加边轻轻用弯管吹打混匀,时间控制在60s左右,随即加入35mL预温的RPMI-1640完全培养液终止融合反应。
(iv)静置1-5min后,离心1000rpm×5min,小心弃上清液,用手指轻柔弹匀细胞后,加入上述完全培养基充分重悬细胞后,全数移入到已经事先添加饲养层细胞的完全培养基中,混匀后,按200ul/孔铺入96孔细胞培养板,放入CO
(v)7天后,用15%HT完全培养基给孔中的细胞上清进行100%的换液;7天后,吸取上清检测。
3.6杂交瘤的筛选:
利用抗原S1初筛,辅助用1个同样是融合pET-32a的抗原差异筛选,载体抗原来自英博迈(货号:E3211),同时用自制的重组抗原S2及S3进行鉴定,筛选方法为间接ELISA,具体方法是包被抗原200ng/mL,每孔包被100ul,加入细胞上清50uL,37℃孵育30min后,洗板机洗板5次,加入100ul 1:5K配制的GAM-HRP,37℃孵育30min后,洗板机洗板5次,加入100ul/孔显色液,37℃孵育15min后,用终止液终止反应,置于酶标仪中用双波长读取信号值,根据实验结果,挑选对应阳性孔细胞进行下一步工作。
3.7杂交瘤细胞的克隆化:采用有限稀释法,先把细胞按一定浓度进行梯度稀释,然后接种到96孔细胞培养板的每个孔中,尽可能使孔内只有一个细胞生长。杂交瘤单克隆阳性细胞株重复克隆至少3次,最后一轮为100%阳性后确认为稳定克隆株。
筛选出抗体分别如表1所示:
表1.SEZ6L2融合筛选细胞株及其抗原反应性
3.8抗体分型:
抗原S3包被的板中平行加入50ul/孔稳定细胞株上清,于37℃培养箱放置30min后,洗板5次,拍干后加入50ul/孔IgG1、IgG2a、IgG2b、IgG3、IgM分型酶,反应30min后,洗板加入100ul/孔显色液,15min后用终止液终止读板,分型结果如表2所示。
表2.SE6L2筛选获得细胞株分型结果
4.单抗制备
4.1单抗腹水的生产
致敏BALB/c小鼠,1周后,将对数生长期的稳定杂交瘤细胞重悬以1500rpm离心5min收集细胞,沉淀细胞用无血清培养液悬浮,并将细胞数调至(1-2)×10
4.2单抗制备
收集的腹水经硫酸铵沉淀和Protein A亲和层析纯化(购自美国GE公司),纯化获得的单克隆抗体经12%SDS-PAGE跑胶鉴定,纯度均在90%以上。
三、抗SEZ6L2蛋白小鼠单克隆抗体酶联免疫(EIA)配对筛选
以20mmol/L PB7.4作为包被缓冲溶液,按照5ug/mL,100ul/孔,37度2小时将第一种抗体包被于辐照板上;利用辣根过氧化物酶HRP,按照1:1的比例标记第二种抗体,标记终浓度为1mg/mL,标记使用浓度为1:1000。将实施例2中获得的8株抗体依次进行配对,以进行8*8的抗体正交配对评价,评价样本为1000ng/mL抗原S1、1000ng/mL S2以及10mmol/L的PBS,评价结果如表3所示,其中标记中的A1、A10、B4、B8、G2、G7因整体配对活性太低,舍弃,包被中A1、A3、A10、B8、G2、G7因整体配对活性太低,舍弃,保留标记A3及F3,保留包被B4及F3进行进一步配对筛选。
表3 SEZ6L2抗体正交配对结果
/>
/>
将上述结果中获得的2个标记及2个包被,进一步利用S1、S3抗原及S4表达上清进行检测区段鉴定及配对检测灵敏度比较,抗原浓度为1000ng/ml的S4细胞上清原倍使用,包被浓度不变,酶使用浓度提高到1:100,配对结果如表4所示,结果显示,4个配对均识别SEZ6L2的1-395aa区段,其中A3标记整体检测灵敏度低于F3标记,并且存在一定非特异性,B4-F3配对整体检测灵敏度及特异性更优,进行进一步样本评估。
表4.SEZ6L2配对检测区段鉴定
四、SEZ6L2抗体配对临床样本分析性能评估
1、血清样本评估
1.1MS与正常人样本对比:
收集MS血清33例及正常人血清60例,用上述配对B4-F3评估对临床样本的检测效果。具体方法:将所有样本和梯度稀释的S1抗原100ul/孔加入到B4包被抗体的酶标板中,37℃孵育30min,洗板5次,加入100ul/孔1:200稀释的F3-HRP,37℃继续反应30min,洗板5次,加入100ul/孔的显色液,37℃显色反应15min后终止,酶标板读数,利用S1标准曲线返算样本中SEZ6L2浓度,将浓度结果用Graphpad Prism 8.0进行数据的统计学分析。结果如图1所示,正常人血液样本中的SEZ6L2水平显著高于MS患者,提示血样中SEZ6L2水平可以用于MS诊断。
1.2NMOSD与MS样本对比
收集MS血清33例及NMOSD血清48例,用上述配对B4-F3评估对临床样本的检测效果。具体方法:将所有样本和梯度稀释的S1抗原100ul/孔加入到B4包被抗体的酶标板中,37℃孵育30min,洗板5次,加入100ul/孔1:200稀释的F3-HRP,37℃继续反应30min,洗板5次,加入100ul/孔的显色液,37℃显色反应15min后终止,酶标板读数,利用S1标准曲线返算样本中SEZ6L2浓度,将浓度结果用Graphpad Prism 8.0进行数据的统计学分析。结果如图2所示,NMOSD患者血样中的SEZ6L2水平显著高于MS患者,提示血样中SEZ6L2水平可以用于甄别MS与NMOSD患者。
1.3MS、NMOSD及正常人样本对比结果
将MS、NMOSD及正常人血样中的SEZ6L2水平对比结果如图3所示,提示血样中的SEZ6L2水平可以用于诊断MS,进一步甄别NMOSD与MS患者。
2、脑脊液样本评估
2.1MS与其他非MS疾病脑脊液样本比较
收集MS、NON-MS脑脊液样本各33、30例,分析结果如图4所示,多发性硬化患者脑脊液中SEZ6L2水平显著高于非多发性硬化患者。
2.2MS、NMOSD及非脱髓鞘疾病脑脊液样本比较
将MS、NMOSD及非脱髓鞘疾病脑脊液样本各33、30及48例的SEZ6L2水平对比如图5所示,视神经脊髓炎谱系疾病患者脑脊液中的SEZ6L2水平显著高于多发性硬化患者,进一步高于其他非脱髓鞘疾病患者,提示脑脊液SEZ6L2水平可以用于多发性硬化及视神经脊髓炎谱系疾病的诊断,进一步可以用于多发性硬化及视神经脊髓炎谱系疾病的甄别。
3、SEZ6L2体液水平ROC曲线分析
以Graphpad Prism 8.0进行ROC曲线分析。
3.1SEZ6L2体液水平在多发性硬化诊断中的ROC曲线分析
3.1.1血液样本
利用软件分别分析SEZ6L2血液样本水平在多发性硬化诊断中的ROC曲线面如图6所示,结果显示血样中的SEZ6L2分别对多发性硬化诊断有明显临床价值。
3.1.2脑脊液样本
利用软件分别分析SEZ6L2血液样本水平在多发性硬化诊断中的ROC曲线面如图7所示,结果显示脑脊液的SEZ6L2分别对多发性硬化诊断有一定临床价值,但是不如血样中显著。
3.2SEZ6L2体液水平在多发性硬化疾病及视神经脊髓炎谱系疾病甄别中的ROC曲线分析
3.2.1血液样本
利用软件分别分析SEZ6L2血液样本水平在多发性硬化和视神经脊髓炎谱系疾病的ROC曲线,结果如图8所示,结果显示血液样本中的SEZ6L2水平分别对多发性硬化与视神经脊髓炎在临床上的甄别有明显的价值。
3.2.2脑脊液样本
利用软件分别分析SEZ6L2脑脊液样本水平在多发性硬化和视神经脊髓炎谱系疾病的ROC曲线,结果如图9所示,结果显示脑脊液样本中的SEZ6L2水平分别对多发性硬化与视神经脊髓炎在临床上的甄别有明显的价值。
综上,本发明提供一种通过检测人体生物样本中生物标记物SEZ6L2基因或其片段的mRNA或编码蛋白的表达水平诊断MS的方法,本发明方法可量化、操作更便捷,对操作人员专业性要求不高,比现有诊断方法更客观、更有利于开展规模化筛查工作,更有利于疾病的发现和确诊以及提供有针对性的个体化治疗方案。
虽然以上描述了本发明的具体实施方式,但是熟悉本技术领域的技术人员应当理解,我们所描述的具体的实施例只是说明性的,而不是用于对本发明的范围的限定,熟悉本领域的技术人员在依照本发明的精神所作的等效的修饰以及变化,都应当涵盖在本发明的权利要求所保护的范围内。
- 与多发性骨髓瘤诊断与预后相关的RAB3B生物标记物及其应用
- TREM-2在制备多发性硬化症的治疗药物和/或诊断试剂中的应用
