一种NO-S-S-AurB耦合物及其制备方法与应用
文献发布时间:2024-07-23 01:35:21
技术领域
本发明涉及一种NO-S-S-AurB耦合物和NO-S-S-AurB耦合物的制备方法,以及NO-S-S-AurB耦合物在抗TNBC的活性和选择性的药物中的应用,属于医药技术领域。
背景技术
乳腺癌是女性常见的恶性肿瘤之一,是全球女性的第二大死亡原因。美国癌症协会公布的2021癌症年度统计报告结果提示,癌症死亡率从1991年的215.1/100000的峰值下降到2018年的149.0/100000,虽然癌症死亡率在逐年下降,但乳腺癌发病率已超越肺癌,成为全球发病率最高的癌症,发病率位居女性恶性肿瘤首位,极大危害着女性的生命安全。三阴乳腺癌(TNBC)是乳腺癌的一种分型,指癌组织免疫组织化学检查结果为雌激素受体(ER)、孕激素受体(PR)和原癌基因(Her-2)均为阴性的乳腺癌,约占所有乳腺癌类型的15%20%。当前对TNBC发病的分子机制研究有限,缺乏明确的治疗靶点,且由于其复发风险高,转移潜力大,预后极差,晚期TNBC患者5年内生存率极低。临床常规的乳腺癌治疗方法,比如激素疗法和Her-2靶向疗法对TNBC几乎没有治疗效果,临床治疗方案选择十分有限,传统的化疗仍是治疗TNBC的主流方法,目前临床上使用的一线化疗药物主要为蒽环类、紫杉醇类、环磷酰胺类、铂类等,然而传统的化疗存在明显的缺点,如耐药性及各种毒副作用等。目前唯一显著延长TNBC患者总生存期的药物是2020年由FDA加速批准上市的Trodelvy,Trodelvy是一种靶向Trop-2蛋白并与拓扑异构酶I抑制剂SN-38连接的ADC药物,用于治疗晚期TNBC患者。尽管Trodelvy的上市标志着TNBC治疗的重大进步,但当前对TNBC发病的分子机制研究不足,临床上可选择的疗法依然有限。因此,亟需寻找治疗TNBC的潜在靶向药物。
Aurovertins化合物是一类从大型真菌子实体Calcarisporium arbuscular发酵液中分离得到的多烯-吡喃酮类衍生物,是一种高度还原的聚酮,它含有2,6-二噁二环-[3,2,1]-辛烷环核心结构,通过三烯连接链与甲基化的-吡喃酮连接。自1964年鉴定出aurovertins AD以来,目前已发现的aurovertins化合物有21种,其中AurB能选择性抑制TNBC细胞的生长,在非细胞毒剂量时在体外对多种TNBC细胞株均有显著的抗转移作用。虽然aurovertins具有多方面的生物活性,但该类化合物毒性很大。研究人员将该类化合物分别注射至兔子和狗体内,给药剂量达1mg/kg时,它们在50分钟内均死亡。结果表明,该类化合物毒性较大,不适合直接开发成药,需要对其进行结构优化,当前对AurB构效关系的研究不足,结构修饰缺少目的性。
一氧化氮(NO)是有机体内重要的信号分子,可以参与多种生理功能的调节,也可以影响肿瘤细胞的生长、增殖和转移、血管生成以及促进肿瘤细胞的凋亡过程。NO供体药物也已成为抗肿瘤药物研究的热点,低浓度NO能促进肿瘤血管生长,而高浓度NO则能通过直接或间接方式发挥抗肿瘤作用。NO供体是指在体内经酶或非酶作用后能够释放NO的化合物,该类化合物可以克服NO本身难携带、难定量、半衰期短等缺点。现有的供体按化学结构可分为有机硝酸酯类、金属NO复合物类、呋咱氮氧化物类、偶氮二醇烯鎓盐类等。其中呋咱氮氧化物类供体较之其他供体释放NO更加稳定持久,其NO释放活性更强,并在游离巯基和巯基阴离子作用下均可释放NO,而经典的硝酸酯类NO供体需在游离巯基作用下才可释放NO。由于体内游离巯基基团分布很广,呋咱氮氧化物可在多种组织或器官中通过非酶催化途径释放NO而产生生物活性。
孪药(Twin drug)是指通过共价键将两种或多种药理活性相近的化合物缀合成新的药物分子,在体内经过一系列代谢作用将母体药物释放出来。设计的孪药兼容母体药物的特性,或改善药物原有的理化性质,或提高药物选择性及活性,或产生新的药理活性等。孪药设计在神经退行性疾病、精神疾病、恶性肿瘤治疗中较为常见。
本发明选用一种可断裂的二硫键作为连接链,将AurB和NO供体拼合制成一种可分解的孪药,该耦合物在体内基于氧化还原响应发生自消除(self-immolative)将原药释放出来。由于肿瘤具有GSH高表达的特性,因此本发明有望提高AurB抗TNBC的活性和选择性。
发明内容
为达到上述目的,本发明提供了一种NO-S-S-AurB耦合物和NO-S-S-AurB耦合物的制备方法,以及NO-S-S-AurB耦合物在制备抗TNBC的活性和选择性的药物中的应用,
第一方面,本发明提供了一系列可释放的NO-aurovertin B耦合物(6a-8g):
第二方面,本发明提供了一系列可释放的NO-S-S-AurB耦合物在制备抗TNBC的活性和选择性的药物中的应用。
第三方面,本发明提供了一系列可释放的NO-S-S-AurB耦合物的制备方法,所述方法包括以下步骤:
步骤一,一氧化氮供体及其衍生物的合成:
步骤(i)和(ii):取苯硫基乙酸于圆底烧瓶中,加入冰醋酸,冰浴,缓慢滴加30%过氧化氢,滴毕,常温反应3-5h,TLC监测反应。反应结束后,冰浴,缓慢滴加发烟硝酸,之后将反应液置于80℃水浴锅中回流反应3h,反应结束后冷却至室温,将反应液置于-20℃防爆冰箱静置一夜,待白色针状晶体大量析出后,过滤并用少量水洗涤,收集固体,干燥称重得到产物2。
步骤(iii):取产物2于圆底烧瓶中,加入四氢呋喃溶解,冰浴条件下反应,加入NaOH溶液,室温下反应,TLC监测反应,待反应终止,用水和乙酸乙酯少量多次萃取,减压浓缩得粗品。粗品用粗硅胶柱层析,以石油醚:丙酮洗脱,减压浓缩得化合物4a-4e。
步骤(iv):取产物2于圆底烧瓶中,加入二氯甲烷,冰浴反应,加入DBU,室温下反应3h,TLC监测反应,待反应终止,用水和乙酸乙酯少量多次萃取,减压浓缩得粗品。粗品用粗硅胶柱层析,以二氯甲烷:甲醇洗脱,减压浓缩得化合物4f-4g。
进一步,所述步骤(iii)中,所述NaOH溶液的浓度为25%,用量为产物2的2.5倍,且常温下反应时间为2.5-3.5h。在该反应中氢氧化钠溶液的浓度不能过高,要适量,且反应时间不可过长,否则会导致3号位苯磺酰基也会被取代,生成双取代副产物。
步骤二NO-S-S-AurB耦合物的合成:
步骤(a):取2,2-二硫代二乙酸溶于二氯甲烷中,加入DMAP和DCC,室温下反应后加入AurB,室温下反应。TLC监测反应,待反应终止,悬干,加入乙醚过滤,取过滤液减压浓缩得粗品,粗品用粗硅胶柱层析,以石油醚:丙酮洗脱,减压浓缩得黄色油状物。取3,3-二硫代二丙酸(4,4-二硫代二丁酸)和DMAP溶于二氯甲烷中,室温下反应后加入AurB和EDCI,室温下反应。待反应终止,用水和二氯甲烷萃取,取减压浓缩得粗品。粗品用粗硅胶柱层析,以石油醚:丙酮洗脱,减压浓缩得黄色油状物,5X1,5X2,5X3。
步骤(b):分别取5X1,5X2,5X3和DMAP溶于适量二氯甲烷,室温下反应后分别加入4a-4e和EDCI,室温下反应,TLC监测反应,待反应终止,用水和二氯甲烷萃取,取减压浓缩得粗品。粗品用粗硅胶柱层析,以石油醚:丙酮洗脱,减压浓缩得黄色油状物,6a-6e,7a-7e,8a-8e。
步骤(c):分别取5X1,5X2,5X3和HOBT溶于适量二氯甲烷,室温下反应后分别加入4f-4g和EDCI,室温下反应,TLC监测反应,待反应终止,用水和二氯甲烷萃取,取减压浓缩得粗品。粗品层析分析,梯度洗脱,减压浓缩得白色固体,6f-6g,7f-7g,8f-8g。
进一步,所述步骤(a)中,所述2,2-二硫代二乙酸、DMAP、DCC催化剂的量之比为1.1:0.5:2。在2,2-二硫代二乙酸与AurB的反应过程中,要注意催化剂DMAP的量,DMAP碱性较强,投料量过多会导致二硫键断裂,生成巯基乙酸与AurB耦合的副产物。且缩合剂不能使用EDCI,使用EDCI反应不发生,且反应液由黄色澄清液变成棕褐色浑浊液。
进一步,所述步骤(a)中,所述3,3-二硫代二丙酸(4,4-二硫代二丁酸)、DMAP、AurB、EDCI量之比为1.1:0.5:1:1。在3,3-二硫代二丙酸(4,4-二硫代二丁酸)与AurB的反应过程中,要注意DMAP和EDCI的量,且反应时间不宜过长,二硫键在碱性环境下容易断裂,生成相关副产物。
进一步,所述步骤(b)中,在分离纯化过程中,要将Rf值压到0.1以下。在分离纯化过程中,要将Rf值压到0.1以下,才能够分离到较多纯化合物。
进一步,所述步骤(c)中,所述粗品用用RP-18反向柱层析,以甲醇:水=40:60→100:0梯度洗脱。步骤(c)需要将HOBT和DMAP搭配使用,反应产率较高,但是分离比较困难。f和g系列化合物不适宜用硅胶柱层析,容易吸附,产率很低。使用反向柱层析分离产物,不易吸附,分离产率和纯度都较高。
与现有技术相比,本发明的有益效果在于:
本发明利用肿瘤组织中谷胱甘肽(GSH)高表达的特性,引入GSH敏感的二硫键自消除连接链,基于自消除策略合成NO-AurB耦合体,将苯磺酰基呋喃氮氧化物类NO供体与AurB拼合制成孪药,合成了3个系列共20个衍生物,并通过波谱表征确认其化合物结构,合成的NO-AurB耦合体中的AurB和NO供体的连接形式是二硫键,这样的结构可以被高表达谷胱甘肽酶的肿瘤细胞剪切,从而在肿瘤组织中靶向释放两部分药物。
本发明提供了一种基于自消除策略合成NO-AurB耦合体的制备方法,路线合理,产物产率高、便于分离,纯度高。
本发明合成的NO-AurB耦合体对三阴乳腺癌MDA-MB-231细胞具有显著的抑制作用,抑制效果明显强于阳性药紫杉醇及母药AurB,对小鼠三阴乳腺癌4T1细胞也表现出良好的抑制作用,说明该系列NO-AurB耦合体显著提升了母药AurB抗TNBC的活性和选择性。
附图说明
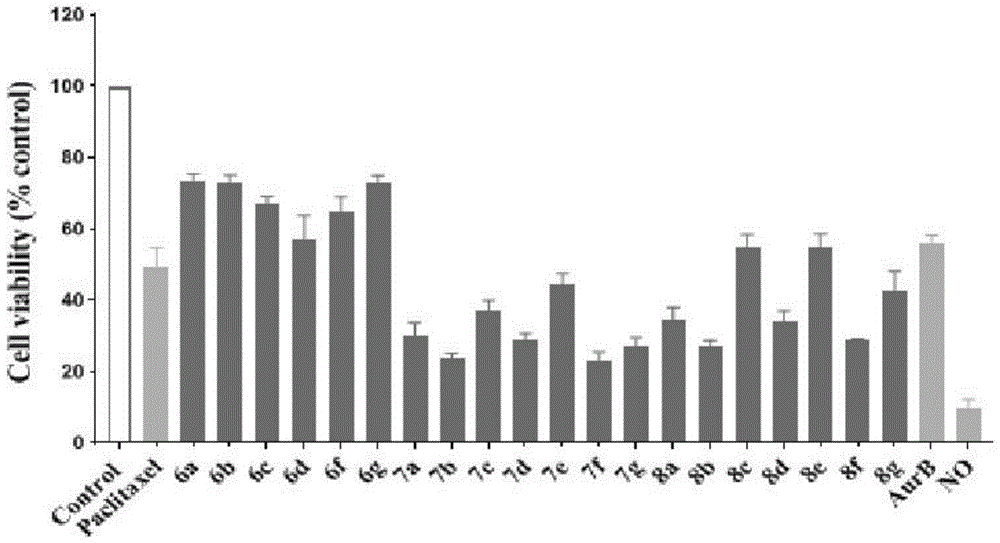
图1为耦合物对MDA-MB-231细胞存活率评价
图2为耦合物对4T1细胞存活率评价
图3为耦合物对A549细胞存活率评价
图4为各浓度6g,7g,8g,2*对MDA-MB-231和4T1细胞的抑制率
具体实施方式
为使本发明的目的、技术方案及优点更加清楚明白,以下结合实例,对本发明进一步详细的说明。应当理解,此处所述的具体实施例用以说明本发明,并不用于限定本发明的范围。
实验材料与设备
实验仪器
实验所需主要实验仪器与设备见表1。
表1实验仪器与设备
实验试剂
实验所需主要化学试剂见表2。
表2实验试剂
注:AurB来源于大型真菌子实体Calcarisporium arbuscula的次级代谢产物。
符号说明
实施例1一氧化氮供体及其衍生物的合成
一氧化氮供体及其衍生物的合成路线如下:
步骤(i)和(ii):取苯硫基乙酸于圆底烧瓶中,加入冰醋酸,冰浴,缓慢滴加30%过氧化氢,滴毕,常温反应3-5h,TLC监测反应。反应结束后,冰浴,缓慢滴加发烟硝酸,之后将反应液置于80℃水浴锅中回流反应3h,反应结束后冷却至室温,将反应液置于-20℃防爆冰箱静置一夜,待白色针状晶体大量析出后,过滤并用少量水洗涤,收集固体,干燥称重得到产物2。
步骤(iii):取1eq.NO供体于圆底烧瓶中,加入5mL四氢呋喃溶解,冰浴条件下反应5min,加入2.5eq.25%的NaOH溶液和5eq.3a-3e,室温下反应3h,TLC监测反应(以石油醚:丙酮=3:1为展开剂,产物点Rf值约为0.2),待反应终止,用水和乙酸乙酯少量多次萃取,减压浓缩得粗品。粗品用200-300目粗硅胶柱层析,以石油醚:丙酮=3:1洗脱,减压浓缩得化合物4a-4e,为白色粉末状固体,以NO供体投料量计算收率,4a-4e为50%-95%。
步骤(iv):取1eq.NO供体于圆底烧瓶中,加入5mL二氯甲烷,冰浴反应5min,加入3eq.的DBU和5eq.3f-3g,室温下反应3h,TLC监测反应(以二氯甲烷:甲醇=10:1为展开剂,产物点R
实施例2:NO-S-S-AurB耦合物的合成
NO-S-S-AurB耦合物的合成路线如下:
步骤(a):取1.1eq.2,2-二硫代二乙酸溶于二氯甲烷中,加入0.5eq.DMAP和2eq.DCC,室温下反应2h后加入1eq.AurB,室温下反应24h。TLC监测反应,待反应终止,将二氯甲烷悬干,加入乙醚过滤三遍,取过滤液减压浓缩得粗品,粗品用200-300目粗硅胶柱层析,以石油醚:丙酮=3:2洗脱,减压浓缩得黄色油状物。取1.1eq.3,3-二硫代二丙酸(4,4-二硫代二丁酸)和0.5eq.DMAP溶于二氯甲烷中,室温下反应20min后加入1eq.AurB和1eq.EDCI,室温下反应24h。待反应终止,用水和二氯甲烷少量多次萃取,取二氯甲烷层减压浓缩得粗品。粗品用200-300目粗硅胶柱层析,以石油醚:丙酮=3:2洗脱,减压浓缩得黄色油状物,以AurB投料量计算收率,化合物5X1为60%,5X2为85%,5X3为88%。
步骤(b):分别取1eq.5X1,5X2,5X3和0.5eq.DMAP溶于适量二氯甲烷,室温下反应20min后分别加入1eq.4a4e和1eq.EDCI,室温下反应24h。TLC监测反应,待反应终止,用水和二氯甲烷少量多次萃取,取二氯甲烷层减压浓缩得粗品。粗品用200-300目粗硅胶柱层析,以石油醚:丙酮=3:1洗脱,减压浓缩得黄色油状物,以AurB投料量计算收率,化合物6a-6e为60%-88%,7a-7e为65%-90%,8a-8e为70%-90%。。
步骤(c):分别取1eq.5X1,5X2,5X3和1eq.HOBT溶于适量二氯甲烷,室温下反应20min后分别加入1eq.4f-4g和1eq.EDCI,室温下反应24h。TLC监测反应(以石油醚:丙酮=3:2为展开剂,产物点Rf值约为0.2),待反应终止,用水和二氯甲烷少量多次萃取,取二氯甲烷层减压浓缩得粗品。粗品用RP-18反向柱层析,以甲醇:水=40:60→100:0梯度洗脱,减压浓缩得白色固体,以AurB投料量计算收率,化合物6f-6g为79%-83%,7f-7g为85%-87%,8f-8g为82%-88%。
部分化合物波谱表征确认其化合物结构如下
表3部分化合物核磁共振谱图及质谱数据
实施例3:AurB-NO耦合物对MDA-MB-231细胞,4T1细胞及A549细胞的活性研究
1.实验仪器
本实验所需的主要实验仪器见表4。
表4实验仪器与设备
2.实验试剂
本实验所需的主要化学试剂见表5。
表5实验材料及试剂
主要试剂配制
DMEM完全培养基:将50mL FBS和5mL青霉素-链霉素溶液加入445mL DMEM中,摇匀,4℃备用。
RPMI-1640完全培养基:将50mL FBS和5mL青霉素-链霉素溶液加入445mL RPMI-1640中,摇匀,4℃备用。
10%过硫酸铵(APS)溶液:称取1g APS于离心管中,加入10mL超纯水,涡旋溶解。
10%分离胶:向烧杯中加入5.9mL超纯水,5mL的Acrylamide Bis,3.8mL的1.5MTris-HCl(pH 8.8),0.15mL的10%SDS,0.15mL的10%AP,0.015mL TEMED,搅拌混匀。
5%浓缩胶:向烧杯中分别加入4.2mL超纯水,1mL Acrylamide Bis,0.76mL 0.5MTris-HCl(pH 6.8),0.06mL 10%SDS,0.06mL 10%AP,0.006mL TEMED,搅拌混匀。
电泳液:量取100mL电泳液(10×),900mL超纯水于烧杯中,搅拌均匀。
电转液:称取2.42g Tris-base,11.5g甘氨酸于烧杯中,加入800mL蒸馏水,搅拌溶解后再加入200mL甲醇,混匀,用于电转,现配现用。
TBS缓冲液(10×):称取24.2g Tris-base,80g NaCl于烧杯中,加入1000mL蒸馏水,搅拌溶解后用HCl调节pH=7.6。
TBST缓冲液:将100mL TBS缓冲液(10×)和1mL Tween-20加到900mL超纯水中,搅拌混匀。
5%封闭液:称取5g脱脂奶粉于烧杯中,加入100mL TBST缓冲液,搅拌溶解,可回收重复使用,-20℃储存。
化合物储备液:分别称取适量化合物于EP管中,加入对应体积的DMSO溶液,涡旋溶解,配制成20mM化合物储备液,-20℃储存。
MTT溶液:称取1g的MTT粉末于烧杯中,加入200mL的PBS,避光超声溶解,4℃避光储存。
3.实验方法
3.1细胞培养条件
MDA-MB-231细胞:来自中国科学院细胞库。培养条件:DMEM完全培养基(含10%FBS及1%PS),5%CO
4T1细胞:来自ATCC(美国典型培养物保藏中心)。培养条件:RPMI-1640完全培养基(含10%FBS及1%PS),5%CO
A549细胞:来自中国科学院细胞库。培养条件:RPMI-1640完全培养基(含10%FBS及1%PS),5%CO2,37℃恒温培养。
3.2细胞复苏、传代及冻存
(1)细胞复苏
自液氮中取出细胞株冻存管,将冻存管插在浮漂上置于37℃恒温水浴锅中快速融化解冻。将融化的细胞悬液转入提前准备好的15mL离心管中(内含5mL培养液),1000rpm的速度下离心10min,弃上清,用1mL新鲜培养基重悬细胞,随后转移至培养瓶,于37℃,5%CO
(2)细胞传代
从培养箱中取出培养瓶,吸弃旧的培养液,用2mL PBS冲洗2遍。加入1mL胰酶溶液,摇匀,置于37℃恒温培养箱孵育1-3min。观察细胞生长状态,加入培养液终止消化,吹打混匀后转移至合适的离心管,1000rpm的速度下离心5min。弃上清,加入新鲜培养基重悬,取适量悬液于含有适量完全培养基培养瓶中,转移至恒温培养箱继续培养。
(3)细胞冻存
当细胞融合度达80%时进行冻存,吸弃旧培养基,用PBS清洗三遍,加入1mL胰酶溶液消化,观察细胞变圆后,加入新鲜培养基终止消化。混匀后将悬液转移至事先准备好的15mL离心管中,1000rpm离心机离心5min,弃上清,加入1mL细胞冻存液,吹打重悬。将细胞悬液转至预先准备好且温度恢复至室温的冻存管中,拧紧冻存管盖,将冻存管放入-80℃冰箱,24h后将细胞转移至液氮罐。
3.3细胞增殖实验
使用MTT法测定系列耦合物抗TNBC细胞增殖活性。其作用机制为外源性MTT在活细胞中还原为不溶于水的蓝紫色结晶并沉积,而死细胞中无法沉积,因此可以利用沉积结晶量来判断细胞毒性。活细胞中的甲臜可溶于DMSO,用酶标仪测定其吸光值,可计算细胞存活数量。
(1)细胞计数及铺板
当细胞融合度达80%时,从培养箱中取出培养瓶,吸弃旧培养液,用2mL PBS冲洗2遍,加入1mL胰蛋白酶溶液,摇匀,置于37℃培养箱孵育1-3min。显微镜下观察细胞变圆后,加入适量培养液,终止消化,吹打混匀后转移至合适的离心管,离心5min(1000rpm)。吸弃上清,加入新鲜培养基重悬。吸取适量细胞混悬液,转移至血球计数板中,计数。
用移液枪将适量均等的细胞悬液转移至96孔板中,在孔板最外层背景板中加入PBS,铺板结束后,轻轻敲打96孔板侧壁,使孔板中的细胞分布均匀,并在显微镜下观察均匀程度,随后放入37℃恒温培养箱培养24h。
(2)加药
化合物初筛时加药:根据样品的计算结果用相应培养基稀释样品,将不同浓度稀释后的样品加入到96孔板中,每孔加入10μL,使药品在每孔中的终浓度为10μM,每个样品三个复孔。向空白对照组加入10μL的新鲜培养基。加样结束后,轻轻拍打96孔板,置于37℃细胞培养箱培养48h。
测定IC
(3)OD值的检测
给药处理48h后,每孔加入20μLMTT溶液(5mg/mL),37℃继续孵育3h。终止培养,用移液枪轻轻吸去培养液,每孔加入100μL DMSO,摇床轻微振荡,使结晶物完全溶解,用酶标仪测定其490nm吸光度。按公式计算细胞相对存活率:
相对存活率(%)=OD
4.结果与讨论
耦合物NO-S-S-AurB活性检测结果
如图1-3所示,以10μM的浓度分别将耦合物NO-S-S-AurB(6a-8g)给药48h后测得细胞存活率,可得耦合物对MDA-MB-231细胞有显著的抑制作用,抑制效果明显强于阳性药紫杉醇及母药AurB,对4T1细胞也表现出良好的抑制作用,但对肺癌A549细胞无明显细胞活性。结果表明该系列耦合物对三阴乳腺癌细胞具有选择性,能选择性抑制三阴乳腺癌细胞活性,而对肺癌细胞无明显抑制作用。反观NO供体对以上三株细胞均具有较强的抑制作用,并不具备选择性。综上可知,合成的系列化合物活性与最初设计思路基本一致,提高了母药AurB抗TNBC细胞的活性和选择性,且显著提升了NO供体对TNBC细胞的选择性。观察化合物6a-8g对三阴乳腺癌MDA-MB-231和小鼠乳腺癌细胞4T1细胞抑制作用。
耦合物NO-S-S-AurB IC50测定结果
选择化合物6b、6g、7b、7d、7f、7g、8b、8d、8f、8g及2(NO供体)针对MDA-MB-231及4T1细胞测定IC50值,实验结果见表6及图4。
表6各耦合物对MDA-MB-231和4T1细胞的抑制率
注:ND=Not Determined;NA=Not available;2*=control group(NO donor)
在所有化合物中6g、7g、8g及2的活性及稳定性较好,对MDA-MB-231的IC50值分别为4.32μM、1.41μM、2.42μM及1.32μM,而对4T1的抑制作用不及MDA-MB-231。其中化合物7g对MDA-MB-231细胞的IC50值与对照组2接近,但选择性较2明显提高。结果表明以上几种化合物对TNBC细胞具有选择性抑制作用,而对照组2对这两株细胞均具有较强的抑制作用,说明耦合物显著提升了对照组2的选择性。
实施例3选取了MDA-MB-231细胞,4T1细胞及A549细胞三株肿瘤细胞,对合成的20个NO-S-S-AurB耦连物进行了活性初筛检测。初步的实验结果表明,合成的耦合物在相同浓度下,能显著抑制MDA-MB-231细胞增殖,抑制效果明显强于阳性药紫杉醇及母药AurB,对4T1细胞也表现出良好的抑制作用,但对肺癌A549细胞无明显细胞活性。进一步的IC50结果表明,在所有化合物中6g、7g、8g及NO供体的活性及稳定性较好,IC50分别为4.32μM、1.41μM、2.42μM及1.32μM,其中化合物7g对MDA-MB-231细胞表现出较强的抑制作用和选择性,IC
- 一种红树内生真菌来源的1,4-萘醌类化合物及其制备方法和在制备抗炎药物中的应用
- 一种三萜类化合物及其制备方法和在制备抗癌药物中的应用
- 一种光热增强降解化学战剂模拟物的纳米核壳复合物及其复合纤维膜的制备方法与应用
- 一种金属氧化物纳米白芨地龙蛋白复合物制备方法及应用
- 咪唑类离子多孔有机聚合物及制备和催化CO2与环氧化物耦合制备环状碳酸酯的应用方法
- 金属耦合三嗪多孔有机框架及其构筑方法和催化CO2与环氧化物耦合制备环状碳酸酯应用
