用于体内支气管再生的方法和装置
文献发布时间:2023-06-19 12:24:27
相关申请的交叉引用
2018年10月5日提交的美国临时专利申请系列号62/741,544、和2018年10月4日提交的美国临时专利申请系列号62/740,962,前述的全部公开内容通过引用结合在此。
技术领域
本申请涉及在支气管吻合处或靠近支气管吻合处促进和/或实现体内组织再生的合成细胞递送装置。
背景技术
肺切除术公知对于非小细胞肺癌的管理具有高手术后死亡风险,并且其也与长期心肺并发症的增加的风险相关,对生活质量和长期生存具有不良影响。为了避免肺切除术的并发症,袖式叶切除术应运而生作为中心型非小细胞肺癌的情况中的优选操作,因为其有利于保留肺实质并由此提供更好的生活质量。然而,该技术的使用有时在大支气管疾病中不可用,这是因为支气管端部对于进行安全的无张力吻合而言过远。此外,袖式叶切除术疑似有更高的癌细胞的局部复发率。其选择性使用可提供更符合解剖学的气道再生/重建。这将使得器官切除的纳入时间(inclusion time)更长,具有更高的安全保障,因此降低局部复发的风险和进行肺切除术的必要性。
本文公开了解决或消除可在包括但不限于袖式叶切除术的过程中出现的一个或多个问题和并发症的方法和装置。
因此,需要可临床上有利地促进中空器官、如肺系统中的中空器官等的切除的支气管替代品。需要可完全替代中空器官的受损部分并允许受损区域的完全重建的支气管替代品。需要允许替代品的在内窥镜下插入的方法,其最终导致替代品的彻底移除,使得受损中空器官的引导性组织生长完全重建受损局部区域。
发明内容
含有纺丝聚合物纤维的合成支架提供用于永久性细胞桥的内窥镜递送系统,所述内窥镜递送系统重建气道使得在不轴向移动气道的任一端部的情况下完全修复受损吻合。含有纺丝聚合物纤维的合成支架进一步提供传播从纺丝聚合物纤维扩散至切除的气管的端部的脂肪组织的手段,使得合成支架在最小或不剩余细胞组织、电纺丝纤维、或二者的情况下是可移动的。本教导进一步提供用于由电纺丝纤维和自体或同种异体细胞合成支架的方法,所述支架在内窥镜下插入至肺气道,产生促进引导性组织生长的永久性器官桥,使得合成支架在无细胞材料的情况下是可移动的,并且电纺丝纤维是可移动的或生物可吸收的。
在某些实施方案中,合成支架包括主体部和至少一种定植细胞系。主体部具有第一端和与第一端相对的第二端,并且可至少一部分配置成管状。主体部还具有向外取向表面,所述向外取向表面具有至少一个由纺丝聚合物纤维组成的区域,所述纺丝聚合物纤维具有15nm和10微米之间的平均纤维直径。纺丝聚合物纤维的至少一部分连结来形成具有小于50微米的平均开口区的孔,孔限定存在于向外取向表面上的至少一个多孔区域。至少一种定植细胞单元粘附至限定在主体部的向外取向面上的多孔区域。
还公开用于处理和治疗存在于受试者的呼吸系统中的中空器官中的创伤的方法,所述方法包括以下的步骤:切除受试者的呼吸系统中的管状器官的一部分,产生切除的中空器官部分,其中切除的中空器官部分保留在受试者中。所述方法还包括在切除部位植入合成支架的步骤,合成支架包括外聚合物表面和粘附至合成支架的外聚合物表面的至少一种定植细胞系。以足以沿合成支架实现引导性组织生长的时间间隔、将合成支架保持在切除部位,引导性组织生长源自存在于保留在受试者中的切除的器官部分中的组织或与其接触。在实现引导性组织生长后,从植入部位移除合成支架,所述移除以如下方式进行:使引导性组织生长保持与保留在受试者中的管状器官的切除部分的接触。
在对实施方案、所附权利要求和附图的详细描述中公开了本公开的这些和其它方面。
附图说明
结合附图阅读时,从以下详细描述最好地理解本文的教导。应强调的是,根据惯例,附图的各种特征不是按比例绘制的。相反,为清楚起见,各种特征的尺寸可被任意扩大或缩小。
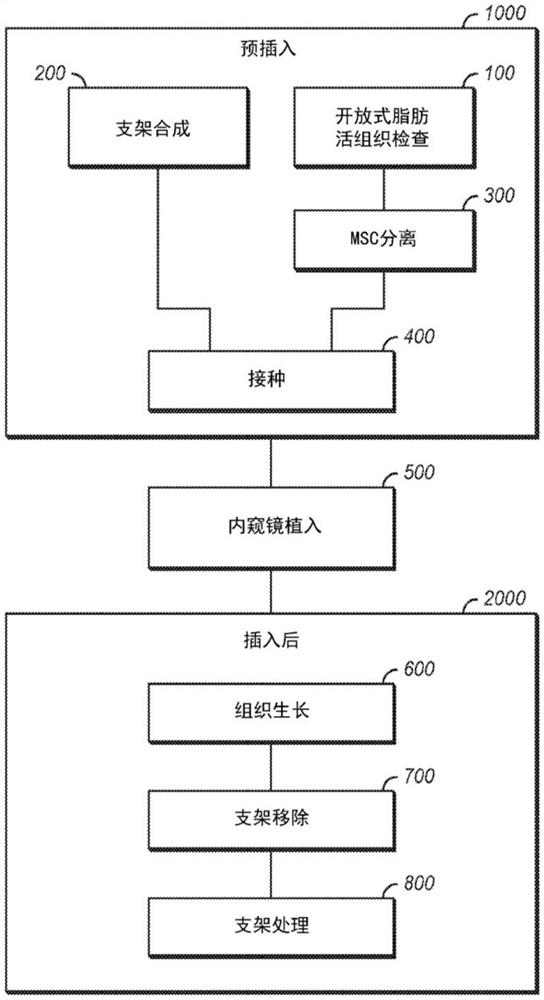
图1是用于处理呼吸系统中的中空器官中的切除的方法的流程图,是根据本文所描述的实施方案的脂肪活组织检查、支架电纺丝、接种、手术植入和相关特征的流程图;
图1A是1000X的放大率下的图1C的合成细胞递送装置的实施方案,主体的纺丝表面的实施方案的局部表面的扫描电子显微镜(“SEM”)图;
图2是根据图1中概述的方法的切除区域的第8天的支气管镜检查图像;
图3是根据图1中概述的方法的切除区域的第8天的支气管镜检查图像;
图4是根据图1中概述的方法的切除区域的第69天的支气管镜检查图像;
图5是从试验受试者移除的支架的第69天的检查;
图6是根据图1中概述的方法的切除区域的支架移除后第76天的支气管镜检查;
图7是根据图1中概述的方法的切除区域的支架移除后第76天的支气管镜检查图像;
图8是移除的气管和周围的肺的图像;
图9是支架移除后第76天的支气管镜检查图像的图像;
图10是概述支气管手术后试验动物的体重变化的图。
图11是具有在部分截面中示出的部分的如本文所公开的合成支架的实施方案的透视图;
图12是如本文所公开的合成支架的实施方案的管状表面的表面的显微照片;
图13是如本文所公开的合成支架的第二实施方案的侧透视图;
图14是在5000X下获得的如本文所公开的合成支架的实施方案的外表面区域的(扫描电子显微镜)SEM显微照片,其显示七天的生物反应后的细胞生长;和
图15是如本文所公开的合成支架的实施方案的外表面区域的显微照片,其显示七天的生物反应后的细胞生长。
具体实施方式
本公开的方面部分涉及以下显著的发现:将临时合成支架插入至存在于受试者的呼吸系统中的中空器官的目标区域,可以促进或增强受试者中新的支气管组织(例如,完整且功能性的支气管)的再生,且无需将支架完全并入至再生的组织中。在某些实施方案中,中空器官是支气管。因此,在一些实施方案中,本公开提供用于促进或增强支气管组织的生长的方法,所述方法包括:将临时合成支架组件递送至受试者的支气管区域,其中临时合成支架组件的递送导致桥连存在于受试者中的吻合的受试者的区域中的新分化的组织的生长。
在一些方面,本公开是部分地基于令人惊讶的发现:本文所述的方法导致例如包括肌肉组织、神经系统组织、或二者的支气管组织等中空器官组织的再生。
本文公开使用接种有例如脂肪来源的间充质干细胞(aMSC)等自体来源的细胞的临时合成支架组件的用于体内支气管再生的方法和装置。临时合成支架组件在植入时支持支气管切除后的支气管组织再生。
临时合成支架组件包括主体部,所述主体部的至少一部分配置成管状构件。主体部具有内表面和相对的外表面,至少一部分的外表面具有限定在其上的多孔区域。合成支架还在覆盖外表面、特别是覆盖多孔区域的至少一部分的细胞层上包括粘附至主体部的多孔区域限定的外表面的至少一种定植细胞系。覆盖外表面的细胞可至少部分地源自其中已可移除地植入临时合成支架组件的相关患者。
还公开了用于使限定在例如支气管等受试者的气道中的吻合处的组织再生的方法,所述方法包括以下的步骤:在靠近限定在支气管中的吻合的位置处植入临时合成支架组件,使得原支气管的至少一个切除边缘与临时合成支架组件的外表面相接触。
在一些实施方案中,临时合成支架组件在生理条件下(例如,在大致对应于组织再生所需时间的时间段内)是可再吸收的或可溶解的。在一些实施方案中,至少一部分的合成支架在合适的生理条件下是可再吸收的或可溶解的。
在一些实施方案中,在形成连接至至少一个切除边缘的再生的功能性支气管组织后,从受试者移除临时合成支架组件。
在一些实施方案中,支架通过具有以下被设计为可容易取回的:a)一种或多种可比缝合线更容易移除的可逆附件,例如,在组织再生后帮助从周围组织分离支架;和/或b)可例如在已从周围组织(例如相邻支气管组织)分离支架后用于帮助取回支架的一个或多个特征。
可逆附件的非限制性实例包括机械机构(例如钩和环,例如内支架(stent)等连接器,或可分离的其它机械附件)和/或化学机构(例如可生物降解或可吸收的附件和/或可通过化学或酶促手段选择性去除的附件)。在一些实施方案中,可使用可吸收钉(absorbablestaple)。在一些实施方案中,可吸收钉包括例如聚乳酸-聚乙交酯(polylactide-polyglycolide)的共聚物、或材料的任何其它可吸收共混物。
在一些实施方案中,支架的手术植入和/或取回可在胸腔镜的辅助下进行。
可帮助取回或移除支架(例如,在已从周围支气管组织分离支架后)的结构特征的非限制性实例包括孔洞、凹口(indent)、凸起、或其它结构特征、或其任何组合,这些结构特征仅位于支架的外表面上。可以使用这些结构特征中的一个或多个来帮助抓住或握住已被用于取回支架的工具(例如,抓紧器)。在一些实施方案中,这些结构特征中的一个或多个可仅位于支架的仅一端部(例如,靠近受试者的口腔的端部)。在一些实施方案中,这些结构特征中的一个或多个可位于支架的两端部或遍及整个支架长度。在一些实施方案中,这些结构特征中的一个或多个仅位于支架的外表面上。在一些实施方案中,这些结构特征中的一个或多个仅位于支架的内表面上。在一些实施方案中,这些结构特征中的一个或多个位于支架的外表面和内表面上。在一些实施方案中,在用于取回支架的一个或多个支架结构的位置处或周围加固支架(例如,支架更厚和/或包括更坚固的材料)。
在一些实施方案中,分离的支架可经由通向支气管的气道的内腔而在内窥镜下移除。在一些实施方案中,分离的支架可以手术移除。
在一些实施方案中,受试者具有患病的(例如,癌性)或受损的支气管或相关的肺。预期如本文所公开的临时支架组件可用于经典肺切除术过程,其中去除患病的肺作为用于给定的受试者的治疗方案的一部分。在某些情况下,可通过使用例如袖式叶切除术等过程来解决治疗问题。认为如本文所公开的临时支架组件可增加其中可成功采用袖式叶切除术以及例如袖式切除术等其它合适的过程的情况。
不受任何特定理论的限制,本文所描述的合成支架促进受试者中新组织(例如,支气管组织)的生长,因此,向受试者提供治疗益处。
在一些实施方案中,新支气管组织的生长导致受试者中功能性支气管的形成。在一些实施方案中,新支气管组织不将支架并入再生的支气管壁。在一些实施方案中,支架被设计并制造成在已再生支气管组织后可吸收的和/或可容易取回的。在一些实施方案中,支架被设计成至少部分地可吸收的。
在一些实施方案中,合成支架的大小和形状近似于被替换的患病的、切除的或受损的(例如,支气管的)区域的大小和形状。
图1中记载如本文所公开的方法的实施方案。作为概括地描述,所述方法包括预插入阶段1000,接着内窥镜植入阶段500和插入后阶段。
在预插入阶段1000中,预期适于接种在支架的表面上的细胞可通过例如附图标记100的开放式脂肪活组织检查等合适的方法来获得。合适的干细胞可通过如附图标记200的合适的方法来分离和扩增。可如附图标记200完成支架合成。在某些实施方案中,具有电纺丝纳米纤维的聚合物结构可通过合适的方法构建。在某些实施方案中,合成方法可为如本公开中所概述的。在某些实施方案中,电纺丝纳米纤维可以是如本公开中所概述的聚合物材料的一种或多种连续线料。在某些实施方案中,电纺丝聚合物材料可以是以下的一种或多种:聚偏二氟乙烯、间规聚苯乙烯、偏二氟乙烯和六氟丙烯的共聚物、聚乙烯醇、聚乙酸乙烯酯、聚(丙烯腈)、聚丙烯腈和丙烯酸的共聚物、聚丙烯腈和甲基丙烯酸酯的共聚物、聚苯乙烯、聚(氯乙烯)、聚(氯乙烯)的共聚物、聚(甲基丙烯酸甲酯)、聚(甲基丙烯酸甲酯)的共聚物、聚对苯二甲酸乙二醇酯、聚氨酯。
如所示的,方法还包括收集可源自合适的来源的合适的干细胞。在某些实施方案中,干细胞可获得自来自寻求治疗的个体的一种或多种自体干细胞收集物。在本公开的范围内,也可采用其它干细胞来源。
获得的干细胞可以在干细胞扩增的合适的方法下适当地处理来获得合适的细胞群以接种在如附图标记222所述生产的聚合物电纺丝结构的表面。合适的细胞扩增技术是本领域技术人员公知的。在某些实施方案中,细胞扩增技术可提供富有例如脂肪来源的间充质干细胞(aMSC)等间充质干细胞(MSC)的培养物。
可如附图标记400进行将合适的干细胞接种至合成的支架上。在某些实施方案中,可将管状支架引入至合适的旋转生物反应器中并且可附接至位于限定在生物反应器中的腔室中的能够在灌注有扩增的细胞材料的液体介质的浴中旋转的支承体。期望或需要时,旋转机构可包括磁力驱动器,其使支承体与附接的支架一起在液浴中沿其纵轴旋转。
通过使细胞溶液沉积在支架外表面上,使聚合物管状结构与液体介质接触来用例如MSC或其它干细胞等细胞接种所生产的支架。随着支架在生物反应器腔室中的液体介质浴中旋转,在存在于支持细胞生长的液体介质中的液体生长培养基中孵育接种的支架。孵育时间间隔可以是足以完成至少一个细胞集落粘附至聚合物管状结构的第一面或外面的时间间隔。在某些实施方案中,孵育时间间隔在24小时和336小时之间。在某些实施方案中,孵育时间间隔可在36小时和336小时之间。在某些实施方案中,孵育时间间隔可在48小时和336小时之间。在某些实施方案中,孵育时间间隔可在72小时和336小时之间。在某些实施方案中,孵育时间间隔可在96小时和336小时之间。在某些实施方案中,孵育时间间隔可在120小时和336小时之间。在某些实施方案中,孵育时间间隔可在144小时和336小时之间。在某些实施方案中,孵育时间间隔可在168小时和336小时之间。在某些实施方案中,孵育时间间隔可在36小时和240小时之间。在某些实施方案中,孵育时间间隔可在36小时和216小时之间。在某些实施方案中,孵育时间间隔可在36小时和192小时之间。在某些实施方案中,孵育时间间隔可在36小时和168小时之间。在某些实施方案中,孵育时间间隔可在72小时和240小时之间。在某些实施方案中,孵育时间间隔可在72小时和216小时之间。在某些实施方案中,孵育时间间隔可在72小时和192小时之间。在某些实施方案中,孵育时间间隔可在72小时和168小时之间。
孵育后,所得的聚合物支架结构将具有粘附至其第一表面或外表面的至少一个细胞集落。在某些实施方案中,所得构建体可具有分散在聚合物支架结构的外表面上的多个离散的细胞集落。在某些实施方案中,细胞材料可在合适的生物材料中作为多个离散的细胞集落存在。在某些实施方案中,所得支架包括与聚合物支架结构的外表面呈覆盖关系的细胞鞘。在某些实施方案中,细胞鞘可具有足以为鞘层提供结构完整性的厚度。鞘层可为连续的或不连续的。在某些实施方案中,可由平均1和100个细胞厚之间的内衬(lining)组成。某些实施方案可具有10和100个细胞之间;10和30个细胞之间;20和30个细胞之间;20和40个细胞之间;20和50个细胞之间;10和20个细胞之间;30和50个细胞之间;30和60个细胞之间;40和60个细胞之间;40和70个细胞之间;70和90个细胞之间的细胞厚度。
在某些实施方案中,聚合物管状结构可在细胞化后在生物反应器中保持一段时间,其后所述结构可被用于如附图标记500的内窥镜植入。
在某些实施方案中,聚合物支架的外表面将具有多孔表面区域,所述多孔表面区域将使一个或多个细胞跨越纤维之间的区域。在某些实施方案中,表面可在表面开口区中具有多个范围为约10nm至约100微米的孔。在某些实施方案中,孔可为不规则形状的且由覆盖的且不同位置的电纺丝纤维限定。不受任何理论的限制,认为如本文所述的方法生产的聚合物管状结构的表面结构,孔径可促进细胞化和/或至少一个细胞集落的细胞粘附。还认为当如本文所公开的细胞递送装置就位时,如本文所采用的的孔径和/或孔构造可预防或减少受试者中的免疫应答或其它不希望的宿主应答。在一些实施方案中,孔具有小于50微米、小于40微米、小于30微米、小于20微米、或小于10微米(例如,约5、约10、或约15微米)的平均孔径。预期使用计算机和/或实验技术(例如,使用孔隙度测定法)计算和/或估算孔径。然而,应理解,在制品的表面上还可存在其它大小的孔。
聚合物管状结构的实施方案的表面的非限制性实例可通过本文所公开的方法来合成和/或可被用于合成细胞递送装置,和可组成图1A中所示的本文所公开的合成细胞递送装置的主体的第一面的至少一部分。图1A中所示的表面301的实施方案包括彼此为覆盖熔合关系的多个电纺丝聚合物纤维部分。各种电纺丝纤维部分包括支承并直接地连接至位于最表面-一次纤维部分(surface-most primary fiber section)310正下方的最表面-二次纤维部分310’的多个最表面-一次纤维部分310。例如上部中间纤维部分312等上部中间纤维可位于最表面-二次纤维部分310’之下并且可与最表面-二次纤维部分310’的一个或多个为熔合关系。应理解,在某些实施方案中,各种纤维部分310、310’、312可由连续的电纺丝纤维组成。在某些实施方案中,各种纤维部分310、310’和312将以通过生产的聚合物管状结构的外表面中的纤维提供通道和连通的方式覆盖另外的内部纤维部分。在某些实施方案中,表面将具有多个限定在最外表面中的表面孔324。在某些实施方案中,至少一部分的孔324可以是非圆形的并且包括由至少两个纤维部分的交叉(intersection)限定的至少一个角域326。
在一些实施方案中,支架将具有至少两层。在某些实施方案中,支架可具有近似的管状结构。图11说明具有近似管状体12的支架10的非限制性实例,所述近似管状体12具有内部取向表面14和外部取向表面16。在一些实施方案中,支架10的侧截面是近似圆形的。在一些实施方案中,侧截面是近似“D”形的。然而,可使用具有其它截面形状的支架10。取决于待再生的相应组织的大小,支架10可具有任何合适的长度和直径。在一些实施方案中,支架10的长度在某些实施方案中可为约1-10cm(例如3-6cm,例如约4cm),或在其它实施方案中为1至3cm长。然而,预期根据应用、患者的需求、和/或在需治疗的支气管或相关肺中的位置,可使用更短或更长的支架10。在一些实施方案中,支架10可具有0.5至5cm的内径。然而,根据应用、患者的需求、和/或在需治疗的支气管中的位置,可使用具有更小或更大内径的支架。
在一些实施方案中,支架10可由单层合成材料组成。然而,在本公开的范围内,支架10可包括多于一层的合成材料。
因此,在一些实施方案中,合成支架10可由多层(例如,2层或多层,例如2、3、4、5层或更多层)组成。在一些实施方案中,一层或多层由相同材料制成。在一些实施方案中,不同层由不同材料(例如,不同聚合物和/或不同聚合物排列)制成。如本文所公开的合成支架10可包括两种或多种不同组件,在存在这些组件时可将其组装以形成支架(例如,细胞化和/或植入之前)。在一些实施方案中,合成支架10包括例如通过用于制造支架10的合成技术来彼此接触的两层或多层。在一些实施方案中,支架10可使用涉及几个步骤的技术来合成,所述步骤导致两层或多层聚在一起。例如,将电纺丝材料的层施涂至预先制造的支架的一部分上,例如电喷涂材料前层(prior layer of electro sprayed material)、电纺丝材料前层、已混入至支架的不同组分的表面(例如,编织管(braided tube)或网状物)、或其两种或多种的组合。
在如图11中所示的实施方案中,支架10包括限定支架主体12的外表面14的至少一个外层18。支架10包括至少一个另外的向内取向层20。在如图所示的实施方案中,至少一个另外的向内取向层20与外层18的向内取向面直接接触。期望或需要时,至少一个向内取向层20可配置成为相关的支架主体12提供结构支承。在图11所示的实施方案中,至少一个向内取向层20可被配置为围绕支架主体12的纵向长度的至少一部分周向定位的合适的网状物或编织物。在其它实施方案中,预期至少一个向内取向层20可由合适的聚合物层组成。在如图11所示的实施方案中,支架10的主体12包括至少一个位于网状物或编织层20内部的层22。
期望或需要时,支架10可具有大致均匀的壁厚。然而,在一些实施方案中,壁厚可在主体12的特定区域变化。在一些实施方案中,支架10的主体12的一端部或两端部24、26的壁厚与支架10的中心部28(未示出)的壁不同(例如,更厚)。在一些实施方案中,当将支架连接至周围的支气管组织时,更厚的壁区域更坚固且对连接至支架10的一端部或两端部24、26的缝合线提供更大的支承。较厚的壁区域(一个或多个)还可包括有利于缝合的离散构造。此类构造的非限制性实例包括管、孔洞等。
在某些实施方案中,至少限定在向外取向层18上的外部取向表面14可由电纺丝聚合物材料组成。在某些实施方案中,预期向外取向壁18可由电纺丝聚合物材料组成。在某些实施方案中,电纺丝向外取向层可与合适的编织材料层20直接接触。
纤维取向
电纺丝纤维可以是各向同性的或各向异性的。在一些实施方案中,不同层中的纤维可具有不同的相对取向。在一些实施方案中,不同层中的纤维可具有实质上相同的取向。纤维取向可以在复合物或夹式支架的各层中改变。
在一些实施方案中,可使用具有不同孔隙率的支架。在一些实施方案中,支架的一层或多层实质上允许完全的细胞渗透和均匀接种。在一些实施方案中,可例如通过密集包装纤维构建支架的一层或多层以防止一种或多种细胞类型的渗透。由于孔隙率随着纤维直径的变化而变化,控制纤维直径可用于改变支架孔隙率。可选地,可以将不同聚合物的共混物电纺丝在一起并优选溶解一种聚合物来增加支架孔隙率。可控制的纤维的性质来优化纤维直径、纤维间距或孔隙率、例如纤维的孔隙率或长径比等各纤维的形态以及将形状从圆形变为带状。在一些实施方案中,可例如通过改变纤维的组成和/或降解速率控制或优化各纤维的机械性能。
在某些实施方案中,电纺丝纤维材料可提供起伏的表面(contoured surface),例如图12中所示。在某些实施方案中,支架10中的至少一个电纺丝层可以是例如聚碳酸酯-聚氨酯等聚合物纤维材料并且可通过在例如六氟异丙醇(HFIP)等合适的溶剂中溶解聚碳酸酯-聚氨酯、纺丝并干燥来生产。
电纺丝纤维材料的间距和孔隙率可以是:使得接种在支架表面上的细胞可以在各纤维之间以悬浮的覆盖关系粘附,以使接种的细胞材料在其上形成片,如图14和15中所示。
合成支架的分层
本公开的方面涉及合成支架的生产方法。在一些实施方案中,在芯轴上(例如,通过电喷涂和/或电纺丝沉积材料)生产管状合成支架(例如,合成支气管支架)。
在一些实施方案中,合成支架的一层或多层为支架提供结构支承,赋予支架期望的机械性能。在一些实施方案中,可在支架的两个不同层之间插入编织材料(例如编织管,例如镍钛诺编织物、PET编织物、或其它金属或非金属材料的编织物)以提供结构支承。可以通过控制编织物的经纬密度来控制编织材料的压缩力(例如,编织物可施加于例如材料的外电纺丝层等下一层材料的力)。在一些实施方案中,可在有机溶剂中涂布(例如,通过浸涂或其它技术)编织物以帮助将其附接至支架10的一个或多个其它层。在一些实施方案中,编织物20的长度不超过支架主体12的端部。在一些实施方案中,支架10的一端或两端包括两层或多层的材料而无编织层,然而,支架主体12的中心部28包括附加的编织层。
在一些实施方案中,合成支架的一层或多层在支架中提供屏障,在内部空间(例如,腔空间(luminal space))和外部空间之间产生间隔(例如,相对不可渗透的间隔)。在一些实施方案中,屏障可以是电喷涂的聚氨酯(PU)层。
在一些实施方案中,支架10的不同层可包括一种或多种聚合物(例如,聚对苯二甲酸乙二醇酯(PET)、PU、或其共混物)。在一些实施方案中,支架10可包括夹在内部PU层(例如,电喷涂或电纺丝至芯轴上)和外部PU层(例如,电喷涂至编织材料上)之间的镍钛诺编织物。
在某些实施方案中,可使用支架支承体或芯轴形成支架10。在一些实施方案中,可在沉积一层或多层PU、PET、或其组合之前,用材料(例如,聚(乳酸-羟基乙酸共聚物)(poly(lactic-co-glycolic acid),PLGA)或其它聚合物)涂布支架支承体或芯轴。
在某些实施方案中,编织层或网状物层中的材料可由可吸收聚合物材料组成。可吸收聚合物材料可包括可溶解的、可扩散的、或二者的材料。
支架生产-纤维材料
在一些实施方案中,支架的一层或多层可由纤维材料构成。在一些实施方案中,支架包括一种或多种类型的纤维(例如,纳米纤维)。在一些实施方案中,支架包括一种或多种天然纤维、一种或多种合成纤维、一种或多种聚合物、或其任何组合。应理解,不同材料(例如,不同纤维)可用于本文所述的方法和组成。在一些实施方案中,材料为生物相容性的,使得其可支承细胞生长。在一些实施方案中,材料是永久的、半永久的(例如,其在植入宿主后持续数年)、或可快速降解的(例如,其在植入宿主后数周或数月内被吸收)。
在一些实施方案中,支架包括电纺丝材料(例如,微米纤维或纳米纤维)。在一些实施方案中,电纺丝材料包括PET(聚对苯二甲酸乙二醇酯(有时写作聚(对苯二甲酸乙二醇酯))。在一些实施方案中,电纺丝材料包括聚氨酯(PU)。在一些实施方案中,电纺丝材料包括PET和PU。
在一些实施方案中,人造支架可包括以下材料的任何一种或多种:弹性聚合物(例如,一种或多种聚氨酯(PU),例如聚碳酸酯和/或聚酯)、丙烯酰胺聚合物、尼龙、可再吸收的聚砜类聚合物、及其混合物。在一些实施方案中,支架可包括聚乙烯、聚丙烯、聚(氯乙烯)、聚甲基丙烯酸甲酯(和其它丙烯酸系树脂)、聚苯乙烯、其共聚物(包括ABA型嵌段共聚物)、聚(偏二氟乙烯)、聚(偏二氯乙烯)、和交联和非交联形式的、不同水解程度(例如,87%至99.5%)的聚乙烯醇。在某些实施方案中,聚合化合物还可包括增加聚合物的亲水性的化合物或过程。在某些实施方案中,这可包括混入例如基于环氧乙烷和环氧丙烷的嵌段共聚物等化合物。还可预期,如果期望或需要,可通过合适的等离子体处理来增加聚合物的亲水性。
在一些实施方案中,支架可包括嵌段共聚物。在一些实施方案中,例如聚偏二氟乙烯、间规聚苯乙烯、偏二氟乙烯和六氟丙烯的共聚物、聚乙烯醇、聚乙酸乙烯酯等加聚物,例如聚(丙烯腈)和其与丙烯酸和甲基丙烯酸酯的共聚物、聚苯乙烯、聚(氯乙烯)及其各种共聚物、聚(甲基丙烯酸甲酯)及其各种共聚物、和PET(聚对苯二甲酸乙二醇酯(有时写作聚(对苯二甲酸乙二醇酯)))等非结晶性加聚物,可进行溶液纺丝或电纺丝,并与本文所公开的任何其它材料组合以生产支架。在一些实施方案中,例如聚乙烯和聚丙烯等高度结晶性聚合物可进行溶液纺丝或与本文所公开的任何其它材料组合以生产支架。
在一些实施方案中,在支架合成之后、但支架细胞化和/或植入前,可对一种或多种聚合物进行改性以降低其疏水性和/或增加其亲水性。
在某些实施方案中,电纺丝纤维可具有小于10微米的直径。在某些实施方案中,电纺丝纤维。在某些实施方案中,电纺丝纤维可具有3和10微米之间的直径。在某些实施方案中,电纺丝纤维可具有3和5微米之间的直径。
在某些实施方案中,预期编织层中的材料可全部或部分地由例如PLGA等生物可吸收材料制成。还预期,在某些配置中,编织材料可以是可促进和/或支承组织生长和再生的负载材料(loaded material)和化合物。此类化合物和材料的非限制性实例包括以下的一种或多种:抗生素、和生长因子等。
电纺丝
在一些实施方案中,生产包括通过电纺丝生产的(例如,PU和/或PET的)一层或多层的支架。电纺丝材料可用于各种应用,包括用于组织工程化的支架。电纺丝聚合物的合适的方法可包括在以下文献中描述的那些方法:Doshi和Reneker.Electrospinning processand application of electrospun fibers.JElectrostat.1995;35:151–60.;RenekerDH,Chun I.Nanometer diameter fibers of polymer produced by electrospinning.Nanotechnology.1996;7:216–23;Dzenis Y.Spinning continuous fibers fornanotechnology.Science.2004;304:1917–19;或Vasita和Katti.Nanofibers and theirapplications in tissue engineering.Int J.Nanomedicine.2006;1(1):15-30,其中涉及电纺丝的内容通过引用结合在此。电纺丝是可用于生产实质上具有基本上任何化学性质和从nm级(例如,约15nm)至微米级(例如,约10微米)的范围内的直径的、随机取向或排列的纤维的通用技术。
在一些实施方案中,本文使用的电纺丝和电喷涂技术涉及使用高压电场来使聚合物溶液(或熔融物)带电,所述聚合物溶液(或熔融物)通过喷嘴递送(例如,作为聚合物溶液射流)并沉积在目标表面上。目标表面可以是静电板的表面、转筒(例如,芯轴)的表面、或导电且电接地的其他形式的收集器(collector)表面,使得带电的聚合物溶液向表面移动。
在一些实施方案中,所采用的电场通常为几kV的量级,喷嘴与目标表面之间的距离通常为几cm以上。聚合物溶液的溶剂在离开喷嘴和到达目标表面之间(至少部分地)蒸发。这导致聚合物纤维沉积在所述表面上。典型的纤维直径范围为几纳米至几微米。纤维的相对取向可受到目标表面相对于喷嘴的移动的影响。例如,如果目标表面是旋转芯轴的表面,纤维将沿旋转的方向在芯轴的表面上(至少部分地)排列。在一些情况下,喷嘴可在旋转芯轴的两端部之间来回扫描。
在一些实施方案中,聚合物纤维的尺寸和密度、纤维排列的程度、电纺丝材料的其它物理特性可受到以下因素的影响,所述因素包括但不限于:聚合物溶液的性质、喷嘴的尺寸、电场、喷嘴与目标表面之间的距离、目标表面的性质、喷嘴与目标表面之间的相对运动(例如,距离和/或速度)、和可影响溶剂蒸发和聚合物沉积的其它因素。
电纺丝和电喷涂过程可用于在芯轴上产生连结的聚合物纤维支架(例如,中空合成支架)。
支承体/芯轴
在一些实施方案中,支架10(例如,具有两层或多层的支架)可使用在其上可形成支架10的支承体(例如,实心或中空支承体)来产生。例如,支承体可以是电纺丝收集器,例如芯轴、或管、或任何其它形状的支承体。应理解,支承体可具有任何尺寸或形状。然而,在一些实施方案中,支承体的尺寸和形状设计成生产将支承与宿主中被替换或补充的支气管组织(或其部分)相同或相似尺寸的人造组织的支架。应理解,用于电纺丝的芯轴应具有导电的表面。在一些实施方案中,电纺丝芯轴由导电材料(例如,包括一种或多种金属)制成。然而,在一些实施方案中,电纺丝芯轴包括覆盖非导电的中心支承体的导电涂层(例如,包括一种或多种金属)。
已发现,将待整合的合适的编织物材料置于所得支架10中靠近芯轴的表面的位置处,可起到帮助促进从与芯轴的接触部移除所得支架10。
支架性质
应理解,本公开的方面用于增强任何支架的物理和功能性质,并且用于例如基于电纺丝和/或电喷涂纤维的支架。在一些实施方案中,一个或多个支架组件可以是具有不同尺寸的薄片、圆柱体、厚肋(thick rib)、实心块、分支网格等、或其任何组合。在一些实施方案中,一体的和/或组装的支架的尺寸与被替换的组织或器官的尺寸相似或相同。在一些实施方案中,支架的单个组件或层具有更小的尺寸。例如,纳米纤维层具有1nm以上、10nm以上、100nm以上、500nm以上、或900nm以上的厚度。纳米纤维层具有1微米以上、10微米以上、100微米以上、或500微米以上的厚度。纳米纤维层具有10mm以下、5mm以下、1mm以下、或800微米以下的厚度。然而,在一些实施方案中,一个或多个支架组件的尺寸可为约1mm至50cm。然而,可如本文所述制造更大、更小、或中间尺寸的结构。
在一些实施方案中,支架形成为可接种有细胞的管状结构以形成例如支气管等管状组织区域。应理解,管状区域可以是具有均匀直径的圆柱体。然而,在一些实施方案中,管状区域可具有任何合适的管状形状(例如,包括沿管状区域的长度具有不同直径的部分)。管状区域还可包括一个分支或一系列分支。在一些实施方案中,生产具有一端开口、两端开口、或多端开口的(例如,在分支支架的情况中)管状支架。然而,管状支架可在一端、两端、或所有端封闭,本发明的方面在这方面不受限制。还应理解,由于本发明的在此方面不受限制,本公开的方面可用于生产用于任何类型或器官、包括中空和实质器官的支架。在一些实施方案中,本发明的方面用于增强支架或其它结构的稳定性,所述其它结构包括非物理连接的两个或多个纤维区域或纤维层(例如,电纺丝纳米纤维)。
在一些实施方案中,支架被设计为具有多孔表面,所述多孔表面具有直径在约10nm至约100微米范围内的、可促进细胞化的孔。在一些实施方案中,孔具有小于50微米、小于40微米、小于30微米、小于20微米或小于10微米的平均直径(例如,约5、约10、或约15微米)。在一些实施方案中,孔具有20-40微米的平均直径。在一些实施方案中,选择孔径以防止或减少受试者中的免疫应答或其它不期望的宿主应答。可使用计算机和/或实验技术(例如,使用孔隙度测定法)估计孔径。然而,应理解,还可包括其它尺寸的孔。
在一些实施方案中,使用包含可在合成期间或之后溶解(例如暴露于溶剂、水溶液,例如水或缓冲液)以留下可溶性颗粒的尺寸的孔的一种或多种可溶性颗粒的纤维合成支架的表面层。在一些实施方案中,聚合物混合物中包含颗粒,所述聚合物混合物被泵送至电纺丝装置的喷嘴。因此,颗粒可与纤维一起沉积。在一些实施方案中,电纺丝过程配置为沉积厚纤维(例如,具有几微米、约10微米、和更厚的平均直径)。在一些实施方案中,如果纤维以密集形式沉积,一种或多种纤维将在固化前合并以形成更大的宏观结构(例如,10-100微米厚或更厚)。在一些实施方案中,这些宏观结构可缠结两个或多个纤维层和/或来自支架的两个或多个不同构件的部分(例如,纤维),从而增加支架的机械完整性。在一些实施方案中,当在支架合成期间的一个或多个阶段中形成(例如,通过本文所述的电纺丝)此类宏观结构(例如,连接两个或多个层和/或组件)时,可处理(例如,使用如本文所述的可溶性颗粒蚀刻或使其多孔)宏观结构(一个或多个)的表面以提供适于细胞化的表面。
在一些实施方案中,在两个或多个结构组件(例如,环)之间、单个连续结构组件的结构构件(例如,弧形构件)之间、和/或编织支承材料之间的柔性支架材料的量(例如,松弛)可用于确定合成支架的机械性能(例如,拉伸强度、伸长率、旋转、压缩、活动范围、弯曲度、阻力、柔量、自由度、弹性、或任何其它机械性能、或其组合)。
在某些实施方案中,支架10还可包括细胞鞘,其源自在孵育期间接种在支架的外表面上的细胞。所述细胞鞘粘附至支架的外表面并与其呈覆盖关系。预期存在于细胞鞘的大部分细胞将连接至外表面的最外层表面并且将跨越在其中限定的孔以形成连续的或大致连续的表面。
在某些实施方案中,所述细胞鞘可具有足以为鞘层提供结构完整性的厚度。在某些实施方案中,所述细胞鞘将由与支架的外表面接触的多个细胞组成,所述多个细胞足以引导再生细胞与鞘接触以产生覆盖鞘但不与其整合的组织壁。在某些实施方案中,鞘可由平均1和100个细胞厚之间的内衬组成。某些实施方案可具有10和100个之间;10和30个之间;20和30个之间;20和40个之间;20和50个之间;10和20个之间;30和50个之间;30和60个之间;40和60个之间;40和70个之间;70和90个之间的细胞厚度。
具有相关细胞鞘的支架10提供可定位在合适的支气管切除部位的可移动的可插入装置。具有与其接触的相关细胞鞘的支架10可被运送至期望的切除部位进行植入。在某些实施方案中,支架10被配置为在切除的器官的合适的再生后可从植入部位移除。在某些实施方案中,移除的支架将包括与其连接的一些或全部的细胞鞘。
还公开了例如支气管等管状器官的再生方法的各种实施方案。在某些实施方案中,方法100包括切除受试者中的部分管状器官的切除步骤,如附图标记110。待切除的器官可以是已因疾病损伤受损或连累、创伤或先天性病况的例如支气管等管状器官。在某些实施方案中,合适的器官的非限制性实例包括细支气管之一等。
可通过任何合适的手术过程实现切除,产生保持连接至支气管并在切除后保留在受试者中的切除的器官部分。在某些实施方案中,切除操作可产生合适的切除边缘。
在完成切除后,在切除部位植入合成支架,如附图标记120。在某些实施方案中,植入可包括以下的步骤:将保留在受试者中的切除的器官的相应端部连接至合成支架的相应端部,使得合成支架和切除的器官可实现各个构件之间合适的连接。这可通过一种或多种缝合线、生物有机组织胶等来实现。
在某些实施方案中,植入的合成支架可以是具有外聚合物表面和覆盖至少一部分的外聚合物表面的细胞化鞘层的管状构件。已讨论合成支架的各种实施方案并且可在本文所公开的方法中采用和使用。在某些实施方案中,合成支架将包括第一端和与第一端相对的第二端,位于第一端和第二端之间的外聚合物表面和覆盖至少一部分的外聚合物表面的细胞化鞘层。在某些实施方案中,植入步骤可以是使至少一部分的细胞化鞘层与切除的器官部分的至少一个切除边缘靠近接触的步骤。
在某些实施方案中,如本文所公开的方法还包括以下的步骤:以足以沿合成支架实现引导性组织生长的时间间隔,将合成支架保持在切除部位,如附图标记130。在某些实施方案中,引导性组织生长源自存在于保留在受试者中的切除的器官部分中的组织并与其接触。在某些实施方案中,引导性组织生长将与切除的器官的相关区域相邻。在某些实施方案中,引导性组织生长将表现分化的组织。在某些实施方案中,引导性组织生长将与细胞化鞘层的外表面在其向外的位置处平行。在某些实施方案中,引导性组织生长源自存在于保留在受试者中的切除的器官部分中的组织并与其接触,并且将与切除的器官的相关区域邻接(contiguous)。引导性组织生长将表现分化的组织生长并可与细胞化鞘层的外表面在其向外的位置处平行。
在已实现引导性组织生长后,如本文所公开的方法100可包括合成支架的移除步骤,如附图标记140。在某些实施方案中,移除步骤以使得引导性组织生长维持与保留在受试者中的器官的切除部分相接触的方式进行。在某些实施方案中,移除过程可包括从引导性组织生长的内部内窥镜地(intrascopically)移除合成支架。
在某些实施方案中,合成支架可全部或部分地由生物可吸收聚合物材料构成。在此类情况中,如本文所公开的方法可包括以下的步骤:以足以沿合成支架实现引导性组织生长的时间间隔,维持合成支架与切除边缘之间的接触,使得至少一部分的合成支架在足以沿合成支架实现引导性组织生长的时间段内在切除部位被吸收。在其中支架完全由生物可吸收材料组成的某些实施方案中,支架将被配置成在引导性组织生长期间维持结构完整性。在其中合成支架在选定区域由生物可吸收材料组成的某些实施方案中,预期支架的剩余部分可在已实现引导性组织生长后通过合适的过程移除。
引导性组织生长可通过合适的手段监测。在某些实施方案中,组织生长可在内窥镜下监测。
在本文所公开的方法的某些实施方案中,所述方法还可包括以下的步骤:将细胞材料赋予至合成支架的聚合物表面并允许细胞材料生长以形成细胞鞘层,该赋予和允许步骤在切除步骤之前发生。
在某些实施方案中,在本文所公开的方法中采用的合成支架,是外表面包含纺丝聚合物纤维的管状构件。在某些实施方案中,纺丝纤维可通过例如本公开中所描述的那些合适的方法电纺丝。在某些实施方案中,细胞化鞘层跨越向外定位的电纺丝纤维的至少一部分。细胞化鞘层可由细胞材料组成,所述细胞材料包括间充质细胞、干细胞、多能细胞中的至少一种。细胞材料可为从受试者自体来源的或可为同种异体来源的。
不受任何理论的限制,认为植入例如本文所公开的各种合成支架、特别是接种有覆盖的细胞鞘的合成支架,促进与植入的合成支架的位置接触或与其靠近的受试者组织的生长、再生和分化。生长的再生组织由合成支架和相关鞘引导以产生管状细胞主体,所述管状细胞主体一体化地连接至剩余管状器官的切除端并向外扩张以包封合成支架和相关细胞鞘层。认为支架和相关细胞鞘层可以促进或刺激切除的组织的再生生长,同时最小化组织排斥反应。还认为细胞鞘层的存在可以在生长和分化过程中减小或最小化再生组织对鞘层的渗透。在某些实施方案中,组织再生从各个端部向中间进行。一旦再生组织就位,可移除合成支架。在某些实施方案中,在一经移除合成支架后,再生的组织结构将缺少内上皮层。
如分别地在支架移除后即刻、移除后2个月和移除后3个月获得的图11A、11B、和11C所示,已经看到该层在移除支架后再生。
为了进一步理解本公开,参考以下实施例。包含这些实施例是为了说明的目的,并且应被认为是对本公开和权利要求书中记载的发明内容的说明。
实施例
合成的支气管替代品是由聚氨酯材料采用图1中概述的方法通过电纺丝工艺接着表面等离子体处理而制成的,所述方法包括脂肪活组织检查、支架电纺丝、接种、手术植入、和相关特征。
在采用的方法中,电纺丝聚氨酯支架由乙烯/O
然后,采用的支架接种有分离自尤卡坦微型猪(Yucatan mini-pig)的自体aMSC。在袖式叶切除术期间从猪切除部分的左主支气管,并使用末端-至-末端吻合技术手术植入接种的支架。几周后通过支气管镜移除聚氨酯支架并且通过新再生的组织桥连支气管缺损。根据需要,采用支气管内支架以支承后续的组织再生。
试验对象动物幸存于植入过程并在其整个613天生命周期中进展良好。通过一系列支气管镜评估来监测支气管的组织生长。以特定间隔获得支气管镜的代表图像。在第8天的支气管镜期间获得的图像确认吻合是完整的,并且气道干净。图2和3中展示图像。
第69天的支气管镜检查表明支架保持完整。剪断远端和近端处的缝合线并分析支架结构。2cm的支气管缺损由新形成的组织覆盖。图4和5中描述了图像。
在第76天的第76天支气管镜检查包括狭窄放置的气管支气管内支架的插入以将气道打开至4.5mm。检查表明完整的上皮层具有一些发红表现。图6和7描述了图像。
尸检和支气管说明:
左肺叶粘附至胸壁-中等强度。在第613天移除整个气管和肺并解剖至左支气管。移植再生区域和周围组织、切片并保存在10%NBF中。图8和9中展示了图像。
试验动物显示正常的生长模式并在保持饮食(maintenance diet)中获得显著增重。所有动物在主治兽医的照料下饲养。
综上所述,初步的动物研究显示,新型aMSC接种的聚氨酯支架支承支气管组织再生并在由新形成的组织桥连支气管缺损后可去除/可取回。此类支气管替代品的选择性使用将是手术器械的安全辅助手段并且将有助于降低肺切除术比率和与袖式支气管切除术相关的局部复发。
虽然已结合某些实施方案描述了本发明,应理解的是,本发明不限于所公开的实施方案,相反,本公开旨在覆盖所附权利要求的范围内所包含的各种修改和等效变形,所附权利要求的范围应得到最广泛的解释,以包括法律所允许的全部此类修改和等效结构。
- 用于体内支气管再生的方法和装置
- 衍生自干细胞的微泡(MVs)用于制备用于受损或损伤组织或器官的内皮/上皮再生的药物的用途、以及相关体外和体内方法
