一种具有脂肪酶抑制活性黄酮类化合物及其制备方法和应用
文献发布时间:2024-04-18 19:58:53
技术领域
本发明属于天然产物化学技术领域,具体涉及一种首次从桑科菠萝蜜属植物尖蜜拉中提取分离得到的异戊烯基黄酮类化合物,以及其作为脂肪酶抑制剂的用途。
背景技术
随着生活水平的提高和体力劳动的减少,我国肥胖人口日益增多,目前我国肥胖人群已超过9500万,其中1000多人万属于重度肥胖。长期肥胖容易引起运动系统疾患,发生关节炎、肌肉劳损或脊神经根压迫,引起腰腿肩背酸痛,甚至造成关节变形,严重影响肢体活动。还会导致甘油三酯大量堆积在肝脏,就形成了脂肪肝,或加心脏负荷,造成血液积聚在心血管系统的状态,严重者甚至会出现心功能衰竭。
造成肥胖的外因主要是由于饮食过多而活动过少,使脂肪摄入和合成增加,进而导致肥胖。内因是主要是体内脂肪代谢紊乱而致肥胖。由于胃肠道的脂肪酶主要负责水解甘油三酯,将其降解为甘油二酯、单甘油酯和脂肪酸等产物被人体吸收。因此,控制膳食中脂肪的吸收可以有效控制体重,而存在于脂肪酶抑制剂已经成为治疗肥胖症药物的重要靶点。目前市场上已有商业化的脂肪酶抑制剂上市,例如奥利司他,虽然表现出良好的抑制效果,但是也有多种胃肠道不良反应伴随发生。因此从天然产物中寻找新型高效安全的脂肪酶抑制剂势在必行。
黄酮(flavone),是黄酮类化合物的总称,泛指两个具有酚羟基的苯环(A-与B-环)通过中央三碳原子相互连结而成的一系列化合物。研究表明,黄酮类化合物具有脂肪酶抑制、抗病毒活性、抗肿瘤、抗氧化自由基活性、抗炎、镇痛、抑制脂肪酶、改善心血管系统等多种药理活性。同时已有研究证实,黄酮药理作用与化学结构密切相关,为了获得这类化合物更有效的构效关系,可进一步研究和开发更多的黄酮类化合物,从中寻找有效的先导化合物和活性基团,开发更多的黄酮类新药。
尖蜜拉原产于马来西亚和墨西哥,中国海南、福建、广西和云南也有栽培。尖蜜拉成熟果肉味浓甜而芳香、营养丰富,可鲜食,也可加工制果酱、蜜饯、果汁、果冻和制罐头等。此外,现代医学研究证实,尖蜜拉具有抗水肿、脂肪酶抑制、消炎等作用。本发明从尖蜜拉中分离得到了一种新的异戊烯基黄酮类化合物,该化合物至今尚未见到相关报道。值得一提的是该化合物除具有显著的脂肪酶抑制作用,可作为新型、高效、安全的脂肪酶抑制剂。此外,本发明化合物为首次在天然产物中发现的异戊烯基形成了4-甲基呋喃环的黄酮类化合物,其化合物结构具有较高的新颖度,对完善黄酮类化合物的构效关系具有主要的科学意义。
发明内容
本发明的第一目的在于提供一种具有脂肪酶抑制活性黄酮类化合物;第二目的在于提供所述的具有脂肪酶抑制活性黄酮类化合物的制备方法;第三目的在于提供所述的具有脂肪酶抑制活性黄酮类化合物的应用。
本发明的第一目的是这样实现的,是以药用植物尖蜜拉(
。
本发明的第二目的是这样实现的,是以药用植物尖蜜拉细枝为原料,经前处理、浸膏提取、硅胶柱层析和高效液相色谱分离制备得到,具体包括以下步骤:
A、前处理:将原料药用植物尖蜜拉细枝粉碎得到物料a;
B、浸膏提取:将物料a中加入物料a质量2~6倍的有机提取溶剂,于常温下浸泡提取2~5次,每次提取时间为12~20h,合并提取液并过滤得到样品提取液b;
C、MCI脱色:将样品提取液上MCI柱脱色,收集流出液并减压浓缩得到浸膏c;
D、硅胶柱层析:
1)将浸膏c中加入浸膏c重量3~10倍量的200~250目硅胶装柱,以体积配比为20:1~1:1的氯仿-甲醇溶液进行梯度洗脱,经TLC监测,合并相同的部分;
2)将9:1配比的氯仿-甲醇溶液进行洗脱得到的洗脱液中,加入其浸膏重量3~10倍量的200~250目硅胶装柱,以体积配比为1:0~1:2的氯仿-丙酮溶液进行梯度洗脱,经TLC监测,合并相同的部分;
E、高效液相色谱分离:将以8:2配比的氯仿-丙酮溶液进行洗脱得到的洗脱液经高压液相色谱分离纯化得到目标物具有脂肪酶抑制活性的异戊烯基黄酮类化合物。
所制备的异戊烯基黄酮类化合物结构是通过以下方法进行鉴定:
化合物的HRESI-MS显示其准分子离子峰为385.1049[M+Na]
红外光谱中显示了羰基(1669)和芳环(1617、1542、1464cm
化合物的
表1.本发明化合物的
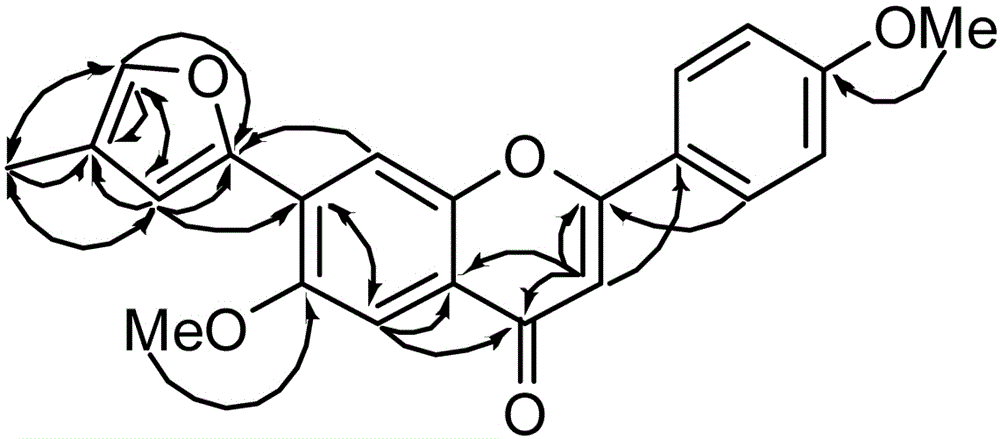
化合物的母体确定后,其余的取代基如(4''-甲基呋喃-2-基)结构片段和甲氧基,可视为黄酮上的取代基。(4''-甲基呋喃-2-基)结构片段的存在也可通过H-3′′和C-2′′、C-4′′、C-5′′、C-6′′;H-5′′和C-2′′、C-3′′、C-4′′、C-6′′;以及H-6′′和C-3′′、C-4′′、C-5′′的HMBC相关性中得到证实。同时,通过进一步的HMBC相关分析可知,两个甲氧基质子信号(δ
通过文献查询,本发明化合物为首次在天然产物中发现的异戊烯基形成了4-甲基呋喃环的黄酮类化合物,其化合物结构具有较高的新颖度。
化合物的红外、紫外和质谱数据:紫外光谱(甲醇),
本发明的第三目的,即所述的异戊烯基黄酮类化合物脂肪酶抑制剂活性测试,是这样实现的:
反应底物4-methylumbelliferyl oleate(4-MUO75164)和猪胰腺淀粉酶(EC3.1.1.3,L3126)购自Sigma公司,磷酸缓冲液PBS购自Life公司(Thermo FisherScientific,China)。DMSO,MeOH均为分析纯,购自天津富宇精细化工有限公司;柠檬酸、柠檬酸钠购自天津市福晨化学试剂厂。
酶标仪Tecan GENios(Tecan Group Ltd.,Swizerland);96孔板(CorningCostar,Cambridge,MA,USA)。
脂肪酶抑制活性评价采用比色法(Ercan et al,
用超纯水配制0.1M的柠檬酸-柠檬酸钠缓冲液(pH=4.2);用PBS(pH=7.4)配制1.0mg/mL的胰脂肪酶溶液、0.1mM的4-MUO溶液、0.2M的Na
取部分配制好的脂肪酶溶液(1.0mg/ml)90℃水浴锅中加热20分钟使酶失活。
将化合物和阳性对照分别用DMSO等比稀释成初始浓度为10、5、2.5、1.25、0.625、0.3125mM的待测液。
按如下反应体系加样(DMSO浓度不超过整个体系的5%):样品组:1.0μL样品+24μLPBS+25μL酶;样品空白组:1.0μL样品+24μL PBS+25μL灭活酶;阴性组:1μL DMSO+24μL PBS+25μL酶;阴性空白组:1.0μL DMSO+24μL PBS+25μL灭活酶。
加样完成混匀后每孔再加入50μL反应底物4-MUO(0.1mM),25℃恒温培养箱中反应20min后,每个样品孔中加入100μL的柠檬酸-柠檬酸钠溶液(0.1M pH=4.2)终止反应,用酶标仪测定各孔的荧光吸光值,激发光波长为320nm,检测波长为450nm。每个样品至少重复3次,计算抑制率,公式如下:
抑制率(%)=[1-(A样品–A样品空白)/(A阴性–A阴性空白)]×100
采用SPSS 19.0统计分析软件计算半数抑制浓度IC
本发明的优点为:
(1)本发明化合物是本发明的异戊烯基黄酮是从药用植物尖蜜拉中分离得到,尖蜜拉细枝生物产量大,原料来源非常广泛,成本低,化合物分离制备容易实现。
(2)本发明中采用溶剂提取、再用常规柱层析和高效液相色谱结合的制备方法,化合物制备操作流程简单,所获得的本发明化合物纯度高,后续的工业化生产容易实现。
(3)本发明化合物对动物无毒,使用安全,其IC
(4)本发明化合物为首次在天然产物中发现的异戊烯基形成了4-甲基呋喃环的黄酮类化合物,其化合物结构具有较高的新颖度,对完善黄酮类化合物的构效关系就有重要的科学意义。
附图说明
图1本发明脂肪酶抑制活性黄酮类化合物的核磁共振碳谱(
图2为本发明脂肪酶抑制活性黄酮类化合物的核磁共振氢谱(
图3本发明脂肪酶抑制活性黄酮类化合物的关键HMBC相关图。
具体实施方式
下面结合实施例和附图对本发明作进一步的说明,但不以任何方式对本发明加以限制,基于本发明教导所作的任何变换或替换,均属于本发明的保护范围。
是以药用植物尖蜜拉(
本发明所述的具有脂肪酶抑制活性黄酮类化合物,是以药用植物尖蜜拉细枝为原料,经前处理、浸膏提取、硅胶柱层析和高效液相色谱分离制备得到,具体包括以下步骤:
A、前处理:将原料云南民族药用植物植物尖蜜拉细枝粉碎得到物料a;
B、浸膏提取:将物料a中加入物料a质量2~6倍的有机提取溶剂,于常温下浸泡提取2~5次,每次提取时间为12~20h,合并提取液并过滤得到样品提取液b;
C、MCI脱色:将样品提取液上MCI柱脱色,收集流出液并减压浓缩得到浸膏c;
D、硅胶柱层析:
1)将浸膏c中加入浸膏c重量3~10倍量的200~250目硅胶装柱,以体积配比为20:1~1:1的氯仿-甲醇溶液进行梯度洗脱,经TLC监测,合并相同的部分;
2)将9:1配比的氯仿-甲醇溶液进行洗脱得到的洗脱液中,加入其浸膏重量3~10倍量的200~250目硅胶装柱,以体积配比为1:0~1:2的氯仿-丙酮溶液进行梯度洗脱,经TLC监测,合并相同的部分;
E、高效液相色谱分离:将以8:2配比的氯仿-丙酮溶液进行洗脱得到的洗脱液经高压液相色谱分离纯化得到目标物具有脂肪酶抑制活性黄酮类化合物。
B步骤中所述的有机提取溶剂为质量浓度70%~100%甲醇水溶液、质量浓度70%~100%的乙醇水溶液或质量浓度70%~100%的丙酮水溶液。
D步骤上柱前还包括用物料c重量1.5~3倍的有机溶剂溶解后加入物料c重量0.8~2.0倍的80~100目硅胶进行拌样步骤。
所述的有机溶剂为纯甲醇或纯丙酮。
D步骤1)中所述的氯仿-甲醇溶液体积配比为20:1、9:1、8:2、7:3、6:4和1:1。
E步骤中高效液相色谱分离纯化是以体积浓度为60~75%的甲醇水溶液为流动相,流速12mL/min,以2.12×250mm,5μm的Zorbax PrepHT GF反相制备柱为固定相,紫外检测器检测波长为380nm,每次进样0.5~1.0mL,收集30~42min的色谱峰,多次累加后蒸干得到目标物脂肪酶抑制活性黄酮类化合物。
本发明所述的异戊烯基黄酮化合物的应用为:作为脂肪酶抑制剂。
制备方法具体操作如下:
A、样品提取和净化:将尖蜜拉细枝晒干,粉碎到20~50目,然后用溶剂提取2~5次,每次提取溶剂为原料的2-6倍,提取时间为12~20小时,滤除沉淀物得到样品提取液,减压浓缩得浸膏。制备的乙醇提取物在乙酸乙酯和水溶液中进行分配。将乙酸乙酯层在减压下浓缩以获得粗提取物。所得粗提取物滤除沉淀后的提取液上MCI柱脱色,收集流出液并减压浓缩成浸膏,供柱层析分离用。
B、初次硅胶柱层析:将所得浸膏用1.5~3倍的丙酮或者甲醇稀释,然后用浸膏重量0.8~2.0倍硅胶拌样,拌样硅胶为100-150目。将拌好的样品上硅胶柱层析进行粗分,装柱硅胶为200~250目,所用硅胶的重量为浸膏重量3~10倍量;以体积比为20:1~1:1的氯仿和甲醇混合有机溶剂梯度洗脱,收集各梯度的梯度洗脱液并浓缩,经TLC监测,合并相同的部分得6个组分(A-F)。
C、再次硅胶柱层析:将B步骤中的组分b(氯仿-甲醇9:1部分)进一步进行硅胶柱层析:装柱硅胶为200~250目,所用硅胶的重量为浸膏重量3~10倍量,以体积比为1:0~1:2的氯仿和丙酮混合有机溶剂梯度洗脱,收集各梯度的梯度洗脱液并浓缩。
D、高效液相色谱分离:将采用C步骤中组分C(氯仿-丙酮8:2混合有机溶剂洗脱得到的部分)采用高效液相色谱分离纯化,即得所述的黄酮类化合物。
进一步,优选的是,所述A步骤的溶剂为体积浓度为70~100%的丙酮水溶液、体积浓度为70~100%的乙醇水溶液或体积浓度为70~100%的甲醇水溶液。
进一步,优选的是,所述C步骤中浸膏在经硅胶柱层析前,先用重量是浸膏1.5~3倍的丙酮或者甲醇稀释,然后用重量是浸膏0.8~2.0倍的80~100目硅胶拌样,之后上样。
进一步,优选的是,所述C步骤中,梯度洗脱时,所使用的氯仿和甲醇混合有机溶剂的体积比依次为20:1、9:1、8:2、7:3、6:4和1:1。(每次要洗脱到没有组分流出,即蒸干溶剂后蒸馏瓶中没有成分残留,然后换下一个梯度)。
进一步,优选的是,所述E步骤的高效液相色谱分离纯化是以体积浓度为60~75%的甲醇水溶液为流动相,流速12mL/min,以2.12×250mm,5μm的Zorbax PrepHT GF反相制备柱为固定相,紫外检测器检测波长为380nm,每次进样0.5~1.0mL,收集30~42min的色谱峰,多次累加后蒸干可得化合物纯品。
本发明所用原料药用植物尖蜜拉不受地区和品种限制,均可以实现本发明的内容,
下面以来源于云南不同产地的尖蜜拉原料对本发明做进一步说明:
实施例1
本实施例提供本发明所述的脂肪酶抑制活性黄酮类化合物的制备方法,所述制备方法包括:浸膏提取、硅胶柱层析和高效液相色谱分离步骤,将药用植物尖蜜拉作为原料,具体操作如下:
所用的药用植物尖蜜拉产自于云南红河河口,原料为药用植物尖蜜拉细枝粉碎或切段后的样品,用质量浓度70%甲醇水溶液浸泡提取4次,每次15h。合并提取液上MCI柱脱色,洗脱液减压浓缩得到浸膏;浸膏用浸膏质量2倍的甲醇2溶解,然后加入90目硅胶拌样,用220目硅胶装柱,拌样后上柱;用体积比分别为20:1,9:1,8:2,7:3,6:4和1:1的氯仿-甲醇洗脱液进行梯度洗脱,收集梯度洗脱液、浓缩,经TLC监测,合并相同的部分,得到6个部分A-F,其中,对收集到的样品B(9:1)部分235g,加入浸膏8倍量的220目硅胶装柱,用体积比分别为1:0,1:1,1:2的氯仿-丙酮洗脱液进行梯度洗脱,收集梯度洗脱液、浓缩,经TLC监测,合并相同的部分,得到3个部分,其中8:2部分28.5g,再以66%的甲醇为流动相,流速12ml/min,2.12×250mm,5
所制备的具有脂肪酶抑制活性的异戊烯基黄酮类化合物结构是通过以下方法进行鉴定:
化合物的HRESI-MS显示其准分子离子峰为385.1049[M+Na]
红外光谱中显示了羰基(1669)和芳环(1617、1542、1464cm
化合物的
化合物的母体确定后,其余的取代基如(4''-甲基呋喃-2-基)结构片段和甲氧基,可视为黄酮上的取代基。(4''-甲基呋喃-2-基)结构片段的存在也可通过H-3′′和C-2′′、C-4′′、C-5′′、C-6′′;H-5′′和C-2′′、C-3′′、C-4′′、C-6′′;以及H-6′′和C-3′′、C-4′′、C-5′′的HMBC相关性中得到证实。同时,通过进一步的HMBC相关分析可知,两个甲氧基质子信号(δ
实施例2
本实施例提供本发明所述的脂肪酶抑制活性黄酮类化合物的制备方法,所述制备方法包括:浸膏提取、硅胶柱层析和高效液相色谱分离步骤,将药用植物尖蜜拉作为原料,具体操作如下:
所用的药用植物尖蜜拉产自于云南玉溪元江,原料为药用植物尖蜜拉细枝粉碎或切段后的样品,用质量浓度80%的乙醇水溶液浸泡提取5次,每次12h。合并提取液上MCI柱脱色,洗脱液减压浓缩得到浸膏;浸膏用浸膏质量3倍的丙酮溶解,然后加入100目硅胶拌样,用250目硅胶装柱,拌样后上柱;用体积比分别为20:1,9:1,8:2,7:3,6:4和1:1的氯仿-甲醇洗脱液进行梯度洗脱,收集梯度洗脱液、浓缩,经TLC监测,合并相同的部分,得到6个部分A-F,其中,对收集到的样品B(9:1)部分271g,加入浸膏10倍量的250目硅胶装柱,用体积比分别为1:0,1:1,1:2的氯仿-丙酮洗脱液进行梯度洗脱,收集梯度洗脱液、浓缩,经TLC监测,合并相同的部分,得到3个部分,其中8:2部分26.7g,再以66%的甲醇为流动相,流速12ml/min,2.12×250mm,5
实施例3
本实施例提供本发明所述的脂肪酶抑制活性黄酮类化合物的制备方法,所述制备方法包括:浸膏提取、硅胶柱层析和高效液相色谱分离步骤,将药用植物尖蜜拉作为原料,具体操作如下:
所用的药用植物尖蜜拉产自于云南西双版纳勐海,原料为药用植物尖蜜拉(细枝粉碎或切段后的样品,用质量浓度80%的丙酮水溶液浸泡提取2次,每次12h。合并提取液上MCI柱脱色,洗脱液减压浓缩得到浸膏;浸膏用浸膏质量1.5倍的甲醇溶解,然后加入80目硅胶拌样,用200目硅胶装柱,拌样后上柱;用体积比分别为20:1,9:1,8:2,7:3,6:4和1:1的氯仿-甲醇洗脱液进行梯度洗脱,收集梯度洗脱液、浓缩,经TLC监测,合并相同的部分,得到6个部分A-F,其中,对收集到的样品B(9:1)部分229g,加入浸膏3倍量的200目硅胶装柱,用体积比分别为1:0,1:1,1:2的氯仿-丙酮洗脱液进行梯度洗脱,收集梯度洗脱液、浓缩,经TLC监测,合并相同的部分,得到3个部分,其中8:2部分23.6g,再以66%的甲醇为流动相,流速12ml/min,2.12×250mm,5
实施例4
取实施例1-3制备的任一化合物,为黄色胶状物。测定方法与实施例1相同,确认实施例1-3制备的化合物为所述的6,4'-二甲氧基-7-(4-甲基呋喃-2-基)-黄酮。
实施例5
取实施例1-3制备的任一苯并吡喃内酯类化合物进行安全性评价,试验情况如下:通过小鼠骨髓微核实验、Ames实验和TK基因突变实验均证明本发明化合物对动物毒性低,使用安全。
实施例6
取实施例1-3制备的任一异戊烯基黄酮类化合物进行脂肪酶抑制活性试验,试验情况和结果如下:
反应底物4-methylumbelliferyl oleate(4-MUO 75164)和猪胰腺淀粉酶(EC3.1.1.3,L3126)购自Sigma公司,磷酸缓冲液PBS购自Life公司(Thermo FisherScientific,China)。DMSO,MeOH均为分析纯,购自天津富宇精细化工有限公司;柠檬酸、柠檬酸钠购自天津市福晨化学试剂厂。
酶标仪Tecan GENios(Tecan Group Ltd.,Swizerland);96孔板(CorningCostar,Cambridge,MA,USA)。
脂肪酶抑制活性评价采用比色法(Ercan et al,
用超纯水配制0.1M的柠檬酸-柠檬酸钠缓冲液(pH=4.2);用PBS(pH=7.4)配制1.0mg/mL的胰脂肪酶溶液、0.1mM的4-MUO溶液、0.2M的Na
取部分配制好的脂肪酶溶液(1.0mg/ml)90℃水浴锅中加热20分钟使酶失活。
将化合物和阳性对照分别用DMSO等比稀释成初始浓度为10、5、2.5、1.25、0.625、0.3125mM的待测液。
按如下反应体系加样(DMSO浓度不超过整个体系的5%):样品组:1.0μL样品+24μLPBS+25μL酶;样品空白组:1.0μL样品+24μL PBS+25μL灭活酶;阴性组:1μL DMSO+24μL PBS+25μL酶;阴性空白组:1.0μL DMSO+24μL PBS+25μL灭活酶。
加样完成混匀后每孔再加入50μL反应底物4-MUO(0.1mM),25℃恒温培养箱中反应20min后,每个样品孔中加入100μL的柠檬酸-柠檬酸钠溶液(0.1M pH=4.2)终止反应,用酶标仪测定各孔的荧光吸光值,激发光波长为320nm,检测波长为450nm。每个样品至少重复3次,计算抑制率,公式如下:
抑制率(%)=[1-(A样品–A样品空白)/(A阴性–A阴性空白)]×100
采用SPSS 19.0统计分析软件计算半数抑制浓度IC
- 一种具有免疫抑制活性的PKS I型聚酮类化合物及其制备方法和应用
- 一种具有COX-2抑制活性的系列酚性化合物及制备方法
- 一种具有PD-L1抑制活性的化合物、其制备方法及用途
- 一种具有淀粉酶抑制活性基团的新型抗性淀粉的制备方法及应用
- 具有脂肪酶抑制活性的酰基他定类化合物、其制备方法及应用
- 一种具有脂肪酶抑制活性的米糠生物碱、药物组合物及其制备方法和应用
