一种磺酸盐类三联吡啶衍生物及其制备方法和应用
文献发布时间:2024-04-18 19:58:53
技术领域
本发明涉及磺酸盐类三联吡啶衍生物材料技术领域,具体涉及一种磺酸盐类三联吡啶衍生物及其制备方法和应用。
背景技术
溶酶体一般为真核细胞中的一种细胞器,为单层膜包被的囊状结构,内含多种水解酶,专为分解各种外源和内源的大分子物质。长期以来,溶酶体通常被认为细胞的主要再循环细胞器,对于细胞内的代谢至关重要;代谢的信号中枢,可感知营养物质和生长因子的可利用状态。大量研究表明溶酶体参与许多生理过程,包括细胞正常代谢活动、防御功能和其他重要功能。此外,溶酶体在各种疾病中发挥着重要作用,如各类溶酶体贮积症、遗传性疾病、类风湿关节炎和肿瘤等。由于其独特的结构,需要特定的荧光探针来特异性检测溶酶体,在疾病诊断和治疗等方面有着巨大的使用价值。目前研究较多的溶酶体荧光探针主要存在毒性较大、激发波长较短和光稳定性差等问题,限制了其在生物学上的应用。
公开号为CN113845462A的中国专利文件,公开了一种溶酶体荧光探针、其制备方法及其应用,存在的问题是:用MTT法检测细胞存活率,在较低浓度时探针表现出低毒性,但在高浓度时会存在细胞毒性较大;且激发波长较短,可能会导致组织受损或出现不必要的背景信号。
发明内容
本发明的目的是提供一种磺酸盐类三联吡啶衍生物及其制备方法和应用,磺酸盐类三联吡啶衍生物,原料易得,合成简单,可特异性染色于溶酶体,并且具有毒性小、良好的非线性光学活性等优点。
本发明的技术方案是:
一种基于磺酸盐类三联吡啶衍生物,该荧光探针是4,4'-(吡啶-2,6-diylbis(1H-苯并[d]咪唑-2,1-diyl))bis(丁基-1-磺酸盐),简记为N3,其结构式如下所示:
。
本发明中,磺酸盐类三联吡啶衍生物的制备方法,包括如下步骤:
将2,6-bis(1H-苯并[d]咪唑-2-yl)吡啶(简记为L1)、氢氧化钾、四丁基溴化铵溶解于二甲基亚砜和水,配制成混合溶液,搅拌状态下,向混合溶液中逐滴加入1,4-丁基磺酸内酯,控制反应温度135-160℃,反应10-20 h;将反应完成液滴入适量蒸馏水中,加酸调节PH至5.0~6.0,静置,将析出的固体抽滤、干燥,得白色针状固体产物4,4'-(吡啶-2,6-diylbis(1H-苯并[d]咪唑-2,1-diyl))bis(丁基-1-磺酸盐)。即为目标产物磺酸盐类三联吡啶衍生物,简记为N3。
所述的N3可采用挥发法培养晶体结构,得到无色透明方块状晶体。
合成路线如下所示:
进一步地,所述的2,6-bis(1H-苯并[d]咪唑-2-yl)吡啶、氢氧化钾、四丁基溴化铵的摩尔比为20-35:60-72:1。
进一步地,所述的2,6-bis(1H-苯并[d]咪唑-2-yl)吡啶与二甲基亚砜的摩尔比为1:25-38;氢氧化钾和水的摩尔比为1:10-20。
进一步地,所述的2,6-bis(1H-苯并[d]咪唑-2-yl)吡啶与1,4-丁基磺酸内酯的摩尔比为1:1.5-2.8。
进一步地,所述的反应完成液与蒸馏水的体积比为1:1-3。
本发明的磺酸盐类三联吡啶衍生物的应用,将所述的基于磺酸盐类三联吡啶衍生物用于特异性靶向溶酶体的分析和追踪。
本发明的有益效果体现在:
本发明的N3在波长为770nm激光的激发下,具有较大的双光子吸收截面(523 GM),是一种具有优良非线性光学性质的多光子吸收材料(如图2)。
本发明的N3中可自由旋转单键和长烷基链磺酸盐的引入,在其DMSO溶液中随着乙醇的加入,表现出明显的聚集诱导发射(AIE)性质,荧光发射强度逐渐增强(如图3)。
本发明的N3细胞毒性试验表明,对Hela细胞毒性较低,完全可以满足在生物学应用要求。亲水基团磺酸基(-SO
本发明的N3能很好地被细胞摄取并且细胞中靶向于溶酶体,且特异性较高(如图5)。
本发明的制备方法原料易得,合成简单。
附图说明
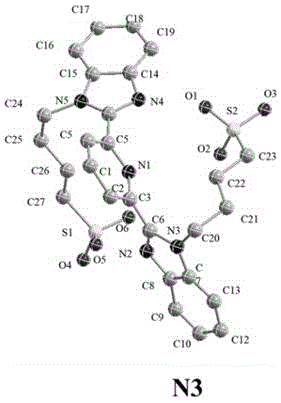
图1为本发明实施例1中N3的晶体结构图(为了便于观察,省略氢原子)。
图2(a)为本发明实施例1中N3在波长为770 nm激光下的双光子Z-扫描测试图。(b)为本发明实施例1中N3在波长为680-980 nm激光下的双光子吸收截面图。
图3 为本发明实施例1中N3的AIE图。
图4为本发明实施例1中N3的细胞毒性试验图。
图5为本发明实施例1中N3的共定位实验图。
具体实施方式
以下结合附图和实施例对本发明做进一步详细说明。
实施例1
将12.8 mmol 2,6-bis(1H-苯并[d]咪唑-2-yl)吡啶、38.4mmol氢氧化钾、0.64mmol四丁基溴化铵溶解于22.73 mL二甲基亚砜和9.47 mL水,配制成混合溶液,搅拌状态下,向混合溶液中逐滴加入19.2 mmol1,4-丁基磺酸内酯,控制反应温度135℃,反应20h;将反应完成液滴入32.2 mL蒸馏水中,加酸调节PH至5.0~6.0,静置,将析出的固体抽滤、干燥,得白色针状固体产物4,4'-(吡啶-2,6-diylbis(1H-苯并[d]咪唑-2,1-diyl))bis(丁基-1-磺酸盐)。即为目标产物磺酸盐类三联吡啶衍生物,简记为N3。本实施例N3的基本数据为:
实施例2
将12.8 mmol 2,6-bis(1H-苯并[d]咪唑-2-yl)吡啶、32.77mmol氢氧化钾、0.52mmol四丁基溴化铵溶解于27.27 mL二甲基亚砜和8.34 mL水,配制成混合溶液,搅拌状态下,向混合溶液中逐滴加入25.6 mmol 1,4-丁基磺酸内酯,控制反应温度145℃,反应15h;将反应完成液滴入53.42 mL蒸馏水中,加酸调节PH至5.0~6.0,静置,将析出的固体抽滤、干燥,得白色针状固体产物4,4'-(吡啶-2,6-diylbis(1H-苯并[d]咪唑-2,1-diyl))bis(丁基-1-磺酸盐)。即为目标产物磺酸盐类三联吡啶衍生物,简记为N3。
实施例3
将12.8 mmol 2,6-bis(1H-苯并[d]咪唑-2-yl)吡啶、29.01mmol氢氧化钾、0.43mmol四丁基溴化铵溶解于31.81 mL二甲基亚砜和7.66 mL水,配制成混合溶液,搅拌状态下,向混合溶液中逐滴加入32mmol 1,4-丁基磺酸内酯,控制反应温度150℃,反应13 h;将反应完成液滴入86.99 mL蒸馏水中,加酸调节PH至5.0~6.0,静置,将析出的固体抽滤、干燥,得白色针状固体产物4,4'-(吡啶-2,6-diylbis(1H-苯并[d]咪唑-2,1-diyl))bis(丁基-1-磺酸盐)。即为目标产物磺酸盐类三联吡啶衍生物,简记为N3。
实施例4
将12.8 mmol 2,6-bis(1H-苯并[d]咪唑-2-yl)吡啶、26.33mmol氢氧化钾、0.37mmol四丁基溴化铵溶解于36.36 mL二甲基亚砜和6.91 mL水,配制成混合溶液,搅拌状态下,向混合溶液中逐滴加入35.84mmol 1,4-丁基磺酸内酯,控制反应温度160℃,反应10h;将反应完成液滴入129.81 mL蒸馏水中,加酸调节PH至5.0~6.0,静置,将析出的固体抽滤、干燥,得白色针状固体产物4,4'-(吡啶-2,6-diylbis(1H-苯并[d]咪唑-2,1-diyl))bis(丁基-1-磺酸盐)。即为目标产物磺酸盐类三联吡啶衍生物,简记为N3。
实施例5
称取15 mgN3于25mL烧杯中,加入4 mL甲醇,过滤后加入到25mL锥形瓶中,再依次逐滴加入2mL丙酮和4mL乙腈,封口、静置,采用挥发法培养晶体结构,得到无色透明方块状晶体,CCDC号为2257933,图1说明目标分子N3是本发明首次合成的化合物。
实施例6
配制N3的DMSO(1×10
实施例7
配制N3的DMSO(1×10
实施例8
1.MTT方法测试了N3的细胞毒性,在0-25μM浓度范围的培养液中孵育Hela细胞24h,观察细胞存活率。图4说明该荧光探针对Hela细胞毒性较低,可以满足在生物学应用的要求。
2.取5 μM的N3对Hela细胞进行染色,共同孵育40 min,用PBS缓冲液轻轻洗涤培养皿3-4次,共聚焦显微镜观察,该荧光探针能穿过细胞膜并在细胞中着色。为了确认荧光探针靶向细胞的部位,利用溶酶体商染Lyso-tracker deep red进行共定位显影,结果显示该荧光探针与lysosome的着色部位和现象一致。图5说明荧光探针可以靶向细胞内的溶酶体。
