具有抗炎活性的肽及其用途
文献发布时间:2024-07-23 01:35:12
技术领域
本发明涉及具有抗炎活性的肽和抗炎组合物以及包含其作为活性成分的抗炎组合物。
背景技术
炎症是活组织对外部刺激的防御反应,是修复和再生由物理作用或有害物质、化学刺激、细菌感染引起的损伤的机制,而持续的炎症反应反而会促进粘膜损伤,这在某些情况下会引起各种疾病,包括癌症。脂多糖(LPS)是革兰氏阴性菌的外膜成分,会引起各种反应(诸如局部炎症、抗体产生和败血症)。巨噬细胞在LPS感染的早期阶段做出反应,并且在宿主防御和内平衡中发挥核心作用。然而,高浓度LPS刺激引起巨噬细胞分泌促炎介质(pro-inflammatory mediator),诸如肿瘤坏死因子-α(TNF-α)、白介素(IL)-1和IL-6以及一氧化氮(NO),从而导致宿主的致命后果。通常,当巨噬细胞被激活时,由诱导型NO合酶(iNOS)产生NO,并且其具有抑制某些病毒和寄生虫的抗菌作用;然而,已知过量的NO形成会引起炎症并导致组织损伤、基因突变、神经损伤等。
促炎细胞因子(诸如TNF-α、IL-1和IL-6)的表达受丝裂原活化蛋白激酶(MAPKs),诸如细胞外信号调节激酶1/2(ERK1/2)、p38激酶(p38)、c-Jun NH2-末端激酶(JNK)和核因子κB(NF-κB)调节。NF-κB在与免疫和炎性反应相关的基因表达中起重要作用,并且当NF-κB被激活时,与NF-κB结合的抑制性κBα(IκBα)被分解,NF-κB从细胞质进入细胞核,然后作为转录因子用于细胞因子(诸如TNF-α、IL-12和IL-6)的表达。
同时,已知白介素-17(IL-17)与慢性炎症密切相关。IL-17是一种炎性细胞因子,在宿主抵抗细胞外细菌和真菌感染的防御机制中起重要作用,尤其是T辅助性17(Th17)细胞在IL-17的产生和分化中起重要作用。体内IL-17产生和分泌的增加与包括以下的各种炎症和自身免疫性疾病密切相关:银屑病、银屑病关节炎(PsA)、类风湿性关节炎(RA)、特应性皮炎(AD)、痤疮病变和强直性脊柱炎(AS)。随着鉴定出IL-17和Th17细胞在炎症和自身免疫疾病中的主要致病作用,已经提出了对它们进行抑制和调节来作为治疗疾病的重要策略,以及正在研究通过抑制和调节Th17细胞系细胞因子以及抑制和调节特定转录因子的潜在靶向治疗方法等。
非甾体抗炎药(NSAIDS)目前用作抗炎药,其通过抑制被称为环氧合酶(COX)的酶的活性而表现出抗炎作用,该被称为环氧合酶(COX)的酶参与由花生四烯酸生物合成前列腺素;然而,除了主要的治疗作用之外,它们还会引起严重的副作用,诸如胃肠道疾病、肝脏疾病和肾脏疾病,因此这些药物的长期使用受到限制。
因此,需要开发能够克服作用于中枢神经系统和胃肠道的药物的局限性的下一代抗炎药。最近,通过从作用于中枢神经系统和胃肠道的药物转向开发具有局部作用的药物,以及从用于口服施用的小分子合成化合物转向开发用于皮下或血管内注射的合成肽,抗炎药物开发方向的重要性得以扩大(非专利文献)。合成肽疗法的开发是未来生物制药行业的有希望的驱动力,因为其在抗炎药物开发领域具有巨大的临床有效性潜力,发现新的药物靶点和机制,开发基于肽的药物以及开发递送优化技术非常重要。
[现有技术文件]
[非专利文件]
(非专利文献1)Sara La Manna et al.,Peptides as Therapeutic Agents forInflammatory-Related Diseases.Int.J.Mol.Sci.2018;19:2714
发明内容
技术问题
本发明的目的是提供一种具有抗炎活性的肽。
本发明的另一目的是提供一种包含具有上述活性的肽作为活性成分的抗炎组合物。
本发明的又一目的是提供一种用于预防或治疗炎性疾病的组合物,所述组合物包含具有上述活性的肽作为活性成分。
本发明的又一目的是提供一种用于抗炎的化妆品组合物,所述化妆品组合物包含具有上述活性的肽作为活性成分。
技术方案
为了实现上述目的,本发明的一个方面提供了一种肽,其包含如SEQ ID NO:1所示的氨基酸序列。
本发明的另一方面提供了一种抗炎组合物,所述抗炎组合物包含所述肽作为活性成分。
本发明的又一方面提供了一种用于预防或治疗炎性疾病的药物组合物,所述药物组合物包含所述肽作为活性成分。
本发明的又一方面提供了一种用于抗炎的化妆品组合物,所述化妆品组合物包含所述肽作为活性成分。
有利效果
根据本发明的包含SEQ ID NO:1的氨基酸序列的肽具有抗炎活性,因此可用作用于预防、改善或治疗炎性疾病的药物或化妆品的原料。
本发明的效果不限于上述效果,而本领域技术人员将从下文描述中清楚地了解未提及的其他效果。
附图说明
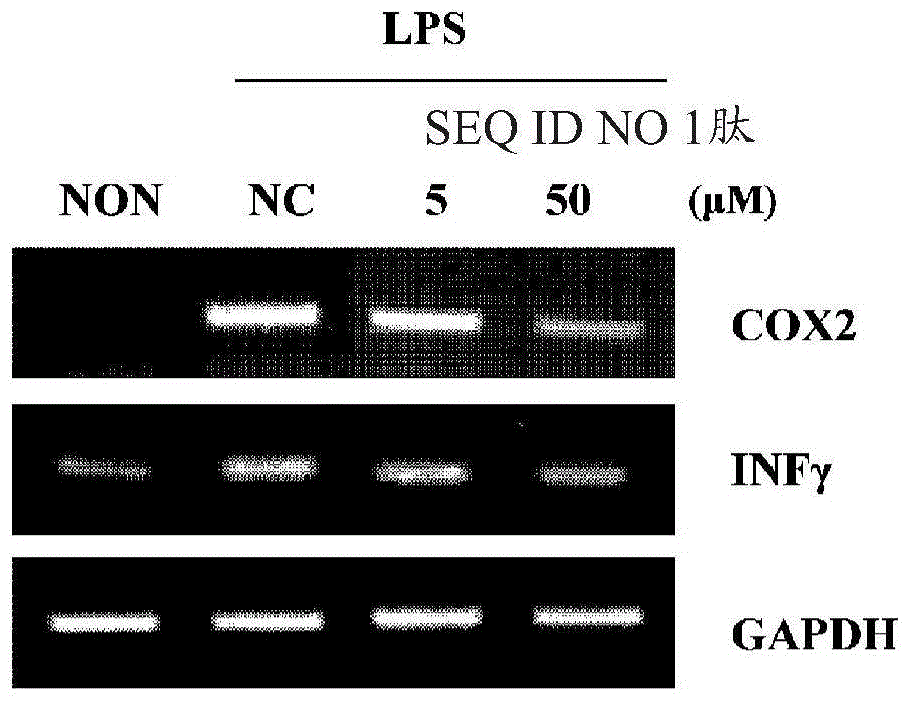
图1是RT-PCR电泳图像,示出了本发明的肽对脾细胞中由LPS诱导的COX-2和IFN-γ表达的影响。
图2a是ELISA结果的图,示出了本发明的肽对脾细胞中由LPS诱导的TNF-α分泌的影响。
图2b是ELISA结果的图,示出了本发明的肽对脾细胞中由LPS诱导的IFN-γ分泌的影响。
图2c是ELISA结果的图,示出了本发明的肽对脾细胞中由LPS诱导的IL-17分泌的影响。
图3a是ELISA结果的图,示出了本发明的肽对脾细胞中TNF-α分泌的影响。
图3b是ELISA结果的图,示出了本发明的肽对脾细胞中由TNF-α诱导的IL-1β分泌的影响。
图3c是ELISA结果的图,示出了本发明的肽对脾细胞中由TNF-α诱导的IFN-γ分泌的影响。
图4是ELISA结果的图,示出了本发明的肽对脾细胞中由LPS、TGF-β和IL-23诱导的IFN-γ分泌的影响。
图5是ELISA结果的图,示出了本发明的肽对脾细胞中由TNF-α和IL-17A诱导的IL-17分泌的影响。
图6是RT-PCR电泳图像,示出了本发明的肽对角质细胞中由TNF-α和hIL-17A诱导的TNF-α、COX2、IL-6和IL-8表达的影响。
图7是蛋白质印迹电泳图像,示出了本发明的肽对角质细胞中由TNF-α和hIL-17A诱导的iNOS和JNK表达的影响。
具体实施方式
下文,将详细描述本发明。
本发明的一个方面提供了包含SEQ ID NO:1所示的氨基酸序列的肽。
如本文中所使用的,术语“肽”是指由氨基酸残基组成的线性分子,并且具体地,本发明的肽可包含SEQ ID NO:1所示的氨基酸序列。
“肽”可以是由于氨基酸残基的缺失、插入、取代或组合而具有不同序列的氨基酸的变体或片段,只要它们不影响其功能即可。不改变肽整体活性的氨基酸交换是本领域已知的。在某些情况下,肽可以通过磷酸化、硫酸化、丙烯酸化、糖基化、甲基化、法尼基化等进行修饰。因此,本发明的肽包括具有与包含SEQ ID NO:1的氨基酸序列的肽基本相同的氨基酸序列的肽,及其变体或活性片段。
基本相同的蛋白是指与SEQ ID NO:1的氨基酸序列具有75%或更高、优选80%或更高、例如85%或更高、90%或更高、95%或更高、98%或更高或者99%或更高的序列同源性的氨基酸序列,但不限于此,只要该蛋白具有75%或更高的氨基酸序列同源性并具有相同的活性,其就涵盖在本发明的范围内。
此外,本发明的肽可额外地包括靶向序列、标签、经标记的残基、用于增加肽的半衰期或稳定性的特定目的而制备的氨基酸序列。
此外,为了获得更好的化学稳定性、增强的药理学性质(半衰期、吸收、效价、功效等)、改变的特异性(例如广谱生物活性)和降低的抗原性,可以将保护基团附接到本发明肽的N-末端或C-末端。术语“稳定性”用于不仅涵盖体内稳定性(其保护本发明的肽免受体内蛋白酶的攻击),还涵盖储存稳定性(例如室温下的储存稳定性)。
N-末端修饰可以是其中选自由乙酰基、芴基甲氧羰基、甲酰基、棕榈酰基、肉豆蔻基、硬脂基和聚乙二醇(PEG)组成的组的保护基团结合到肽的N-末端的修饰,但不限于此。
C-末端修饰可以是其中羟基(-OH)、氨基(-NH
本发明肽的合成可例如使用装置或基因工程技术来进行。当使用装置进行合成时,可以在自动肽合成仪中使用Fmoc固相法来合成所需的肽。
在本发明的具体实施例中,使用Fmoc固相方法合成并鉴定本发明的包含SEQ IDNO:1的氨基酸序列的肽,并通过验证其功效来选择所鉴定的肽。
在本发明的具体实施例中,为了验证所鉴定的肽的功效,通过验证抑制炎性细胞因子的表达或活性的效果来选择本发明的肽。
因此,本发明的包含SEQ ID NO:1的氨基酸序列的肽具有抗炎活性。
本发明的另一方面提供了一种抗炎组合物,其包括:包含SEQ ID NO:1的氨基酸序列的肽作为活性成分。
所使用的术语“抗炎”或“抑制炎症”的含义包括改善(缓解症状)、治疗和抑制或延迟炎性疾病的发生,定义如下。
在本发明的具体实施方式中,表明本发明的包含SEQ ID NO:1的氨基酸序列的肽抑制用LPS刺激的脾细胞中环氧合酶-2(COX-2)和干扰素-γ(IFN-γ)的表达,并且抑制选自由肿瘤坏死因子α(TNF-α)、INF-γ和白介素17(IL-17)组成的组中的任一种炎性细胞因子的分泌。
此外,该肽显示出抑制用TNF-α刺激的脾细胞中炎性细胞因子的分泌,所述炎性细胞因子选自由TNF-α、白介素-1β(IL-1β)和IFN-γ组成的组中的任一种。
此外,发现,该肽抑制LPS、TGF-β和IL-23刺激的脾细胞中IFN-γ的分泌,并且抑制TNF-α和IL-17A刺激的脾细胞中IL-17的分泌。
此外,发现该肽抑制HaCaT细胞中炎性细胞因子(例如,TNF-α、IL-6和IL-8)和COX2的表达,这是TNF-α和IL-17A诱导的用于银屑病皮炎的体外测试模型,并降低炎性介质(例如,iNOS和JNK)的活性。
从这些结果可以看出,本发明的肽通过调节炎性细胞因子基因的表达来抑制炎性细胞因子并阻断炎性反应,例如通过调节COX-2和INOS的表达来抑制PGE2和NO的产生并抑制JNK活性,来具有抗炎作用。此外,这些结果表明,本发明的肽不仅通过其具有的抗炎活性对一般炎性疾病具有治疗作用,而且对治疗包括银屑病在内的自身免疫性疾病也具有作用。
本发明的又一方面提供了一种用于预防或治疗炎性疾病的药物组合物,其包括包含SEQ ID NO:1的氨基酸序列的肽作为活性成分。
如本文中所使用的,术语“炎性疾病”可定义为病理症状,其由炎性反应引起,该炎性反应特征为对来自外部物理和化学刺激或外部感染因子(例如,细菌、真菌、病毒、各种过敏原等)的自身免疫或感染的局部或全身生物防御反应。炎性反应涉及一系列复杂的生理反应,诸如各种炎性介质和与免疫细胞相关的酶(例如,iNOS、COX-2等)的激活、炎性介质的分泌(例如,TNF-α、IL-6、IL-8、IL-17、IL-1β、IFN-γ等的分泌)、体液的渗透、细胞迁移、组织破坏等,并可能通过诸如红斑、疼痛、水肿、发烧和身体某些功能的退化或丧失等症状在外部出现。
由于炎性疾病可以是急性、慢性、溃疡性、过敏性或坏死性疾病,因此其包括所有急性、慢性、溃疡性、过敏性或坏死性疾病,只要所有疾病被包括为如上所述的炎性疾病。
具体地,所述炎性疾病可以是炎性皮肤疾病或炎性自身免疫性疾病。
炎性皮肤疾病可包括特应性皮炎、接触性皮炎、过敏性皮肤病、痤疮和荨麻疹。
炎性自身免疫性疾病可以是银屑病、系统性硬皮病、系统性红斑狼疮、类风湿性关节炎、哮喘、溃疡性结肠炎、白塞氏病(Behcet's disease)、克罗恩病、多发性硬化症、皮肌炎、胶原病、血管炎、关节炎、肉芽肿病、器官特异性自身免疫性病变、移植物抗宿主病(GvHD)等。
如本文中所使用的,术语“预防”是指通过本发明的肽或包含本发明的肽的组合物抑制或延迟炎症的发生、扩散和复发的所有行为。
如本文中所使用的,术语“改善或治疗”是指通过本发明的肽或包含本发明的肽的组合物有益地改变炎症,例如延迟、停止或逆转炎症的进展的所有行为。
在本发明的具体实施方式中,肽可通过抑制脾细胞中COX-2和IFN-γ的表达以及TNF-α、IL-17、IFN-γ、IL-1β和IL-17的分泌来预防、改善或治疗炎性疾病。
此外,肽可通过抑制角质细胞中炎性细胞因子(例如,TNF-α、IL-6和IL-8)和COX2的表达并减少炎性介质(例如,iNOS和JNK)的表达来预防、改善或治疗炎性疾病。
本发明的药物组合物可进一步包括药学上可接受的载体。
作为药学上可接受的载体,可进一步包括用于口服施用的载体或用于肠胃外施用的载体。用于口服施用的载体可包括乳糖、淀粉、纤维素衍生物、硬脂酸镁、硬脂酸等。此外,用于肠胃外施用的载体还可包括水、合适的油、盐水、水性葡萄糖(aqueous glucose)和二醇类等。此外,可包括稳定剂和防腐剂。合适的稳定剂包括抗氧化剂,诸如亚硫酸氢钠、亚硫酸钠或抗坏血酸。合适的防腐剂包括苯扎氯铵、对羟基苯甲酸甲酯或对羟基苯甲酸丙酯,以及氯丁醇。作为合适的药学上可接受的载体,可提及描述在Remington's PharmaceuticalSciences(19th ed.,Mack Publishing Company,Easton,PA,1995)中的那些。
本发明的药物组合物可通过任何方法施用至包括人类在内的哺乳动物。例如,组合物可以口服或肠胃外施用,并且肠胃外施用方法可以是静脉内、肌内、动脉内、髓内、鞘内、心内、经皮、皮下、腹膜内、鼻内、肠内、局部、舌下或直肠施用,但不限于此。
本发明的药物组合物可依据如上所述的施用途径配制成口服或肠胃外施用制剂,并且肠胃外施用制剂可在配制成注射用制剂或外用制剂后特定使用。
本发明的药物组合物以药学有效量来施用。在本发明中,“药学有效量”是指足以以适用于医学治疗的合理益处/风险比来治疗疾病的量,并且有效剂量水平可以基于包括患者疾病的类型和严重程度、药物的活性、对药物的敏感性、施用时间、施用途径和排泄率、治疗持续时间和同时使用的药物在内的因素以及医学领域公知的其他因素来确定。该药物组合物可以作为单独的治疗剂或与其他抗炎剂组合来施用,并且可以与常规治疗剂同时、分别或依次施用,且可以施用一次或多次。考虑所有上述因素,重要的是施用能够以最小量实现最大作用而没有副作用的量,这可以由本领域技术人员容易地确定
药物组合物的有效量可根据患者的年龄、性别、状况、体重、活性成分在体内的吸收程度、灭活率、排泄率、疾病类型以及联合施用的药物而变化,可依据施用途径、严重程度、性别、体重、年龄等来增加或减少,例如,药物组合物可以以每天每kg患者体重约0.0001μg至约500mg,优选0.01μg至100mg的量来施用。
本发明的又一方面提供了用于抗炎的化妆品组合物,其包括包含SEQ ID NO:1的氨基酸序列的肽作为活性成分。
化妆品组合物可制备成本领域常用的任何制剂,例如,可配制成溶液、悬浮液、乳液、糊剂、凝胶、霜剂、化妆水、粉末、皂剂(soap)、含表面活性剂的清洁剂、油(oil)、粉状粉底液(powder foundation)、乳状粉底液(an emulsion foundation)、蜡状粉底液(waxfoundation)、喷雾剂等,但不限于此。
化妆品组合物包括柔肤水(softening lotion)、营养水(nourishing lotion)、润肤霜(nourishing cream)、按摩霜、精华液、眼霜、清洁霜、清洁泡沫、清洁水、面膜、喷雾剂、粉末、生发油(hair tonic)、发乳(hair cream)、发液(hair lotion)、洗发香波(hairshampoo)、护发素、发胶(hair spray)、气雾型喷发胶(hair aerosol)、润发油(pomade)、溶液(例如凝胶等)、溶胶-凝胶、乳液、油、蜡、气雾剂等,但不限于此。
本发明的化妆品组合物可包括其他添加剂,诸如赋形剂和载体,并且必要时可施加并混合通用皮肤化妆品中混合的常用成分。
当化妆品组合物的制剂为糊剂、霜剂或凝胶时,可使用动物油、植物油、蜡、石蜡、淀粉、黄蓍胶、纤维素衍生物、聚乙二醇、硅酮、膨润土、二氧化硅、滑石、氧化锌等作为载体成分。
当化妆品组合物的制剂为粉末或喷雾剂时,可使用乳糖、滑石粉、二氧化硅、氢氧化铝、硅酸钙或聚酰胺粉末作为载体成分;并且特别是在喷雾剂的情况下,可包括额外的推进剂(例如氯氟烃、丙烷/丁烷,或二甲醚),但不限于此。
当化妆品组合物的制剂为溶液或乳液的形式时,可使用溶剂、增溶剂或乳化剂作为载体成分,例如使用水、乙醇、异丙醇、碳酸乙酯、乙酸乙酯、苯甲醇、苯甲酸苄酯、丙二醇、1,3-丁二醇油、甘油脂肪酸酯、聚乙二醇或脱水山梨聚醇(sorbitan)的脂肪酸酯等。
当化妆品组合物的制剂为悬浮液的形式时,可使用液体稀释剂(例如水、乙醇、丙二醇等)、悬浮剂(例如乙氧基化异硬脂醇、聚氧乙烯山梨醇酯、聚氧乙烯脱水山梨醇酯等)、微晶纤维素、偏氢氧化铝(aluminum metahydroxide)、膨润土、琼脂、黄蓍胶等作为载体成分。
当化妆品组合物的制剂为含表面活性剂的清洁剂时,可使用脂肪醇硫酸盐/酯、脂肪醇醚硫酸盐/酯、磺基琥珀酸单酯、羟乙磺酸盐/酯、咪唑啉衍生物、牛磺酸甲酯、肌氨酸盐/酯、脂肪酸酰胺醚硫酸盐/酯、烷基酰胺甜菜碱、脂肪醇、脂肪酸甘油酯、脂肪酸二乙醇酰胺、植物油、羊毛脂衍生物、乙氧基化甘油脂肪酸酯等作为载体成分。
当化妆品组合物的制剂为洗发香波时,本发明的肽可与配制香波的基本成分混合,诸如与增稠剂、表面活性剂、粘度调节剂、润湿剂、pH调节剂、防腐剂、精油等混合。可使用CDE作为增稠剂;可使用LES(即阴离子表面活性剂)和椰油甜菜碱(即两性表面活性剂)作为表面活性剂;可使用聚季(poly quarter)作为粘度调节剂;可使用甘油作为润湿剂;并且可使用柠檬酸和氢氧化钠作为pH调节剂。可使用葡萄柚提取物(grapefruit extract)等作为防腐剂;并且,此外,可加入使用精油(例如雪松、薄荷和迷迭香等)、蚕丝氨基酸(silkamino acids)、戊醇或维生素E。
除本发明的肽和载体成分之外,化妆品组合物中包含的成分可进一步包括化妆品组合物中常用的佐剂作为活性成分,诸如抗氧化剂、稳定剂、增溶剂、维生素、色素和香料等,但不限于此。
如上所述,本发明的肽具有优异的抑制炎症的效果,且因此可用作用于预防、改善或治疗炎性疾病的药物或者用于改善皮肤炎症的化妆品的原料。
本发明的又一方面提供了用于预防或治疗炎性疾病的方法,该方法包括向受试者施用治疗有效量的包含SEQ ID NO:1的氨基酸序列的肽。
包含SEQ ID NO:1的氨基酸序列的肽与在“用于预防或治疗炎性疾病的药物组合物”部分中描述的肽相同,因此使用上文具体描述。
如本文中所使用的,术语“治疗有效量”是指在用肽治疗期间能够实现改善疾病发生率的目标,但能够避免通常与其他治疗相关的有害副作用的肽的量。
本发明的又一方面提供了SEQ ID NO:1的氨基酸序列在制备用于预防或治疗炎性疾病的药物中的用途。
下文中,将通过实施例和实验例详细来描述本发明。
然而,以下实施例和实验实施例仅用于说明本发明,本发明的内容不受以下实施例和实验例的限制。
实施本发明的方式
[合成例1]
包含SEQ ID NO:1的氨基酸序列的肽的合成
使用自动肽合成仪(Liberty,CEM Corporation,USA)来合成下[表1]中所示的具有SEQ ID NO:1的氨基酸序列的肽,并且使用C18反相高效液相色谱(HPLC)(U-3000,hermoFisher Scientific,USA)来对这些合成的肽进行纯化。使用的柱是Pursuit XRs C18(250mm×4.65mm
[表1]
[实验例1]
证实抑制脾细胞中LPS诱导的炎症的效果
<1-1>
为了证实合成例1中合成的本发明的肽对LPS诱导的炎性反应的效果,通过RT-PCR测量炎性细胞因子COX2和INFγ的mRNA表达水平。
具体地,处死6至7周龄的小鼠(C57BL/6,Young Bio Co.,Ltd.)以获得脾,使用细胞滤器破碎脾,然后与无血清RPMI-1640介质一起离心。弃去上清液,使用红细胞(RBC)裂解缓冲液去除RBC两次。然后,在用无血清RPMI-164介质洗涤所得物后,加入适量的无血清RPMI-1640介质。测量小鼠脾细胞的数量,并且以1×10
接下来,在培养后回收细胞,使用RNA提取试剂盒(Qiagen RNeasy试剂盒)提取总RNA,并且在RNA定量后,使用cDNA合成试剂盒(Intron,Korea)合成cDNA。通过混合PCR预混物(Intron,Korea)、所合成的cDNA,以及下[表2]示出的对于每个基因COX2、INFγ和GAPDH特异的引物来进行聚合酶链式反应(PCR)。PCR产物在5%琼脂糖凝胶上进行电泳,并用溴化乙锭染色以证实与炎症和自身免疫性疾病相关的基因COX2和INFγ的mRNA表达水平。
[表2]
结果,如[图1]所示,证实了用本发明的肽处理可显著降低脾细胞中由LPS产生炎性环境后相关的炎症相关基因的表达。
<1-2>
为了证实在合成例1中合成的本发明的肽对由LPS诱导的炎性反应的效果,通过ELISA测量炎性细胞因子TNF-α、IL-17和INFγ的分泌量。
具体地,处死6至7周龄的小鼠(C57BL/6,Young Bio Co.,Ltd.)以获得脾,使用细胞过滤器破碎脾,然后与无血清RPMI-1640介质离心。弃去上清液,使用红细胞(RBC)裂解缓冲液去除RBC两次。然后,在用无血清RPMI-164介质洗涤所得物后,向其中加入适量的无血清RPMI-1640介质。测量小鼠脾细胞的数量,并且以1×10
接下来,在培养后回收细胞培养物,使用对IL-17、IFN-γ和TNF-α特异的ELISA试剂盒(Quantikine ELISA试剂盒,R&D System,USA)测量为Th17分化期间的分泌标志物的IL-17、IFN-γ和TNF-α的分泌量,使用Spectramax M2(Molecular Devices)测量吸光度。
结果,如图2a至图2c所示,证实了本发明的肽可显著减少为炎性细胞因子的TNF-α、IFN-γ和IL-17的分泌。
[实验例2]
证实抑制由脾细胞中各种炎症诱导物质诱导的炎症的效果
<2-1>
为了证实在合成例1中合成的本发明的肽对由TNF-α诱导的炎性反应的效果,通过ELISA测量为炎性细胞因子的TNF-α、IL-1β和INFγ的分泌量。
具体地,处死6至7周龄的小鼠(C57BL/6,Young Bio Co.,Ltd.)以获得脾,使用细胞滤器破碎脾,然后与无血清RPMI-1640介质离心。弃去上清液,使用红细胞(RBC)裂解缓冲液去除RBC两次。然后,在用无血清RPMI-164介质洗涤所得物后,向其中加入适量的无血清RPMI-1640介质。测量小鼠脾细胞的数量,并且以1×10
接下来,在培养后回收细胞培养物,并使用对TNF-α、IL-1β和INFγ特异的ELISA试剂盒(Quantikine ELISA试剂盒,R&D System,USA)测量作为炎性细胞因子的TNF-α、IL-1β和INFγ的分泌量,并使用Spectramax M2(Molecular Devices)测量吸光度。
结果,如图3a至图3c所示,证实了本发明的肽可显著减少为炎性细胞因子的TNF-α、IL-1β和INFγ的分泌。
<2-2>
为了证实在合成例1中合成的本发明的肽对由LPS、TGF-β和IL-23诱导的炎性反应的效果,通过ELISA测量为炎性细胞因子的INFγ的分泌量。
具体地,处死6至7周龄的小鼠(C57BL/6,Young Bio Co.,Ltd.)以获得脾,使用细胞滤器破碎脾,然后与无血清RPMI-1640介质离心。弃去上清液,使用红细胞(RBC)裂解缓冲液去除RBC两次。然后,在用无血清RPMI-164介质洗涤所得物后,向其中加入适量的无血清RPMI-1640介质。测量小鼠脾细胞的数量,并且以1×10
接下来,在培养后回收细胞培养物,并使用对INFγ特异的ELISA试剂盒(Quantikine ELISA试剂盒,R&D System,USA)测量作为炎性细胞因子的INFγ的分泌量,并使用Spectramax M2(Molecular Devices)测量吸光度。
结果,如图4所示,证实了本发明的肽可显著减少为炎性细胞因子的INFγ的分泌。
<2-3>
为了证实在合成例1中合成的本发明的肽对由TNF-α和IL-17A诱导的炎性反应的效果,通过ELISA测量了为炎症细胞因子的IL-17的分泌量。
具体地,处死6至7周龄的小鼠以获得脾,使用细胞滤器破碎脾,然后与无血清RPMI-1640介质离心。弃去上清液,使用红细胞(RBC)裂解缓冲液去除RBC两次。然后,在用无血清RPMI-164介质洗涤所得物后,向其中加入适量的无血清RPMI-1640介质。测量小鼠脾细胞的数量,并且以1×10
接下来,在培养后回收细胞培养物,并使用对INFγ特异的ELISA试剂盒(Quantikine ELISA试剂盒,R&D System,USA)测量作为炎性细胞因子的IL-17的分泌量,并使用Spectramax M2(Molecular Devices)测量吸光度。
结果,如图5所示,证实了本发明的肽可显著减少为炎性细胞因子的IL-17的分泌。
[实验例3]
证实抑制角质细胞中Th17诱导的炎症的效果
<3-1>
为了证实合成例1中合成的本发明的肽对Th17介导的炎性反应的效果,通过RT-PCR测量TNF-α、COX2、IL-6和IL-8的mRNA表达水平。
具体地,测量人角质细胞HaCaT(CLS,Cell Lines Service)的数量,并将细胞以3×10
接下来,在培养后回收细胞,使用RNA提取试剂盒(Qiagen RNeasy试剂盒)提取总RNA,并且在RNA定量后,使用cDNA合成试剂盒(Intron,Korea)合成cDNA。通过混合PCR预混物(Intron,Korea)、所合成的cDNA,以及下[表3]中示出的对于每个基因TNF-α、COX2、IL-6、IL-8和GAPDH特异的引物来进行聚合酶链式反应(PCR)。PCR产物在5%琼脂糖凝胶上进行电泳,并用溴化乙锭染色以证实与炎症和自身免疫性疾病有关的基因TNF-α、COX2、IL-6和IL-8的mRNA表达水平。
[表3]
结果,如[图6]所示,证实了本发明的肽可显著降低与炎症和自身免疫相关的基因的表达。
<3-2>证实炎性细胞因子活性中的变化
为了证实在合成例1中合成的本发明的肽对Th17介导的炎性反应的作用,通过蛋白质印迹测量iNOS和pJNK的磷酸化程度,其中iNOS和pJNK是炎症诱导因子和信号传导蛋白。
具体地,测量人角质细胞HaCaT(CLS,Cell Lines Service)的数量,并将细胞以1×10
孵育后,回收细胞以制备细胞裂解物,并使用抗iNOS和pJNK(Cell SignalingTechnology,USA)的抗体进行蛋白质印迹以证实蛋白表达模式。
结果,如[图7]所示,证实了本发明的肽即使在Th17介导的炎症诱导环境中也能够降低为炎症诱导因子和信号传导蛋白的iNOS和JNK的磷酸化。
综上所述,本发明仅针对所描述的实施方式进行了详细描述,但对本领域技术人员明显的是,能够在本发明的技术范围内进行各种变动和修改,这些变动和修改自然属于所附权利要求的范围。
- 具有皮肤美白活性的凝血酸-肽及其用途
- 具有抗白血病活性的土甘草A衍生物及其制备方法和用途
- 具有抗HIV活性的双甲氧基取代咔唑类化合物制备及用途
- 具有免疫调节活性、抗炎活性和抗病毒活性的肽和肽模仿物
- 具有抗炎活性的拟肽类化合物及其制备方法和药物用途
