检测甲氨蝶呤、叶酸、5-甲酰四氢叶酸和5-甲基四氢叶酸的试剂套装
文献发布时间:2023-06-19 19:30:30
技术领域
本发明属于分析检测技术领域,涉及一种检测甲氨蝶呤、叶酸、5-甲酰四氢叶酸和5-甲基四氢叶酸的试剂套装,具体涉及一种检测甲氨蝶呤、叶酸、5-甲酰四氢叶酸和5-甲基四氢叶酸的试剂套装、试剂盒及其应用。
背景技术
叶酸又称蝶酰谷氨酸,是重要的外源性B族维生素。人体吸收的叶酸在肝内转化为四氢叶酸和其他还原型衍生物。其中,5-甲基四氢叶酸是最主要的活性代谢物,约占血浆中叶酸含量的98%,其主要的生物学功能是作为体内生化反应中的一碳单位载体,参与DNA、RNA的合成以及氨基酸的代谢。
甲氨蝶呤是一种与叶酸结构相似的抗肿瘤药物,通过干扰叶酸代谢,抑制肿瘤细胞增殖,在提高疾病缓解率和延长生存期方面具有重要作用。目前,大剂量甲氨蝶呤治疗策略广泛应用于急性淋巴细胞白血病、骨肉瘤和非霍奇金淋巴瘤等疾病的治疗。然而,甲氨蝶呤作用于肿瘤细胞的同时也会影响正常细胞代谢,造成骨髓抑制、肝肾功能损伤、消化道反应、黏膜损害以及神经系统损伤等毒副作用。临床上,通常使用5-甲酰四氢叶酸钙(人体内以5-甲酰四氢叶酸形式存在)进行毒副作用解救。5-甲酰四氢叶酸钙为5-甲酰四氢叶酸的钙盐,作为大剂量甲氨蝶呤的解毒剂被补充入体内时,可越过叶酸转变为四氢叶酸的过程,直接转变为5-甲基四氢叶酸发挥生理学效应,因而不受大剂量甲氨蝶呤的干扰。
在使用甲酰四氢叶酸钙解救甲氨蝶呤毒副作用过程中,解救次数因患者而异。例如,对于急性淋巴细胞白血病患儿,多数患儿在解救1~5次后甲氨蝶呤血药浓度降至安全范围,少数患儿则需经历30余次解救,甲氨蝶呤血药浓度才能降至可接受范围。因此,采用大剂量甲氨蝶呤治疗/5-甲酰四氢叶酸钙解救策略时,测定用药前和用药后的甲氨蝶呤、叶酸、5-甲酰四氢叶酸钙及5-甲基四氢叶酸的水平,对于急性淋巴细胞白血病、骨肉瘤和非霍奇金淋巴瘤的治疗具有重要意义。
现阶段检测人体叶酸及其代谢物的方法包括放射免疫分析法、化学发光分析法、微生物法、气相色谱-串联质谱法等,上述方法普遍存在灵敏度低、稳定性差等局限。超高效液相色谱-串联质谱是将超高效液相色谱与质谱分析技术相结合的检测方法,可以同时呈现各组分的分子量和结构信息,提高了临床检测的灵敏度和准确性。
专利CN 112083108 B公开了一种利用高效液相色谱-串联质谱联用技术定量检测人体内叶酸及其主要代谢产物(5-甲基四氢叶酸和5-甲酰四氢叶酸)的方法。专利CN112834677 A公开了一种液相色谱-串联质谱联用技术同时检测同型半胱氨酸及代谢相关物质(甲硫氨酸、吡哆醇、叶酸和5-甲基四氢叶酸)的方法。此外,专利CN 105181829 B公开了一种超高效液相色谱-串联质谱联用技术同步检测植物叶片总叶酸及叶酸衍生物(四氢叶酸、5-甲基四氢叶酸、5-甲酰四氢叶酸、5,10-亚甲基四氢叶酸、10-甲酰叶酸、10-甲酰四氢叶酸)含量的方法。专利CN110146626A公开了一种高效液相色谱-串联质谱联用技术测定血斑中叶酸和5-甲基四氢叶酸含量的方法。专利CN 11309033 A公开了一种高效液相色谱-串联质谱联用技术测定人体内叶酸、四氢叶酸、5-甲基四氢叶酸、5-甲酰四氢叶酸、5,10-亚甲基四氢叶酸、S-腺苷甲硫氨酸、S-腺苷同型半胱氨酸和同型半胱氨酸含量的方法。上述方法能够对叶酸及其代谢物进行测定,但未能对与叶酸结构相似的治疗药物甲氨蝶呤进行联合检测。因而,现有技术无法解决急性淋巴细胞白血病、骨肉瘤和非霍奇金淋巴瘤等疾病治疗过程中治疗药物、解救药物及相关物质的体内水平的同时监测。
发明内容
本发明所要解决的技术问题是针对上述现有技术不足和临床治疗重大需求提供一种检测甲氨蝶呤、叶酸、5-甲酰四氢叶酸和5-甲基四氢叶酸的试剂套装和试剂盒,利用该试剂套装或试剂盒能够同时定量检测检测甲氨蝶呤、叶酸、5-甲酰四氢叶酸和5-甲基四氢叶酸。
本发明还提供了上述试剂套装在制造所述试剂盒中的应用,利用该试剂盒能够准确掌握治疗药物、解救药物及相关物质的体内水平。
为此,本发明第一方面提供了一种检测甲氨蝶呤、叶酸、5-甲酰四氢叶酸和5-甲基四氢叶酸的试剂套装,其能够同时定量检测甲氨蝶呤、叶酸、5-甲酰四氢叶酸和5-甲基四氢叶酸,其由固相萃取板、标准溶液、内标溶液、活化溶液、溶液A、溶液B和质控样本组成。
本发明中,所述固相萃取板为混合阴离子型固相萃取板,其能够特异性结合酸性化合物。
根据本发明,所述溶液A由溶剂A与抗氧化剂配制而成;其中,溶剂A为99.9%纯水+0.1%氨水,所述抗氧化剂为抗坏血酸、柠檬酸、2-巯基乙醇和二硫苏糖醇;在所述溶液A中,所述抗坏血酸、柠檬酸、2-巯基乙醇和二硫苏糖醇浓度分别独立地为20-100μg/mL。
在本发明的一些实施例中,所述标准溶液为用溶液A配制的甲氨蝶呤、叶酸、5-甲酰四氢叶酸和5-甲基四氢叶酸的标准品溶液,其中,甲氨蝶呤、叶酸、5-甲酰四氢叶酸和5-甲基四氢叶酸标准品的浓度范围为0.1ng/mL~5000ng/mL。
在本发明的另一些实施例中,所述内标溶液为用溶液A配制的甲氨蝶呤、叶酸、5-甲酰四氢叶酸和5-甲基四氢叶酸的同位素标准品溶液,其中,甲氨蝶呤、叶酸、5-甲酰四氢叶酸和5-甲基四氢叶酸同位素标准品的浓度范围为0.1ng/mL~500ng/mL。
根据本发明,所述溶液B由溶剂B与抗氧化剂配制而成;其中,溶剂B为98%甲醇+2%甲酸,所述抗氧化剂为抗坏血酸、柠檬酸、2-巯基乙醇和二硫苏糖醇;在所述溶液B中,所述抗坏血酸、柠檬酸、2-巯基乙醇和二硫苏糖醇浓度分别独立地为20-100μg/mL。
本发明中,采用含抗坏血酸、柠檬酸、2-巯基乙醇和二硫苏糖醇的氧化剂的混合液作为叶酸代谢物的保护剂,增加了叶酸代谢物的稳定性,提高了叶酸代谢物定量检测的可靠度。
在本发明的一些实施例中,所述活化溶液为甲醇;和/或,所述质控样本为含有甲氨蝶呤、叶酸、5-甲酰四氢叶酸和5-甲基四氢叶酸的血清样本,共有低浓度、中浓度和高浓度3份样本。
本领域技术人员应该了解的是,用作质控样本的血清样本中的甲氨蝶呤、叶酸、5-甲酰四氢叶酸和5-甲基四氢叶酸的低浓度、中浓度和高浓度范围并不完全相同。
例如,在一些例子中,用作质控样本的血清样本中所含叶酸的的低浓度为5ng/mL、中浓度为20ng/mL、高浓度为100ng/mL。
在另一些例子中,用作质控样本的血清样本中所含5甲基四氢叶酸、5甲酰四氢叶酸和甲氨喋呤的低、中浓度分别独立地为50、200和1000ng/mL。
本发明第二方面提供了一种检测甲氨蝶呤、叶酸、5-甲酰四氢叶酸和5-甲基四氢叶酸的试剂盒,其含有如本发明第一方面所述的试剂套装。
本发明第三方面提供了一种如本发明第一方面所述的试剂套装在制备检测人体内甲氨蝶呤、叶酸、5-甲酰四氢叶酸和5-甲基四氢叶酸的试剂盒中的应用,其包括:
步骤L,将待测样本或标准溶液与内标溶液和溶液A混合均匀,获得第Ⅰ混合液;
步骤M,用活化溶液和溶液A依次对固相萃取板进行活化、平衡处理;加入步骤L的第Ⅰ混合液进行上样;用溶液A洗涤固相萃取板;用溶液B洗脱得到目标组分溶液;氮吹至干燥;加入溶液A复溶,得到待测溶液;
步骤N,采用超高效液相色谱-串联质谱联用技术测定步骤M得到的待测溶液,采用内标外标曲线法,计算样品溶液中甲氨蝶呤、叶酸、5-甲酰四氢叶酸和5-甲基四氢叶酸的含量。
在本发明的一些实施例中,步骤M中的超高效液相色谱条件如下:色谱柱:HSS T32.1(内径)×100mm(长度),粒径1.8μm;柱温:40℃;流动相A为水+0.1%甲酸;流动相B为乙腈;梯度洗脱:0~0.5min,A 92%~92%;0.5~2.5min,A 92%~75%;2.5~2.6min,A75%~5%;2.6~3.0min,A 5%~5%;3.0~4.0min,A 5%~92%;
和/或,步骤M中的质谱条件如下:离子化模式:ESI+,多反应监测模式。毛细管电压:1KV,锥孔电压:50V,锥孔气流速:50L/Hr,脱溶剂温度:500℃,脱溶剂流速:1000L/Hr(小时)。
目标物质的检测参数如下:
表1.目标物质检测参数表
本发明中上述应用可以理解为利用本发明所提供的试剂套装或试剂盒同检测甲氨蝶呤、叶酸、5-甲酰四氢叶酸和5-甲基四氢叶酸的方法。
本发明中所述用语“日内精密度”是指在同一天内不同时间对同一被测物进行次平行测定时,各个结果间的接近程度。
本发明中所述用语“日间精密度”是指在不同天内对同一被测物进行重复测量所得结果间的一致程度。
本发明提供了一种同时检测甲氨蝶呤、叶酸、5-甲酰四氢叶酸和5-甲基四氢叶酸的试剂套装和试剂盒。本发明还提供了利用该试剂套装或试剂盒同时检测甲氨蝶呤、叶酸、5-甲酰四氢叶酸和5-甲基四氢叶酸的方法。与背景技术部分的现有技术方案相比,该方法通过特异性固相萃取板,对血液中的上述物质进行有效富集;同时,用含抗坏血酸、柠檬酸、2-巯基乙醇和二硫苏糖醇的混合液作为叶酸代谢物的保护剂,增加了叶酸代谢物的稳定性,提高了叶酸代谢物定量检测的精确度和可靠度;从而实现了甲氨蝶呤、叶酸、5-甲酰四氢叶酸和5-甲基四氢叶酸的高效、稳定、精准检测。本方法具有线性范围宽、精密度高、重现性好、操作简便、易于推广等优点,对于推动急性淋巴细胞白血病、骨肉瘤和非霍奇金淋巴瘤治疗过程中药物监测技术的更新与升级以及患者的治疗安全具有重要意义。
附图说明
下面结合附图来对本发明作进一步详细说明:
图1为四种待测物的标准品定量限色谱图,其中,a)为甲氨蝶呤,b)为叶酸,c)为5-甲酰四氢叶酸,d)为5-甲基四氢叶酸。
图2示出四种待测物的标准曲线,其中,a)为甲氨蝶呤,b)为叶酸,c)为5-甲酰四氢叶酸,d)为5-甲基四氢叶酸。
图3示出四种待测物的QC血清样本分离结果。
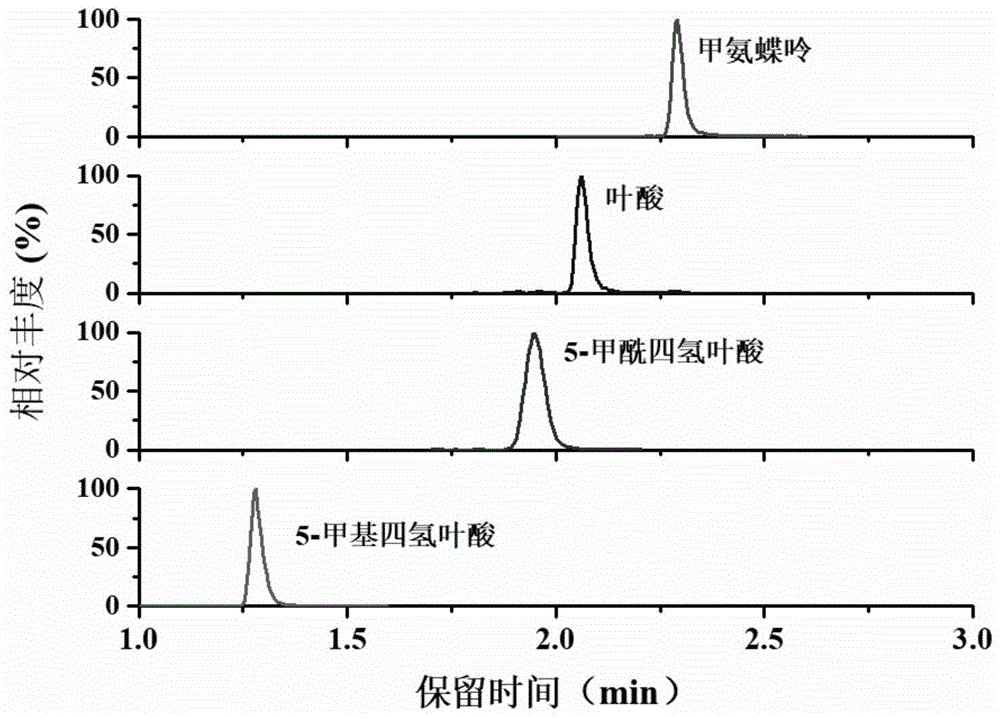
图4示出四种待测物的标准品溶液分离结果。
具体实施方式
为使本发明容易理解,下面将结合附图详细说明本发明。但在详细描述本发明前,应当理解本发明不限于描述的具体实施方式。还应当理解,本文中使用的术语仅为了描述具体实施方式,而并不表示限制性的。
在提供了数值范围的情况下,应当理解所述范围的上限和下限和所述规定范围中的任何其他规定或居间数值之间的每个居间数值均涵盖在本发明内。这些较小范围的上限和下限可以独立包括在较小的范围中,并且也涵盖在本发明内,服从规定范围中任何明确排除的限度。在规定的范围包含一个或两个限度的情况下,排除那些包括的限度之任一或两者的范围也包含在本发明中。
除非另有定义,本文中使用的所有术语与本发明所属领域的普通技术人员的通常理解具有相同的意义。虽然与本文中描述的方法和材料类似或等同的任何方法和材料也可以在本发明的实施或测试中使用,但是现在描述了优选的方法和材料。
实施例
以下通过具体实施例对于本发明进行具体说明。下文所述实验方法,如无特殊说明,均为实验室常规方法。下文所述实验材料,如无特别说明,均可由商业渠道获得。
实施例1:
一种精准测定血液中甲氨蝶呤、叶酸、5-甲酰四氢叶酸和5-甲基四氢叶酸的试剂盒,所述试剂盒组成如下:
表2.试剂盒组成
上述质控样本包含3个浓度的甲氨蝶呤、叶酸、5-甲酰四氢叶酸和5-甲基四氢叶酸血清样本;其中,叶酸的低浓度为5ng/mL、中浓度为20ng/mL、高浓度为100ng/mL;5甲基四氢叶酸、5甲酰四氢叶酸和甲氨喋呤的低、中、高浓度分别独立地为50、200和1000ng/mL。
标准溶液中甲氨蝶呤、5-甲酰四氢叶酸和5-甲基四氢叶酸的浓度分别独立地如下:5、10、20、50、100、500、1000和2000ng/mL;叶酸的浓度如下:1、2、5、10、20、50、100和200ng/mL。
实施例2:
一种精准测定血液中甲氨蝶呤、叶酸、5-甲酰四氢叶酸和5-甲基四氢叶酸的方法,其包括:
A.将100μL质控样本或标准溶液与20μL内标溶液和300μL溶液A混合均匀,获得第Ⅰ混合液;
B.用200μL活化溶液和200μL溶液A依次对固相萃取板进行活化、平衡处理;加入步骤A的第Ⅰ混合液进行上样;用200μL溶液A洗涤固相萃取板;用40μL溶液B洗脱得到目标组分溶液;氮吹至干燥;加入80μL溶液A复溶,得到待测溶液。
C.采用超高效液相色谱-串联质谱联用技术测定步骤B)得到的待测溶液,采用内标外标曲线法,计算样品溶液中甲氨蝶呤、叶酸、5-甲酰四氢叶酸和5-甲基四氢叶酸的含量。
色谱条件如下:色谱柱:HSS T3 2.1(内径)×100mm(长度),粒径1.8μm;柱温:40℃;流动相A为水+0.1%甲酸;流动相B为乙腈;梯度洗脱:0~0.5min,A 92%~92%;0.5~2.5min,A 92%~75%;2.5~2.6min,A 75%~5%;2.6~3.0min,A 5%~5%;3.0~4.0min,A 5%~92%。
质谱条件如下:离子化模式:ESI+,多反应监测模式。毛细管电压:1KV,锥孔电压:50V,锥孔气流速:50L/Hr,脱溶剂温度:500℃,脱溶剂流速:1000L/Hr。目标物质的检测参数如下:
表3.目标物质检测参数表
备注:使用叶酸的同位素内标进行5-甲酰四氢叶酸定量。
参照美国临床实验室标准协会发布的《质谱分析方法开发和验证的标准规程》CLSI C62-A文件以及中国医师协会检验医师分会临床质谱检验医学专业委员会发表的《液相色谱串联质谱临床检测方法的开发与验证》等文件,对该方法的定量限、线性范围、精密度、准确度、专属性和干扰试验等方面性能进行了评价,考察了该方法的临床适用性。
定量限
将甲氨蝶呤、叶酸、5-甲酰四氢叶酸和5-甲基四氢叶酸的标准品待测溶液进样检测,根据待测物的标准曲线,满足平均信噪比大于10时对应的标准品中待测物的浓度即可定义为本次检测方法的定量限。四种待测物定量限如表4所示,四种待测物的色谱图见图1,均满足临床检测需求。
表4.四种待测物的定量限
线性范围
分别进样不同浓度的标准溶液待测溶液。结果显示四种待测物的浓度和响应值之间呈线性,线性相关系数R
表5.四种待测物线的性范围
连续3天,分别测定3个浓度(低、中、高浓度)的质控样本,每个浓度平行测定5次,计算日内精密度和日间精密度。结果如表6所示,待测物的日内精密度和日间精密度均在可接受范围(±15%)内。
表6.方法测定待测物的日内精密度和日间精密度
准确度
分别测定3个浓度(低、中、高浓度)的质控样本,其中,叶酸的低浓度为5ng/mL、中浓度为20ng/mL、高浓度为100ng/mL;5-甲基四氢叶酸、CF和甲氨蝶呤的浓度分别为50、200和1000ng/mL。每个浓度分别设置5个平行样本,将样本进样检测后定量分析,计算加标回收率。结果见表7,待测物的加标回收率均在可接受范围(±15%)内,验证结果符合要求。
表7.方法测定待测物的准确度
专属性和干扰试验
将低浓度质控样品和标准溶液待测溶液分别进样测定,四种待测物的QC血清样本分离结果如图3所示,四种待测物的标准品溶液分离结果如图4所示,对比图3和图4可以看出,甲氨蝶呤、叶酸、5-甲酰四氢叶酸和5-甲基四氢叶酸可通过超高效液相色谱完全分离,因此该检测方法可以有效避免血清样品中的基质干扰以及待测物之间的相互干扰,专属性强。
应当注意的是,以上所述的实施例仅为本发明较佳实施例,用于解释本发明,并不构成对本发明的任何限制。通过参照典型实施例对本发明进行了描述,但应当理解为其中所用的词语为描述性和解释性词汇,而不是限定性词汇。可以按规定在本发明权利要求的范围内对本发明做出修改,以及在不背离本发明的范围和精神内对本发明进行修订。尽管其中描述的本发明涉及特定的方法、材料和实施例,但是并不意味着本发明限于其中公开的特定例,相反,本发明可扩展至其他所有具有相同功能的方法和应用。
- 一种5-甲基四氢叶酸化学发光检测试剂盒及其制备方法
- 一种5-甲基四氢叶酸化学发光检测试剂盒及其制备方法
