一种用于基因治疗的组成型启动子
文献发布时间:2024-04-18 19:52:40
技术领域
本发明涉及基因工程技术领域,具体涉及一种用于基因治疗的组成型启动子。
背景技术
CYP4V2基因属于细胞色素氧化酶P450家族V亚科,基因全长19.28kb,包含11个外显子,编码产物为525个氨基酸的蛋白质,主要发挥脂肪酸的ω-氢基化作用,在生物体内主要催化多不饱和脂肪酸代谢,其内源性的底物是ω-3族多不饱和脂肪酸。在眼部,CYP4V2是最主要的细胞色素酶,底物主要为二十二碳六烯酸(DHA)。
结晶样视网膜变性(BCD)是常染色体隐性遗传性疾病,主要是由于CYP4V2基因突变引起的一种相对罕见的视网膜变性,在1937年由Bietti首次报道。典型的症状为黄白色闪光结晶样物质沉积于视网膜,伴有视网膜色素上皮萎缩、变性和脉络膜毛细血管硬化。BCD患者在世界范围内比较罕见,发病率大约为1/67000,在亚洲的病例相对较多,发病率大约为1/24000。研究表明,CYP4V2蛋白在人的视网膜和ARPE-19细胞的内质网中呈高表达,在角膜上皮也可检测到其表达。
基因疗法是一种通过将治疗性遗传物质转移到靶细胞来治疗某些疾病的方法。近年来,基因治疗研究发展迅速,在多种罕见病中表现优异,是一种理想的治疗方法。基因治疗的三个要素包括靶细胞、核酸和转移方法。因此,在基因治疗过程中,选择合适的载体,可控有效的表达,是成功的关键之一。目前已确定CYP4V2基因为BCD的致病基因,可用基因诊断的方法对患者及携带者进行筛查,但尚无有效的治疗方法,因此利用基因疗法建立针对BCD的治疗体系对于结晶样视网膜变性的临床研究和诊断具有重要的意义。
发明内容
有鉴于此,本发明要解决的技术问题在于提供一种用于基因治疗的组成型启动子。本发明提供了经过两轮优化后的CYP4V2基因的核心启动子,以及该组成型启动子在治疗结晶样视网膜变性疾病中的应用。
本发明提供了一种组成型启动子,其包括启动子、特异性元件和/或转录因子;
所述启动子为cyp4v2基因上游的启动子,其核酸序列如SEQ ID NO:1~6中的任一项所示;
所述特异性元件为RPE特异性元件,其特异性靶向视网膜色素上皮蛋白;
所述转录因子为构成性转录因子。
其中,所述启动子的核酸序列如SEQ ID NO:2所示;
所述RPE特异性元件的核酸序列如SEQ ID NO:7所示;
所述构成性转录因子的核酸序列如SEQ ID NO:8所示。
本发明提供的所述组成型启动子,包含cyp4v2基因上游约600bp的核心启动子,其核酸序列如SEQ ID NO:2所示,其表达活性比SEQ ID NO:1、SEQ ID NO:3~6所示的cyp4v2基因上游的300bp启动子、900bp启动子、1200bp启动子、1500bp启动子或2000bp启动子的表达活性都要高。所述启动子表达活性通过双荧光系统试验来检测,不同的组成型启动子中分别增加有荧光素酶。所述RPE特异性元件为视网膜色素上皮启动子,特异性靶向视网膜色素上皮相关蛋白,所述构成性转录因子能够与cyp4v2基因5’端上游特定序列专一性结合,保证了cyp4v2基因的稳定转录,进一步增强了所述组成型启动子的表达活性。
进一步的,本发明所述的组成型启动子还包括增强子;所述增强子为CMVenhancer,是巨噬细胞病毒增强子,能够进一步增强细胞中重组蛋白的高效表达,其具有如SEQ ID NO:9所示的核酸序列。
更进一步的,所述组成型启动子还包括内含子;所述内含子选自CBAintron、Shorten CBA intron、Hybrid intron和/或EF1αintron。
具体的,在本发明的实施例中,通过对所述cyp4v2基因上游约600bp的核心启动子增加增强子和不同的内含子来筛选表达活性最高的组成型启动子,通过在不同组合的启动子中分别增加荧光素酶来检测启动子的表达活性。结果表明,增加CMV enhancer和CBAintron、Shorten CBA intron、Hybrid intron或EF1αintron中的任意一种启动子后的组成型启动子比没有增强子或者含有其他内含子的表达活性更好。更具体的,cyp4v2基因上游约600bp的核心启动子增加有RPE特异性元件、构成性转录因子sp1、CMV enhancer和CBAintron的组成型启动子表达活性最高。
本发明提供了所述的组成型启动子在转录cyp4v2基因中的应用。
本发明提供了包括本发明所述的组成型启动子的包装载体。
本发明所述的包装载体,能够将核酸或者蛋白包被起来,传递至培养的细胞或者人体内,具有递送遗传物质的功能,其可以是病毒载体也可以是质粒载体,其中病毒载体包括腺病毒、腺相关病毒、慢病毒和逆转录病毒;质粒载体包括原核载体和真核载体。在本发明的实施例中,选择腺相关病毒载体转染本发明的组成型启动子。
具体的,本发明所述的腺相关病毒载体中的腺相关病毒为单链线状DNA缺陷型病毒,无包膜,在腺病毒或者单纯疱疹病毒的辅助下能感染多种细胞。腺相关病毒载体则是不需要腺病毒辅助的包装系统,其在宿主体内的感染效率极高。
所述腺相关病毒载体包括但不限于AAV2、AAV8和/或AAVGL。
本发明提供了表达质粒,其包括cyp4v2基因、表达载体和所述的包装载体。
本发明所述的表达载体,是能够让目的基因在宿主细胞内稳定表达的载体,包括克隆载体的基本骨架、目的基因和表达元件。常用细菌质粒进行表达载体的构建,在本发明的实施例中,采用大肠杆菌质粒来进行表达载体的构建。
本发明提供了宿主细胞,其包括所述的包装载体或表达质粒。
本发明所述的宿主细胞,能够在体内稳定表达外源DNA,其包括动物细胞、植物细胞、微生物细胞、细菌和酵母。在本发明的实施例中,采用动物细胞293T和ARPE19作为宿主细胞,来进行cyp4v2基因的表达。
本发明还提供了所述包装载体、表达质粒或宿主细胞在制备治疗和/或预防结晶样视网膜变性的产品中的应用。
具体的,在本发明的实施例中,将含有本发明所述启动子的cyp4v2基因用AAV外壳包装后注射到小鼠眼球中,检测cyp4v2蛋白的表达情况。结果表明,含有本发明提供的组成型启动子的cyp4v2蛋白在小鼠眼睛中均有表达,且都比含有已知EF1α启动子的cyp4v2蛋白表达量高。
本发明还提供了治疗和/或预防结晶样视网膜变性的药物,包括本发明所述的包装载体、表达质粒或宿主细胞的产物,及药学上可接受的辅料。
本发明所述的药学上可接受的辅料包括但不限于稀释剂、吸收剂、润湿剂、粘合剂、崩解剂、润滑剂、着色剂、包衣材料、溶剂、pH调节剂、缓冲剂、抗氧化剂、金属离子螯合剂、抑菌剂或等渗调节剂。
本发明提供的治疗和/或预防结晶样视网膜变性的药物,其剂型包括但不限于溶液型、胶体溶液型、乳剂型、混悬性、气体分散型、微粒分散性或固体分散型。
本发明还提供了治疗结晶样视网膜变性的方法,包括给予本发明所述的药物。
本发明提供的组成型启动子,在贴近CYP4V2基因表达模式的同时,表达的活性更强,在小鼠体内的试验表明本发明提供的启动子用不同的腺病毒相关载体递送后均能有效表达,从而达到治疗的目的。
附图说明
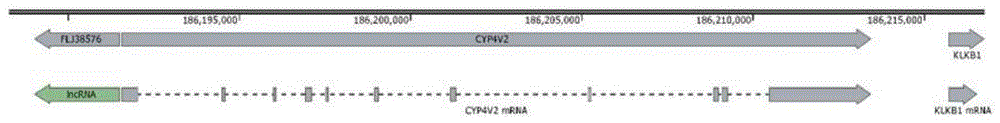
图1示cyp4v2 mRNA序列;
图2示不同长度启动子的载体设计;
图3示不同长度启动子双荧光结果;
图4示E600启动子的第一轮优化设计;
图5示E600启动子第一轮优化双荧光结果;
图6示E600启动子的第二轮优化设计;
图7示E600启动子第二轮优化双荧光结果;
图8示CYP4V2蛋白表达WB结果;
图9示CYP4V2蛋白相对表达量。
具体实施方式
本发明提供了一种用于基因治疗的组成型启动子,本领域技术人员可以借鉴本文内容,适当改进工艺参数实现。特别需要指出的是,所有类似的替换和改动对本领域技术人员来说是显而易见的,它们都被视为包括在本发明。本发明的方法及应用已经通过较佳实施例进行了描述,相关人员明显能在不脱离本发明内容、精神和范围内对本文的方法和应用进行改动或适当变更与组合,来实现和应用本发明技术。
本发明采用的试材皆为普通市售品,皆可于市场购得。
其中,cyp4v2基因上游约300bp的启动子的核酸序列为:
cyp4v2基因上游约600bp的启动子的核酸序列为:
cyp4v2基因上游约900bp的启动子的核酸序列为:
cyp4v2基因上游约1200bp的启动子的核酸序列为:
cyp4v2基因上游约1500bp的启动子的核酸序列为:
/>
cyp4v2基因上游约2000bp的启动子的核酸序列为:
/>
下面结合实施例,进一步阐述本发明:
实施例1不同长度启动子的获得
1、实验材料
试剂:2×PrimerStar GXLPremix(Takara);引物Oligo(杭州有康生物科技有限公司);pGL-TK(购买自淼灵生物);VB201120-1020ffc(购买自云舟生物);2×F8 FastLongPCR MasterMix(北京艾德莱生物科技有限公司,PC8002);EPI300感受态(上海唯地生物,DL1084);胶回收试剂盒(Promega,A9282);限制性内切酶(NEB or Thermo);DNALadder(Generay,DL2502);质粒小提试剂盒(TIANGEN,DP103);T4 DNA Ligase(NEB,M0569S);Dual-Luciferase Reporter 1000 Assay system(Promega,E1980);DneasyBlood&TissueKit(QIAGEN,69506)。
设备:PCR扩增仪(BioRad);凝胶成像系统(BioRad);电热恒温水浴槽(Thermofisher);离心机(Eppendorf);二氧化碳细胞培养箱(Thermofisher);酶标仪(spectra Max TD3)。
在cyp4v2的基因上游寻找转录起始位点,选择不同长度的片段进行克隆,利用双荧光系统进行筛选,获得核心启动子。具体步骤如下:
从NCBI上检索得到cyp4v2所在的染色体,NCBI:NC_000004,找到cyp4v2的基因序列,详见图1。
根据检索的序列,提取ARPE19细胞的基因组DNA为模板,设计引物PCR得到不同长度的启动子,构建含Luciferase的载体,其中CB启动子为阳性对照,GFP为阴性对照。结果见图2。
实施例2双荧光系统筛选
1、细胞转染
分别用293T细胞和ARPE19细胞铺96孔板,细胞数量为1*10^
转染体系(每孔)见表1:
表1
转染完后继续培养48h,进行荧光检测。
2、双荧光检测
用Promega的Dual-Luciferase Reporter 1000 Assay system试剂盒进行检测:(1)、吸去96孔板中培养基后用PBS洗一遍细胞,弃PBS;
(2)、每孔加入20uL的1×PLB裂解液,室温放置15min裂解细胞;
(3)、每孔加入100uL的LARII,放入酶标仪中读取Firefly Luciferase的数值;
(4)、读取完后取出96孔板,立即每孔加入100uL的Stop&Glo Reagent,酶标仪中读取Renilla Luciferase的数值;
(5)、处理数据。
双荧光的结果见图3。结果显示,启动子E600在293T细胞和ARPE19细胞中均有活性。
实施例3 E600启动子的优化
1、E600启动子加Enhancer和Intron元件的优化
根据不同长度启动子的筛选结果,发现E600是较为核心的启动子区,所以在E600的基础上加入CMVenhancer(CMVe)和不同的intron,来增强E600的启动子活性,详见图4。
按照设计构建含1uciferase的载体,根据实施例2中的方法进行双荧光检测,结果详见图5。
结果显示:一轮优化后发现CMV enhancer和不同intron都有增强启动子活性的作用;其中E600加上CMV enhancer和CBA intron,启动子活性跟CB启动子相当
2、E600启动子加转录因子和RPE特异性元件的优化
根据加入CMV enhancer和intron发现,这些元件都有一定提升启动子活性的作用。但原有的E600启动的活性相对较低,因此在E600的基础上增加了一些转录因子结合位点数据库中的转录因子和RPE特异的元件,并组合不同CMV enhancer和intron,进一步增强启动子活性,详见图6。
按照设计构建含1uciferase的载体,根据实施例2中的方法进行双荧光检测,结果详见图7。
结果显示:二轮优化后发现,加上转录因子后可以提高启动子的活性,C6M1比E600提高了25倍,比CB启动子提高了5倍。在C6M1的基础上增加CMV enhancer和不同intron,发现CBA intron(CI),Hybrid intron(HI)and EF1αintron(EI)可以进一步提升C6M1的活性,其中发现截短的CBA intron(CIT)也可以增加C6M1的活性。
实施例4小鼠体内验证试验
用不同的AAV外壳包装含不同启动子的CYP4V2,小鼠玻璃体注射AAV后4周取小鼠眼球,提取蛋白,WB检测CYP4V2蛋白在小鼠眼睛中的表达情况。其中106-104K为阳性对照。WB的实验步骤如下:
(1)、取小鼠眼球加入裂解液(含蛋白酶和磷酸酶抑制剂),震荡匀浆后离心,取上清;
(2)、蛋白定量:用BCA试剂盒对蛋白样品进行蛋白含量的分析;
(3)、加入Loading Buffer,75℃变性10min,冷却至室温;
(4)、上样,180V电泳50min;
(5)、转膜;
(6)、5%奶粉封闭30min;
(7)、一抗(5%奶粉配制)4℃孵育过夜;
(8)、倒去液体,用1*TBST洗膜3次,二抗室温孵育2h;
(9)、倒去液体,1*TBST洗膜3~5次;
(10)、显色。
CYP4V2蛋白表达结果详见图8和图9,其中阳性对照106-104K使用的是通用性的启动子EF1α;106-105K使用的启动子为CMV enhancer+C6M1+Hybrid intron;106-108K、106-121K、106-122K使用的启动子为C6M1启动子;106-123K使用的启动子为CMV enhancer+C6M1。注射方案如表2所示:
表2
不同C6M1的启动子用不同AAV外壳递送,在小鼠眼睛中均有表达,其中C6M1启动子结合CMV enhancer和HI intron的启动子具有最高的表达效果,单独使用C6M1启动子时表达量较低,但都比已知的EF1α启动子表达量高。
以上仅是本发明的优选实施方式,应当指出,对于本技术领域的普通技术人员来说,在不脱离本发明原理的前提下,还可以做出若干改进和润饰,这些改进和润饰也应视为本发明的保护范围。
- 一种用于成型毡成型模具的冲切结构
- 一种用于基因治疗及疫苗研制的人工合成启动子
- 一种用于基因治疗及疫苗研制的人工合成启动子
