一种茯苓多糖凝胶微球的制备方法及其应用
文献发布时间:2024-04-18 20:01:55
技术领域
本发明属于茯苓多糖加工技术领域,具体涉及一种茯苓多糖凝胶微球的制备方法及其应用。
背景技术
茯苓是多孔菌科真菌茯苓Poria cocos(Schw)Wolf的干燥菌核。多糖为茯苓的主要化学成分之一,约占茯苓菌核总重70~90%。茯苓中酸性多糖含量占茯苓药材的80%以上,为水不溶性成分,但临床应用中多采用水煎煮提取茯苓多糖,药理学研究也主要针对的是茯苓中水溶性部分,对其碱溶性部分研究甚少,从而造成了茯苓中有效成分的损失。因此,进一步拓展水不溶茯苓多糖的功能研究,对开发以茯苓多糖作为载体的材料具有重要意义,同时也可以对茯苓药渣的充分利用具有一定的指导意义。
发明内容
鉴于此,本发明提供一种茯苓多糖凝胶微球的制备方法及其应用,以提供一种碱溶性多糖的应用场景及对茯苓药渣充分利用的方法。
为达到上述目的,本发明采用以下技术方案:
一种茯苓多糖凝胶微球的制备方法,包括如下步骤:
将茯苓多糖溶于pH为11~14碱液,得多糖溶液;
取异辛烷与第一表面活性剂混合搅拌,得油相Ⅰ;
将多糖溶液滴加到油相Ⅰ中,搅拌,得油包水体系;
取异辛烷与第二表面活性剂混合搅拌,得油相Ⅱ;
将油相Ⅱ滴加到油包水体系中,搅拌,得混合液;
取1.0mol/L~2.0mol/L的HCl溶液滴加到混合液中,在250rpm~500rpm条件下搅拌,并依次用乙醇、去离子水洗涤,静置分层,分离,得茯苓多糖凝胶微球粗品;
往茯苓多糖凝胶微球粗品中加入叔丁醇搅拌,冻干,得茯苓多糖凝胶微球。
进一步地,所述多糖溶液中茯苓多糖的浓度为5mg/mL~50mg/mL。
进一步地,所述第一表面活性剂为Span85,所述第二表面活性剂为Tween85。
进一步地,所述Span85与多糖溶液质量体积比为1:(5~10),所述Span85与Tween85质量比为2:1。
进一步地,所述油相Ⅰ、Ⅱ中异辛烷总和与多糖溶液质量体积比为5:(1~3),所述油相Ⅰ中异辛烷与所述油相Ⅱ中异辛烷质量比为10:1。
进一步地,所述叔丁醇与茯苓多糖凝胶微球粗品体积比为2:1,搅拌条件:25~35℃、70~90rpm、1~3天,期间按照浓度梯度每隔4~8h更换一次叔丁醇。
上述制备方法制备得到的茯苓多糖凝胶微球作为药物载体在医药领域中的应用。
一种茯苓多糖纳米银凝胶微球的制备方法,包括如下步骤:在上述茯苓多糖凝胶微球的制备方法的基础上,还包括将硝酸银溶液逐滴滴加到所述多糖溶液中,得茯苓多糖纳米银混合溶液,经过余下相同步骤,即得茯苓多糖纳米银凝胶微球。
进一步地,所述硝酸银溶液浓度为25mM~500mM,硝酸银溶液和多糖溶液体积比为1:10。
上述制备方法制备得到的茯苓多糖纳米银凝胶微球作为催化剂在污水处理、光催化降解和光催化制氢中的应用。
与现有技术相比,本发明的有益效果为:
(1)本发明采用乳化法,以天然多糖为原料,利用茯苓多糖碱溶酸不溶的特性,采用酸再生的方法使微球固化,利用分子间氢键使之自组装从而制备出一种天然的多糖凝胶微球,具有良好的生物安全性及稳定性。
(2)本发明乳化法制备的茯苓多糖凝胶微球可以通过调整多糖浓度、异辛烷与多糖溶液比例、表面活性剂的含量、酸液浓度、转速等条件对微球的形貌、粒径进行调控。
(3)本发明制备工艺简单,原料易得,绿色环保,既没有改变多糖的化学结构也没有采用化学交联剂。
(4)本发明制备的茯苓多糖纳米银凝胶微球制备条件简单、纳米银得率高、分散均匀、催化效率好;相较于常规化学法而言避免了多种有毒化学还原剂和分散剂的使用;相较于以葡萄糖作为还原剂制备纳米银(需加热至90℃及以上,还原率低)而言室温下即可反应、反应迅速、还原率高。
附图说明
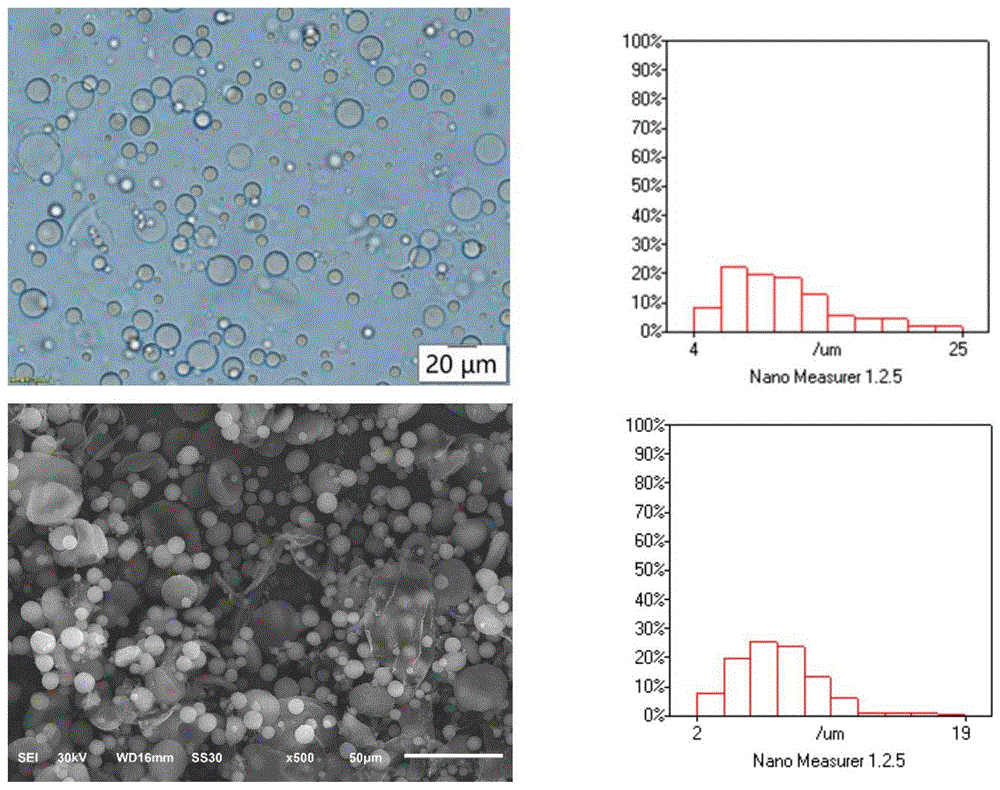
图1为实施例1所提供微球电子显微镜图和对应粒径分布图以及SEM图和对应粒径分布图;
图2为对比例1所提供微球电子显微镜图和SEM图;
图3为实施例2所提供微球电子显微镜图和对应粒径分布图以及SEM图和对应粒径分布图;
图4为对比例2所提供微球电子显微镜图和SEM图;
图5为对比例3所提供微球电子显微镜图和SEM图;
图6为对比例4所提供微球电子显微镜图和SEM图;
图7为实施例3所提供微球电子显微镜图和对应粒径分布图以及SEM图和对应粒径分布图;
图8为实施例4所提供微球电子显微镜图和对应粒径分布图以及SEM图和对应粒径分布图;
图9为实施例5所提供微球电子显微镜图和对应粒径分布图以及SEM图和对应粒径分布图;
图10为实施例6所提供微球电子显微镜图和SEM图;
图11为实施例7所提供微球电子显微镜图和SEM图;
图12为实施例8所提供微球电子显微镜图和SEM图;
图13为实施例9所提供微球电子显微镜图和SEM图;
图14为实施例10所提供微球电子显微镜图和SEM图;
图15为实施例11所提供微球电子显微镜图和SEM图;
图16为实施例12所提供微球电子显微镜图和SEM图;
图17为对比例5所提供微球电子显微镜图和SEM图;
图18为对比例6所提供微球电子显微镜图和SEM图;
图19为对比例7所提供微球电子显微镜图和SEM图;
图20为对比例8所提供微球SEM图;
图21为实施例13、对比例9、10所提供载银微球的XRD图;
图22为实施例13、对比例9、10所提供载银微球的TG图;
图23为实施例13、对比例9、10所提供载银微球的FT-IR图;
图24为实施例13所提供载银微球的催化效率图。
具体实施方式
下面结合具体实施例对本发明作进一步的详细说明,以使本领域的技术人员更加清楚地理解本发明。
关键试验材料来源及理化参数:
茯苓由湖北辰美中药有限公司提供,生产批号:2121110220;
茯苓多糖提取步骤如下:
S1、将茯苓丁粉碎过80目筛,用150目纱布样品袋装载后放入索氏提取器,使用丙酮和乙酸乙酯分别回流6h,收集脱脂残渣。
S2、取上述脱脂残渣加入0.9%氯化钠溶液,加热到90℃搅拌4h,收集滤渣,并重复多次,采用苯酚硫酸法检测,直至滤液中检测不出糖含量,收集二次残渣。
S3、取上述二次滤渣加入0.5mol/L NaOH水溶液,在5℃条件下搅拌2h,收集滤液,并重复2次,收集所有滤液。
S4、取S3中滤液,按照滤液:氯仿:正丁醇=25:5:1,采用Sevage法脱蛋白,搅拌30min,并重复3次过滤,收集所有上清液,向上清液中加99%冰醋酸调pH至中性并不断搅拌,直至产生大量沉淀,收集沉淀,并将沉淀按照质量体积比1:1加入95%乙醇,混合均匀后静置6h,收集沉淀,再取醇洗后的沉淀,按照质量体积比1:10加入蒸馏水,搅拌均匀后收集沉淀,并重复3次后收集所得沉淀即为茯苓粗多糖。
S5、取上述茯苓粗多糖溶于二甲基亚砜(DMSO)中,得浓度为1mg/mL的茯苓粗多糖DMSO溶液,使用恒压滴液漏斗逐滴滴加超纯水并不断搅拌,收集产生的沉淀并冷冻干燥,即得茯苓多糖,
本发明中未对具体原料进行说明均为已经存在物质,可以从市面上直接购买得到。
实施例1
本实施例提供一种茯苓多糖凝胶微球的制备方法,具体包括以下步骤:
S1、取上述制备的660mg茯苓多糖溶于22mL 0.5mol/L的NaOH溶液中配制成浓度为30mg/mL的多糖溶液;
S2、取50g异辛烷与2.2g Span85在500rpm条件下混合搅拌1h,得油相Ⅰ;
S3、将多糖溶液使用恒压滴液漏斗滴加到油相Ⅰ中,边滴加边搅拌,于10min滴加完毕,继续以500rpm速率进行搅拌1h,得油包水体系;
S4、取5g异辛烷与1.1g Tween85在500rpm条件下混合搅拌1h,得油相Ⅱ;
S5、将油相Ⅱ滴加到油包水体系中,边滴加边搅拌,于5min滴加完毕,继续以500rpm速率搅拌1h,得混合液;
S6、取22mL 1mol/L的HCl溶液滴加到混合液中,边滴边搅拌,于5min滴加完毕,继续以500rpm速率搅拌1h,静置6h后先用等体积的乙醇清洗3次,再用等体积的去离子水清洗3次,静置分层,过滤,得茯苓多糖凝胶微球粗品;
S7、往茯苓多糖凝胶微球粗品中加入2倍体积的叔丁醇(t-BuOH),在温度30℃、80rpm的条件下浸泡2-3天,期间每隔4-6h按照浓度梯度(按20%、40%、60%、80%、100%,从低到高依次替换)更换1-3次t-BuOH,冻干,得茯苓多糖凝胶微球。
实施例2
本实施例提供一种茯苓多糖凝胶微球的制备方法,其步骤和原料来源和实施例1基本相同,区别在于:将步骤S6中1mol/L的HCl溶液替换成2mol/L的HCl溶液,其余不变。
实施例3
本实施例提供一种茯苓多糖凝胶微球的制备方法,其步骤和原料来源和实施例1基本相同,区别在于:将步骤S1中茯苓多糖为220mg,其余不变。
实施例4
本实施例提供一种茯苓多糖凝胶微球的制备方法,其步骤和原料来源和实施例1基本相同,区别在于:将步骤S1中茯苓多糖为1100mg,其余不变。
实施例5
本实施例提供一种茯苓多糖凝胶微球的制备方法,其步骤和原料来源和实施例1基本相同,区别在于:步骤S2中Span85为4.4g,步骤S4中Tween85的质量为2.2g,其余不变。
实施例6
本实施例提供一种茯苓多糖凝胶微球的制备方法,其步骤和原料来源和实施例1基本相同,区别在于:步骤S1中茯苓多糖为220mg,步骤S2中Span85为4.4g,步骤S4中Tween85的质量为2.2g,其余不变。
实施例7
本实施例提供一种茯苓多糖凝胶微球的制备方法,其步骤和原料来源和实施例1基本相同,区别在于:步骤S1中茯苓多糖为1100mg,步骤S2中Span85为4.4g,步骤S4中Tween85的质量为2.2g,其余不变。
实施例8
本实施例提供一种茯苓多糖凝胶微球的制备方法,其步骤和原料来源和实施例1基本相同,区别在于:步骤S1中茯苓多糖为440mg,步骤S2中Span85为4.4g,步骤S4中Tween85的质量为2.2g,其余不变。
实施例9
本实施例提供一种茯苓多糖凝胶微球的制备方法,其步骤和原料来源和实施例1基本相同,区别在于:步骤S1中茯苓多糖为110mg,步骤S2中Span85为4.4g,步骤S4中Tween85的质量为2.2g,其余不变。
实施例10
本实施例提供一种茯苓多糖凝胶微球的制备方法,其步骤和原料来源和实施例1基本相同,区别在于:步骤S1中多糖溶液由330mg茯苓多糖溶于11mL 0.5mol/L的NaOH溶液中配制而成,其余不变。
实施例11
本实施例提供一种茯苓多糖凝胶微球的制备方法,其步骤和原料来源和实施例1基本相同,区别在于:步骤S1中多糖溶液由990mg茯苓多糖溶于33mL 0.5mol/L的NaOH溶液中配制而成,其余不变。
实施例12
本实施例提供一种茯苓多糖凝胶微球的制备方法,其步骤和原料来源和实施例1基本相同,区别在于:将步骤S2-S6中搅拌速率由500rpm变成250rpm,其余不变。
实施例13
本实施例提供一种茯苓多糖纳米银凝胶微球的制备方法,具体包括以下步骤:
S1、取上述制备的440mg茯苓多糖溶于22mL 0.5mol/L的NaOH溶液中配制成浓度为20mg/mL的多糖溶液;
S2、将50mM的硝酸银逐滴滴加到多糖溶液中,搅拌30min得茯苓多糖纳米银溶液;
S2、取50g异辛烷与2.2g Span85在500rpm条件下混合搅拌1h,得油相Ⅰ;
S3、将茯苓多糖纳米银溶液使用恒压滴液漏斗滴加到油相Ⅰ中,边滴加边搅拌,于10min滴加完毕,继续以500rpm速率进行搅拌1h,得油包水体系;
S4、取5g异辛烷与1.1g Tween85在500rpm条件下混合搅拌1h,得油相Ⅱ;
S5、将油相Ⅱ滴加到油包水体系中,边滴加边搅拌,于5min滴加完毕,继续以500rpm速率搅拌1h,得混合液;
S6、取22mL 1mol/L的HCl溶液滴加到混合液中,边滴边搅拌,于5min滴加完毕,继续以500rpm速率搅拌1h,静置6h后先用等体积的乙醇清洗3次,再用等体积的去离子水清洗3次,静置分层,过滤,得茯苓多糖纳米银凝胶微球粗品;
S7、往茯苓多糖纳米银凝胶微球粗品中加入2倍体积的t-BuOH,在温度30℃、80rpm的条件下浸泡2-3天,期间每隔4-6h按照浓度梯度更换1-3次t-BuOH,冻干,得茯苓多糖纳米银凝胶微球。
对比例1
本实施例提供一种茯苓多糖凝胶微球的制备方法,其步骤和原料来源和实施例1基本相同,区别在于:将步骤S6中1mol/L的HCl溶液替换成0.5mol/L的HCl溶液,其余不变。
对比例2
本实施例提供一种茯苓多糖凝胶微球的制备方法,其步骤和原料来源和实施例1基本相同,区别在于:将步骤S6中1mol/L的HCl溶液替换成质量分数为20%的醋酸,其余不变。
对比例3
本实施例提供一种茯苓多糖凝胶微球的制备方法,其步骤和原料来源和实施例1基本相同,区别在于:将步骤S6中1mol/L的HCl溶液替换成质量分数为40%的醋酸,其余不变。
对比例4
本实施例提供一种茯苓多糖凝胶微球的制备方法,其步骤和原料来源和实施例1基本相同,区别在于:将步骤S6中1mol/L的HCl溶液替换成质量分数为80%的醋酸,其余不变。
对比例5
本实施例提供一种茯苓多糖凝胶微球的制备方法,其步骤和原料来源和实施例1基本相同,区别在于:将步骤S2中Span85的质量为0.74g,步骤S4中Tween85的质量为0.37g,其余不变。
对比例6
本实施例提供一种茯苓多糖凝胶微球的制备方法,其步骤和原料来源和实施例1基本相同,区别在于:步骤S2-S6中搅拌速率为1000rpm,其余不变。
对比例7
本实施例提供一种茯苓多糖凝胶微球的制备方法,其步骤和原料来源和实施例1基本相同,区别在于:步骤S4中不添加Tween85,其余不变。
对比例8
本实施例提供一种茯苓多糖凝胶微球的制备方法,其步骤和原料来源和实施例1基本相同,区别在于:去掉步骤S7,其余不变。
对比例9
本实施例提供一种茯苓多糖纳米银凝胶微球的制备方法,其步骤和原料来源和实施例13基本相同,区别在于:步骤S2中硝酸银浓度为100mM,其余不变。
对比例10
本实施例提供一种茯苓多糖纳米银凝胶微球的制备方法,其步骤和原料来源和实施例13基本相同,区别在于:步骤S2中硝酸银浓度为200mM,其余不变。
茯苓多糖凝胶微球各指标测试
对实施例1-12,对比例1-8制备的茯苓多糖凝胶微球形貌及粒径分布进行表征。具体包括以下步骤:
1)电子显微镜
将水洗后的微球取100-200μL置于倒置显微镜下观察微球的形貌,采用NanoMeasurer 1.2.5对粒径分布进行计算。
2)扫描电镜
取少量冻干后的微球置于导电胶上,在15Kv下加压,观察微球的形貌,采用NanoMeasurer 1.2.5对粒径分布进行计算。
结果分析
表1酸浓度对微球粒径分布的影响
结合表1和图2-6结果可以看出:当HCl浓度越高时,微球的整体粒径越大,而在酸浓度为0.5mol/L时,微球的成球性很差,几乎不形成微球;使用醋酸再生的微球成球性较差,其中80%的醋酸较其他两组而言成球性较好,酸液对微球的形成有很大影响,为保证良好的成球性,应使用强酸(HCl)进行再生。
表2多糖浓度对微球粒径分布的影响(Span85:多糖溶=1:10(m/v))
结合表2、图1、7、8结果可以看出:当Span85:多糖溶液质量体积比为1:10时,糖浓度为微球粒径影响较小粒径分布差异较小,但50mg/mL时,微球粒径分布不均匀。
表3多糖浓度对微球粒径分布的影响(Span85:多糖溶液=1:5(m/v))
结合表3、图9-13结果可以看出:当Span85:多糖溶液质量体积比为1:5时,糖浓度越高微球粒径越大,同样可以看出,浓度为50mg/mL微球粒径分布不均匀,因此,不推荐糖浓度过高。
表4 Span85与多糖溶液的比例(m/v)对微球粒径分布的影响
结合表4和图1、9、17结果可以看出:Span85的含量越高,微球粒径越大,当Span85与水相的比例为1:30时成球性较差,基本不形成微球,但形成了凝胶碎片。
表5转速对微球粒径分布的影响
结合表5和图1、16、18结果可以看出:当转速增大时,微球粒径越小,但是当转速超过1000rpm时,则无法形成微球结构。
表6异辛烷与多糖溶液的比例(m/v)对微球粒径分布的影响
结合表6和图1、14、15结果可以看出:当异辛烷与多糖溶液的比在5:(1-3)(m/v)时均能形成微球,随着异辛烷与多糖溶液的比例增加,多糖微球粒径有变小趋势。
由图1、19可以看出:不添加Tween85根本无法形成多糖微球。
由图1、20可以看出:将茯苓多糖凝胶微球置于t-BuOH中搅拌后冻干,微球的表面光滑,形态完整;而直接冻干后形态不够完整光滑。
综上所述,本发明方案通过确定合适多糖浓度、异辛烷与多糖溶液比例、Tween85和Span85的含量、酸液浓度、转速等条件使得制备的微球粒径大小呈正态分布,微球表面光滑。
茯苓多糖纳米银凝胶微球各指标数据
对实施例13、对比例9、对比例10制备的茯苓多糖纳米银凝胶微球(载银微球)各指标进行测定。具体包括以下步骤:
1)X射线衍射(XRD)
使用日本Rigaku SmartLab SE对载银微球的晶型及特征衍射峰进行分析,测试角度为:5-90°,扫描速度2°/min,结果见图21
2)热重分析(TG)
使用美国TA TGA550对载银微球的热稳定性进行分析,测试条件为30-800℃,升温速率10℃/min,结果见图22。
3)傅里叶红外光谱(FT-IR)
使用美国Thermo Scientific Nicolet iS20对载银微球的特征官能团进行检测分析,扫描范围为400-4000cm
由图21可知:在2θ约为38.18°、44.18°、64.25°、77.46°、81.70处出现尖锐的衍射峰,通过查阅纳米银的PDF标准卡片号(PDF04-004-4773)发现,所测得AgNPs的衍射峰与标准图谱中的衍射峰完全一致,这也证实了AgNPs以晶体的形式存在。这五个衍射峰分别对应纳米银粒子(111)、(200)、(220)、(311)、(222)面心立方结构的5个晶面,这说明微球中负载的银的是单质银而非Ag
由图22可知:载银微球在100℃时重量有所下降,是由于样品中的结合水蒸发所致,主要的失重区是在250~400℃的范围内,表明多糖被分解。热重分析是在氮气氛围内进行热分解,微球负载的银不会被氧化,因此,残留的固体含量即为载银微球中纳米银颗粒的质量,微球含银量分别为1.20%、1.85%、7.62%。
由图23可知:与空白微球相比载银微球的吸收峰在相同的位置几乎一致,表明微球中没有特殊的官能团与Ag发生明显反应。纳米银被微球包裹后具有一定的屏蔽能力,因而,红外的吸收强度略微减小,与空白微球相比,载银微球在3419cm
茯苓多糖纳米银凝胶微球的催化性能进行测试
对实施例13、对比例9、10制备的茯苓多糖纳米银凝胶微球的催化性能进行测定,具体包括以下步骤:
在25℃下将2.0mL浓度为0.4mol/L的硼氢化钠(NaBH
采用NaBH
由图24可知:由于4-硝基苯酚的吸收峰强度(A
以上仅为本发明的较佳实施方案,并非用于限定本发明的保护范围。凡在本发明的精神和原则之内,所作的任何修改、等同替换、改进等,均应包含在本发明的保护范围之内。
