一种来源于GMC氧化酶家族的新型氯霉素耐药基因的PCR检测方法
文献发布时间:2023-06-19 11:59:12
技术领域
本发明涉及生物技术领域,特别涉及一种来源于GMC氧化酶家族的新型氯霉素耐药基因的PCR检测方法。
背景技术
抗生素的广泛使用以及滥用造成了抗生素耐药性在微生物中的发展和传播,并且加速了全球多重耐药细菌和抗生素抗性基因(Antibiotic resistance genes,ARGs)的出现和传播。在医疗和农业中对抗生素的需求日益增加,这使得环境中细菌耐药性水平日益加剧,并且破坏了微生物和抗生素之间的自然平衡。
ARGs作为一种新型的环境污染物,广泛存在于人类、动物体内以及复杂的环境中。人和动物会将未代谢完的抗生素及ARGs通过粪便和肠道细菌排放到环境中,环境中的耐药细菌会在抗生素选择压力下获得富集,或通过水平基因转移(Horizontal gene transfer,HGT)的方式将它们携带的ARGs传播到水原微生物中,造成ARGs在不同菌之间的传播,这些原因共同促成了ARGs在畜禽养殖废水、医院废水和生活污水中的传播和扩散,从而造成耐药细菌的聚集,尤其是致病耐药菌的聚集危害极大。
氯霉素是目前市场上最广谱抗菌素药物之一,其抗菌作用机制是与核蛋白体50S亚基结合,抑制肽酰基转移酶,从而抑制蛋白质合成。氯霉素对大多数革兰氏阴性以及阳性细菌、流感杆菌、百日咳杆菌、痢疾杆菌、大肠杆菌、肺炎杆菌、变形杆菌、绿脓杆菌、立克次体、沙眼衣原体等都能有效控制。正是由于其在生物医药领域应用非常广泛,大量的氯霉素类抗生素被投入使用,细菌对氯霉素类耐药的现象也越趋严重。
申请人在专利名称为“氯霉素的新型抗性基因及其应用”,专利公开号为“CN112111502 A”的在先申请中,公开了从环境中分离到一株对氯霉素具有很高的耐药性的鞘氨醇单胞菌,通过RNA转录组测序,发现GMC氧化酶家族编码的一个氧化还原酶基因在氯霉素的刺激下显著高表达,而且也通过异源表达的方式验证了这个基因的耐药功能。现有技术中还未报道关于该氯霉素抗性基因的检测相关的技术。
发明内容
本发明的主要目的是提供一种检测氯霉素抗性基因的引物对,旨在实现对氯霉素抗性基的快速检测,提高氯霉素耐药性的检出率。
为实现上述目的,本发明提出一种检测氯霉素抗性基因的引物对,包括:
上游引物,所述上游引物的核苷酸序列为SEQ ID NO.1;
下游引物,所述下游引物的核苷酸序列为SEQ ID NO.2。
本发明还提出一种检测氯霉素抗性基因的引物对,所述上游引物的核苷酸序列包括与SEQ ID NO.1差别为任意一个碱基的核苷酸序列,所述下游引物的核苷酸序列为SEQID NO.2。
本发明还提出一种检测氯霉素抗性基因的引物对,所述上游引物的核苷酸序列为SEQ ID NO.1,所述下游引物的核苷酸序列包括与SEQ ID NO.2差别为任意一个碱基的核苷酸序列。
本发明还提出一种检测氯霉素抗性基因的引物对,所述上游引物的核苷酸序列包括与SEQ ID NO.1差别为任意一个碱基的核苷酸序列;
所述下游引物的核苷酸序列包括与SEQ ID NO.2差别为任意一个碱基的核苷酸序列。
本发明还提出如上述任意一项所述的一种检测氯霉素抗性基因的引物对在制备检测氯霉素抗性基因的试剂盒中的用途。
本发明还提出一种检测氯霉素抗性基因的试剂盒,包括上述任意一项所述的一种检测氯霉素抗性基因的引物对。
可选地,所述试剂盒还包括DNA聚合酶和扩增缓冲液。
可选地,50μL PCR反应体系包括:
本发明还提出如上述任意一项所述的一种检测氯霉素抗性基因的引物对,或上述任意一项所述的一种检测氯霉素抗性基因的试剂盒在检测氯霉素抗性基因用于评估环境风险中的用途。
本发明技术方案通过对GMC氧化酶家族的新型氯霉素耐药基因设计全长扩增引物,通过优选获得最佳特异性引物的上游引物核苷酸序列为SEQ ID NO.1,下游引物核苷酸序列为SEQ ID NO.2,进而建立快速的氯霉素抗性基因PCR检测方法,实现环境样品中该新型耐药基因的快速检测,以便及时评估环境风险。
附图说明
为了更清楚地说明本发明实施例或现有技术中的技术方案,下面将对实施例或现有技术描述中所需要使用的附图作简单地介绍,显而易见地,下面描述中的附图仅仅是本发明的一些实施例,对于本领域普通技术人员来讲,在不付出创造性劳动的前提下,还可以根据这些附图示出的结构获得其他的附图。
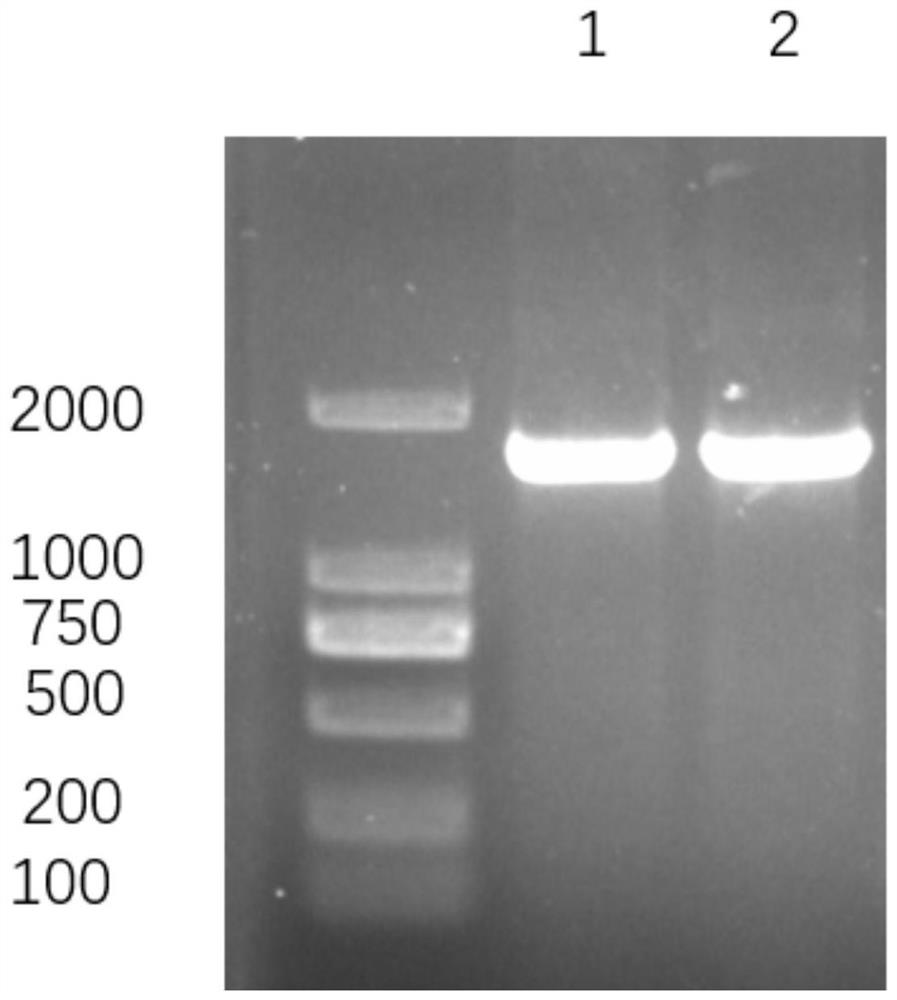
图1为本发明的检测氯霉素抗性基因的引物对检测不同样品的PCR扩增产物电泳结果图,其中泳道1是活性污泥样品,泳道2是土壤样品;
图2本发明的检测氯霉素抗性基因的引物对检测不同样品的PCR扩增产物的基因测序比对图。
本发明目的的实现、功能特点及优点将结合实施例,参照附图做进一步说明。
具体实施方式
下面将结合本发明实施例中的附图,对本发明实施例中的技术方案进行清楚、完整地描述,显然,所描述的实施例仅仅是本发明的一部分实施例,而不是全部的实施例。基于本发明中的实施例,本领域普通技术人员在没有作出创造性劳动前提下所获得的所有其他实施例,都属于本发明保护的范围。
本发明提出一种检测氯霉素抗性基因的引物对,包括:上游引物,所述上游引物的核苷酸序列为SEQ ID NO.1;下游引物,所述下游引物的核苷酸序列为SEQ ID NO.2。
申请人在之前的研究中发现一株鞘氨醇单胞菌对氯霉素具有很高的耐药性,经基因组的三代测序后,没有在基因组上发现目前已知的耐药基因,之后通过RNA转录组测序,发现GMC氧化酶家族编码的一种氧化还原酶在抗生素的作用时,具有很高的转录表达量,而且也通过构建重组载体的方式验证了这个基因的功能,从而发现了一种GMC氧化酶家族的新型氯霉素耐药基因,其核苷酸序列为SEQ ID NO.3。
氯霉素抗性基因作为ARGs的一种,同样是一种环境污染物,会促进氯霉素抗性菌的产生和传播,因此,有必要对环境样品中氯霉素抗性基因进行检测,评估环境风险。
本发明技术方案通过对GMC氧化酶家族的新型氯霉素耐药基因设计全长扩增引物,通过优选获得最佳特异性引物的上游引物核苷酸序列为SEQ ID NO.1,下游引物核苷酸序列为SEQ ID NO.2,进而建立快速的氯霉素抗性基因PCR检测方法,实现环境样品中该新型耐药基因的快速检测,便于快速评估环境风险。
在一实施例中,所述上游引物的核苷酸序列包括与SEQ ID NO.1差别为任意一个碱基的核苷酸序列,所述下游引物的核苷酸序列为SEQ ID NO.2。
在另一实施例中,所述上游引物的核苷酸序列为SEQ ID NO.1,所述下游引物的核苷酸序列包括与SEQ ID NO.2差别为任意一个碱基的核苷酸序列。
可选地,所述上游引物的核苷酸序列还包括与SEQ ID NO.1差别为任意一个碱基的核苷酸序列;
所述下游引物的核苷酸序列还包括与SEQ ID NO.2差别为任意一个碱基的核苷酸序列。
上述检测氯霉素抗性基因的引物对的上游引物核苷酸序列为SEQ ID NO.1,下游引物核苷酸序列为SEQ ID NO.2为该引物对的最佳引物序列,PCR扩增效果好,无杂带。可以理解的是,PCR扩增中,引物与模板通过碱基互补配对原理一一结合,其中引物的核苷酸序列突变一个碱基不能与对应的模板位置结合并不影响扩增效果。
本发明还提出如上述任意一项所述的一种检测氯霉素抗性基因的引物对在制备检测氯霉素抗性基因的试剂盒中的用途。
本发明还提出一种检测氯霉素抗性基因的试剂盒,包括上述的一种检测氯霉素抗性基因的引物对。
可选地,所述试剂盒还包括DNA聚合酶和扩增缓冲液。
可选地,50μL PCR反应体系包括:
本发明还提出如上述任意一项所述的一种检测氯霉素抗性基因的引物对,或上述任意一项所述的一种检测氯霉素抗性基因的试剂盒在检测氯霉素抗性基因用于评估环境风险中的用途。
下面将结合具体实施例对本发明的实施方案进行详细描述,但是本领域技术人员将会理解,下列实施例仅用于说明本发明,而不应视为限制本发明的范围。实施例中未注明具体条件者,按照常规条件或制造商建议的条件进行。所用试剂或仪器未注明生产厂商者,均为可以通过市售购买获得的常规产品。
实施例1检测氯霉素抗性基因的引物对的设计
(1)GMC氧化酶家族的新型氯霉素耐药基因含有1605bp的开放阅读框架,编码538个氨基酸。
(2)以上述参考序列利用DNAman软件进行引物设计,生成候选引物。
(3)通过以下筛选条件从候选引物中得到特异性引物
由于需要扩增出GMC氧化酶家族的新型氯霉素耐药基因的全长序列,因此上游引物和下游引物需与基因序列的起始序列和结束序列互补配对,上游引物从基因序列首端开始,下游引物从基因序列末端结束,因此引物设计的软件不能够自动生成特异性好的引物,需要使用软件并结合一些引物设计的原则去筛选引物,具体引物筛选原则如下:
a.引物长度:18-25bp。引物长度需要稍长,以便提高退火温度,从而提高反应的特异性。但是引物长度不能太长,应避免引物间3′端序列发生互补配对,以防止或减少形成二级结构的可能性。
b.G+C含量:40~60%。PCR扩增中的复性温度一般是较低Tm值引物的Tm值减去5~10度。上下游引物的解链温度应平衡,差别不要超过1℃。
c.碱基分布的随机性:尽量避免连续出现4个以上的单一碱基。尤其是不应在其3′端出现超过3个的连续G或C,否则会使引物在G+C富集序列区错误引发。
d.3′末端:3′末端碱基优选为G或C,不能为A。然而,并不推荐使用3′端有NNCG或NNGC序列的引物,因为末端GC碱基高的自由能可以促进发卡结构的形成,还可能产生引物二聚体。
e.引物应当超出限制性内切酶识别位点3个核苷酸以上。
f.引物之间:上下游引物之间不应有多于4个的互补或同源碱基,否则会形成引物二聚体,应避免上下游引物的3′端的互补重叠。
g.上下游引物的互补性:一个引物的3′末端序列不能结合到另一个引物的任何位点上。由于PCR中引物的浓度往往较高,即便引物之间的微弱互补也会导致引物之间形成杂交,随后是引物二聚体的形成和扩增。如果引物二聚体在PCR早期形成,其将与DNA聚合酶、引物、核苷酸竞争进而抑制目的DNA的扩增。
其它还包括对解链温度等的要求,包括上游引物和下游引物的Tm值相差不能大于5℃,上游引物和下游引物的PCR扩增产物的Tm值与引物的Tm值相差不能大于10℃。
通过上述方法设计筛选得到的检测氯霉素抗性基因的引物对的核苷酸序列分别如下:
上游引物(GMC-F):GTGCAAGATATTAGAACTACGGAC(SEQ ID NO.1);
下游引物(GMC-R):TCAGTGGCTTCTTCGGATCA(SEQ ID NO.2)。
实施例2实施例1的引物对进行PCR扩增检测环境样品的氯霉素抗性基因
(1)分别提取活性污泥和土壤样品的基因组DNA。
(2)以步骤1提取的各个基因组DNA为模板,用实施例1筛选得到的特异性引物对进行PCR扩增,其中,PCR反应体系为:
总反应体系为50μL
PCR的扩增程序为:95℃预变性5min,95℃变性1min,55℃退火1min,60℃延伸1min,35个循环之后,72℃、10min。
活性污泥和土壤样品基因组DNA通过PCR反应得到对应的PCR产物,PCR产物进行琼脂糖凝胶电泳,结果如图1所示,图1中泳道1为活性污泥样品,泳道2是土壤样品,从图1中可以看出,泳道1和泳道2使用实施例1得到的特异性引物对扩增的结果很好,没有出现非特异性条带和引物二聚体,条带的大小也符合GMC氧化酶家族的新型氯霉素耐药基因的全长大小。
(3)回收PCR产物,送至华大基因公司进行基因测序,测序结果通过blast与新型氯霉素耐药基因序列进行序列比对,比对的结果如图2所示,根据图2可知,PCR产物的基因序列与该GMC氧化酶家族的新型氯霉素耐药基因序列完全相同,证明实施例1得到的特异性引物对扩增GMC氧化酶家族的新型氯霉素耐药基因结果很好,从而可以快速评估环境风险。
以上所述仅为本发明的可选实施例,并非因此限制本发明的专利范围,凡是在本发明的发明构思下,利用本发明说明书及附图内容所作的等效结构变换,或直接/间接运用在其他相关的技术领域均包括在本发明的专利保护范围内。
SEQUENCE LISTING
<110> 清华大学深圳国际研究生院
<120> 一种来源于GMC氧化酶家族的新型氯霉素耐药基因的PCR检测方法
<130> 2021-06-01
<160> 3
<170> PatentIn version 3.5
<210> 1
<211> 24
<212> DNA
<213> 人工序列
<400> 1
gtgcaagata ttagaactac ggac 24
<210> 2
<211> 20
<212> DNA
<213> 人工序列
<400> 2
tcagtggctt cttcggatca 20
<210> 3
<211> 1605
<212> DNA
<213> 鞘氨醇单胞菌
<400> 3
gtgcaagata ttagaactac ggactttatc gtcgttgggg gcggttcgag tggcgcggtg 60
gtcgcatctc ggctaagcga agagaagcgt tttgaggtcg cgttgctcga agccggcggg 120
tgggacagct cgcctttcat tcggattccg gcgggctcga tcaaagcgat catgaatcct 180
gagtacaact ggttctatca agcggaaccg gatgcctcac gaaacgatcg agcagacatg 240
tggccggccg gcaaagtcct cggcggcggc tcgtcgatca acgggatgat gtatgttcgc 300
ggcaatcgcg gcgattatga tcaatgggct cagctcggct gcaagggctg gtcctatgac 360
gacgtgcttc cgttctttaa caaggccgag acgaacgaaa acggcggctc gcgctttcgc 420
ggcgacaagg gccctctgcg cgtatcgaat gcccgcctat cgaccacgtt ggccgacgca 480
ttcatcgctt ctggcgtacg tgcggggatt ccgcacaatc cggataccaa cggtgccgag 540
caagagggta tcggcccctg ccaagccacc cagaacaagg gttggcgaca ttcaacggca 600
cgcgcctatc tggccaaggc gaagcgccga tccaatctga aggtcgagac gcatttcatg 660
gtcagtcggg tactgatcga gaaaggccgc gcgatcggcg tcgaaggcgt tcagaacggg 720
cgcacggttc gctacttggc aaacaaggag gtcattcttt gcggcggcgc gttgtcgtcg 780
ccgaaaatat tgatgctctc gggcattggc ccggcaaagc atcttggcga gcatggcatc 840
cctgttgtcg tcgattcccc gggagtgggg caaaatctgc aggaacatcc cggagtgttg 900
atgtcgaccc atgtcggcat cgatagcctc aatgtcgaag tgcaaagcgt cgccaggata 960
gtcaagcatg gcttgaactt cgctttgttt gggcgagggc cagccacggc atgcgttgcc 1020
tccgctctcg cgttcattcg cacgcgagac catctcgagt ggcccaacat ccaactgtcg 1080
ttctcgccga tcgcgtacga cttcacgccg gacggcgtac acctgtacaa gcgtgcggca 1140
attggcgttg ccatcaacat ctgccggccc gagacgcgcg gtcagttgct gctccgctcc 1200
accgatccaa gtgagcggcc gattatccaa catgagctgc tcggcggaga tgatgagatc 1260
aagcagctca tcgaaggatg ccggatcgtg cgcaagattt tccgttccaa gccattcagt 1320
gaatatgaca aaggtgaacg cttacccgga aagcaggtcg aaaccgacgc tgattggatc 1380
gagtatatcc gtcagagcgc cttcctgatg taccacccga ctggcacttg cgcgatggga 1440
attgggccga cagcggttct cgatccggag ttgcgcgtca agggcgtcac cggtcttcgc 1500
gttgcggatg cctcgatcat gccgacgctg gttagcgcga atacaaatgc accgtgcatc 1560
atgattggcg aacgggcggc cgatctgatc cgaagaagcc actga 1605
- 一种来源于GMC氧化酶家族的新型氯霉素耐药基因的PCR检测方法
- 一种动物源细菌氯霉素类药物耐药基因多重PCR检测技术
