一种应用于荧光定量PCR的双探针方法
文献发布时间:2023-06-19 18:30:43
技术领域
本发明涉及分子生物学技术领域,尤其是一种应用于荧光定量PCR的双探针方法。
背景技术
聚合酶链反应(Polymerase Chain Reaction,PCR)是Kary Mullis在20世纪80年代开发的一种革命性方法,原理为利用DNA聚合酶的能力合成与所提供的模板链互补的新DNA链。因为DNA聚合酶只能将核苷酸添加到预先存在的3'-OH基团上,所以扩增体系中需要添加引物来起始反应。PCR反应结束时,特异性序列被富集,可以得到数十亿个拷贝(扩增子)。
PCR技术发展至今更新至第三代数字PCR技术,但第二代荧光定量PCR技术因其操作简便、结果判读方式简单等诸多优点,仍旧是市场上的主流应用技术。该技术中荧光信号的产生至关重要,以TaqMan荧光标记探针为基础的实时荧光PCR技术,在目前国内的临床诊断中应用最为广泛。热稳定DNA聚合酶Taq在具有5'→3'方向的聚合酶活性的同时,还具有对聚合延伸过程中遇到的与靶序列结合的核苷酸序列的5'→3'核酸外切酶活性。扩增中,当引物通过Taq DNA聚合酶的聚合反应延伸至接近已与靶核酸序列结合的探针时,Taq DNA聚合酶的5'→3'外切酶活性将探针降解成小片段。TaqMan荧光探针在其5'端标记一个荧光报告基团,3'端标记一个荧光淬灭基团,根据荧光共振能量传递原理,完整探针因荧光基团和淬灭剂距离很近而使荧光基团发射的荧光被淬灭,当探针降解时,荧光报告基团和淬灭剂分离,荧光得以发射出来。在PCR过程中,Taq DNA聚合酶利用其5'核酸外切酶活性切割与靶序列结合的寡核苷酸探针,最终释放荧光。
qPCR方法通常需要两对引物、探针来实现对于目的基因及参比基因的分别扩增。参比基因通常为距目的基因较远的管家基因保守区段,其表达水平在不同组织、不同细胞周期间存在较大差异,PCR结束后利用目的基因与参比基因荧光信号的差值进行判读,但该判读结果容易受到参比基因拷贝数变化的影响。依赖qPCR方法的检测试剂在研发阶段通常需要针对每一种突变进行引物或探针进行大量筛选,耗费样本且测试周期较长,提高了测试成本。
发明内容
针对上述问题,本发明提出一种应用于荧光定量PCR的双探针方法,且该方法可适用于多种类型的基因突变检测。
为实现以上目的,本发明通过以下技术方案予以实现:
一种应用于荧光定量PCR的双探针方法,双探针分别为检测探针和参比探针,两种探针带不同的荧光标记;
所述检测探针靶向热点突变位置的野生型序列,参比探针靶向紧邻目的序列的野生型序列,两探针共用同一对上下游引物。
进一步的,为使用同一对引物的Taqman双探针检测体系。
进一步的,所述检测探针及参比探针携带的荧光基团均为FAM、VIC(HEX)、CY3、CY5、ROX中的一种,且检测探针及参比探针所携带的荧光基团不同;所述检测探针及参比探针携带的淬灭基团均为BHQ1、BHQ2、TAMRA、MGB NFQ中的一种。
与现有技术相比较,本发明的有益效果如下:
本发明提供的应用于荧光定量PCR的双探针方法使用单反应qPCR方法,可以同时检测邻近的多种突变,有效节约了组织样本,并使测试周期大大缩短,且靶序列与参比序列位置靠近提高了结果的可信程度与准确性,具有广泛的应用前景。
附图说明
为了更清楚地说明本发明实施方式的技术方案,下面将对实施方式中所需要使用的附图作简单地介绍,应当理解,以下附图仅示出了本发明的某些实施例,因此不应被看作是对范围的限定,对于本领域普通技术人员来讲,在不付出创造性劳动的前提下,还可以根据这些附图获得其他相关的附图。
图1为本发明实施例1中样本的PCR扩增曲线图;
图2为本发明实施例2中样本的PCR扩增曲线图;
图3为本发明实施例3中样本的PCR扩增曲线图;
图4为本发明实施例4中样本的PCR扩增曲线图;
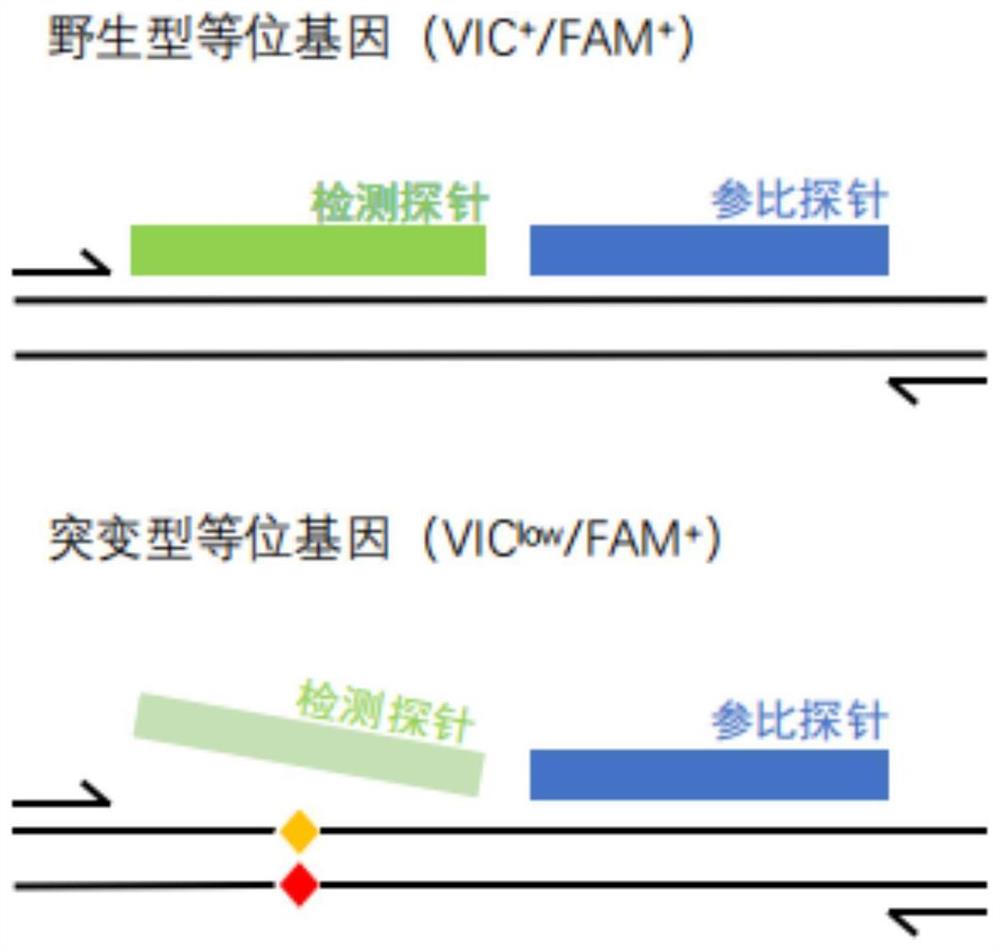
图5为本发明的检测原理示意图。
具体实施方式
为使本发明实施例的目的、技术方案和优点更加清楚,下面将结合本发明实施例,对本发明实施例中的技术方案进行清楚、完整地描述,显然,所描述的实施例是本发明一部分实施例,而不是全部的实施例。基于本发明中的实施例,本领域普通技术人员在没有作出创造性劳动前提下所获得的所有其他实施例,都属于本发明保护的范围。
本发明使用同一对引物的Taqman双探针检测体系,双探针分别为检测探针和参比探针,两种探针带不同的荧光标记;检测探针靶向热点突变位置的野生型序列,突变位置可以覆盖邻近的多种突变,参比探针靶向紧邻目的序列的野生型序列,两探针共用同一对上下游引物。
其中,检测探针及参比探针携带的荧光基团均为FAM、VIC(HEX)、CY3、CY5、ROX中的一种,且检测探针及参比探针所携带的荧光基团不同;检测探针及参比探针携带的淬灭基团均为BHQ1、BHQ2、TAMRA、MGB NFQ中的一种。
本发明原理如图5所示,当模板内不存在突变序列时,检测探针与模板完全匹配并释放荧光信号,参比探针正常释放荧光信号(VIC
实验部分
主要试剂:TAKARA-RR390,水
主要仪器:掌上离心机、漩涡振荡器、荧光定量PCR仪
反应体系成分如下表1所示:
表1
实施例1:突变频率5%模拟样本的EGFR T790M检测
参照表1配制反应体系,上游引物序列为:
5’-GCGAAGCCACACTGACGT-3’、下游引物序列为:
5’-AAGGGCATGAGCTGCGT-3’、检测探针序列为:
5’-(VIC)-GTGGACAACCCCCACGTGT-(MGB NFQ)-3’、参比探针序列为:
5’-(6-FAM)-CTGCTGGGCATCTGCCT-(MGB NFQ)-3’。检测模板为野生型人类基因组DNA与含EGFR T790M突变基因片段的质粒混合制备的突变频率为5%的T790M模拟样本,野生型样本为与模拟样本相同拷贝数的野生型人类基因组DNA。
如图1所示,模拟样本与对照组样本的扩增曲线存在明显差异,即反应体系可以区分野生型样本与突变样本。表2为本次测试的Ct值,由表可知野生型样本两荧光通道之间的ΔCt为4.53,模拟样本两荧光通道之间的ΔCt为5.96,两样本ΔCt之间的差值,即ΔΔCt为1.43,对两样本的ΔCt进行显著性分析,检验p值<0.0001,表明反应体系可以区分野生型样本与突变样本。
表2
实施例2:突变频率5%模拟样本的KRAS G12D检测
参照表1配制反应体系,上游引物序列为:
5’-CTGAAAATGACTGAATATAAACTTGTGGTA-3’、下游引物序列为:
5’-TCTATTGTTGGAT CATATTCGTCCAC-3’、检测探针序列为:
5’-(VIC)-AGCTGGTGGCGTAGGC-(MGB NFQ)-3’、参比探针序列为:
5’-(6-FAM)-AGTGCCTTGACGATACAGCT-(MGB NFQ)-3’。检测模板为野生型人类基因组DNA与含KRAS G12D突变基因片段的质粒混合制备的突变频率为5%的G12D模拟样本,野生型样本为与模拟样本相同拷贝数的野生型人类基因组DNA。
如图2所示,模拟样本与对照组样本的扩增曲线存在明显差异,即反应体系可以区分野生型样本与突变样本。表3为本次测试的Ct值,由表可知野生型样本两荧光通道之间的ΔCt为5.24,模拟样本两荧光通道之间的ΔCt为5.75,两样本ΔCt之间的差值,即ΔΔCt为0.51,对两样本的ΔCt进行显著性分析,检验p值<0.0001,表明反应体系可以区分野生型样本与突变样本。
表3
实施例3:突变频率5%模拟样本的KRAS G12C检测
参照表1配制反应体系,上下游引物及检测、参比探针序列同实施例2。检测模板为野生型人类基因组DNA与含KRAS G12C突变基因片段的质粒混合制备的突变频率为5%的G12C模拟样本,野生型样本为与模拟样本相同拷贝数的野生型人类基因组DNA。
如图3所示,模拟样本与对照组样本的扩增曲线存在明显差异,即反应体系可以区分野生型样本与突变样本。表4为本次测试的Ct值,由表可知野生型样本两荧光通道之间的ΔCt为4.66,模拟样本两荧光通道之间的ΔCt为3.62,两样本ΔCt之间的差值,即ΔΔCt为1.04,对两样本的ΔCt进行显著性分析,检验p值<0.0001,表明反应体系可以区分野生型样本与突变样本。
表4
实施例4:突变频率5%模拟样本的BRAF V600E检测
参照表1配制反应体系,上游引物序列为:
5’-TCATAATGCTTGCTCTGATAGGA-3’、下游引物序列为:
5’-CTGTTCAAACTGATGGGACCC-3’、检测探针序列为:
5’-(VIC)-CTACAGAGAAATCTCGA TGGA-3’、参比探针序列为:
5’-(6-FAM)-TCTTCATGAAGACCTCACAGT-3’。检测模板为野生型人类基因组DNA与含BRAF V600E突变基因片段的质粒混合制备的突变频率为5%的V600E模拟样本,野生型样本为与模拟样本相同拷贝数的野生型人类基因组DNA。
如图4所示,模拟样本与对照组样本的扩增曲线存在明显差异,即反应体系可以区分野生型样本与突变样本。表5为本次测试的Ct值,由表可知野生型样本两荧光通道之间的ΔCt为3.06,模拟样本两荧光通道之间的ΔCt为4.24,两样本ΔCt之间的差值,即ΔΔCt为1.18,对两样本的ΔCt进行显著性分析,检验p值<0.0001,表明反应体系可以区分野生型样本与突变样本。
表5
以上实施例仅用以说明本发明的技术方案,而非对其限制;尽管参照前述实施例对本发明进行了详细的说明,本领域的普通技术人员应当理解:其依然可以对前述各实施例所记载的技术方案进行修改,或者对其中部分技术特征进行等同替换;而这些修改或者替换,并不使相应技术方案的本质脱离本发明各实施例技术方案的精神和范围。
- 一种实时荧光定量PCR通用型荧光探针及其应用
- 用于荧光定量PCR的双探针组合物、试剂盒、用途及方法
- 用于荧光定量PCR的双探针组合物、试剂盒、用途及方法
