一种缓冲液、试剂盒和蛋白酶体检测方法
文献发布时间:2023-06-19 18:34:06
技术领域
本发明涉及生物技术领域,具体为一种缓冲液、试剂盒和蛋白酶体检测方法。
背景技术
蛋白质降解主要通过溶酶体降解和蛋白酶体介导的降解两种机制发生,前者通过蛋白水解酶活性发生,且几乎无特异性,而后者介导的降解通过靶蛋白的泛素化进行。靶蛋白通常是多泛素化的,并可激活26S蛋白酶体进行蛋白水解。蛋白酶体26S是蛋白酶体最常见的形式,是普遍存在于所有真核细胞的细胞核和细胞质的多蛋白复合物,分子量约为2500kDa,是一种ATP依赖性蛋白水解复合物,包括一个20S核心颗粒结构和两个19S调控颗粒。20S核心颗粒由28个蛋白亚基构成,具有糜蛋白酶样、胰蛋白酶样、caspase样三种主要的蛋白酶活性。这三种活性负责了体内包括关键的细胞周期蛋白、肿瘤抑制蛋白、转录因子和受损的胞内蛋白等大部分的蛋白降解,是维持细胞动态平衡所必需的。
已经有商品试剂盒(abcam,ProteasomeActivityAssayKit,ab107921)针对于糜蛋白酶 (又称胰凝乳蛋白酶)样蛋白酶活性进行检测,利用AMC标记的肽底物物被20S识别后释放高荧光AMC,在激发/发射波长为Ex/Em=350/440nm下进行荧光检测。
该商品试剂盒的检查下限介于10万至20万细胞之间。
该商品试剂盒采用的荧光标记物和底物分别为AMC和Suc-LLVY-AMC,缓冲溶液不详。
对于本领域技术人员来说,基于Suc-LLVY-AMC实现糜蛋白酶样蛋白酶活性的监测下限不能低于10万细胞。
实现1万细胞以下检测精度是本领域技术人员期待解决但是一直没有解决的技术问题。
所以,本案解决的技术问题是:如何降低糜蛋白酶样蛋白酶活性检测下限,即如何提高试剂盒检测蛋白酶体活性的灵敏度。
发明内容
本发明的目的在于提供一种缓冲液,该缓冲液应用于糜蛋白酶样蛋白酶体检测试剂盒后极大的提高了试剂盒的灵敏度,适用于微量穿刺样本;提供不同病人样本的定量试剂,便于病理分析,使其应用于临床成为可能。
同时,本发明还提供了试剂盒和糜蛋白酶样蛋白酶体活性的检测方法。
在不做特殊说明的情况下,M代表摩尔/升;mM代表毫摩尔/升,pmol代表皮摩尔/升。
为实现上述目的,本发明提供如下技术方案:一种蛋白酶体检测试剂盒用缓冲液,含 10~250毫摩尔/升Tris-HCl、2~40毫摩尔/升EDTA、水,pH为6~7。
优选地,上述缓冲液含50~250毫摩尔/升Tris-HCl、10~40毫摩尔/升EDTA、水,pH为6~7。
更优选地,上述缓冲液含50~250毫摩尔/升Tris-HCl、10毫摩尔/升EDTA、水,pH为6~7。
在上述的蛋白酶体检测试剂盒用缓冲液中,还含有0~50毫摩尔/升KCl、0~20毫摩尔/升NaCl、0~2毫摩尔/升MgCl
优选地,各无机盐的浓度为:0~50毫摩尔/升KCl、20毫摩尔/升NaCl、2毫摩尔/升MgCl
同时,本发明还公开了一种适用于肿瘤病人穿刺样本的高灵敏度蛋白酶体检测试剂盒,包括:如上述的缓冲液以及底物;
所述底物包括荧光标记物、20S蛋白酶体荧光底物、蛋白酶体抑制剂、水。
在上述的适用于肿瘤病人穿刺样本的高灵敏度蛋白酶体检测试剂盒中,所述荧光标记物的浓度为0.9-1.1毫摩尔/升;20S蛋白酶体荧光底物的浓度为4.5-5.5毫摩尔/升;蛋白酶体抑制剂的浓度为95-100微摩尔/升。
需要说明的是:基于本发明的底物中各物质是要加到孔中进行反应的,因此本发明的试剂盒所提供的浓度最终在反应体系中都是被稀释的,上述底物中各物质的浓度并不代表对本发明的限制。
本发明的试剂盒中关于荧光标记物、蛋白酶体荧光底物、蛋白酶体抑制剂的可用浓度均在本发明的保护范围内。
优选地,所述荧光标记物的浓度为1毫摩尔/升;20S蛋白酶体荧光底物的浓度为5毫摩尔/升;蛋白酶体抑制剂的浓度为100微摩尔/升。
在上述的适用于肿瘤病人穿刺样本的高灵敏度蛋白酶体检测试剂盒中,所述荧光标记物为7-氨基-4-甲基香豆素;所述20S蛋白酶体荧光底物为Suc-LLVY-AMC;所述蛋白酶体抑制剂为硼替佐米。
在上述的适用于肿瘤病人穿刺样本的高灵敏度蛋白酶体检测试剂盒中,还包括考马斯亮蓝。
优选地,所述考马斯亮蓝的浓度为1.8-2.2毫摩尔/升。
优选地,所述考马斯亮蓝的浓度为2毫摩尔/升。
此外,本发明还公开了一种蛋白酶体检测方法,采用如上任一所述的试剂盒对样品进行检测,得到蛋白酶体活性。
在上述的蛋白酶体检测方法中,包括如下步骤:
步骤1:采用荧光标记物绘制标准曲线;
步骤2:将样品、20S蛋白酶体荧光底物、抑制剂、缓冲液、超纯水得到第一混合液;
每100微升第一混合液中含50微升缓冲液、10微升样本、1微升20S蛋白酶体荧光底物、1微升抑制剂;
将样品、20S蛋白酶体荧光底物、缓冲液、超纯水得到第二混合液;
每100微升第二混合液中含50微升缓冲液、10微升样本、1微升20S蛋白酶体荧光底物;
步骤3:测定不同时刻的第一混合液的荧光值、第二混合液的荧光值,并结合标准曲线计算得到蛋白酶体活性。
上述方法中,各物质浓度并不限于以上点值,在本领域常规的荧光标记物、蛋白酶体荧光底物、蛋白酶体抑制剂的用量情况下,均可以达到本发明的目的。因此本领域常用浓度均在本发明的保护范围内。
与现有技术相比,本发明的有益效果是:
本试剂盒检测糜蛋白酶(又称胰凝乳蛋白酶)样蛋白酶活性,利用AMC标记的肽底物物被20S识别后释放高荧光AMC,在激发/发射波长为Ex/Em=350/440nm下进行荧光检测。本试剂盒配合检测缓冲液可提高检测灵敏度,配合蛋白酶体抑制剂及AMC标准品可实现样本蛋白酶体活性的精确定量,适用于高通量测定蛋白酶体活性并或可用于临床相关指标检测,该试验可在96孔或384孔板中进行。
通过一系列的实验证明,本案具有如下优势:
1.采用了本缓冲溶液的试剂盒,检测下限介于4000至8000细胞之间(满足临床微量穿刺样本的需求);
2.采用了本缓冲溶液的试剂盒能够对样本进行定量;
3.采用了本缓冲溶液的试剂盒的底物可以最大稀释3倍,可以检测临床微量穿刺样本。
附图说明
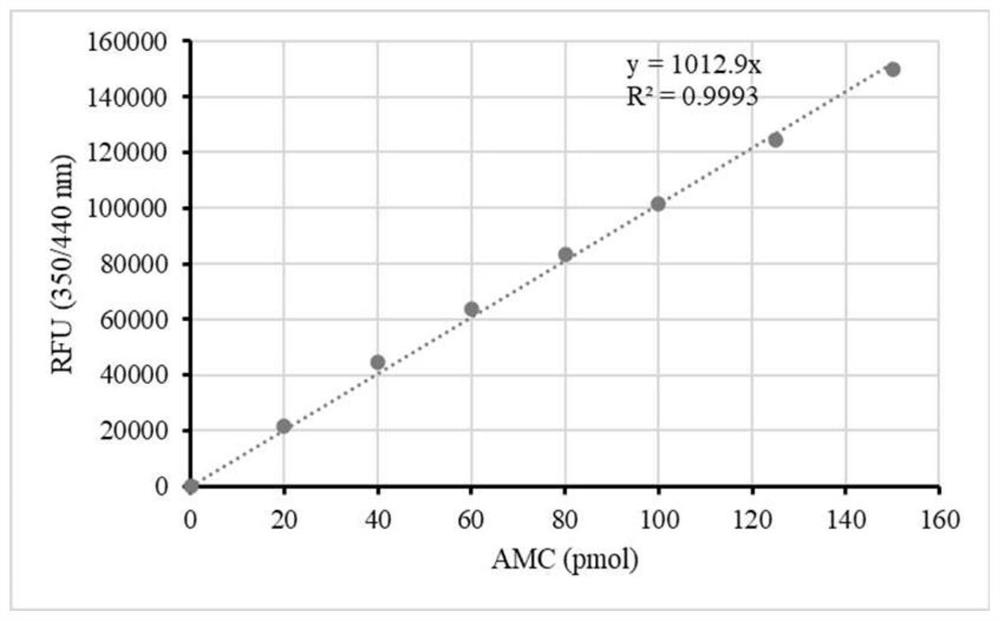
图1是本发明制备的标准样品后酶标仪检测吸光值曲线图;
图2是本发明试剂盒与商业试剂盒检测20万Jurkat细胞中蛋白酶体活性的吸光值曲线图;
图3是本发明试剂盒与商业试剂盒检测10万Jurkat细胞中蛋白酶体活性的吸光值曲线图;
图4是本发明试剂盒与商业试剂盒检测5万Jurkat细胞中蛋白酶体活性的吸光值曲线图;
图5是本发明的试剂盒与某种商业试剂盒对相同样本进行检测的荧光值;
图6是本发明的试剂盒与商品试剂盒(abcam,ab107921)的底物和缓冲液比较;
图7是本发明对不同来源样本的蛋白酶体活性的灵敏度检测结果图;
图8是本发明的试剂盒通过考马斯亮蓝测蛋白浓度定量不同样本的曲线;
图9是本发明的试剂盒和商业化试剂盒对临床微量穿刺样本的检测结果;
图10是本发明的试剂盒对对底物的稀释和使用的检测结果;
图10A是商业化试剂盒的试剂盒对对底物的稀释和使用的检测结果;
图11是本发明的缓冲溶液的Tris-HCl的用量变化后的检测结果图;
图12是本发明的缓冲溶液的Tris-HCl被同类物质替换后的检测结果图;
图13是本发明的缓冲溶液的EDTA的用量变化后的检测结果图;
图14是本发明的缓冲溶液的EDTA被同类物质替换后的检测结果图;
图15是本发明的缓冲溶液的的KCl用量变化后的检测结果图;
图16是本发明的缓冲溶液的的NaCl用量变化后的检测结果图;
图17是本发明的缓冲溶液的的MgCl
图18是本发明的缓冲溶液的的ATP用量变化后的检测结果图。
具体实施方式
下面将结合本发明实施例中的附图,对本发明实施例中的技术方案进行清楚、完整地描述,显然,所描述的实施例仅仅是本发明一部分实施例,而不是全部的实施例。基于本发明中的实施例,本领域普通技术人员在没有做出创造性劳动前提下所获得的所有其他实施例,都属于本发明保护的范围。
实施例1
一、试剂盒组成
本发明的试剂盒包括如下表1所示的单独包装的成分,表2示出了缓冲液的成分;
表1试剂盒成分表
表2缓冲液成分表
二、操作步骤
(1)样本制备
细胞消化离心后用预冷的PBS清洗一遍,弃掉PBS,将细胞沉淀用预冷的0.5%的NP-40 水溶液(需自备)反复吹打裂解,并于12000转/分钟4℃离心10分钟,取上清置于冰上待用。
(2)准备标曲
2.1准备0.01毫摩尔/升的AMC标准瓶:5微升的1毫摩尔/升AMC标准品加入到495微升超纯水中。
2.2在96孔不透明白板中按下表3依次加入0.01毫摩尔/升AMC,超纯水及2×缓冲液。
表3标准曲线绘制所涉及的配方表
(3)上样及检测
3.1配制底物工作液:10微升底物/100微升、2×缓冲液/样品,混匀;
3.2按下表4依次加入样品,超纯水,抑制剂及2×缓冲液。96孔不透明白板对应孔中,震荡混匀15s。
表4上样配方表
3.3 37℃避光孵育0~30分钟(需根据样品量及预实验结果确定具体时间)。
3.4检测T1时不同浓度标准品荧光值、样本的荧光值RFU1及样本加入抑制剂后的荧光值iRFU1(37℃避光,Ex/Em=350/440nm)。
3.5 37℃避光孵育30分钟。
3.6检测T2时不同浓度标准品荧光值、样本的荧光值RFU1及样本加入抑制剂后的荧光值iRFU2(37℃避光,Ex/Em=350/440nm)。
(4)蛋白酶体活性计算
4.1根据不同浓度标准品荧光值及对应的AMC量绘制标准曲线并计算线性方程。
4.2计算ΔRFU=(RFU2–iRFU2)–(RFU1–iRFU1),并将其代入标曲的线性方程计算得到对应的孔内AMC含量B(皮摩尔)。
4.3根据公式计算蛋白酶体活性:
B:单位为皮摩尔;T2,T1:单位为分钟;V:为加入孔内的样品体积(微升); D:为加入孔内之前样品的稀释倍数。
(5)注意事项
5.1建议采用白色不透明96孔板在酶标仪设置顶读模式下进行实验,设置复孔以提高检测准确度。
5.2为选择合适的检测时间T1及T2,步骤3.3-3.6可优化为酶标仪设置37℃,连续测读12次,间隔5分钟,选择线性区间内的荧光读值进行后续计算。
5.3理论样品可上样量为1~50微升,实验中应调整样品上样量使测得的RFU值落在标曲线性区间内(荧光信号值一般在0~160000)。
应用实例:
30万Jurkat细胞离心后以100微升0.5%NP-40裂解,上样10、5及2.5微升进行蛋白酶体活性检测。
(仪器
标准曲线如图1,5-20万Jurkat细胞中蛋白酶体活性测试曲线如图2-4。
结果:
结果1:本发明的试剂盒荧光值显著提高
如图2所示,首先比较了本发明的试剂盒与某种商业试剂盒对相同样本的荧光值,结果显示商业试剂盒的检查下限介于10万至20万细胞之间,而本发明的试剂盒的荧光值显著提高,灵敏度也显著提高。
进一步测试本发明的试剂盒的检测下限介于4000至8000细胞之间(图5)。
同时,比较了具体的试剂盒组分,通过相互组合比较,发现本发明的试剂盒缓冲液作用显著提高(图6)。
图6中,横坐标代表本发明的试剂盒的底物+本发明的缓冲液、商业试剂盒底物+本发明的缓冲液、商业试剂盒底物+商业试剂盒缓冲液、本发明的试剂盒的底物+商品试剂盒的缓冲液四种方案;
商业试剂盒底物包括荧光标记物、20S蛋白酶体荧光底物、蛋白酶体抑制剂以及水,各物质的浓度和本发明的试剂盒的底物的中荧光标记物、20S蛋白酶体荧光底物、蛋白酶体抑制剂以及水相似;其中,商业试剂盒底物中的20S蛋白酶体荧光底物为MG-132蛋白酶体抑制剂;荧光标记物、20S蛋白酶体荧光底物和本发明的试剂盒的底物的对应的物质相同;
本发明的试剂盒的底物包括荧光标记物、20S蛋白酶体荧光底物、蛋白酶体抑制剂、考马斯亮蓝以及水,其用量和配比参考表1。
商业试剂盒的缓冲溶液成分、配比不详。
图6的结果也从另外一个侧面也表明了本发明的荧光标记物、20S蛋白酶体荧光底物、蛋白酶体抑制剂的配合也是非常关键的,本发明的试剂盒的底物中的各组分的配合更加适用于本发明的缓冲溶液。
同时,图6也证明了本发明的缓冲溶液对于同样采用20S蛋白酶体荧光底物的商业试剂盒的底物也具有促进的作用。
在图6中,商业试剂盒所用酶体抑制剂为MG-132蛋白酶体抑制剂,本案所使用的是硼替佐米蛋白酶体抑制剂;通过上述的实验也可以证明,在本试剂盒中,硼替佐米蛋白酶体抑制剂能够和本案的缓冲溶液更好适配。
商业试剂盒底物+商业试剂盒缓冲液的方案、本发明的试剂盒的底物+商品试剂盒的缓冲液的方案的比对结果可见:商品缓冲液不管配合那种试剂盒底物,都不会表现不同的效果,其也说明了MG-132蛋白酶体抑制剂、硼替佐米蛋白酶体抑制剂在商品试剂盒缓冲液中无特异性表现。
本发明的试剂盒的底物+本发明的缓冲液的方案、商业试剂盒底物+本发明的缓冲液的方案的比对结果可见:本发明的缓冲液不管对于商品试剂盒底物还是对于本发明的试剂盒底物都有促进作用;同时,还证明了硼替佐米蛋白酶体抑制剂在本发明的缓冲液中能够产生于明显区别于MG-132蛋白酶体抑制剂的特异性表现。
综上所述,本发明的试剂盒的底物和本发明的缓冲液之间的复配是最优的。
本试剂盒有可能广泛用于研究和临床使用,因此选取了细胞系、小鼠肌肉组织和结肠癌病人肿瘤组织,分别使用本发明的试剂盒和某种商业试剂盒检测蛋白酶体活性。结果表明,本发明的试剂盒能够成功检测不同来源样本的蛋白酶体活性,并且灵敏度显著提高(图 7)。而商业化试剂盒有4例样本检测失败,荧光值处于负数区间(图7)。
图5:Jurkat细胞稀释至图示细胞数,使用本发明的试剂盒的检测下限。
图6:通过本发明的试剂盒和商业化试剂盒组分的不同组合,比较两种试剂盒的缓冲液和底物。
图7:分别收取5例细胞系样本,8例小鼠样本,2例结肠癌病人样本,分别使用两种试剂盒检测蛋白酶体活性。
结果2:本发明的试剂盒能够对样本进行定量
商业试剂盒未有多个样本之间定量的工具,导致临床病人样本无法相互比较。本试剂盒通过考马斯亮蓝测蛋白浓度定量不同样本,实现不同病人样本之间的蛋白酶体活性的科学比较。首先通过配制蛋白质标准品,使用考马斯亮蓝绘制标准曲线,得出计算蛋白质浓度的方程式(图8)。根据方程式,实测10万细胞样本和5万细胞样本,结果显示样本定量准确(表5)。
表5
结果3:本发明的试剂盒能够检测临床微量穿刺样本
本试剂盒有望用于临床样本检测,预测病人的治疗耐药性。然而临床微量穿刺样本细胞数量少,现有商业试剂盒灵敏度不高。因此进一步检测了本发明的试剂盒对临床病人微量穿刺样本的检测。结果表明,本发明的试剂盒能够检测全部3例微量穿刺样本,而商业化试剂盒仅成功检测1例样本(图9)。同时,检测了本发明的试剂盒对底物的稀释和使用,便于降低检测成本。结果表明,本发明的试剂盒的底物可以最大稀释3倍(图10),而商业化试剂盒的底物不能进一步稀释使用(图10A)。
对比案例
为了探讨本发明的缓冲液中各成分的重要性,按照每100微升的0.5%NP-40裂解约20 万Jurkat细胞的比例进行样本制备,取10微升上样连续测读,计算不同时间点的绝对RFU 值(RFU-iRFU),进行了如下实验:
对比实验1
在上述实验案例的基础上,改变Tris-HCl的用量,观察检测灵敏度。
Tris-HCl的用量从0-250毫摩尔/升变化,结果参考图11;
Tris-HCl采用PBS替换,结果参考图12;
可见,Tris-HCl缺失后绝对RFU值(RFU-iRFU)明显降低,且替换为PBS,TBS以及同等浓度的Hepes均导致RFU值明显降低,Tris-HCl为保证试剂盒检测灵敏性必需,本试剂盒Tris-HCl浓度范围为10-250毫摩尔/升。
对比实验2
在上述实验案例的基础上,改变EDTA的用量,观察检测灵敏度。
EDTA的用量从0-40毫摩尔/升变化,结果参考图13;
EDTA采用DTT、TCEP、β-ME替代后,结果参考图14;
可见,EDTA缺失后绝对RFU值(RFU-iRFU)明显降低,且替换为同等浓度的具有类似功能的成分二硫苏糖醇(DTT),三(2-羧乙基)膦盐酸盐(TCEP)以及β巯基乙醇(β -ME)均导致RFU值明显降低,EDTA为保证试剂盒检测灵敏性必需,本试剂盒EDTA浓度范围为2-40毫摩尔/升。
对比实验3
在上述实验案例的基础上,改变无机盐的用量,观察检测灵敏度。
结果参考图16-图18;
可见,缓冲液中KCl浓度在0-50毫摩尔/升内均能使得本试剂盒有很高的灵敏性;
NaCl浓度在0-20毫摩尔/升,MgCl
综上所述,本发明通过上述实验证明了如下结论:
1.采用了本缓冲溶液的试剂盒,检测下限介于4000至8000细胞之间(满足临床微量穿刺样本的需求);
2.采用了本缓冲溶液的试剂盒能够对样本进行定量;
3.采用了本缓冲溶液的试剂盒的底物可以最大稀释3倍,可以检测临床微量穿刺样本。
4.商业化的同类试剂盒在性能1-3上不占优势,本发明认为其缓冲溶液并没有调整到合适的组合和用量;
虽然Tris-HCl、EDTA均为常用的缓冲溶液的成分,但是在酶活性检测的试剂盒中,基于底物、检测对象的性能的巨大差异以及荧光标记物的种类和具体物质之间的差异,缓冲溶液往往需要反复实验才能得到最适合该酶、底物的缓冲溶液。
通过本发明的相关实验,本发明的缓冲溶液已经接近该系列试剂盒的最优缓冲溶液的选择。
- 一种含特定PCR缓冲液的乙肝DNA检测试剂盒
- 一种检测葡萄糖-6-磷酸异构酶的试剂盒及试剂盒的使用方法
- 一种NSE检测试纸条的制备方法、试纸条、检测卡及NSE检测试剂盒
- 一种水稻黄单胞菌的环介导等温扩增检测引物组、检测方法和检测试剂盒
- 一种尿液中氧化三甲胺快速检测方法及检测试剂盒
- 一种混合蛋白酶体系、包含该混合蛋白酶体系的试剂盒及其使用方法
- 一种糖类抗原CA125表面Tn抗原检测用校准品缓冲液及其制备方法、检测试剂盒
