常温检测超微量新冠病毒RNA的试剂盒及方法
文献发布时间:2023-06-19 19:30:30
技术领域
本发明属于核酸检测技术领域,具体而言,涉及一种由靶RNA识别扩增模块和基于CRISPR-Cas12a的二重信号放大模块构成的常温检测超微量新冠病毒RNA的试剂盒及方法。
背景技术
传统的RNA检测方法主要包括测序、Northern分析、PCR、微阵列和荧光探针等方法。测序法能够较为全面的展示样本内的RNA信息,但是该方法成本较高、耗时较长,需要利用复杂、昂贵的仪器,难以在基层进行广泛地推广。Northern分析简单易行,成本低廉,但该方法耗时长、灵敏度低、特异性差。微阵列方法能够进行高通量的miRNA分析,灵敏度较低,但是该方法成本较高,且特异性有待进一步提升。PCR法需要对RNA进行逆转录的预处理,将其转换为cDNA后再进行分析,该步骤需要进行多步的不同温度下的反应,增加了检测时长与操作的复杂度。此外,PCR方法需要对升温、退火温度进行严格地控制,需要配备相关的仪器与经过专业培训的加样人员,提高了该方法的成本与操作复杂性,限制了向基层的进一步推广。
近年来,基于CRISPR-Cas12a的核酸检测体系因其较好的特异性和灵敏度受到人们的广泛关注。当底物DNA激活CRISPR-Cas12a系统后,可激活其反式切割活性,在常温下循环切割体系内的单链DNA荧光探针,实现信号的放大。然而对于RNA检测而言,仍然具有两大瓶颈问题。一是需要进行较为复杂的逆转录过程,将RNA转换为cDNA形式;二是基于CRISPR-Cas12a的RNA检测系统的检测限无法满足超低丰度RNA检测的需求,极大地限制了这一系统的推广与运用。如,CN113337638A公开了一种新型冠状病毒(SARS-CoV-2)的检测方法和试剂盒,然而该方法是将CRISPR反式切割与PCR技术结合,需要进行PCR扩增。CN111154919A公开了一种单独闭管一步法检测新型冠状病毒核酸的试剂盒,通过滚环扩增(RCA)产生大量G4链体纳米线,进而催化显色反应实现新冠状病毒核酸的快速直接检测,但是其检测限1pM。CN113151591A公开了一种用于检测SARS-CoV-2的核酸组合物和试剂盒,将滚环扩增技术和重组酶聚合酶扩增技术进行了巧妙的融合,可在等温条件下对待测样本进行检测,无需价值昂贵、步骤繁琐的温度循环仪器,但是其灵敏度仅为100pg/μL。
发明内容
针对现有技术的不足,本发明的目的在于提供一种简单、快速、高灵敏的由靶RNA识别扩增模块和基于CRISPR-Cas12a的二重信号放大模块构成的试剂盒及超微量新冠病毒RNA的常温检测方法,以完成快速、廉价、特异的低丰度新冠病毒核酸常温检测。
本发明采用的技术方案如下:
第一方面,本发明提供一种用于检测SARS-CoV-2的核酸组合物,包括DNA识别链和DNA辅助链;所述DNA识别链用于靶RNA的信号识别,识别区域为新冠病毒基因的保守序列;所述DNA辅助链用于辅助识别链与靶RNA滚环扩增。
在其中一些实施方式中,所述DNA识别链的序列选自SEQ ID NO.1~SEQ ID NO.4中的一个或多个序列;所述DNA辅助链的序列如SEQ ID NO.5所示。
在其中一些较优的实施方式中,所述DNA识别链的序列如SEQ ID NO.1、SEQ IDNO.3和SEQ ID NO.4所示。
第二方面,本发明提供一种用于检测SARS-CoV-2的试剂盒,包括靶RNA识别扩增模块和二重信号放大模块;所述靶RNA识别扩增模块包括本发明第一方面提供的核酸组合物、DNA连接酶和DNA聚合酶;所述二重信号放大模块包括Cas12a反应系统、iCas12a反应系统和荧光探针;所述Cas12a反应系统包括Cas12a和crRNA;所述iCas12a反应系统包括crRNA、Blocker链和Cas12a。
在其中一些实施方式中,所述核酸组合物由DNA识别链和DNA辅助链溶解于DNA聚合酶缓冲液中,85℃变性3分钟,55℃退火3分钟,放置于37℃孵育制得。
在其中一些实施方式中,所述DNA连接酶为T4连接酶;和/或,所述DNA聚合酶为Phi29 DNA聚合酶。
在其中一些实施方式中,所述Cas12a反应系统由Cas12a和crRNA在缓冲液环境下混匀,37℃孵育制得。
在其中一些实施方式中,所述iCas12a反应系统由crRNA与Blocker链溶解于缓冲液中,85℃变性3分钟,55℃退火3分钟,放置于37℃孵育得到的crRNA-Blocker复合物,与Cas12a在缓冲液环境下混匀,37℃孵育制得。
在其中一些实施方式中,所述crRNA的序列如SEQ ID NO.6所示;和/或,所述Blocker链的序列如SEQ ID NO.7所示;和/或,所述荧光探针的序列如SEQ ID NO.8所示。
第三方面,本发明提供一种常温检测超微量新冠病毒RNA的方法,基于本发明第二方面提供的试剂盒,具体包括如下步骤:
S1.将待测核酸样本置于靶RNA识别扩增模块进行扩增,得扩增产物;
S2.将扩增产物与二重信号放大模块混合,避光检测;
步骤S1中,扩增反应条件为37℃下反应15分钟;
步骤S2中,检测反应条件为37℃,激发光波长485nm,发射光波长520nm。
与现有技术相比,本发明的有益效果在于:
本发明提供的试剂盒和检测方法能够常温(25℃~40℃,优选37℃)下检测超微量新冠病毒RNA,反应条件温和,无需逆转录过程,操作简便,且兼顾检测的高特异性与高灵敏度。当体系中不存在新冠病毒靶RNA时,靶RNA识别扩增模块无法进行反应,进而无法激活二重信号放大模块,具有低背景的优势。此外,本发明采用的核酸组合物能够充分发挥CRIPSR-Cas12a检测系统灵敏度高的特点,检测限可达到100aM级别,能够实现对超微量RNA的检测。
附图说明
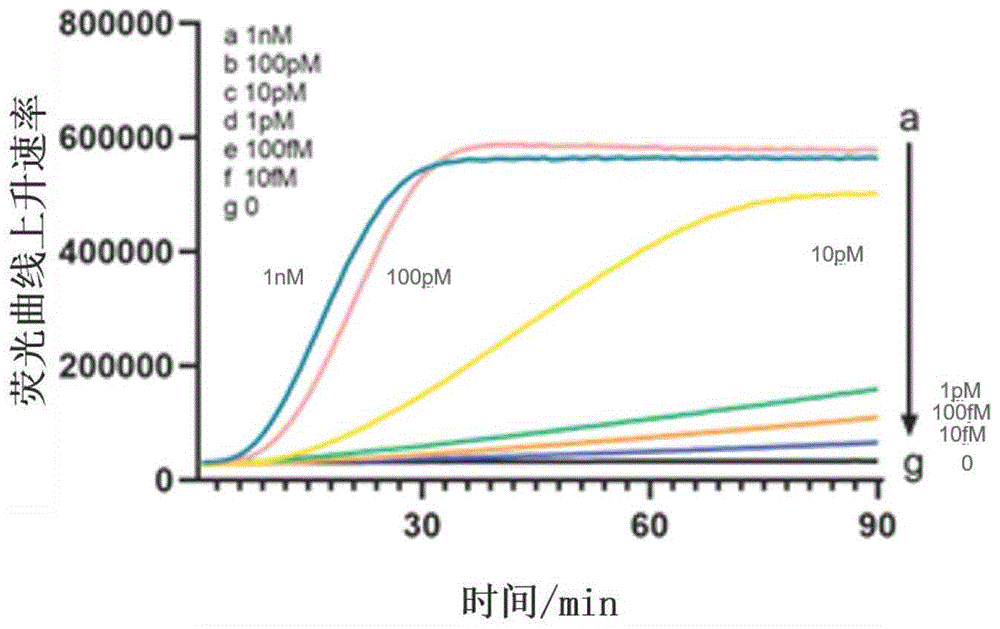
图1为实施例1对新冠病毒N基因RNA检测的检测限。
图2为实施例2对新冠病毒N基因RNA检测限的统计评估。
图3为实施例3对新冠病毒N基因RNA检测限的统计评估。
图4为实施例4对新冠病毒N基因RNA检测限的统计评估。
图5为实施例5对新冠病毒N基因RNA检测限的统计评估。
图6为对比例1对新冠病毒N基因RNA检测限的统计评估。
图7为对比例2对新冠病毒N基因RNA检测限的统计评估。
具体实施方式
以下结合具体实施例对本发明作进一步的详细说明,以使本领域的技术人员更加清楚地理解本发明。所举实例只用于解释本发明,并非用于限定本发明的范围。在本发明实施例中,若无特殊说明,所有原料组分均为本领域技术人员熟知的市售产品;若未具体指明,所用的技术手段均为本领域技术人员所熟知的常规手段。
本发明的技术构思在于提供一种简单、快速、高灵敏的由靶RNA识别扩增模块和基于CRISPR-Cas12a的二重信号放大模块构成的试剂盒及超微量新冠病毒RNA的常温检测方法。
第一方面,本发明提供一种用于检测SARS-CoV-2的核酸组合物,包括DNA识别链和DNA辅助链;DNA识别链用于靶RNA的信号识别,识别区域为新冠病毒基因的保守序列;DNA辅助链用于辅助识别链与靶RNA滚环扩增。
具体的,DNA识别链的序列选自SEQ ID NO.1~SEQ ID NO.4中的一个或多个序列;
CTACTGCTGCCTGGATTTTTTAAGGGCATGAGCTAGGTGATACTCTGGGTGAGTATGCAGGAGAAGTTCCC(SEQ ID NO.1);
CTACTGCTGCCTGGAGTTGAATTTTTTAAGGGCATGAGCTAGGTGATACTCTGGGTGAGTATCTAGCAGGAGAAG(SEQ ID NO.2);
TGGTTCAATCTGTCAAGCAGTTTTTTAAGGGCATGAGCTAGGTGATACTCTGGGTGAGTATCAGCAAAGCAAGAGCAGCA(SEQ ID NO.3);
TCCCTTCTGCGTAGAAGCCTTTTTTAAGGGCATGAGCTAGGTGATACTCTGGGTGAGTATCTTGACTGCCGCCTCTGC(SEQ ID NO.4)。
DNA辅助链的序列设计为:ATACTCACCCAGAGT(SEQ ID NO.5)。
第二方面,本发明提供一种用于检测SARS-CoV-2的试剂盒,包括靶RNA识别扩增模块和二重信号放大模块;靶RNA识别扩增模块包括本发明第一方面提供的核酸组合物、DNA连接酶和DNA聚合酶;二重信号放大模块包括Cas12a反应系统、iCas12a反应系统和荧光探针;Cas12a反应系统包括Cas12a和crRNA;iCas12a反应系统包括crRNA、Blocker链和Cas12a。
具体的,核酸组合物由DNA识别链和DNA辅助链溶解于DNA聚合酶缓冲液中,85℃变性3分钟,55℃退火3分钟,放置于37℃孵育制得。
DNA连接酶为T4连接酶;DNA聚合酶为Phi29 DNA聚合酶。
Cas12a反应系统由Cas12a和crRNA在缓冲液环境下混匀,37℃孵育制得。
iCas12a反应系统先由crRNA与Blocker链溶解于缓冲液中,85℃变性3分钟,55℃退火3分钟,放置于37℃孵育得到的crRNA-Blocker复合物,在由crRNA-Blocker复合物与Cas12a在缓冲液环境下混匀,37℃孵育制得。
crRNA的序列设计为:
UAAUUUCUACUAAGUGUAGAUAAGGGCAUGAGCUAGGUGAU(SEQ ID NO.6)。
Blocker链的序列设计为:
ATCACCTAGTATATCTCATGCCCTTATCTACACTTAGTAGTTTTTAAATTA(SEQ ID NO.7)。
荧光探针的序列设计为:FAM-TTTTTATTTTT-BHQ(SEQ ID NO.8)。
第三方面,本发明提供一种常温检测超微量新冠病毒RNA的方法,基于本发明第二方面提供的试剂盒,具体包括如下步骤:
S1.将待测核酸样本置于靶RNA识别扩增模块进行扩增,得扩增产物;
S2.将扩增产物与二重信号放大模块混合,避光检测;
步骤S1中,扩增反应条件为37℃下反应15分钟;
步骤S2中,检测反应条件为37℃,激发光波长485nm,发射光波长520nm。
当待测核酸样本中存在新冠病毒靶RNA时,靶RNA与DNA识别链结合,并形成环形结构,在DNA辅助链的引导和Phi29 DNA聚合酶的作用下,以DNA识别链作为模板进行环形扩增,得到多个重复的、与DNA识别链互补的扩增DNA产物。扩增产物中包含能与下游二重信号放大模块反应的DNA序列,因此可直接与后一模块相偶联,完成信号的进一步放大与报告。当不存在靶RNA时,DNA识别链无法形成环形结构,无法扩增出与下游模块反应的产物,因而无法产生报告信号,具有低背景的优势。
进一步地,上游产生的扩增DNA产物一方面可直接激活CRISPR-Cas12a系统的反式切割活性。即激活的CRISPR-Cas12a可切割两端标记有荧光基团FAM和淬灭基团BHQ的单链DNA荧光探针,从而产生循环信号报告。另一方面,激活的CRISPR-Cas12a可以激活二重信号放大模块中被封闭的iCRISPR-Cas12a(inhibit-CRISPR-Cas12a),使之转换具有信号放大活性的aCRISPR-Cas12a。上游扩增产物进入本模块后,Cas12a的非特异性切割活性会被激活,进而切割体系中存在的单链探针,从而产生荧光信号。此外,激活的Cas12a会切割体系中封闭igRNA-T2的DNA链,随后igRNA-T2形成完整的gRNA-T2;然后,gRNA-T2与Cas12a结合,并与辅助目标引物匹配,激活Cas12a。激活的Cas12a一方面会切割体系中的游离探针,另一方面也会切割sgRNA,从而形成正反馈系统,实现信号的二重放大。通过二重循环放大体系,直接增加产生信号的Cas12a的酶的数量,进而提高检测方法的灵敏度,从而在保持体系以及检测程序相对简单的情况下,实现对超微量RNA的检测。
下面针对新冠病毒N基因的实验进行举例说明。
本发明试验例中的寡核苷酸链由上海生工经HPLC纯化合成。
Lba Cas12a和NEBuffer 2.1由New England Biolabs公司购买。
T4 DNA连接酶和Phi 29 DNA聚合酶在BBI生命科学公司购买。
检测仪器:Biotek酶标仪。
实施例1
(1)委托合成如下序列
合成DNA识别链序列:
CTACTGCTGCCTGGATTTTTTAAGGGCATGAGCTAGGTGATACTCTGGGTGAGTATGCAGGAGAAGTTCCC(SEQ ID NO.1)。
合成DNA辅助链序列:ATACTCACCCAGAGT(SEQ ID NO.5)。
合成crRNA序列:
UAAUUUCUACUAAGUGUAGAUAAGGGCAUGAGCUAGGUGAU(SEQ ID NO.6)。
合成Blocker链序列:
ATCACCTAGTATATCTCATGCCCTTATCTACACTTAGTAGTTTTTAAATTA(SEQ ID NO.7)。
合成荧光探针序列:FAM-TTTTTATTTTT-BHQ(SEQ ID NO.8)。
(2)制备识别链-辅助链核酸组合物
将DNA识别链与DNA辅助链以1:1.5比例溶解于phi29 DNA聚合酶缓冲液中,85℃变性3分钟,55℃退火3分钟,放置于37℃孵育10分钟。具体反应体系见下表:
(3)制备靶RNA识别扩增模块
将不同浓度的待测新冠病毒样品、识别链-辅助链核酸组合物、T4连接酶、Phi29DNA聚合酶共同溶解于缓冲溶液,37℃下反应15分钟,得扩增产物。具体反应体系见下表:
(4)预组装Cas12a反应系统
将Cas12a和crRNA在NEBuffer2.1环境下混匀,37℃孵育30分钟。具体反应体系见下表:
(5)预组装iCas12a反应系统
制备crRNA-Blocker复合物:将crRNA与Blocker链以1:2比例溶解于NEBuffer2.1缓冲液中,85℃变性3分钟,55℃退火3分钟,放置于37℃孵育1小时后可放置于4℃备用。具体反应体系见下表:
将crRNA-Blocker复合物与Cas12a在NEBuffer2.1环境下混匀,37℃孵育30分钟。具体反应体系见下表:
(6)CRISPR-Cas12a切割体系的构建与荧光检测:
将预先构建好的扩增产物、Cas12a反应系统、iCas12a反应系统和荧光探针混合。在37℃条件下,在酶标仪内进行避光检测。具体反应体系见下表:
荧光酶标仪反应条件:37℃,激发光波长485nm,发射光波长520nm,检测时间90分钟。
检测结果统计见图1。分析各浓度对应荧光曲线的线性段上升速率,可以看出本系统可检测到10fM级别的新冠病毒RNA。
实施例2
本实施例试验原料及工艺步骤基本与实施例1相同,区别仅在于,设计的DNA识别链的序列为:
CTACTGCTGCCTGGAGTTGAATTTTTTAAGGGCATGAGCTAGGTGATACTCTGGGTGAGTATCTAGCAGGAGAAG(SEQ ID NO.2)。
检测结果如图2所示,检测限可达到10fM。
实施例3
本实施例试验原料及工艺步骤基本与实施例1相同,区别仅在于,设计的DNA识别链的序列为:
TGGTTCAATCTGTCAAGCAGTTTTTTAAGGGCATGAGCTAGGTGATACTCTGGGTGAGTATCAGCAAAGCAAGAGCAGCA(SEQ ID NO.3)。
检测结果如图3所示,检测限可达到1fM。
实施例4
本实施例试验原料及工艺步骤基本与实施例1相同,区别仅在于,设计的DNA识别链的序列为:
TCCCTTCTGCGTAGAAGCCTTTTTTAAGGGCATGAGCTAGGTGATACTCTGGGTGAGTATCTTGACTGCCGCCTCTGC(SEQ ID NO.4)。
检测结果如图4所示,检测限可达到1fM。
实施例5
本实施例试验原料及工艺步骤基本与实施例1相同,区别仅在于,设计的DNA识别链有3条,序列分别为:
CTACTGCTGCCTGGATTTTTATACATATTTATGGGTTTGGCTCTGGGAAAGTATGCAGGAGAAGTTCCC(SEQ ID NO.1);
TGGTTCAATCTGTCAAGCAGTTTTTTAAGGGCATGAGCTAGGTGATACTCTGGGTGAGTATCAGCAAAGCAAGAGCAGCA(SEQ ID NO.3);
TCCCTTCTGCGTAGAAGCCTTTTTTAAGGGCATGAGCTAGGTGATACTCTGGGTGAGTATCTTGACTGCCGCCTCTGC(SEQ ID NO.4)。
制备识别链-辅助链核酸组合物的各识别链序列比例为:1:1:1。
检测结果如图5所示,检测限可达到100aM。
对比例1
本实施例试验原料及工艺步骤基本与实施例1相同,区别仅在于,设计的DNA识别链的序列为:
CATACCGCAGACGGCCCGCCCTACCCAAAACTGAACCCGCCCTACCAAAACCCAACCCGCCCTACCATAACCTTTCCA(SEQ ID NO.9)。
检测结果如图6所示,1nM组与空白组的荧光曲线上升速率没有明显差异,检测限仅1nM。
对比例2
本实施例试验原料及工艺步骤基本与实施例1相同,区别仅在于,设计的DNA识别链的序列为:
GCAGCAGAGACGAAAAAACACAAAGGAACGAGAGGACAGGAACCACAGACAAAGGAGCACGA(SEQ IDNO.10)。
检测结果如图7所示,1nM组与空白组的荧光曲线上升速率没有差异,检测限仅1nM。
以上所述仅为本发明的较佳实施例,并不用以限制本发明,凡在本发明的精神和原则之内,所作的任何修改、等同替换、改进等,均应包含在本发明的保护范围之内。
- 一种定量检测新冠病毒拷贝数的检测试剂盒及检测方法、以及新冠病毒重症预警指标
- 基于RT-RPA和CRISPR的可视化新冠病毒RNA核酸检测试剂盒
