一种检测结核分枝杆菌异烟肼耐药基因突变的核酸组合物、试剂盒及检测方法
文献发布时间:2024-04-18 19:58:53
技术领域
本发明涉及生物检测领域,具体而言,涉及一种检测结核分枝杆菌异烟肼耐药基因突变的核酸组合物、试剂盒及检测方法。
背景技术
结核病是由结核分枝杆菌(Mycobacterium tuberculosis,MTB)引起的一种慢性传染性疾病,多发生在肺部,以肺结核最为常见。在中国,结核潜伏感染者约为2.5-3亿。2021年10月14日,世界卫生组织发布了《2021年全球结核病报告》,报告显示我国2020年估算的结核病新发患者数为84.2万,估算结核病发病率为59/10万。如果病人感染的结核分枝杆菌对一种或一种以上的抗结核药物产生了耐药性,即为耐药结核病。据WHO/IUATLD的最新耐药监测估计,在新病人中,10.2%的病人至少对一种抗结核药物耐药,1.1%为多重耐药结核;在复治病人中,18.4%的病人至少对一种抗结核药物耐药,多重耐药率7.0%。耐药结核病为结核病的防治带来巨大的挑战。
异烟肼(INH)是临床中常用的一线抗结核药物,但是由于治疗疗程长,导致患者中断治疗,可能会产生耐药性,耐药的发生还与MTB的基因突变有关。INH耐药相关的突变主要发生于katG和inhA启动子区,此外还有ahpC、fabG1、kasA、iniA/B/C、ndh、fadE、furA、Rv1592c和Rv1772及其启动子区等与INH耐药相关的基因。临床中常用的其他一二线药物如链霉素、氨硫脲、环丝氨酸和乙(丙)硫异烟胺等药物,MTB对其产生的耐药性比较稳定,耐药后很少复敏;利福平耐药后复敏率约为4.2%;而INH耐药后,停药36周可有88.5%的复敏率。
目前结核分枝杆菌的耐药检测技术有表型药敏法和分子药敏法。表型药敏方法是建立在培养基础上的,通过观察结核菌在含药培养基中的生长情况来检测其耐药性,是目前耐药检测的金标准。但培养法耗时长,通常需要数周以上的时间才能得出结果,对于急需抗结核治疗的患者来说可能会造成延误。分子药敏方法是采用分子生物学技术检测、鉴定结核菌的耐药基因突变型。分子检测的优点是可快速、灵敏地从临床标本中检出耐药结核菌,甚至涂阴、培阴的标本。
目前,市面上主要应用的结核耐药分子诊断试剂有美国赛沛Xpert MTB/RIF,和厦门致善生物的结核分枝杆菌耐药突变检测试剂盒。分子检测方法便捷迅速,但赛沛的异烟肼耐药检测需配备专用检测仪器,价格昂贵,性价比不高,不利于结核病的普及筛查与有效防控;厦门致善的异烟肼耐药检测试剂为双管双体系,操作繁复,且检测样本为分离培养物,不能直接检测人痰液样本。
因此,本领域迫切需要开发操作简便、成本较低、检测效率较高且具有较高灵敏度和准确性的结核分枝杆菌耐药性检测方法以满足临床需求。
鉴于此,特提出本发明。
发明内容
本发明的目的在于提供一种检测结核分枝杆菌异烟肼耐药基因突变的核酸组合物、试剂盒及检测方法,以实现单管单体系检测KatG、InhA、ahpC三个与异烟肼耐药相关基因的九种突变,本发明提供的核酸组合物、试剂盒及检测方法具有操作简便,快捷高效,且具有较高的检测灵敏度和准确性。
本发明是这样实现的:
第一方面,本发明提供了一种用于检测结核分枝杆菌异烟肼耐药基因突变的核酸组合物,其包括:核苷酸序列如SEQ ID No.1~2所示的第一引物对,核苷酸序列如SEQ IDNo.3~4所示的第二引物对,核苷酸序列如SEQ ID No.5~6所示的第三引物对。
在本发明应用较佳的实施方式中,核酸组合物还包括探针,探针包括如SEQ IDNo.7所示的第一探针、如SEQ ID No.8所示的第二探针、如SEQ ID No.9所示的第三探针和如SEQ ID No.10所示的第四探针;
在一种可选的实施方式中,第一探针用于检测KatG S315T和KatG S315N突变;第二探针用于检测ahpC C-6A和ahpC C-12T突变;第三探针用于检测ahpC C-39T、ahpC G-46A和ahpC T-49G突变;第四探针用于检测InhAT-8C和InhA C-15T突变;
在一种可选的实施方式中,第一探针、第二探针、第三探针和第四探针中的至少一个探针含有至少一个修饰的核苷酸基团;
在一种可选的实施方式中,修饰的核苷酸基团为(1)~(3)中的至少一种:
(1)磷酸基团修饰的核苷酸基团;
(2)核糖基团修饰的核苷酸基团。
在一种可选的实施方式中,磷酸基团修饰是对磷酸基团中的氧进行修饰,包括硫代修饰和硼烷化修饰;
在一种可选的实施方式中,核糖基团修饰是对核糖基团中2’-羟基进行修饰,选自如下修饰中的任意一种:2’-氟修饰、2’-甲氧基修饰、2’-甲氧乙基修饰、2’-2,4-二硝基苯酚修饰、锁核酸修饰、2’-氨基修饰和2’-脱氧修饰。
在一种可选的实施方式中,核糖基团修饰是对核糖基团中2’-羟基进行锁核酸修饰;
在一种可选的实施方式中,第一探针的核苷酸序列中第10位碱基G为锁核酸修饰碱基;第四探针的核苷酸序列中第19位碱基T为锁核酸修饰碱基。
在本发明应用较佳的实施方式中,探针的5’设有荧光报告基团,3’设有荧光淬灭基团和/或MGB。
在一种可选的实施方式中,荧光报告基团选自:5-FAM、6-FAM、HEX、TET、VIC、JOE、Cy3、Cy3.5、NED、TAMRA、ROX、Texas Red、Cy5、Cy5.5和Quasar670中的任意一种;
在一种可选的实施方式中,荧光淬灭基团选自:TAMRA、Eclipse、BHQ系列、Dabcyl、Lowa BlackTM RQ和Lowa BlackTM FQ中的至少一种;
在一种可选的实施方式中,BHQ系列选自BHQ0、BHQ1、BHQ2和BHQ3中的至少一种。
在本发明应用较佳的实施方式中,在第一引物对、第二引物对和第三引物对中的任意一对引物对中,上游引物和下游引物的摩尔比独立地为(1~20):(1~20);
在一种可选的实施方式中,上游引物和下游引物的摩尔比独立地为1:(1~20);
在一种可选的实施方式中,第一引物对中上游引物和下游引物的摩尔比独立地为1:(1~20);第二引物对中上游引物和下游引物的摩尔比独立地为1:(1~20);第三引物对中上游引物和下游引物的摩尔比独立地为1:(1~20)。
在一种可选的实施方式中,核酸组合物中第一探针、第二探针、第三探针和第四探针的浓度独立地为0.01~1μM,优选为0.1~0.5μM。
第二方面,本发明还提供了一种试剂或试剂盒,其包括上述的核酸组合物。
在本发明应用较佳的实施方式中,试剂或试剂盒还包括如下物质中的至少一种:PCR反应缓冲液、DNA聚合酶、镁离子、dNTP、野生型对照、阴性对照和水;
在一种可选的实施方式中,DNA聚合酶选自Tth DNA聚合酶或其突变体、Taq DNA聚合酶或其突变体、Pfu酶或其突变体和Hawk Z05聚合酶或其突变体中的至少一种;
DNA聚合酶的浓度为0.01U/μl~5U/μl;
镁离子的工作浓度为0.5mM~1.5mM;
dNTP的工作浓度为0.1mM~25mM;
第一引物对、第二引物对和第三引物对中的任意一对引物对中,上游引物和下游引物的浓度为0.1μmol/L~5μmol/L;
在第一引物对、第二引物对和第三引物对中的任意一对引物对中,上游引物和下游引物的摩尔比独立地为(1~20):(1~20)。
第三方面,本发明还提供了核酸组合物在制备结核分枝杆菌异烟肼耐药基因突变的检测产品中的应用;
在一种可选的实施方式中,检测产品选自试剂、试剂盒和基因芯片中的任一种。
第四方面,本发明还提供了一种结核分枝杆菌异烟肼耐药基因突变的检测方法,其包括:采用上述的核酸组合物或上述的试剂或试剂盒对待测样本进行PCR检测;
检测方法不以疾病的诊断或治疗为目的;
在一种可选的实施方式中,待测样本选自核酸样本、含核酸样本的环境样本、阴性对照、阳性对照、人痰液、痰固体分离物及其培养物和液体分离物及其培养物中的至少一种。
在本发明应用较佳的实施方式中,进行PCR检测时,在第一引物对、第二引物对和第三引物对中的任意一对引物对中,上游引物和下游引物的摩尔比独立地为(1~20):(1~20);
在一种可选的实施方式中,上游引物和下游引物的摩尔比独立地为1:(1~20);
在一种可选的实施方式中,进行PCR检测时,第一引物对、第二引物对和第三引物对中的任意一对引物对中,上游引物和下游引物的工作浓度独立地为0.01~5μM,优选为0.1~1μM;
在一种可选的实施方式中,进行PCR检测时,第一探针、第二探针、第三探针和第四探针的工作浓度独立地为0.01~1μM,优选为0.1~0.5μM;
在一种可选的实施方式中,PCR的反应程序如下:94~96℃15sec~10min(预变性);94~98℃10~30s,55~65℃,20~40s,70~74℃20~30s,30~50个循环;55~56℃20~40s处收集荧光信号;94~96℃1~3min,33~37℃1~3min;35~90℃,持续收集荧光信号。
第五方面,本发明还提供了用于结核分枝杆菌异烟肼耐药基因突变检测的系统,其包括:上述的试剂或试剂盒、第一装置和第二装置;第一装置能够采用试剂或试剂盒对待测DNA样本、野生型对照及阴性对照分别进行实时荧光定量PCR检测,获得熔解曲线图;
第二装置包括:数据输入模块、数据分析与结论输出模块;
数据输入模块被配置为输入第一装置所得的熔解曲线图数据;数据分析与结论输出模块被配置为:根据待测样本与野生型对照在各通道熔解峰的Tm差值的变化判读待测样本是否含有基因突变和确定基因突变的类型。
本发明具有以下有益效果:
本发明提供的试剂基于实时荧光定量PCR,结合了多重不对称PCR技术、Taqman探针技术及熔解曲线分析技术,以结核分枝杆菌异烟肼耐药决定区KatG基因、InhA基因和ahpC基因序列为靶标进行检测。实现了一次性特异的检测并区分KatG S315T、KatG S315N、ahpC C-6A、ahpC C-12T、ahpC C-39T、ahpC G-46A、ahpC T-49G、InhA T-8C、InhA C-15T九种突变位点。
本发明还提供了检测试剂和试剂盒,针对各种突变位点的序列设计特异扩增的引物,以应用多重不对称PCR对多个位点进行同管检测。
使用本发明的试剂检测结核分枝杆菌异烟肼耐药国家参考品盘,敏感参考品符合率100%,耐药参考品符合率100%,检测限参考品S、SI、SID及精密度参考品J(1×10
本发明提供的核酸组合物、试剂以及试剂盒适用于人痰液、肺泡灌洗液或液体分离培养物等不同样本的检测,可在3小时内快速鉴定疑似或确诊结核病患者样本中的结核分枝杆菌异烟肼耐药的情况,为疑似或确诊结核分枝杆菌感染的患者提供了更为方便快捷的辅助诊疗依据。
附图说明
为了更清楚地说明本发明实施例的技术方案,下面将对实施例中所需要使用的附图作简单地介绍,应当理解,以下附图仅示出了本发明的某些实施例,因此不应被看作是对范围的限定,对于本领域普通技术人员来讲,在不付出创造性劳动的前提下,还可以根据这些附图获得其他相关的附图。
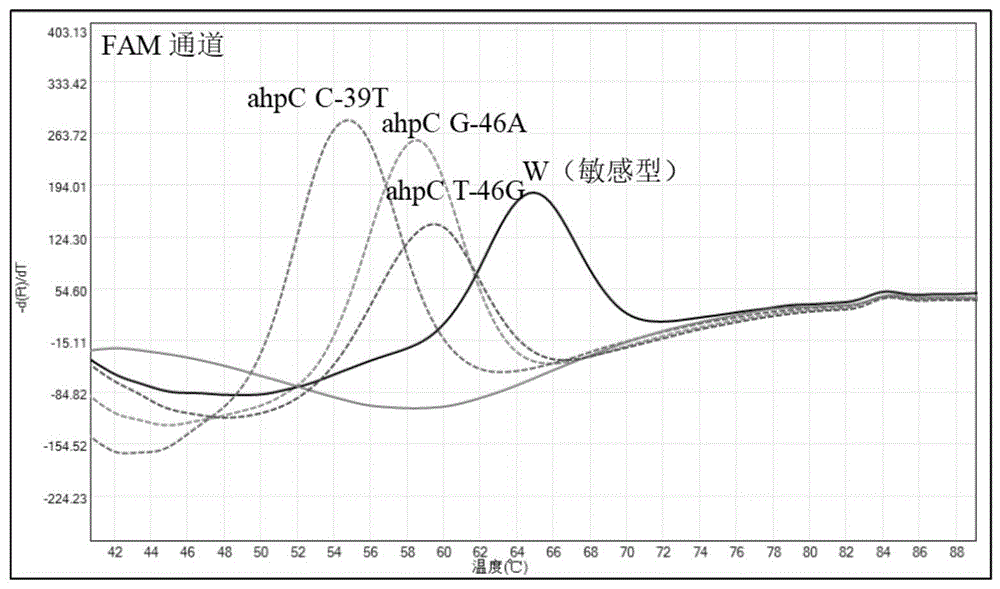
图1为结核分枝杆菌异烟肼耐药检测FAM通道典型曲线图;
图2为结核分枝杆菌异烟肼耐药检测HEX通道典型曲线图;
图3为结核分枝杆菌异烟肼耐药检测ROX通道典型曲线图;
图4为结核分枝杆菌异烟肼耐药检测CY5通道典型曲线图;
图5为本发明KatG基因普通探针检测结果;
图6为本发明KatG基因锁核酸修饰探针检测结果;
图7为本发明InhA基因普通探针检测结果;
图8为本发明InhA基因锁核酸修饰探针检测结果;
图9为本发明试剂对异烟肼耐药国家参考品盘耐药参考品检测结果图(FAM通道);
图10为本发明试剂对异烟肼耐药国家参考品盘耐药参考品检测结果图(HEX通道);
图11为本发明试剂对利福平耐药国家参考品盘耐药参考品检测结果图(ROX通道);
图12为本发明试剂对利福平耐药国家参考品盘耐药参考品检测结果图(CY5通道)。
具体实施方式
现将详细地提供本发明实施方式的参考,其一个或多个实例描述于下文。提供每一实例作为解释而非限制本发明。实际上,对本领域技术人员而言,显而易见的是,可以对本发明进行多种修改和变化而不背离本发明的范围或精神。例如,作为一个实施方式的部分而说明或描述的特征可以用于另一实施方式中,来产生更进一步的实施方式。
除非另外指明,否则实践本发明将采用细胞生物学、分子生物学(包含重组技术)、微生物学、生物化学和免疫学的常规技术,所述常规技术在本领域技术人员的能力范围内。文献中充分解释了这种技术,如《分子克隆:实验室手册(Molecular Cloning:ALaboratory Manual)》,第二版(Sambrook等人,1989);《寡核苷酸合成(OligonucleotideSynthesis)》(M.J.Gait编,1984);《动物细胞培养(Animal Cell Culture)》(R.I.Freshney编,1987);《酶学方法(Methods in Enzymology)》(学术出版社有限公司(Academic Press,Inc.);《实验免疫学手册(Handbook of Experimental Immunology)》(D.M.Weir和C.C.Blackwell编);《哺乳动物细胞用基因转移载体(Gene Transfer Vectors forMammalian Cells)》(J.M.Miller和M.P.Calos编,1987);《当代分子生物学方法(CurrentProtocols in Molecular Biology)》(F.M.Ausubel等人编,1987);《PCR:聚合酶链反应(PCR:The Polymerase Chain Reaction)》(Mullis等人编,1994);以及《当代免疫学方法(Current Protocols in Immunology)》(J.E.Coligan等人编,1991),所述文献中的每个文献均通过引用明确并入本文中。
第一方面,本发明提供了一种用于检测结核分枝杆菌异烟肼耐药基因突变的核酸组合物,其包括:核苷酸序列如SEQ ID No.1~2所示的第一引物对,核苷酸序列如SEQ IDNo.3~4所示的第二引物对,核苷酸序列如SEQ ID No.5~6所示的第三引物对。
本发明提供的引物对覆盖了异烟肼类药物耐基因KatG、ahpC和InhA的九种突变位点:KatG S315T、KatG S315N、ahpC C-6A、ahpC C-12T、ahpC C-39T、ahpC G-46A、ahpC T-49G、InhAT-8C、InhA C-15T。相对于现有的其他引物组合而言,本发明的引物对具有更好的检测特异性和灵敏度。
具体地,第一引物对覆盖异烟肼物耐基因KatG,检测的突变位点包括:KatGS315T、KatG S315N。
第二引物对覆盖异烟肼物耐基因ahpC,检测的突变位点包括:ahpC C-6A、ahpC C-12T、ahpC C-39T、ahpC G-46A、ahpC T-49G。
第三引物对覆盖异烟肼物耐基因InhA,检测的突变位点包括InhA T-8C、InhA C-15T。
在本发明应用较佳的实施方式中,核酸组合物还包括探针,探针包括如SEQ IDNo.7所示的第一探针、如SEQ ID No.8所示的第二探针、如SEQ ID No.9所示的第三探针和如SEQ ID No.10所示的第四探针;
在一种可选的实施方式中,第一探针用于检测KatG S315T和KatG S315N突变;第二探针用于检测ahpC C-6A和ahpC C-12T突变;第三探针用于检测ahpC C-39T、ahpC G-46A和ahpC T-49G突变;第四探针用于检测InhAT-8C和InhA C-15T突变。
在一种可选的实施方式中,第一探针、第二探针、第三探针和第四探针中的至少一个探针含有至少一个修饰的核苷酸基团。
通过设置探针含有至少一个修饰的核苷酸基团,从而改善探针的稳定性和活性,修饰的核苷酸基团不会导致探针的功能丧失。
在一种可选的实施方式中,修饰的核苷酸基团为(1)~(3)中的至少一种:
(1)磷酸基团修饰的核苷酸基团;
(2)核糖基团修饰的核苷酸基团。
在一种可选的实施方式中,磷酸基团修饰是对磷酸基团中的氧进行修饰,包括硫代修饰和硼烷化修饰;
在一种可选的实施方式中,核糖基团修饰是对核糖基团中2’-羟基进行修饰,选自如下修饰中的任意一种:2’-氟修饰、2’-甲氧基修饰、2’-甲氧乙基修饰、2’-2,4-二硝基苯酚修饰、锁核酸修饰、2’-氨基修饰和2’-脱氧修饰;
在一种可选的实施方式中,核糖基团修饰是对核糖基团中2’-羟基进行锁核酸修饰。探针序列采用锁核酸修饰,能够更好地区分错配。采用锁核酸修饰的探针,对SNP的区分能力更强,荧光背景低。
在一种可选的实施方式中,第一探针的核苷酸序列中第10位碱基G为锁核酸修饰碱基;第四探针的核苷酸序列中第19位碱基T为锁核酸修饰碱基。
在本发明应用较佳的实施方式中,探针的5’设有荧光报告基团,3’设有荧光淬灭基团和/或MGB。
在一种可选的实施方式中,荧光报告基团包括不限于:5-FAM、6-FAM、HEX、TET、VIC、JOE、Cy3、Cy3.5、NED、TAMRA、ROX、Texas Red、Cy5、Cy5.5和Quasar670中的任意一种。
在一种可选的实施方式中,荧光淬灭基团包括不限于:TAMRA、Eclipse、BHQ系列、Dabcyl、Lowa BlackTM RQ和Lowa BlackTM FQ中的至少一种;
在一种可选的实施方式中,BHQ系列包括不限于BHQ0、BHQ1、BHQ2和BHQ3中的至少一种。
在本发明应用较佳的实施方式中,在第一引物对、第二引物对和第三引物对中的任意一对引物对中,上游引物和下游引物的摩尔比独立地为(1~10):(1~10)。
例如该摩尔比可以为1:1、1:5、1:10、1:15、1:20中的任意一种或任意两种之间的范围;
或者该摩尔比可以为5:1、10:1、15:1、20:1中的任意一种或任意两种之间的范围。
在一种可选的实施方式中,上游引物和下游引物的摩尔比独立地为1:(1~20)。
在一种可选的实施方式中,第一引物对中上游引物和下游引物的摩尔比独立地为1:(1~20);第二引物对中上游引物和下游引物的摩尔比独立地为1:(1~20);第三引物对中上游引物和下游引物的摩尔比独立地为1:(1~20)。
此外,本领域的技术人员可以根据需要进行调整摩尔比,并不限于上述的情形。
在一种可选的实施方式中,核酸组合物中第一探针、第二探针、第三探针和第四探针的浓度独立地为0.01~1μM,具体可以为0.01μM、0.1μM、0.2μM、0.5μM、1μM、1.5μM、2μM、2.5μM、3μM、3.5μM、4μM、4.5μM、5μM中的任意一种或任意两种之间的范围;优选为0.05~1μM。优选为0.1~0.5μM。
需要说明的是,上述核酸组合物包括不限于:第一引物对、第二引物对、第三引物对、第一探针、第二探针、第三探针和第四探针分别单独设置,并将单独设置的各引物对和探针组合为一个产品;或者将第一引物对、第二引物对、第三引物对中的至少两种组合设置(如包装),第一探针、第二探针、第三探针和第四探针中的至少两种组合设置;或者将所有的引物对和探针混合设置。
第二方面,本发明还提供了一种试剂或试剂盒,其包括上述的核酸组合物。
在本发明应用较佳的实施方式中,试剂或试剂盒还包括如下物质中的至少一种:PCR反应缓冲液、DNA聚合酶、镁离子、dNTP、野生型对照、阴性对照和水。
野生对照为:KatG、ahpC和InhA三基因质粒的TE溶液。
阴性对照为:TE溶液。
在一种可选的实施方式中,DNA聚合酶选自Tth DNA聚合酶或其突变体、Taq DNA聚合酶或其突变体、Pfu酶或其突变体和Hawk Z05聚合酶或其突变体中的至少一种;
DNA聚合酶的浓度为0.01U/μl~5U/μl。
在一些实施例中,DNA聚合酶的作用浓度(也即工作浓度)为0.01U、0.015U、0.02U、0.025U、0.03U、0.035U、0.04U、0.045U、0.05U、0.055U、0.06U、0.065U、0.07U、0.075U、0.08U、0.085U、0.09U、0.095U、0.1U、0.2U、0.3U、0.4U、0.5U、0.6U、0.7U、0.8U、0.9U和1U中的任意一种或任意两种之间的范围。
镁离子的浓度为0.5mM~1.5mM;
dNTP的(试剂盒以及试剂中)浓度为0.1mM-25mM;
在一些实施例中,进行PCR检测时,dNTP的作用浓度为0.1~5mM,具体可以为0.1mM、0.5mM、1mM、1.5mM、2mM、2.5mM、3mM、3.5mM、4mM、4.5mM和5mM中的任意一种或任意两种之间的范围。
第一引物对、第二引物对和第三引物对中的任意一对引物对中,上游引物和下游引物的浓度为0.1μmol/L~5μmol/L;
具体可以为0.01μM、0.1μM、0.2μM、0.5μM、1μM、1.5μM、2μM、2.5μM、3μM、3.5μM、4μM、4.5μM、5μM中的任意一种或任意两种之间的范围;优选为0.05~1μM。
在第一引物对、第二引物对和第三引物对中的任意一对引物对中,上游引物和下游引物的摩尔比独立地为(1~20):(1~20)。
例如该摩尔比可以为1:1、1:2、1:3、1:4、1:5、1:6、1:7、1:8、1:9和1:10中的任意一种或任意两种之间的范围;
或者该摩尔比可以为2:1、3:1、4:1、5:1、6:1、7:1、8:1、9:1、10:1中的任意一种或任意两种之间的范围。
在一种可选的实施方式中,上游引物和下游引物的摩尔比独立地为1:(1~20)。
在一种可选的实施方式中,第一引物对中上游引物和下游引物的摩尔比独立地为1:(1~20);第二引物对中上游引物和下游引物的摩尔比独立地为1:(1~20);第三引物对中上游引物和下游引物的摩尔比独立地为1:(1~20)。
第三方面,本发明还提供了核酸组合物在制备结核分枝杆菌异烟肼耐药基因突变的检测产品中的应用;
在一种可选的实施方式中,检测产品选自试剂、试剂盒和基因芯片中的任一种。
第四方面,本发明还提供了一种结核分枝杆菌异烟肼耐药基因突变的检测方法,其包括:采用上述的核酸组合物或上述的试剂或试剂盒对待测样本进行PCR检测;
检测方法不以疾病的诊断或治疗为目的;
在一种可选的实施方式中,待测样本选自核酸样本、含核酸样本的环境样本、阴性对照、阳性对照、人痰液、痰固体分离物及其培养物和液体分离物及其培养物中的至少一种。
在本发明应用较佳的实施方式中,进行PCR检测时,在第一引物对、第二引物对和第三引物对中的任意一对引物对中,上游引物和下游引物的摩尔比独立地为(1~20):(1~20);
例如该摩尔比可以为1:1、1:5、1:10、1:15和1:20中的任意一种或任意两种之间的范围;
或者该摩尔比可以为5:1、10:1、15:1和20:1中的任意一种或任意两种之间的范围。
在一种可选的实施方式中,上游引物和下游引物的摩尔比独立地为1:(1~20)。
在一种可选的实施方式中,第一引物对中上游引物和下游引物的摩尔比独立地为1:(1~20);第二引物对中上游引物和下游引物的摩尔比独立地为1:(1~20);第三引物对中上游引物和下游引物的摩尔比独立地为1:(1~20)。
在一种可选的实施方式中,进行PCR检测时,第一引物对、第二引物对和第三引物对中的任意一对引物对中,上游引物和下游引物的工作浓度独立地为0.01~5μM,优选为0.1~1μM;
具体可以为0.01μM、0.1μM、0.2μM、0.5μM、1μM、1.5μM、2μM、2.5μM、3μM、3.5μM、4μM、4.5μM、5μM中的任意一种或任意两种之间的范围;优选为0.05~1μM。
在一种可选的实施方式中,进行PCR检测时,第一探针、第二探针、第三探针和第四探针的浓度独立地为0.01~1μM,具体可以为0.01μM、0.1μM、0.2μM、0.5μM、1μM、1.5μM、2μM、2.5μM、3μM、3.5μM、4μM、4.5μM、5μM中的任意一种或任意两种之间的范围;优选为0.05~1μM。优选为0.1~0.5μM。
本发明通过对结核分枝杆菌异烟肼耐药决定区KatG基因、InhA基因和ahpC基因的保守序列进行分析,设计出可针对异烟肼耐药基因突变检测的引物探针组合,采用多重不对称PCR、Taqman探针熔解技术在一个反应体系中同时检测包含异烟肼耐药决定区KatG基因、InhA基因和ahpC基因的KatG S315T、KatG S315N、ahpC C-6A、ahpC C-12T、ahpC C-39T、ahpC G-46A、ahpC T-49G、InhA T-8C、InhA C-15T等九种耐药突变位点的PCR反应体系,检测灵敏度可达10000CFU/mL,具有检测特异性高,灵敏度强等优势,且结果判定便利、直观,可低成本实现耐药性和耐药基因突变的快速检测,适用范围广泛。
在一种可选的实施方式中,PCR的反应程序如下:94~96℃15sec~10min;94~98℃10~30s,55~65℃,20~40s,70~74℃20~30s,30~50个循环;55~56℃20~40s处收集荧光信号;94~96℃1~3min,33~37℃1~3min;35~90℃,按照每0.04℃/s的升温速度,持续收集荧光信号。
通过比较所检测样品与野生对照之间熔解曲线熔点(Tm)的差异,判断样品是否发生突变;当检测样品的熔点与野生对照的熔点差值ΔTm≤±1℃时判定为野生型;多个通道中任一通道中检测样品的熔点与野生对照熔点差值ΔTm≥±2℃时判定为耐药突变型,再根据相应通道与野生型熔点的差值,判断具体耐药突变位点信息。
第五方面,本发明还提供了用于结核分枝杆菌异烟肼耐药基因突变检测的系统,其包括:上述的试剂或试剂盒、第一装置和第二装置;第一装置能够采用试剂或试剂盒对待测DNA样本、野生型对照及阴性对照分别进行实时荧光定量PCR检测,获得熔解曲线图;
第二装置包括:数据输入模块、数据分析与结论输出模块;
数据输入模块被配置为输入第一装置所得的熔解曲线图数据;数据分析与结论输出模块被配置为:根据待测样本与野生型对照在各通道熔解峰的Tm差值的变化判读待测样本是否含有基因突变和确定基因突变的类型。
为使本发明实施例的目的、技术方案和优点更加清楚,下面将对本发明实施例中的技术方案进行清楚、完整地描述。实施例中未注明具体条件者,按照常规条件或制造商建议的条件进行。所用试剂或仪器未注明生产厂商者,均为可以通过市售购买获得的常规产品。
以下结合实施例对本发明的特征和性能作进一步的详细描述。
实施例1
使用NCBI数据库搜索相关基因序列,根据结核分枝杆菌异烟肼耐药决定区KatG基因、InhA基因和ahpC基因设计引物探针,在突变点外围进行引物的设计,在突变点处进行探针序列的设计,利用软件Oligo 7设计引物和探针。探针采用荧光报告基团和荧光淬灭基团修饰。各个突变位点的扩增引物优选组合序列见表1,优选探针序列见表2。
表1本发明的引物序列
备注:F为上游引物,R为下游引物。
表2本发明的探针序列
备注:带有下划线的碱基为锁核酸修饰碱基,针对其他的碱基进行修饰则达不到预期的检测效果。
锁核酸是一种双环状核酸衍生物,核糖的2’-O位和4’-C位通过缩水作用形成氧亚甲基桥,并连接成环形,这个环形桥锁定了呋喃糖C3内型的N构型,降低了核糖结构的柔韧性,增加了磷酸盐骨架局部结构的稳定性。锁核酸具有序列特异性,它比常规的核酸能更好地区分正确配对和错误配对序列,含有错配碱基的LNA-DNA杂交分子比含有错配碱基的DNA-DNA杂交分子更加不稳定,因而Tm值下降更为显著。本发明采用锁核酸对那些野生和突变型区分能力弱的探针进行修饰,从而达到对单碱基错配的识别能力。
实施例2
本实施例提供了一种结核分枝杆菌异烟肼耐药基因突变的检测试剂,具体包括如下的引物:Primer-F1、Primer-R1、Primer-F2、Primer-R2、Primer-F3、Primer-R3;探针:Probe-P1、Probe-P2、Probe-P3、Probe-P4;PCR反应缓冲液;脱氧核糖核苷三磷酸;Taq DNA聚合酶。
引物和探针的组合如下所示。
PCR反应液包含:PCR反应缓冲液,0.1mmol/L~5mmol/L脱氧核糖核苷三磷酸,靶标基因的上游引物以及下游引物0.1μmol/L~5μmol/L,引物比例为1:(1~20)或(1~20):1,靶标基因的探针0.1μmol/L~5μmol/L,0.01U~1U/μl Taq DNA聚合酶。具体试剂配制如下表所示:
/>
引物、探针的筛选和体系优化是本发明的重点,由于采用多重不对称PCR且还包含了多条探针,多重PCR及易产生各目的片段的相互抑制,而探针之间及探针与引物之间如果形成复杂的二级结构也会影响后续熔解曲线的结果,直接造成没有熔解峰出现。发明人经过大量摸索实验,最终优化出上述的反应体系。
本实施例提供的试剂组合可单管单体系检测KatG基因、ahpC基因和InhA基因的九种突变位点:KatG S315T、KatG S315N、ahpC C-6A、ahpC C-12T、ahpC C-39T、ahpC G-46A、ahpC T-49G、InhA T-8C、InhAC-15T。
实施例3
本实施例提供了一种结核分枝杆菌异烟肼耐药基因突变的检测方法,其包括以下步骤。
1.样本采集:痰液、结核分枝杆菌分离培养物。
2.样本前处理:
2.1痰液处理方式:样本和液化液1:1混合进行液化,直到样品达到所需的流动性。取200μL液化液用于后续核酸提取。
2.2临床分离培养物处理方式:固体培养基上生长的结核分枝杆菌,用22SWG标准接种环收集细菌1环,并重悬于400μL TB DNA提取液中。液体培养基中生长的结核分枝杆菌取1mL,12000rpm离心15min,丢弃上清,沉淀物重悬于200μL TB DNA提取液中,用于后续核酸提取。
2.3肺泡灌洗液处理方式:取1~5ml肺泡灌洗液,以10000rpm离心1分钟,弃上清,沉淀物重悬于200μL TB DNA提取液中用于后续核酸提取。
3.样本核酸提取:
可使用商业化核酸DNA提取试剂盒(如Qiagen DNAMini Kit等),提取过程应按照商业试剂盒的说明书进行操作。PCR扩增前,可采用核酸定量仪或紫外分光光度计对模板DNA浓度和纯度进行测定。
4.试剂加样:
4.1按照实施例2配置的检测试剂,取10μL的PCR试剂加入到PCR管中;
4.2取10μL提取的核酸加入到PCR扩增体系中,混匀,盖上PCR管盖子,待上机。
5.PCR扩增程序设置及运行:
5.1在荧光定量PCR仪器如Roche LightCycler 480,SLAN-96P等上进行PCR扩增。
5.2打开仪器,放入待检测的PCR管。
5.3设置扩增程序。选择相应的荧光通道FAM通道(Reporter:FAM,Quencher:None)、HEX通道(Reporter:HEX,Quencher:None)、ROX通道(Reporter:ROX,Quencher:None)、CY5通道(Reporter:CY5,Quencher:None)。进行样本编辑。
5.4运行扩增程序。
6.结果分析:
6.1反应结束后,仪器自动保存结果,可以利用仪器自带的软件进行自动分析。
6.2通过比较所检测样品与野生对照(未突变的KatG、ahpC、InhA基因质粒混合溶液,等同于阳性对照,即质控品)之间熔解曲线熔点(Tm)的差异,判断样品是否发生突变;当检测样品的熔点与野生对照的熔点差值ΔTm(Tm
7.结果判读:
检测结果各通道典型峰图见图1~4,突变型样本在各通道中的熔点差异值(ΔTm)可参照下表:
注:“-”表示无值;
实施例4
本实施例提供了锁核酸修饰探针和无锁核酸修饰探针使用效果的比较实施例。
分别设计针对KatG基因和InhA基因的普通探针和锁核酸修饰探针,锁核酸修饰的探针核酸序列分别为SEQ ID NO.7和SEQ ID NO.10。SEQ ID NO.7的第10位碱基G为锁核酸修饰碱基;SEQ ID NO.10中第19位碱基T为锁核酸修饰碱基。普通探针的核酸序列与锁核酸修饰的一致。
采用实施例3的方法对野生型和KatG S315T、KatG S315N、InhA T-8C、InhA C-15T突变位点进行检测。
检测结果显示,KatG基因检测探针用锁核酸修饰后,突变型熔点差值(ΔTm)与未修饰的普通探针相近,检测结果如图5和图6所示;InhA基因检测探针采用锁核酸修饰后,突变型与野生型熔点差值增大,即锁核酸修饰探针检测效果均优于普通探针的。检测结果如下表所示,溶解曲线如附图7和图8所示。
注:“-”表示无值;
实施例5
采用本发明实施例2的检测试剂对结核分枝杆菌异烟肼耐药基因国家参考品盘进行检测。
使用本发明的试剂检测结核分枝杆菌异烟肼耐药国家参考品盘,敏感参考品符合率100%,耐药参考品符合率100%,检测限参考品S、SI、SID及精密度参考品J(1×10
/>
实施例6
临床样本进行异烟肼耐药基因突变核酸检测的临床应用实例。
在成都市简阳市人民医院收集疑似结核感染患者的痰液样本和分离培养物共计139例,其中确认结核分枝杆菌阳性痰液样本84例。使用本发明试剂对上述84例结核分枝杆菌阳性样本进行检测,其中存在异烟肼耐药突变阳性结果5例,异烟肼敏感型样本结果79例。5例在异烟肼耐药突变位点的样本经一代测序确认正确。
以上结果显示,本发明的结核分枝杆菌异烟肼耐药的试剂及试剂盒和方法在检测临床样本时展示出了良好的临床应用效果。
以上所述仅为本发明的优选实施例而已,并不用于限制本发明,对于本领域的技术人员来说,本发明可以有各种更改和变化。凡在本发明的精神和原则之内,所作的任何修改、等同替换、改进等,均应包含在本发明的保护范围之内。
- 一种同时检测结核分枝杆菌利福平与异烟肼耐药基因点突变的方法及其试剂盒
- 检测腹泻病毒的核酸组合物、试剂盒及试剂盒的使用方法
- 同时检测四种肠道病毒的核酸组合物及试剂盒和检测方法
- 一种检测结核分枝杆菌异烟肼耐药基因突变的方法及试剂盒
- 一种检测结核分支杆菌耐药基因的核酸组合物、试剂盒及检测结核分支杆菌耐药性的方法
