一种预防带状疱疹复发的分子Prmt6的作用、实施方法及用途
文献发布时间:2024-04-18 19:58:53
技术领域
本发明涉及生物医药技术领域,具体地说,是一种预防带状疱疹复发的分子Prmt6通过调控带状疱疹抗病毒免疫从而预防其复发过程中的效应、作用机制、实施方法和用途。
背景技术
带状疱疹是由于水痘-带状疱疹病毒(varicella zoster virus,VZV)感染人体后通过神经末梢逆向进入神经节或脊髓等部位,在免疫力正常状态下进入休眠状态潜伏起来。当年龄增长、感染等各种因素造成人体免疫力下降时,VZV可再次活化并大量复制通过神经轴突感染神经元,引起神经支配区域出现水疱样皮疹和疼痛,从而出现带状疱疹复发。对于免疫力降低的老年患者,若不及时干预治疗带状疱疹可复发引起后遗神经痛,对患者造成了严重的生理、心理和经济负担。
疱疹病毒是一类种类多样、结构相近的广泛感染人类和动物的病原体,其主要组成包括囊膜、皮层、衣壳、核心等。VZV,即人类疱疹病毒3,基因组包含双链DNA,在感染细胞后进入宿主基因组利用宿主营养物质进行复制和组装,从而大量繁殖并释放到细胞外。VZV以人为天然唯一宿主,初次感染后引起水痘,复发后诱发带状疱疹,并无动物宿主,而I型单纯疱疹病毒(Herpes simplex virus type 1,HSV-1)同VZV具有高度同源性及相似的生物学特征,目前关于带状疱疹的研究主要采用HSV-1创建动物模型。
在正常状态下病毒感染进入人体后可激活体内的天然免疫系统,这是机体抵抗微生物入侵的第一道防线。病毒的蛋白质、脂类、糖类、遗传物质进入人体后成为病原相关分子模式(pathogen-associated molecular patterns,PAMPs),与人体的组成成分差别显著,可被体内免疫细胞上的模式识别受体(pattern recognition receptors,PRRs)所识别,诱发免疫细胞产生级联反应,促进炎症反应和干扰素(interferon,IFN)的产生从而增强细胞的抗病毒免疫,以消除病毒对组织细胞的损伤。病毒感染时,PRRs可识别出病原体的衣壳或核酸成分,启动核内I型干扰素(Type I interferon,IFN-I)的合成与释放,从而快速清除病毒。对于DNA病毒感染,细胞内的DNA识别受体如干扰素γ诱导蛋白16(interferongamma-inducible protein 16,IFI16)、DEAD盒型螺旋酶41(DEAD-box helicase 41,DDX41)、环化GMP-AMP合酶(cyclic GMP-AMP Synthase,cGAS)可敏锐识别“异己”的DAN分子并与其相结合,增加第二信使环化GMP-AMP(cyclic GMP-AMP,cGAMP)的合成并活化干扰素基因刺激蛋白(stimulator of interferon genes,STING),促进IFN-I的转录和翻译。无论是RNA病毒还是DNA病毒感染,PRRs识别病原体核酸后通过相应的接头分子均可进一步募集TANK结合激酶-1(TANK binding kinase-1,TBK1)并使其磷酸化,促进转录因子如干扰素调节因子-3(interferon regulatory factor 3,IRF3)及核因子κB(nuclear factor kappa-B,NF-κB)的入核和磷酸化,进而促进干扰素和促炎因子转录以增强抗病毒免疫和炎症反应,利于病原体的清除。VZV感染人体后,主要通过cGAS-STING通路介导免疫细胞的抗病毒免疫发挥功能,若免疫细胞的cGAS-STING通路被抑制或VZV病毒某些组分帮助病毒逃脱cGAS的识别,则会导致VZV病毒无法及时清除而出现潜伏感染。正常条件下,cGAS可感受受损线粒体DNA或VZV的DNA并与其结合形成多聚复合物导致cGAS自身活化,通过促进cGAMP的合成介导下游信号通路。STING分子是稳定存在于内质网上的跨膜蛋白,当与cGAMP结合后发生磷酸化和空间结构改变,并向临近高尔基体转移以募集并活化TBK1,刺激IRF3入核、磷酸化、二聚化从而促进干扰素的合成和分泌。
小胶质细胞是中枢神经系统内最重要的免疫细胞,也是中枢神经炎症反应的主要效应细胞,对病原微生物感染和微环境的变化极为敏感,能够激活炎症小体、NF-κB等炎症信号通路。在静息状态下,小胶质细胞会随时感受细胞周围微环境变化,当有致伤因子存在时小胶质细胞活化并诱发一系列的应激反应,促炎因子的转录和释放增加,诱导其向M1型极化并进一步增加促炎因子的表达。VZV感染神经元后大量复制并释放进入细胞微环境,同时神经元出现泛细胞死亡产生的细胞碎片导致微环境改变,小胶质细胞内的PRRs可快速感知HSV-1病毒的PAMPs并启动细胞内的抗病毒免疫,此过程主要通过cGAS-STING通路介导的IFN-I的大量合成发挥效应。正常免疫条件下小胶质细胞cGAS-STING通路介导的抗病毒免疫可快速清除病毒,当小胶质细胞稳态失调时IFN-I的产生能力下降,此时病毒不能被及时清除导致神经元大量感染,可进入神经元潜伏起来,造成潜伏感染,是引起带状疱疹复发的潜在机制。外周神经系统发挥抗病毒和促炎反应效应的细胞主要是T细胞和巨噬细胞,中枢神经系统介导抗病毒和促炎反应的效应细胞主要是小胶质细胞。效应细胞在识别PAMPs后通过调节干扰素、促炎因子、趋化因子等小分子物质参与免疫反应,其中IFN-I可杀灭病毒,促炎因子如肿瘤坏死因子α(tumor necrosis factorα,TNF-α)、白细胞介素1β(interleukin-1β,IL-1β)、IL-6、IL-17、IL-18参与炎症级联反应,抗炎因子如IL-4、IL-10、转化生长因子β(transforming growth factorβ,TGF-β)等可在病原体清除后及时终止炎症反应以避免损伤自身组织细胞。关于带状疱疹的临床研究证实带状疱疹复发患者血清中TNF-α、IL-1β、IL-6等促炎因子同正常人群显著增高,提示VZV诱发的带状疱疹复发同外周神经炎症具有较强的相关性。细胞实验同样提示VZV能够显著促进培养的巨噬细胞释放促炎因子TNF-α、IL-1β、IL-6等,动物实验也证明了VZV感染动物后可显著增加脊髓和DRG区域促炎因子的水平,此与带状疱疹复发密切相关。
蛋白精氨酸甲基转移酶(protein arginine methyl transferases,Prmts)是一类广泛存于细胞内的调控蛋白质甲基化修饰的酶类,通过将S腺苷甲硫氨酸(Sadenosinemethionine,SAM)基团上的甲基转移至靶蛋白精氨酸残基上的胍基氮原子上,调控靶蛋白的生物学活性从而参与体内的生理活动。Prmts家族主要参与调控体内蛋白转录翻译、遗传物质的损伤修复、细胞凋亡、mRNA合成及修饰、增殖分化及抗病毒免疫等,且与癌症的进程密切相关。作为甲基转移酶家族的典型代表,Prmt6具有较强的精氨酸甲基转移活性,主要通过对富含甘氨酸和精氨酸的结构域(arginine glycine rich motif,RGG)进行甲基化修饰改蛋白质的生物学活性,例如能够对靶蛋白中组蛋白H3的第2个精氨酸残基及组蛋白H2A第29个精氨酸残基进行甲基化修饰形成ADMA,以改变靶蛋白的活性并影响下游信号分子的功能或特定基因的转录翻译水平。Prmt6还可对其他表观遗传修饰蛋白进行甲基化修饰改变其活性,如能够对去乙酰化酶7(sirtuin 7,Sirt 7)精氨酸进行甲基化从而导致其乙酰化能力降低,对雌激素受体1/2(estrogen receptors 1/2,ESR1/2)、孕激素受体(progesterone receptor,PGR)及糖皮质激素受体(Glucocorticoid receptor,NR3C1)等相关转录因子进行甲基化修饰调节相关激素的合成,Prmt6活性基团甚至可对自身的RGG区域进行甲基化修饰从而调节自身催化活性。在炎症反应进程中,Prmt6可对p65、NF-κB通路关键蛋白进行甲基化修饰,调控促炎基因和抗炎基因的转录水平,维持细胞炎症应激能力的稳态。已有研究证实,Prmt6可通过调控TBK1-IRF3复合体活性调节天然抗病毒免疫功能,但关于Prmt6在调控带状疱疹复发中的作用及其分子机制目前仍没有报道。
综上所述,本领域迫切需要开发出一种可有效预防和治疗带状疱疹复发的分子靶点。
发明内容
本发明的目的在于探索调控小胶质细胞抗病毒免疫并预防和治疗带状疱疹复发的关键分子靶点及其潜在的临床转化用途,提供一种预防带状疱疹复发的分子Prmt6的作用、实施方法及用途。
本发明的第一方面,提供Prmt6蛋白或其编码序列在制备预防和/或治疗带状疱疹复发的药物中的应用。
进一步地,所述的预防和/或治疗带状疱疹复发的药物以Prmt6蛋白或其编码序列作为干预靶点。
进一步地,所述的预防和/或治疗带状疱疹复发的药物靶向抑制Prmt6的表达和功能。
本发明的第二方面,提供抑制Prmt6的表达和功能的试剂在制备预防和/或治疗带状疱疹复发的药物中的应用。
进一步地,所述的抑制Prmt6的表达和功能的试剂是指任何可降低Prmt6的活性、降低Prmt6的稳定性、抑制Prmt6的表达、减少Prmt6的有效作用时间、或抑制Prmt6的转录和加工的物质等。
进一步的,所述的抑制Prmt6的表达和功能的试剂包括但不限于:
特异性结合Prmt6的蛋白;
特异性干扰Prmt6基因表达、加工的小干扰分子,如siRNA分子、miRNA分子、反义核苷酸等;
Prmt6拮抗剂、下调剂、阻滞剂、阻断剂等。
进一步地,所述的应用中,抑制Prmt6的表达和功能的试剂增强抗病毒免疫,清除病毒及其诱发的神经炎症状态,减轻炎症和泛细胞死亡状态。
本发明的第三方面,提供一种预防和/或治疗带状疱疹复发的药物,所述的预防和/或治疗带状疱疹复发的药物中包含抑制Prmt6的表达和功能的试剂。
进一步地,所述的预防和/或治疗带状疱疹复发的药物中还包括其他药学上可接受的成分。
进一步地,所述的其他药学上可接受的成分是与抑制Prmt6的表达和功能的试剂没有拮抗作用的药物,或药学上允许的一种或多种辅料。
本发明优点在于:
本发明提供了Prmt6蛋白或其编码序列在有效预防和治疗带状疱疹复发病理进程中的新用途,采用靶向干预脊髓背角小胶质细胞Prmt6的蛋白表达,可有效预防和治疗带状疱疹复发。
发明人通过大量的研究和动物模型试验,发现Prmt6在带状疱疹复发疾病模型中表达增加,并且其高表达能够抑制小胶质细胞的抗病毒免疫,导致病毒载量增加,引起病毒相关性神经炎症和神经损伤,促进带状疱疹复发,靶向干预小胶质细胞的Prmt6表达和功能能够有效促进抗病毒免疫和清除病毒及其诱发的神经炎症状态。在此基础上完成了本发明。
具体而言,针对影响带状疱疹复发进程中小胶质细胞抗病毒免疫能力的相关基因进行应用研究是分子生物学和细胞生物学研究的热点,通过靶向干预目标分子促进病毒清除的基因的核苷酸和蛋白质应用于带状疱疹复发的预防和治疗是有效的技术,因此无论是在功能基因组研究,还是相关地基因治疗方面均具有广阔地应用前景。
发明人通过研究发现:小胶质细胞的Prmt6在带状疱疹复发过程中发挥重要作用,Prmt6缺陷显著增强带状疱疹复发模型小鼠的抗病毒免疫,清除病毒能力增强导致病毒载量减少,病毒相关性神经炎症和神经损伤减少。在HSV-1刺激体外培养的小胶质细胞抗病毒免疫中,观察到Prmt6敲减能够增强体外培养的小胶质细胞抗病毒能力并降低病毒载量,减轻炎症和泛细胞死亡状态,而Prmt6过表达能够减弱体外培养的小胶质细胞抗病毒能力并增加病毒载量,加重炎症和泛细胞死亡状态。这些发现提示Prmt6可能具备通过调控小胶质细胞抗病毒免疫能力预防和治疗带状疱疹复发的应用前景。由此,本发明提供了将Prmt6分子应用于带状疱疹复发的预防和治疗中的方法和策略。
本发明针对具有调控抗病毒免疫能力的新型分子Prmt6,对小胶质细胞中HSV-1病毒清除的效应进行了研究,并且验证了敲除该分子的序列对带状疱疹复发模型小鼠的治疗和保护作用。实验证明:1、小胶质细胞中Prmt6在带状疱疹复发病理进程中发挥重要作用。2、Prmt6缺陷增强带状疱疹复发模型小鼠抗病毒免疫。3、Prmt6缺陷降低HSV-1病毒载量并减轻病毒相关性神经炎症和神经损伤。4、Prmt6敲减能够增强体外培养的小胶质细胞抗病毒能力并降低病毒载量,减轻炎症和泛细胞死亡状态。5、Prmt6过表达能够减弱体外培养的小胶质细胞抗病毒能力并增加病毒载量,加重炎症和泛细胞死亡状态。6、Prmt6抑制小胶质细胞抗病毒免疫依赖其甲基转移酶功能。
本发明针对Prmt6基因的不同的核苷酸和蛋白质产物,用以调控小胶质细胞清除病毒,提高小鼠的抗病毒免疫能力,从而预防和治疗带状疱疹复发。这些发明证实Prmt6的相关产物可望成为治疗和预防带状疱疹复发的有效手段。
本发明揭示了Prmt6及其编码序列的新功能,即抑制带状疱疹复发病理进程中机体对疱疹病毒的抗病毒免疫能力,靶向抑制Prmt6的表达和功能可有效预防和治疗带状疱疹复发,提高患者生存质量。
附图说明
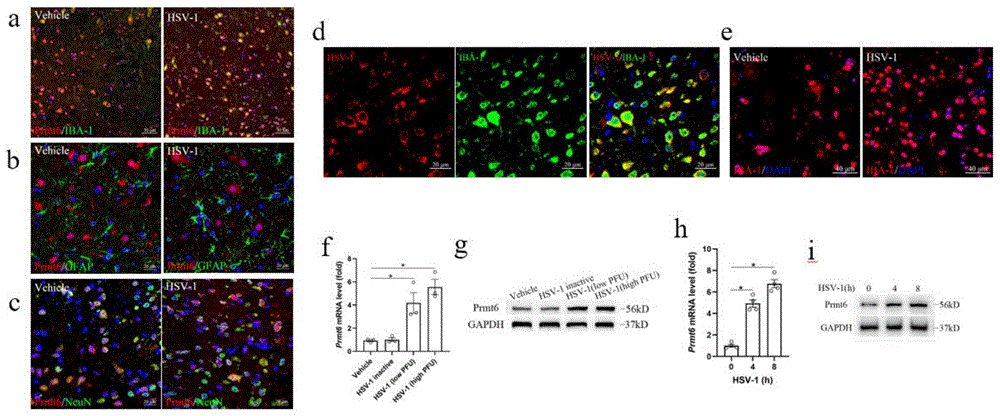
图1:小胶质细胞中Prmt6在带状疱疹复发病理进程中发挥重要作用。a为Prmt6同小胶质细胞标记物IBA-1共染,b为Prmt6同星形胶质细胞标记物GFAP共染,c为Prmt6同神经元标记物NeuN共染,d为HSV-1病毒感染小胶质细胞后HSV-1同小胶质细胞标记物IBA-1共染,e为HSV-1刺激后脊髓背角小胶质细胞激活变化,f为Prmt6的mRNA在带状疱疹复发模型小鼠脊髓背角表达变化,g为Prmt6的蛋白在带状疱疹复发模型小鼠脊髓背角表达变化,h为Prmt6的mRNA在HSV-1刺激后的体外培养的小胶质细胞中表达变化,g为Prmt6的蛋白在HSV-1刺激后的体外培养的小胶质细胞中表达变化。
图2:Prmt6缺陷增强带状疱疹复发小鼠抗病毒免疫。a为带状疱疹复发小鼠脊髓背角抗病毒免疫相关蛋白表达变化,b为带状疱疹复发小鼠脊髓背角I型干扰素产量变化,c为带状疱疹复发小鼠脊髓背角干扰素刺激因子表达变化。
图3:Prmt6缺陷降低HSV-1病毒载量并减轻病毒相关性炎症和神经损伤。a为带状疱疹复发小鼠脊髓背角HSV-1病毒载量变化,b为带状疱疹复发小鼠脊髓背角炎症因子水平,c为带状疱疹复发小鼠脊髓背角神经保护因子及髓鞘相关因子表达变化,d为带状疱疹复发小鼠脊髓背角泛细胞死亡蛋白标记物表达变化,e为带状疱疹复发小鼠脊髓背角透射电镜下脱髓鞘改变,f为带状疱疹复发小鼠脊髓背角透射电镜下线粒体水肿变化。
图4:Prmt6敲减能够增强体外培养的小胶质细胞抗病毒能力并降低病毒载量,减轻炎症和泛细胞死亡状态。a为HSV-1刺激体外培养的敲减Prmt6的小胶质细胞后抗病毒免疫相关蛋白表达变化,b为HSV-1刺激体外培养的敲减Prmt6的小胶质细胞后I型干扰素产量变化,c为HSV-1刺激体外培养的敲减Prmt6的小胶质细胞后干扰素刺激因子表达变化,d为HSV-1刺激体外培养的敲减Prmt6的小胶质细胞后HSV-1病毒载量变化,e为HSV-1刺激体外培养的敲减Prmt6的小胶质细胞后炎症因子水平,f为HSV-1刺激体外培养的敲减Prmt6的小胶质细胞后泛细胞死亡蛋白标记物表达变化。
图5:Prmt6过表达能够减弱体外培养的小胶质细胞抗病毒能力并增加病毒载量,加重炎症和泛细胞死亡状态。a为HSV-1刺激体外培养的过表达Prmt6的小胶质细胞后抗病毒免疫相关蛋白表达变化,b为HSV-1刺激体外培养的过表达Prmt6的小胶质细胞后I型干扰素产量变化,c为HSV-1刺激体外培养的过表达Prmt6的小胶质细胞后干扰素刺激因子表达变化,d为HSV-1刺激体外培养的过表达Prmt6的小胶质细胞后HSV-1病毒载量变化,e为HSV-1刺激体外培养的过表达Prmt6的小胶质细胞后炎症因子水平,f为HSV-1刺激体外培养的过表达Prmt6的小胶质细胞后泛细胞死亡蛋白标记物表达变化。
图6:Prmt6抑制小胶质细胞抗病毒免疫依赖其甲基转移酶功能。a为CO-IP展示Prmt6同STING相结合,b为CO-IP展示STING同Prmt6相结合,c为Prmt6对抗病毒免疫相关蛋白的影响依赖STING,d-e为Prmt6对I型干扰素产量的影响依赖STING,f为Prmt6能够甲基化STING,g为丧失甲基转移酶功能的突变型Prmt6调控抗病毒相关蛋白的能力消失,h为丧失甲基转移酶功能的突变型Prmt6调控I型干扰素产量的能力消失。
具体实施方式
下面结合实施例对本发明提供的具体实施方式作详细说明。
实施例1:小胶质细胞中Prmt6在带状疱疹复发病理进程中发挥重要作用
对C57BL/6J小鼠(6-8周)左下肢股骨处皮下接种0.2mL的HSV-1病毒原液(1×10
实施例1表明:小胶质细胞中Prmt6在带状疱疹复发病理进程中发挥重要作用。
实施例2:Prmt6缺陷增强带状疱疹复发小鼠抗病毒免疫
为了检测Prmt6在带状疱疹复发进程中的作用,我们构建了Prmt6缺陷小鼠,Prmt6基因敲除主要是以非同源重组修复原理及CRISPR/Cas9技术,将Prmt6基因突变,从而引起其蛋白读码框全缺失,无法正常转录、翻译和编码功能蛋白质。首先以Prmt6基因为模板通过外源性合成具有导向功能的gRNA及Cas9的mRNA并将其显微注射至野生型C57BL/6J小鼠受精卵中,Cas9核酸酶在gRNA引导下可特异性结合Prmt6基因序列并进行酶切,随后细胞利用自身非同源末端接合等DNA修复方式修复Prmt6基因序列,造成基因缺失或插入,从而实现Prmt6基因敲除的F0代小鼠。随后F0代小鼠与野生型C57BL/6J小鼠交配获得的F1代均为杂合表型(Prmt6
实施例2表明:Prmt6缺陷增强带状疱疹复发小鼠抗病毒免疫。
实施例3:Prmt6缺陷降低HSV-1病毒载量并减轻病毒相关性炎症和神经损伤
Q-PCR结果显示同Prmt6
实施例3表明:Prmt6缺陷降低HSV-1病毒载量并减轻病毒相关性炎症和神经损伤。
实施例4:Prmt6敲减能够增强体外培养的小胶质细胞抗病毒能力并降低病毒载量,减轻炎症和泛细胞死亡状态
我们进一步在体外培养的小胶质细胞中用siRNA敲减Prmt6后并用HSV-1刺激,观察Prmt6敲减对小胶质细胞抗HSV-1感染能力和细胞炎症的影响。Western blotting结果显示HSV-1刺激后两组小胶质细胞的p-TBK1、p-IRF3蛋白表达均增加,提示抗病毒能力增强,而敲减Prmt6组(si-Prmt6)小胶质细胞p-TBK1、p-IRF3蛋白表达显著高于对照组(sc-Prmt6)小胶质细胞(图4a),Q-PCR结果同样说明了HSV-1刺激后si-Prmt6组小胶质细胞I型干扰素(图4b)、干扰素刺激因子(图4c)的mRNA水平显著增加,导致TK基因显著减少,即病毒载量降低(图4d),同时病毒导致的炎症因子的mRNA水平均显著降低(图4e),进一步检测了小胶质细胞的泛死亡状态发现HSV-1刺激后两组细胞的p-MLKL、cleaved Caspase 3/8、cleaved Gasdermin D蛋白表达均显著增加,而si-Prmt6组小胶质细胞p-MLKL、cleavedCaspase 3/8、cleaved Gasdermin D蛋白表达均显著低于sc-Prmt6组小胶质细胞(图4f),泛细胞死亡有所缓解。
实施例4表明:Prmt6敲减能够增强体外培养的小胶质细胞抗病毒能力并降低病毒载量,减轻神经炎症和泛细胞死亡状态。
实施例5:Prmt6过表达能够减弱体外培养的小胶质细胞抗病毒能力并增加病毒载量,加重炎症和泛细胞死亡状态
我们进一步在体外培养的小胶质细胞中用质粒过表达Prmt6后并用HSV-1刺激,观察Prmt6敲减对小胶质细胞抗HSV-1感染能力和细胞炎症的影响。Western blotting结果显示HSV-1刺激后两组小胶质细胞的p-TBK1、p-IRF3蛋白表达均增加,提示抗病毒能力增强,而过表达组(OE-Prmt6)小胶质细胞p-TBK1、p-IRF3蛋白表达显著低于对照组(sc-Prmt6)小胶质细胞(图5a),Q-PCR结果同样说明了HSV-1刺激后OE-Prmt6组小胶质细胞I型干扰素(图5b)、干扰素刺激因子(图5c)的mRNA水平显著降低,导致TK基因显著增加,即病毒载量增加(图5d),同时病毒导致的炎症因子的mRNA水平均显著增加(图5e),进一步检测了小胶质细胞的泛死亡状态发现HSV-1刺激后两组细胞的p-MLKL、cleaved Caspase 3/8、cleavedGasdermin D蛋白表达均显著增加,而OE-Prmt6组小胶质细胞p-MLKL、cleaved Caspase 3/8、cleaved Gasdermin D蛋白表达均显著高于sc-Prmt6组小胶质细胞(图5f),泛细胞死亡有所缓解。
实施例5表明:Prmt6过表达能够减弱体外培养的小胶质细胞抗病毒能力并增加病毒载量,加重炎症和泛细胞死亡状态。
实施例6:Prmt6抑制小胶质细胞抗病毒免疫依赖其甲基转移酶功能。
为了进一步探索Prmt6调控带状疱疹复发模型中抗病毒免疫的机制,我们用CO-IP的方法观察Prmt6是否同抗病毒免疫关键通路cGAS-STING通路相关蛋白相结合改变其活性从而影响I型干扰素产量,结果显示Prmt6抗体能够同STING相结合,而同cGAS、TBK1、IRF3等均不能结合(图6a),采用STING抗体同样可检测到STING同Prmt6相结合(图6b),进一步证明了两者结合的可能性。为了进一步验证Prmt6与STING结合后对cGAS-STING通路介导的抗病毒能力的影响,我们分别siRNA敲减或质粒过表达了STING、梯度质粒过表达Prmt6,观察HSV-1诱发的抗病毒免疫变化。siRNA敲减STING条件下小胶质细胞过表达Prmt6并未影响p-TBK、p-IRF3蛋白表达及I型干扰素的mRNA水平,而在质粒过表达STING条件下小胶质细胞过表达Prmt6显著降低p-TBK、p-IRF3蛋白表达及I型干扰素的mRNA水平,且具有浓度依赖性,说明Prmt6调控cGAS-STING通路介导的抗病毒能力主要依赖STING分子;相同浓度过表达Prmt6质粒条件下,过表达STING显著增加p-TBK1、p-IRF3蛋白表达及I型干扰素的mRNA水平(图6c-e),进一步说明STING在IFN-I合成中的关键作用,提示Prmt6负向调控抗病毒免疫高度依赖STING分子。由于Prmt6具有较强的精氨酸甲基转移活性,其功能是对富含甘氨酸和精氨酸的结构域进行甲基化修饰,因此我们进一步探讨了Prmt6调控cGAS-STING通路介导的抗病毒免疫是否依赖其甲基转移酶活性。通过在小胶质细胞中质粒梯度过表达Prmt6,用HSV-1刺激8小时后发现总蛋白中可观察到甲基化修饰,通过对获取的总蛋白进行CO-IP检测发现用STING抗体沉淀下来的STING蛋白也存在甲基化修饰,且具有Prmt6浓度依赖性(图6f),说明STING可被Prmt6甲基化修饰。由于Prmt6第27位和第29位氨基酸VLD突变为KLA会导致Prmt6丧失甲基转移酶催化活性,因此为了进一步阐明Prmt6甲基转移活性对cGAS-STING通路的功能影响,我们构建了野生型Prmt6质粒(Prmt6
实施例6表明:Prmt6抑制小胶质细胞抗病毒免疫依赖其甲基转移酶功能。
以上已对本发明创造的较佳实施例进行了具体说明,但本发明创造并不限于所述实施例,熟悉本领域的技术人员在不违背本发明创造精神的前提下还可做出种种的等同的变型或替换,这些等同的变型或替换均包含在本申请权利要求所限定的范围内。
- 一种自修复超分子水凝胶及其制备方法和用途
- 一种钛硅分子筛及其制备方法和用途
- 一种新型膜分子的抗炎作用、实施方法及用途
- 一种新型抗病毒分子DRP的抗病毒作用、实施方法及用途
