一种厚果崖豆藤叶活性成分及提取方法和用途
文献发布时间:2024-04-18 19:52:40
技术领域
本发明属于医药技术领域,具体涉及一种厚果崖豆藤叶活性成分及提取方法和用途。
背景技术
厚果崖豆藤(Millettia pachycarpa Benth)又称毛蕊崖豆藤、冲天子、苦檀子,为白豆科崖豆藤属,植物的藤为巨大藤本,高达15m,多生于海拔2000米以下的山坡常绿阔叶林中。其性热、味苦辛,经过一些崖豆藤属植物药理活性研究,发现此属植物药用价值非常广泛,具有攻毒、止痛、杀虫的作用,且还具有保护心血管、抗肿瘤、保肝和抗雌性激素等多种药理活性。该植物的种子和根含有鱼藤酮,磨粉可用来作为杀虫药,能防治许多种粮棉害虫,茎皮纤维也可供利用。但目前关于厚果崖豆藤叶成分的研究资料较匮乏,其主要活性成分目前并没有得到完全的分离和鉴定,对这些主要活性成分的开发也处于不完善的阶段。
发明内容
针对现有技术中的上述不足,本发明提供一种厚果崖豆藤叶活性成分及提取方法和用途,其可有效的抑制大肠杆菌β葡萄糖醛酸酶活性。
为实现上述目的,本发明解决其技术问题所采用的技术方案是:
一种厚果崖豆藤叶活性成分,其具有如下所示的结构式:
一种提取上述活性成分的方法,包括以下步骤:
(1)取洗净、阴干并经粉碎的厚果崖豆藤叶,按质量比为1:2~1:8加入纯甲醇溶液,提取1~5次,每次0.5~72h,过滤,减压浓缩至原体积的2%~10%,得粗提物;
(2)以乙腈作为洗脱液,对粗提物进行洗脱,并收集获得活性成分。
进一步地,步骤(1)中的提取方式为:常温提取、加热提取、微波辅助提取或超声波辅助。
进一步地,步骤(2)中依次以85%、75%、30%、5%乙腈进行洗脱,然后收集保留时间为35min的色谱峰,浓缩、干燥,获得式Ⅰ所示化合物。
进一步地,步骤(2)中依次以85%、75%、30%、5%乙腈进行洗脱,累加收集保留时间为16.5min的色谱峰,浓缩、干燥,获得式Ⅱ所示化合物。
上述厚果崖豆藤叶活性成分,或采用上述方法提取得到的活性成分在抑制β-葡萄糖醛酸酶活性中的用途。
一种β-葡萄糖醛酸酶抑制剂,其特征在于,包括上述厚果崖豆藤叶活性成分、其衍生物或其盐,以及药学上可接受的载体。
上述厚果崖豆藤叶活性成分,或采用上述方法提取得到的活性成分在制备β-葡萄糖醛酸酶诱导的药物中的用途。
本发明的有益效果:
本发明通过提取方法和柱色谱分离技术从厚果崖豆藤叶中分离得到了活性成分化合物Ⅰ和化合物Ⅱ,对其进行了分离纯化鉴定,并发现其对GUS有较强的抑制效果,为厚果崖豆藤叶的开发提供了新的方向和依据。
附图说明
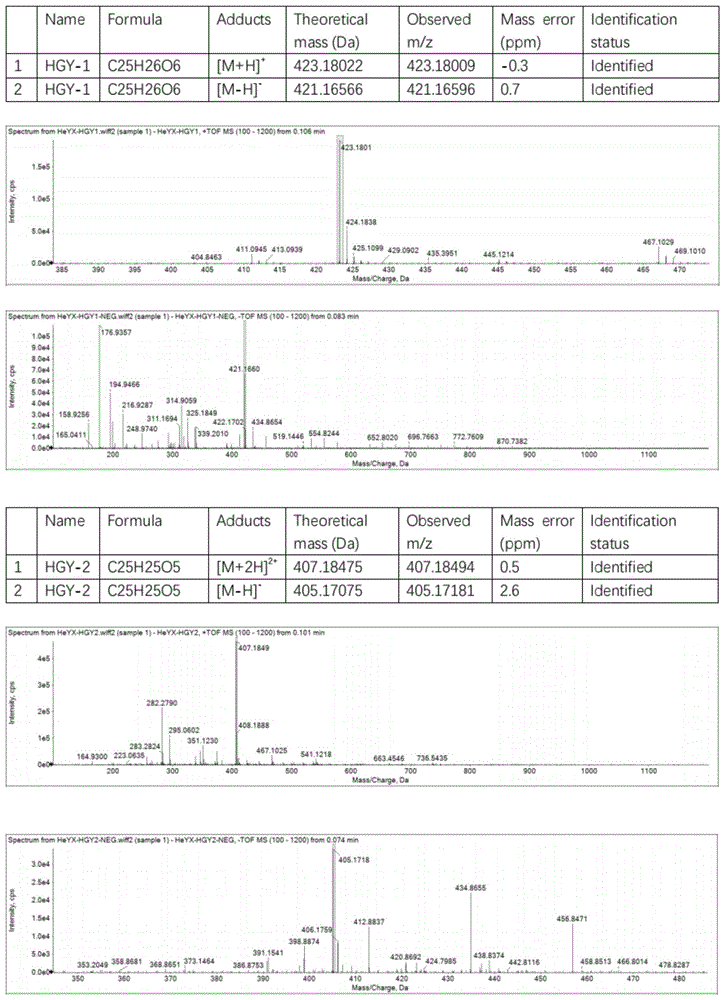
图1为化合物Ⅰ和化合物Ⅱ的HR-ESI-MS谱;
图2为化合物Ⅰ和化合物Ⅱ的1H-NMR谱;
图3为化合物Ⅰ和化合物Ⅱ的13C-NMR谱。
具体实施方式
下面对本发明的具体实施方式进行描述,以便于本技术领域的技术人员理解本发明,但应该清楚,本发明不限于具体实施方式的范围,对本技术领域的普通技术人员来讲,只要各种变化在所附的权利要求限定和确定的本发明的精神和范围内,这些变化是显而易见的,一切利用本发明构思的发明创造均在保护之列。
实施例1活性成分的制备
1、制备化合物Ⅰ
(1)取洗净、阴干并经粉碎的厚果崖豆藤叶为原料,按质量比1:8加入纯甲醇溶液,37℃超声波水浴辅助提取2次,每次0.5h,0.22μm孔径尼龙膜过滤,得粗提物溶液;
(2)粗提物反复多次注入通过经高效液相色谱柱进行制备。高效液相色谱的制备参数为:4.6mm×250mm的Lubex kromasil C18色谱柱,填料的粒度为5μm,柱温为30℃,流动相为体积比的乙腈和0.1%磷酸水,洗脱模式为梯度洗脱:0min,乙腈与0.1%磷酸水的体积比为85:15;15min,乙腈与水的体积比为75:25;25min,乙腈与水的体积比为30:70;35min,乙腈与水的体积比为5:95,累加收集保留时间为35min的色谱峰,浓缩、干燥,得到化合物Ⅰ。
该化合物的结构鉴定:
制备所得的化合物为白色无定型粉末,该制备的化合物电喷雾离子化质谱中的特征离子峰显示其m/z[M+H]+、[M-H]-分别为423、421,表明该化合物分子量为422。结合该制备所得化合物的1H和13C核磁共振图谱(NMR)数据,确定其化学分子式为C
试验测定并解析的该制备所得化合物的核磁共振谱数据:1H NMR(400MHz,Chloroform-d)δ12.91(s,1H),7.89(s,1H),6.98(s,1H),6.86-6.73(m,2H),5.31-5.13(m,2H),3.46(t,J=8.6Hz,4H),1.84(s,3H),1.83(s,3H),1.76(s,3H),1.74(s,3H);13C NMR(100MHz,Chloroform-d)δ181.94,160.08,157.50,153.66,153.38,144.77,144.08,135.67,134.50,123.62,122.97,121.53,121.36,116.57,115.57,110.67,105.86,105.72,25.99,25.93,21.86,18.09,18.05。
综合以上信息,该化合物被确定为3-(3,4-二羟基苯基)-5,7-二羟基-6,8-双(3-甲基丁-2-烯-1-基)-4H-甲烯-4-酮(HGY-1)。其结构式如下:
2、制备化合物Ⅱ
(1)取洗净、阴干并经粉碎的厚果崖豆藤叶为原料,按质量比1:8加入纯甲醇溶液,37℃超声波水浴辅助提取2次,每次0.5h,0.22μm孔径尼龙膜过滤,得粗提物溶液;
(2)粗提物反复多次注入通过经高效液相色谱柱进行制备。高效液相色谱的制备参数为:4.6mm×250mm的Lubex kromasil C18色谱柱,填料的粒度为5μm,柱温为30℃,流动相为体积比的乙腈和0.1%磷酸水,洗脱模式为梯度洗脱:0min,乙腈与0.1%磷酸水的体积比为85:15;15min,乙腈与水的体积比为75:25;25min,乙腈与水的体积比为30:70;35min,乙腈与水的体积比为5:95,累加收集保留时间为16.5min的色谱峰,浓缩、干燥,得到本发明所述的化合物Ⅱ。
该化合物的结构鉴定:
制备所得的化合物为白色无定型粉末.该制备的化合物电喷雾离子化质谱中的特征离子峰显示其m/z[M+H]+、[M-H]-分别为407、405,表明该化合物分子量为406。结合该制备所得化合物的1H和13C核磁共振图谱(NMR)数据,确定其化学分子式为C
试验测定并解析的该制备所得化合物的核磁共振谱数据:1H NMR(400MHz,Chloroform-d)δ13.11(s,1H),7.89(s,1H),7.35(d,J=8.2Hz,2H),6.84(d,J=8.2Hz,2H),6.36(s,1H),5.25(dt,J=15.9,7.2Hz,2H),3.47(t,J=6.0Hz,4H),1.84(s,3H),1.83(s,3H),1.77(s,3H),1.74(s,3H);13C NMR(100MHz,Chloroform-d)δ181.57,159.79,157.67,156.11,153.56,152.82,135.70,134.27,130.49,123.36,123.28,121.68,121.46,115.82,110.40,105.95,105.59,26.00,25.93,21.85,18.09,18.04.
综合以上信息,该化合物被确定为5,7-二羟基-3-(4-羟基苯基)-6,8-双(3-甲基丁-2-烯-1-基)-4H-甲烯-4-酮(HGY-2)。其结构式如下:
实施例2活性成分对抗肠道菌β-葡萄糖醛酸酶活性的影响
以实施例1制备的化合物Ⅰ和化合物Ⅱ作为实验组,经HPLC测定后纯度为98.8%,再以购自Sigma公司的具有显著抗β-葡萄糖醛酸酶活性的D-葡萄糖二酸-1,4-内酯(DSL)标准品(经HPLC测定后,其纯度≥98.8%)作为对照,检测本申请提取得到的活性成分对肠道菌β-葡萄糖醛酸酶活性的影响,试验应用4MUG作为底物的荧光测定方法规程执行。
以抗肠道菌β-葡萄糖醛酸酶经典途径测定法评价化合物Ⅰ和化合物Ⅱ的抗肠道菌β-葡萄糖醛酸酶活性,试验结果如表1所示。
表1化合物Ⅰ和化合物Ⅱ对肠道菌β-葡萄糖醛酸酶抑制活性(IC50值)
a表示三次独立试验的平均值。
由表1可知,本申请提取的化合物Ⅰ和化合物Ⅱ对肠道菌β-葡萄糖醛酸酶50%抑制浓度(IC50)为3.88μM和4.05μM,而平行试验所测的阳性对照组化合物DSL的IC50值为55μM。表明本申请提取得到的化合物Ⅰ和化合物Ⅱ具有显著的抗肠道菌β-葡萄糖醛酸酶作用,可广泛应用在抗肠道菌β-葡萄糖醛酸酶药品制备中。
最后应说明的是,以上具体实施方式仅用以说明本发明的技术方案而非限制,尽管参照实例对本发明进行了详细说明,本领域的普通技术人员应当理解,可以对本发明的技术方案进行修改或者等同替换,而不脱离本发明技术方案的精神和范围,其均应涵盖在本发明的权利要求范围当中。
