用于治疗癌症的组合疗法
文献发布时间:2024-04-18 19:52:40
背景技术
虽然在癌症治疗中已经取得很多进展,但是患者仍然需要新的并且有效的疗法。
发明内容
AZD5305(5-[4-[(7-乙基-6-氧代-5H-1,5-萘啶-3-基)甲基]哌嗪-1-基]-N-甲基-吡啶-2-甲酰胺)是小分子药物,其通过在DNA单链断裂(SSB)的位点处选择性抑制并且捕获PARP1而发挥作用。这阻止DNA修复,并且在DNA复制期间,当DNA复制机器与PARP1-DNA非共价复合物发生冲突时,导致产生更有害的DNA双链断裂(DSB)。在其中精确的DNA修复途径有效的情况下,例如在具有完善的同源重组修复(HR)的细胞中,DSB被精确修复。相反,在具有修复途径缺陷的细胞中,例如在BRCA基因中具有有害突变的那些细胞中,AZD5305治疗导致基因组不稳定性的选择性积累并最终选择性杀死癌细胞、同时不伤害正常细胞。
铂化学治疗剂是用来治疗癌症的药物,经常出现在一线治疗情境中。铂化学治疗剂的实例包括顺铂、奥沙利铂、和卡铂。
在一些实施例中,披露了治疗有需要的人类受试者中的癌症的方法,该方法包括向该人类受试者施用第一量的AZD5305或其药学上可接受的盐,和第二量的铂化学治疗剂或其药学上可接受的盐;其中该第一量和该第二量一起构成治疗有效量。
在一些实施例中,癌症是卵巢癌、乳腺癌、胰腺癌、前列腺癌、血液癌、胃肠道癌(例如胃癌和结肠直肠癌)、或肺癌。
在一些实施例中,癌症是同源重组缺陷性(HRD)癌症。例如,可以通过MyriadGenetics
在某些实施例中,癌细胞包含选自以下的HRD基因突变:BRCA1、BRCA2、ATM、BRIP1、BARD1、CDK12、CHEK1、CHEK2、FANCL、PALB2、PPP2R2A、RAD51B、RAD51C、RAD51D、和RAD54L基因突变。在某些实施例中,癌细胞包含BRCA1、BRCA2、和/或ATM基因突变。在某些实施例中,癌细胞包含BRCA1和/或BRCA2基因突变。例如,在某些实施例中,癌细胞包含tBRCA基因突变。
在本披露的方法的某些实施例中,癌症包括由有害或疑似有害的BRCA突变和/或基因组不稳定性限定的同源重组缺陷(HRD)阳性状态。
在本披露的方法的某些实施例中,癌症是卵巢癌或乳腺癌。在本披露的方法的某些实施例中,癌症是卵巢癌。在某些实施例中,癌症是晚期上皮性卵巢癌。在某些实施例中,癌症是高级别浆液性卵巢癌。在某些实施例中,癌症是高级别子宫内膜样卵巢癌。在某些实施例中,癌症是上皮性卵巢癌,其包含gBRCA1或gBRCA2突变。在本披露的方法的某些实施例中,癌症是输卵管癌。在本披露的方法的某些实施例中,癌症是原发性腹膜癌。
在某些实施例中,癌症是卵巢癌(例如晚期上皮性卵巢癌)、输卵管癌、或原发性腹膜癌。
在某些实施例中,癌症是卵巢癌(例如晚期上皮性卵巢癌)、输卵管癌、或原发性腹膜癌,癌症包括由有害或疑似有害的BRCA突变和/或基因组不稳定性限定的同源重组缺陷(HRD)阳性状态。
在某些实施例中,癌症是乳腺癌。在某些实施例中,癌症是三阴性乳腺癌。
在一些实施例中,癌症是铂抗性的。
在一些实施例中,披露了试剂盒,该试剂盒包含第一药物组合物,其包含AZD5305或其药学上可接受的盐和药学上可接受的载体;和第二药物组合物,其包含铂化学治疗剂或其药学上可接受的盐,以及使用说明书。
附图说明
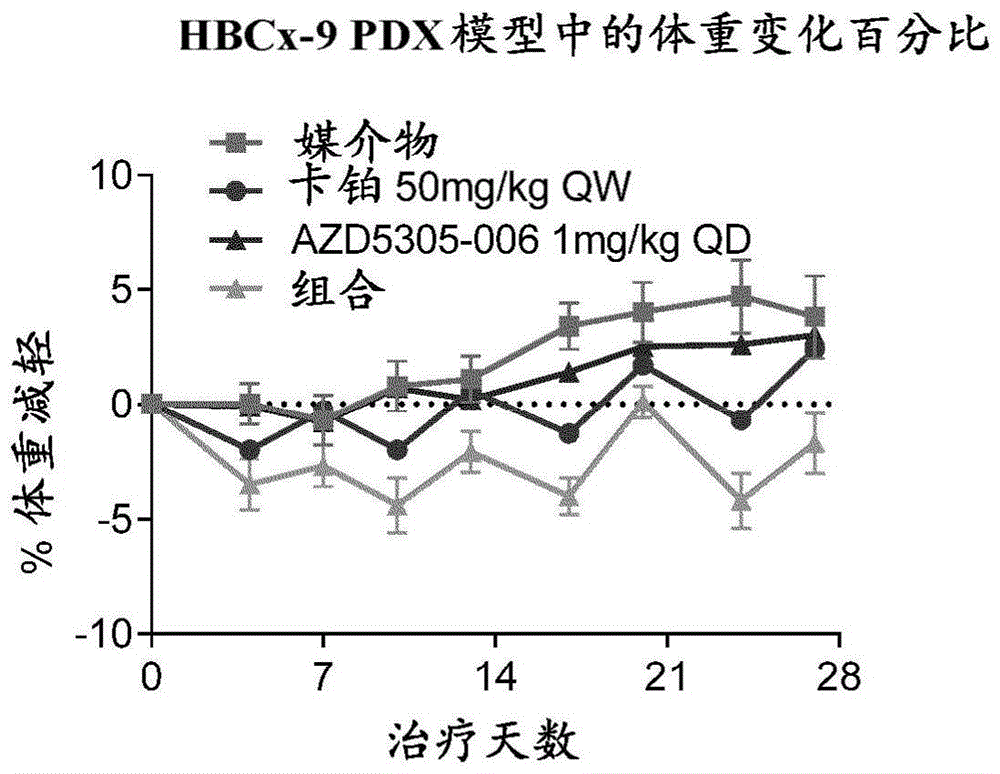
图1展示了在用AZD5305单一疗法、卡铂单一疗法、及组合治疗的PDX模型(HBCx-9)中,小鼠的体重变化。
图2展示了在PDX模型(HBCx-9)中,AZD5305与卡铂组合的抗肿瘤活性。
图3展示了在PDX模型(HBCx-9)中,AZD5305与卡铂组合的抗肿瘤活性。示出了单个动物数据。
图4示出了AZD5305形式A的X射线粉末衍射。
图5展示了在用AZD5305单一疗法、卡铂单一疗法、及组合治疗的异种移植物模型(SUM149PT)中,小鼠的体重变化。
图6展示了在异种移植物模型(SUM149PT)中,AZD5305与卡铂组合的抗肿瘤活性。
图7展示了在用AZD5305单一疗法、卡铂单一疗法、及组合治疗的PDX模型(HBCx-9)中,小鼠的体重变化。
图8展示了在PDX模型(HBCx-9)中,AZD5305与卡铂组合的抗肿瘤活性。
图9展示了在用AZD5305单一疗法、卡铂单一疗法、及组合治疗的PDX模型(HBCx-9)中,在治疗停止后,AZD5305与卡铂组合的抗肿瘤活性。
具体实施方式
在一些实施例中,披露了通过AZD5305与铂化学治疗剂的组合疗法治疗癌症的方法。在一些实施例中,该方法包括向有需要的受试者施用第一量的AZD5305或其药学上可接受的盐,和第二量的铂化学治疗剂或其药学上可接受的盐,其中该第一量和该第二量一起构成治疗有效量。在一些实施例中,铂化学治疗剂包括卡铂、顺铂和奥沙利铂中的任一种。在一些实施例中,铂化学治疗剂包括卡铂。在一个实施例中,首先施用铂化学治疗剂或其药学上可接受的盐,然后施用AZD5305或其药学上可接受的盐。在一个实施例中,首先施用AZD5305或药学上可接受的盐,然后施用铂化学治疗剂或药学上可接受的盐。
术语“AZD5305”是指以下化合物:具有化学名5-[4-[(7-乙基-6-氧代-5H-1,5-萘啶-3-基)甲基]哌嗪-1-基]-N-甲基-吡啶-2-甲酰胺,
并且具有以下显示的结构:
本文披露了AZD5305的制备(参见实例1)。在一些实施例中,向受试者施用AZD5305的游离碱。在一些实施例中,向受试者施用AZD5305的药学上可接受的盐。在一些实施例中,向受试者施用结晶AZD5305。在一些实施例中,向受试者施用晶型A AZD5305。
术语“含铂化学治疗剂”包括含有金属铂的药物,例如顺铂、卡铂、和奥沙利铂。
在一些实施例中,分开地、顺序地或同时地施用AZD5305或其药学上可接受的盐,和铂化学治疗剂或其药学上可接受的盐。在一个实施例中,首先施用铂化学治疗剂或其药学上可接受的盐,然后施用AZD5305或其药学上可接受的盐。在一个实施例中,首先施用AZD5305或药学上可接受的盐,然后施用铂化学治疗剂或药学上可接受的盐。
在一些实施例中,在一个治疗周期中分开地、顺序地或同时地施用AZD5305或其药学上可接受的盐,和铂化学治疗剂或其药学上可接受的盐。
如本文所用的“周期”、“治疗周期”或“给药时间表”是指按规律的时间表重复的组合治疗的时间段。例如,可以给予治疗一周、两周、或三周,其中与以协调的方式施用AZD5305和铂化学治疗剂。在一些实施例中,治疗周期是约1周至约3个月。在一些实施例中,治疗周期是约5天至约1个月。在一些实施例中,治疗周期是约1周至约3周。在一些实施例中,治疗周期是约1周、约10天、约2周、约3周、约4周、约2个月、或约3个月。
在一些实施例中,在一个或多个治疗周期(例如一个疗程)中,向人类受试者施用AZD5305或其药学上可接受的盐,和铂化学治疗剂或其药学上可接受的盐。“疗程”包括多个治疗周期,根据监测的患者的疾病进展,可以按规律的时间表重复这些治疗周期,或将这些治疗周期调整为逐渐减少的时间表。例如,在疗程开始时(例如,当患者被第一次诊断时),患者的治疗周期可以具有更长的治疗期和/或更短的休息期,并且随着癌症渐渐缓解,休息期延长,由此增加一个治疗周期的长度。在整个疗程期间,技术人员可以基于患者的疾病进展、治疗耐受性、和预后来确定并且调整治疗周期中的治疗和休息的时间段、治疗周期数、和疗程的时间长度。在一些实施例中,该方法包括1至10个治疗周期。在一些实施例中,该方法包括2至8个治疗周期。
在一些实施例中,口服施用AZD5305或其药学上可接受的盐。在一些实施例中,AZD5305或其药学上可接受的盐是胶囊剂型。在一些实施例中,AZD5305或其药学上可接受的盐是片剂剂型。
词语“治疗”(“treat”、“treating”和“treatment”)包括减少或抑制受试者中与PARP或癌症相关的酶或蛋白活性,改善在受试者中癌症的一种或多种症状,或减缓或推迟在受试者中癌症的进展。词语“治疗(treat,treatment)”和“治疗中(treating)”还包括减少或抑制受试者中肿瘤的生长或癌细胞的增殖。
词语“抑制”(“inhibit”、“inhibition”或“inhibiting”)包括生物活性或过程的基线活性的降低。
术语“癌症”包括但不限于由身体的一部分中的异常细胞的不受控制的分裂引起的疾病。在一些实施例中,癌症包括易感于用PARP抑制剂(例如AZD5305)治疗的癌症。在一些实施例中,癌症是卵巢癌、乳腺癌、胰腺癌、和前列腺癌。在一些实施例中,癌症是血液癌、胃肠道癌(例如胃癌和结肠直肠癌)、或肺癌。在一些实施例中,癌症是复发性或难治性癌症。在一些实施例中,癌症是铂抗性癌症。
词语“药物组合物”包括:包含活性成分和药学上可接受的赋形剂、载体或稀释剂的组合物,其中活性成分是AZD5305或其药学上可接受的盐、或铂化学治疗剂或其药学上可接受的盐。
在本说明书中,除非另外说明,否则如在此使用的术语“药学上可接受的”是指在合理医学判断范围内,适合用于与人类和动物组织接触使用而没有过多的毒性、刺激、过敏反应或其他问题或并发症(与合理的益处/风险比相称)的那些化合物、材料、组合物、盐、和/或剂型。
词语“药学上可接受的赋形剂、载体或稀释剂”包括如本领域技术人员所确定的那样,在合理的医学判断范围内,适合用于与接触人类和动物的组织接触而无过度毒性、刺激、过敏反应或其他问题或并发症的化合物、材料、组合物和/或剂型。在一些实施例中,药物组合物是固体剂型,例如胶囊、片剂、颗粒剂、粉剂、小袋等。在一些实施例中,药物组合物是以下形式:一种或多种水性或非水性无毒肠胃外可接受的缓冲系统、稀释剂、增溶剂、共溶剂或载体中的无菌可注射溶液。无菌可注射制剂也可以是在非水性稀释剂、载体或共溶剂中的无菌可注射水性或油性悬浮液或悬浮液,其可以根据已知程序利用一种或多种合适的分散剂或润湿剂和悬浮剂配制。药物组合物可以是用于静脉推注/输注的溶液,或者用缓冲剂体系用或不用其他赋形剂重构的冻干体系(单独的或与赋形剂一起)。冻干的冷冻干燥材料可以由非水性溶剂或水性溶剂制备。剂型也可以是进一步稀释用于后续输注的浓缩物。
术语“受试者”包括暖血哺乳类动物,例如灵长类、狗、猫、兔、大鼠和小鼠。在一些实施例中,该受试者是灵长类,例如,人类。在一些实施例中,受试者患有癌症,例如卵巢癌、乳腺癌、胰腺癌、和前列腺癌。在一些实施例中,受试者患有癌症,例如血液癌、胃肠道癌(例如胃癌和结肠直肠癌)、或肺癌。在一些实施例中,受试者患有卵巢癌或乳腺癌。在一些实施例中,受试者患有复发性或难治性卵巢癌。在一些实施例中,受试者患有复发性或难治性乳腺癌。在一些实施例中,该受试者患有癌症且是治疗初试的
词语“治疗有效量”包括AZD5305的量和/或铂化学治疗剂的量,这样的量将一起引起受试者中的生物或医学应答,例如,与PARP或癌症相关的酶或蛋白质活性的降低或抑制;改善癌症症状;或者减缓或推迟癌症的进展。在一些实施例中,词语“治疗有效量”包括在受试者中至少部分地减轻、抑制、和/或改善癌症或抑制PARP、和/或减少或抑制肿瘤的生长或癌性细胞的增殖的有效的AZD5305和铂化学治疗剂一起的量。在一些实施例中,词语“治疗有效量”包括在受试者中至少部分地减少或抑制肿瘤的生长或癌性细胞的增殖的有效的AZD5305和铂化学治疗剂一起的量。
在一些实施例中,披露了试剂盒,该试剂盒包含:第一药物组合物,其包含AZD5305或其药学上可接受的盐和药学上可接受的载体;和第二药物组合物,其包含卡铂或药学上可接受的盐;以及组合使用第一和第二药物组合物的说明书。在一些实施例中,第一药物组合物包含第一量的AZD5305或其药学上可接受的盐,并且第二药物组合物包含第二量的铂化学治疗剂或其药学上可接受的盐;其中该第一量和该第二量一起构成治疗有效量。
实例
现在将通过参考以下非限制性实例来进一步解释本文披露的组合疗法。
实例1
AZD5305的制备
一般实验条件
除非另有说明,否则使用Bruker 300MHz、400MHz或500MHz光谱仪,在27℃下获得
使用以下进行快速色谱法:在来自Biotage
XRPD分析使用Bruker D8衍射仪进行,该衍射仪可商购自布鲁克AXS公司(BrukerAXS Inc
XRPD 2θ值可在合理的范围内变化,例如在±0.2°的范围内变化,并且当由于各种各样的原因(包括例如优选的方向)对基本上相同的晶型进行测量时XRPD强度可能变化。XRPD的原理被描述于出版物中,例如Giacovazzo,C.等人(1995),Fundamentals ofCrystallography[晶体的基本原理],Oxford University Press[牛津大学出版社];Jenkins,R.和Snyder,R.L.(1996),Introduction to X-Ray Powder Diffractometry[对X射线粉末衍射的介绍],John Wiley&Sons[约翰威利父子出版公司],纽约;和Klug,H.P.和Alexander,L.E.(1974),X-ray Diffraction Procedures[X射线衍射程序],John Wileyand Sons[约翰威利父子出版公司],纽约。
使用了以下缩写:aq=水性;CH2Cl2=二氯甲烷;DCM=二氯甲烷;DDQ=2,3-二氯-5,6-二氰基-1,4-苯醌;DIPEA=N,N-二异丙基乙胺;DMSO=二甲基亚砜;DMSO-d
化学合成
中间体2:乙基6-甲酰基-5-硝基-吡啶-3-甲酸酯
将乙基6-甲基-5-硝基-吡啶-3-甲酸酯(中间体1,10g,47.58mmol)和二氧化硒(7.92g,71.36mmol)在1,4-二噁烷(50mL)中的混合物在110℃下搅拌20h。将反应混合物冷却至室温,通过硅藻土垫过滤并将硅藻土用乙酸乙酯洗涤。将合并的滤液浓缩,并将所得残余物通过快速二氧化硅色谱法(洗脱梯度为己烷中的0%至70%乙酸乙酯)进行纯化。将产物级分在减压下浓缩以得到呈棕色油状物的乙基6-甲酰基-5-硝基-吡啶-3-甲酸酯(中间体2,9.70g,91%)。1HNMR(500MHz,氯仿-d)1.48(3H,t),4.54(2H,q),8.81(1H,d),9.51(1H,d),10.32(1H,s);m/z(ES
中间体3:乙基6-[(E)-2-乙氧基羰基丁-1-烯基]-5-确基-吡啶-3-甲酸酯(E/Z异
在0℃下用加料漏斗向氢化钠(9.63g,240.89mmol)(60%,在矿物油中)在无水THF(100mL)中的搅拌溶液中滴加乙基2-(二乙氧基磷酰基)丁酸酯(60.8g,240.89mmol)以给出灰色的混合物。将所得混合物在0℃下搅拌10min并经10分钟加温至室温并在40℃下搅拌持续5分钟。将反应混合物冷却至-78℃,并然后向该冷却的反应混合物中缓慢添加乙基6-甲酰基-5-硝基-吡啶-3-甲酸酯(中间体2,22.5g,100.37mmol)在100mL THF中的溶液。将混合物用饱和NH
中间体4:乙基7-乙基-6-氧代-7,8-二氢-5H-1,5-萘啶-3-甲酸酯
将乙基6-[(E)-2-乙氧基羰基丁-1-烯基]-5-硝基-吡啶-3-甲酸酯(E/Z异构体的1:1混合物)(中间体3,3.75g,11.63mmol)、Pd/C(1.857g,1.75mmol)(10%)在乙醇(30mL)中的混合物脱气,用H2(气囊)充满,并将反应在室温下在H2气氛搅拌过夜。将混合物通过硅藻土床过滤并将硅藻土床用乙醇洗涤。浓缩后,将在二噁烷(15mL)中的4M HCl添加至将所得残余物并将混合物在室温下搅拌30min。将混合物用乙醚稀释并将固体过滤出,用二乙醚洗涤,并在真空下干燥以得到呈白色固体的乙基7-乙基-6-氧代-7,8-二氢-5H-1,5-萘啶-3-甲酸酯(中间体4,2.260g,78%)。1H NMR(500MHz,DMSO-d6)0.94(3H,t),1.33(3H,t),1.41-1.51(1H,m),1.69-1.81(1H,m),2.41-2.48(1H,m),2.94(1H,dd),3.20(1H,dd),4.35(2H,t),7.67(1H,d),8.61(1H,d),10.32(1H,s);m/z(ES
中间体5:乙基7-乙基-6-氧代-5H-1,5-萘啶-3-甲酸酯
将乙基7-乙基-6-氧代-7,8-二氢-5H-1,5-萘啶-3-甲酸酯(中间体4,2.26g,9.10mmol)溶解于1,4-二噁烷(40mL)中,添加DDQ(2.273g,10.01mmol)并将混合物在回流下搅拌3h。在减压下去除溶剂,添加饱和NaHCO
1H NMR(500MHz,DMSO-d6)1.14-1.28(3H,m),1.35(3H,t),2.58(2H,q),4.38(2H,q),7.83(1H,s),8.17(1H,s),8.90(1H,s),12.05(1H,s);m/z(ES
中间体6:3-乙基-7-(羟基甲基)-1H-1,5-萘啶-2-酮
在0℃下经45分钟的时间段在氮下,将氢化铝锂(2M,在THF(29.2mL,58.47mmol)中)滴加至在四氢呋喃(150mL)中的乙基7-乙基-6-氧代-5H-1,5-萘啶-3-甲酸酯(中间体5,7.2g,29.24mmol)中。将所得混合物在0℃下搅拌1.5小时。将反应混合物通过滴加1Maq HCl(29mL)淬灭。将反应混合物浓缩并将固体用水(约150mL)和29mL 1M HCl溶液稀释给出黄色悬浮液。通过过滤收集固体,用水、二乙醚洗涤并干燥以产生呈黄色固体的粗产物(被一些无机盐污染)。将此固体悬浮于甲醇和DCM的混合物(2∶1)(400mL)中并加热至回流。将固体滤出。将此固体重悬于甲醇/DCM混合物中并重复此程序5次以从此混合物中去除大部分产物。然后将合并的滤液浓缩直至约100mL,并将固体通过过滤收集,用乙醚洗涤,在真空下干燥以产生呈黄色固体的3-乙基-7-(羟基甲基)-1H-1,5-萘啶-2-酮(中间体6,4.35g,72.8%)。1H NMR(500MHz,DMSO-d6)1.18(3H,t),2.52-2.56(2H,m),4.61(2H,d),5.44(1H,t),7.61(1H,s),7.74(1H,s),8.37(1H,s),11.87(1H,br s);m/z(ES+)[M+H]+=205.3
实例1:5-[4-[(7-乙基-6-氧代-5H-1,5-萘啶-3-基)甲基]哌嗪-1-基]-N-甲基-吡
在0℃下,将亚硫酰氯(6.41mL,88.14mmol)滴加至3-乙基-7-(羟基甲基)-1,5-萘啶-2(1H)-酮(中间体6,3g,14.69mmol)和N,N-二甲基甲酰胺(0.114mL,1.47mmol)在CH2Cl2(60mL)中的悬浮液中并将所得溶液在室温下搅拌6小时。将混合物浓缩至干燥以给出粗制7-(氯甲基)-3-乙基-1H-1,5-萘啶-2-酮。
在20℃下,将DIPEA(12.83mL,73.45mmol)添加至7-(氯甲基)-3-乙基-1H-1,5-萘啶-2-酮(粗制,来自以上)、碘化钾(0.488g,2.94mmol)和N-甲基-5-哌嗪-1-基-吡啶-2-甲酰胺2HCl(中间体7,4.31g,14.69mmol)在乙腈(50.00mL)中的搅拌溶液中。将所得溶液在80℃下搅拌2小时。将溶剂在真空下去除。将粗材料用水稀释,用NaHCO3水溶液碱化,并用乙酸乙酯萃取。将有机层经硫酸钠干燥并浓缩以给出粗产物。将所得残余物通过快速二氧化硅色谱法(洗脱梯度为DCM中的0%至15%MeOH)进行纯化。将产物级分在减压下浓缩以得到呈灰白色部分结晶固体的5-[4-[(7-乙基-6-氧代-5H-1,5-萘啶-3-基)甲基]哌嗪-1-基]-N-甲基-吡啶-2-甲酰胺(实例1,3.93g,65.8%)。1H NMR(500MHz,DMSO-d6)1.19(3H,t),2.53-2.59(6H,m),2.79(3H,d),3.33-3.39(4H,m),3.66(2H,s),7.39(1H,dd),7.64(1H,s),7.76(1H,s),7.83(1H,d),8.27(1H,d),8.36-8.40(1H,m),8.41(1H,d),11.85(1H,s);m/z(ES
实例1-形式A
在实例1中,通过在减压下蒸发甲醇/二氯甲烷溶液获得呈部分结晶固体的5-[4-[(7-乙基-6-氧代-5H-1,5-萘啶-3-基)甲基]哌嗪-1-基]-N-甲基-吡啶-2-甲酰胺。如此获得的结晶材料被表征为晶型A。
在结晶度较差的情况下,可以通过在环境温度或在50℃下,将20mg粗样品悬浮于0.20ml的水、甲醇、乙醇、丙酮、乙腈、四氢呋喃、乙酸乙酯或其他溶剂中持续1天,获得晶型A。
将形式A通过XRPD进行分析并且将结果如下进行列表(表1)并且在图4中示出。
表1.针对形式A的XRPD峰
/>
形式A的特征在于提供使用CuKα辐射测量的以下2θ值中的至少一者:8.3、12.4和19.4°。
实例2
进行此体内研究,从而在BRCA野生型肿瘤模型(HBCx-9,体内)中研究AZD5305与卡铂(铂化学治疗剂)组合的抗肿瘤效果。研究设计中包括AZD5305单一疗法臂和卡铂单一疗法臂作为对照。
材料和方法
缩写
存活期
HBCx-9是XenTech公司建立的患者源性肿瘤外植体(PDX)模型,无需先前进行体外培养。将肿瘤碎片皮下移植(SC)到供体小鼠上。当肿瘤体积达到700至1764mm
通过比较对照组和治疗组的肿瘤体积的平均变化来评估从治疗开始的肿瘤生长抑制,并且表示为肿瘤生长抑制(TGI,当TV≥起始TV时)或消退(reg,当TV<起始TV时)百分比。还针对所有组计算从治疗开始的平均体重变化百分比。使用单尾t检验来评估统计学显著性。统计学显著性表示如下:*p≤0.05,**p≤0.01,***p≤0.001。
在开始功效研究之前,在SCID雌性小鼠中,使用按10mg/kg PO QD的AZD5305与按50mg/kg IP QW的卡铂的组合进行耐受性研究,并且未显示对动物总体状况的不良影响或体重的显著变化。
测试材料的配制
将AZD5305配制为用于在水/HCl pH3.5-4媒介物中口服给药,按0.1ml/10g剂量体积施用。伴随搅拌/涡旋/超声处理,通过添加适当体积的1N HCl至约1∶1.25药物/HCl摩尔比,和80%最终体积的无菌去离子水来稀释固体,直至获得溶液。根据以下方程式计算所需的1NHCl的体积:
添加的1N HCl的体积(ml)=1.25×[浓度(mg/ml)÷406.48(g/摩尔)÷1M]×最终体积(ml)
用1N HCl或1N NaOH将溶液的pH调节至3.5至4。使用无菌的注射用水或去离子水补足最终体积,并且测量和记录最终pH。每周一次配制给药制剂,并且避光保存。
在给药的每一天,通过在0.9%NaCl中稀释储备溶液至5mg/ml用于50mg/kg剂量(0.1ml/10g剂量体积)新鲜地配制卡铂
结果
HBCx-9是可从法国XenTech公司获得的TNBC PDX模型。已经将其报告为BRCA wt模型,具有BRCA1甲基化[1]。HBCx-9还显示对奥拉帕尼单一疗法具有中度敏感性[2]。
在功效研究中,按1、0.1、和0.01mg/kg QD的AZD5305和按50mg/kg QW的卡铂作为单一疗法和组合进行测试。治疗期持续28天。在整个研究持续期间,所有治疗均耐受性良好,并且没有观察到显著的体重减轻(图1和图7)。AZD5305单一疗法显示了剂量依赖性抗肿瘤功效,产生了72%TGI;而在卡铂单一疗法组中观察到88%TGI。AZD5305和卡铂一起给药通过产生了88%肿瘤消退展示了明显的组合益处(图2和表2)。此外,在组合组中的所有动物(8/8)都达到了完全应答(CR;定义为TV<14mm
总之,在HBCx-9PDX体内模型中,与每个单一疗法相比,AZD5305与卡铂的组合展示了改善的抗肿瘤效果。AZD5305和卡铂的组合在100%的动物中产生了完全应答,并且在小鼠中耐受性良好。
总结
表2:在HBCx-9患者来源的外植体模型中,AZD5305、卡铂和这两种药剂的组合的体内抗肿瘤效果。
[1]Coussy F,de Koning L,Lavigne M等人,A large collection ofintegrated genomically characterized patient-derived xenografts highlightingthe heterogeneity of triple-negative breast cancer[突出三阴性乳腺癌的异质性的整合基因组表征的患者来源的异种移植物的大集合].Int J Cancer.[国际癌症杂志]2019;145(7):1902-1912.doi:10.1002/ijc.32266
[2]LC Riches(2020)Mol Cancer Ther[分子癌症治疗]2020;19∶13-25
实例3
进行此研究,从而在BRCA1突变体肿瘤模型(SUM149PT,体内)中研究AZD5305与卡铂组合的抗肿瘤效果。研究设计中包括AZD5305单一疗法臂和卡铂单一疗法臂作为对照。
材料和方法
将SUM149PT细胞(2×10
通过比较对照组和治疗组的肿瘤体积的平均变化来评估从治疗开始的肿瘤生长抑制,并且表示为肿瘤生长抑制(TGI,当TV≥起始TV时)或消退(reg,当TV<起始TV时)百分比。还针对所有组计算从治疗开始的平均体重变化百分比。使用单尾t检验来评估统计学显著性。统计学显著性表示如下:*p≤0.05,**p≤0.01,***p≤0.001。
在开始功效研究之前,在SCID雌性小鼠中,使用按10mg/kg PO QD的AZD5305与按50mg/kg IP QW的卡铂的组合进行耐受性研究,并且未显示对动物总体状况的不良影响或体重的显著变化。
测试材料的配制
将AZD5305配制为用于在水/HCl pH3.5-4媒介物中口服给药,按0.1ml/10g剂量体积施用。伴随搅拌/涡旋/超声处理,通过添加适当体积的1N HCl至约1:1.25药物/HCl摩尔比,和80%最终体积的无菌去离子水来稀释固体,直至获得溶液。根据以下方程式计算所需的1N HCl的体积:
添加的1N HCl的体积(ml)=1.25×[浓度(mg/ml)÷406.48(g/摩尔)÷1M]×最终体积(ml)
用1N HCl或1N NaOH将溶液的pH调节至3.5-4。使用无菌的注射用水或去离子水补足最终体积,并且测量和记录最终pH。每周一次配制给药制剂,并且避光保存。
在给药的每一天,通过在0.9%NaCl中稀释储备溶液至3.75mg/ml用于37.5mg/kg剂量(0.1ml/10g剂量体积)新鲜地配制卡铂(西格玛奥德里奇公司(Sigma Aldrich))。
结果
在SUM149PT TNBC BRCAlm异种移植物模型中,在功效研究中,按0.1、0.03和0.01mg/kg QD的AZD5305和按37.5mg/kg QW的卡铂作为单一疗法和组合进行测试。在整个研究持续期间(28天),所有治疗均耐受性良好,并且没有观察到显著的体重减轻(图5)。AZD5305单一疗法显示了剂量依赖性抗肿瘤功效,分别在0.1mg/kg QD和0.03mg/kg QD的情况下产生了24%TGI和9%TGI。按0.01mg/kg QD给药AZD5305并不抑制肿瘤生长。卡铂单一疗法产生了61%TGI。0.1mg/kg AZD5305和卡铂的组合展示了组合益处,并且产生了86%TGI。甚至在与卡铂组合的AZD5305的剂量水平减少至0.03mg/kg或0.01mg/kg时,维持了此抗肿瘤效果(分别是75%TGI和79%TGI)(图6和表3)。
总之,在SUM149PT异种移植物体内模型中,与单一疗法组相比,AZD5305与卡铂组合展示了改善的抗肿瘤效果。将与卡铂组合的AZD5305的剂量水平降低10倍(从0.1mg/kg至0.01mg/kg)并不影响肿瘤生长抑制效果。
表3在SUM149PT异种移植物模型中,AZD5305、卡铂和这两种药剂的组合的体内抗肿瘤效果的总结。
实例4
进行此研究,从而在BRCA1/2野生型肿瘤模型(HBCx-9,体内)中研究一定剂量范围的AZD5305与卡铂组合的抗肿瘤效果。研究设计中包括AZD5305单一疗法臂和卡铂单一疗法臂作为对照。
材料和方法
HBCx-9是XenTech公司建立的患者源性肿瘤外植体(PDX)模型,无需先前进行体外培养。将肿瘤碎片皮下移植(SC)到供体小鼠上。当肿瘤体积达到1008至1764mm3时,处死供体小鼠,并且无菌切除肿瘤并且解剖。在取出坏死区域后,将肿瘤切成大小为大约20mm3的碎片,并且转移到培养基中,之后SC移植到受体(实验)雌性裸小鼠中。通过双边游标卡尺测量,每周两次测量肿瘤(长度x宽度),并且使用椭圆公式(π/6×宽度×宽度×长度)计算肿瘤体积。在整个研究期间,监测动物体重和肿瘤情况。当平均肿瘤体积达到大约110mm3时,将小鼠随机分配到治疗组中。从随机化后的第二天开始对动物进行治疗。每天一次(QD)口服(PO)媒介物(用HCl酸化至pH3.5-4的去离子水)治疗对照动物。按1、0.1、或0.01mg/kgPOQD给药AZD5305。按50mg/kg每周一次(QW)IP给药卡铂。在组合组中,小鼠首先给药卡铂,随后在10分钟内施用AZD5305。
通过比较对照组和治疗组的肿瘤体积的平均变化来评估从治疗开始的肿瘤生长抑制,并且表示为肿瘤生长抑制(TGI,当TV≥起始TV时)或消退(reg,当TV<起始TV时)百分比。还针对所有组计算从治疗开始的平均体重变化百分比。使用单尾t检验来评估统计学显著性。统计学显著性表示如下:*p≤0.05,**p≤0.01,***p≤0.001。
在开始功效研究之前,在SCID雌性小鼠中,使用按10mg/kg POQD的AZD5305与按50mg/kg IP QW的卡铂的组合进行耐受性研究,并且未显示对动物总体状况的不良影响或体重的显著变化。
在甲苯噻嗪-氯胺酮麻醉下通过心脏穿刺收集400-600μL的全血获得血浆PK的样品。将血液转移到具有分离器凝胶管的BD Microtainer Hep-Li中,并且在4℃下以5000RPM离心5-10分钟。收集分离的血浆,并且在-80℃下储存。为了确定血浆样品中的化合物水平,使用适当的稀释因子制备每种血浆样品(25μl),并且与在DMSO中制备并且掺入空白血浆中的11点标准校准曲线(1-10000nM)进行比较。与内标一起添加乙腈(100μl),随后在3000RPM下离心10分钟。然后在300μl水中稀释上清液(50μl),并且经由UPLC-MS/MS进行分析。
测试材料的配制
将AZD5305配制为用于在水/HCl pH3.5-4媒介物中口服给药,按0.1ml/10g剂量体积施用。伴随搅拌/涡旋/超声处理,通过添加适当体积的1N HCl至约1∶1.25药物/HCl摩尔比,和80%最终体积的无菌去离子水来稀释固体,直至获得溶液。根据以下方程式计算所需的1N HCl的体积:
添加的1N HCl的体积(ml)=1.25×[浓度(mg/ml)÷406.48(g/摩尔)÷1M]×最终体积(ml)
用1N HCl或1N NaOH将溶液的pH调节至3.5-4。使用无菌的注射用水或去离子水补足最终体积,并且测量和记录最终pH。每周一次配制给药制剂,并且避光保存。
在给药的每一天,通过在0.9%NaCl中稀释储备溶液至5mg/ml,用于50mg/kg剂量(0.1ml/10g剂量体积),新鲜地配制卡铂(山德士公司(Sandoz))。
结果
HBCx-9是可从法国XenTech公司获得的TNBC PDX模型。已经将其报告为具有BRCA1甲基化以及“BRCAness特征”的BRCA1/2Wt模型[1]。HBCx-9还显示对奥拉帕尼单一疗法具有中度敏感性[2]。
在功效研究中,按1、0.1、和0.01mg/kg QD的AZD5305和按50mg/kg QW的卡铂作为单一疗法和组合进行测试。在整个研究持续期间(28天),所有治疗均耐受性良好,并且没有观察到显著的体重减轻(图7)。AZD5305单一疗法显示了剂量依赖性抗肿瘤功效,分别在1、0.1、和0.01mg/kg QD的情况下,产生了66%、44%、和7%TGI。卡铂单一疗法产生了68%TGI。用1mg/kg AZD5305和卡铂进行治疗展示了组合益处,并且产生了90%消退。甚至在与卡铂组合的AZD5305的剂量水平减少至0.1mg/kg时,维持了此抗肿瘤效果(86%消退)。当卡铂与0.01mg/kg的AZD5305组合时,效果略微变差(49%TGI)。然而,甚至这一组与任一单一疗法臂相比时,产生了组合益处(图8和表4)。
在此实验中,继续治疗28天,然后在停止治疗后监测应答持续时间。图3中小图描绘了最有效的组(卡铂与按1或0.1mg/kg的AZD5305组合),在约49天时(在治疗停止后3周)肿瘤开始再生长,并且再生长率在两个组中是类似的。另外,在卡铂+0.01mg/kgAZD5305组中,在治疗中止后约2周肿瘤开始再生长,图9。
总之,在HBCx-9PDX体内模型中,与单一疗法组相比,AZD5305与卡铂组合展示了改善的抗肿瘤效果。将与卡铂组合的AZD5305的剂量水平降低10倍(1mg/kg至0.1mg/kg)并不影响肿瘤消退效果。表4在HBCx-9模型中,AZD5305、卡铂和这两种药剂的组合的体内抗肿瘤效果的总结。
***********
本书面描述使用实例来披露本发明并使本领域技术人员能够实践本发明,包括制造和使用任何本披露的盐、物质或组合物,以及进行任何本披露的方法或过程。本发明的可取得专利的范围由权利要求书限定,并且可以包括本领域技术人员想到的其他实例。如果此类其他实例具有与权利要求书的文字语言无差异的元素,或者如果它们包括与权利要求书的文字语言存在非实质性差异的等同元素,则这些实例旨在涵盖在权利要求书的范围内。虽然本说明书中示出并描述了本发明的优选实施例,但此类实施例仅以实例的方式提供,并且不旨在以其他方式限制本发明的范围。在实施本发明时,可以采用本发明的所述实施例的各种替代选择。本节和整个披露中使用的章节标题不旨在进行限制。
上述所有参考文献(专利和非专利)均通过引用并入本专利申请。对这些参考文献的讨论仅是旨在概述其作者所作的断言。不承认任何参考(或任何参考文献的一部分)是相关的现有技术(或是现有技术)。申请人保留质疑引用的参考文献的准确性和相关性的权利。
