一种天然低共熔溶剂在选择性提取花色苷以及保存花色苷中的应用
文献发布时间:2023-06-19 10:16:30
技术领域
本发明涉及食品科学与工程技术领域,尤其涉及一种天然低共熔溶剂在选择性提取花色苷以及保存花色苷中的应用。
背景技术
花色苷属于黄酮类化合物,广泛存在于人们日常消费的水果、蔬菜及杂粮中。根据具体花色苷的种类及条件,花色苷可呈现多种颜色,并且其安全无毒,同时具有抗氧化、抗炎、抗癌、降血糖、降血脂、保护内脏器官免受氧化应激损伤、抑制肥胖等广泛的生理活性。近年来越来越多的被用到食品加工领域用于替代传统人工合成色素。部分来源的花色苷已经被列入中国食品添加剂的国家标准中(GB2760-2014),可依标准添加至糕点、果冻、软饮料、调制酒、冷冻饮品等食品中。此外,由于其具有一定的保健价值,常常被添加到功能性食品或保健品中,提高商品色泽的同时提高了产品的商业附加值。
根据花色苷B环羟基化和甲基化的程度,可将花色苷分成六大类。飞燕草素-3-半乳糖苷、飞燕草素-3-阿拉伯糖苷以及锦葵色素-3-阿拉伯糖苷均是较为常见的膳食花色苷,但目前现有的提取工艺对花色苷缺乏选择性,或多集中于矢车菊素-3-葡萄糖苷的提取制备,对于飞燕草素-3-半乳糖苷、飞燕草素-3-阿拉伯糖苷和锦葵色素-3-阿拉伯糖苷具有较强选择性的绿色经济的提取方案仍然鲜见报道。
目前市面上现行的花色苷类物质提取技术还多集中于传统的有机溶剂提取的方法,通常会导致提取效率较低,环境污染以及提取溶剂的残留对人身健康造成潜在的危害。天然低共熔溶剂是一种新型的绿色提取溶剂,由于其无挥发,不可燃,常温下稳定,并且是基于存在于众多细胞和组织的天然成分,因此通常被认为是传统提取溶剂的良好替代品。此外,由于天然低共熔溶剂的氢键供体和氢键受体分子种类众多,可以通过不同的氢键供体-受体组合方案定制出具有不同极性、溶解性等理化特性的溶剂;同时,花色苷类物质的稳定性比较差,很容易被环境中的各种因素(如温度、pH、氧气、光照等)诱导发生化学变化,从而影响其呈色表现以及生理活性。超声辅助提取是一种常用于花色苷类物质提取的技术,然而其存在超声探头附近局部高温过热的问题难以解决,因此在提取过程中也造成了大量花色苷的损失。此外,在单元化操作的后续处理过程中,也经常会有高温加热、改变pH及光照等环境的场景,因此,提取技术在具有一定选择性的基础上,对花色苷具有在复杂环境下提高稳定性的作用,在该领域的科研以及产业界也受到了广泛的关注。
目前急需一种对飞燕草素-3-半乳糖苷、飞燕草素-3-阿拉伯糖苷和锦葵色素-3-阿拉伯糖苷均具有较强选择性,并且可以有效保护其稳定性的提取方法。
发明内容
本发明提供了一种天然低共熔溶剂在选择性提取花色苷中的应用,该天然低共熔溶剂对飞燕草素-3-半乳糖苷、飞燕草素-3-阿拉伯糖苷和锦葵色素-3-阿拉伯糖苷均具有较强选择性,并且可以有效提高其稳定性。
本发明的技术方案如下:
一种天然低共熔溶剂在选择性提取花色苷中的应用,包括:
(1)将鲜榨后的蓝莓果渣冷冻、冻干、破碎研磨,得到蓝莓果渣粉末;
(2)将天然低共熔溶剂的水溶液与蓝莓果渣粉末混合均匀,在超声和水浴加热条件下提取蓝莓果渣粉末中的花色苷,经离心、收集上清液,得到花色苷粗提液;
所述的天然低共熔溶剂中包含氯化胆碱、草酸,以氯化胆碱作为氢键受体,以草酸作为氢键供体;氯化胆碱与草酸的摩尔比为1:0.5-2;
所述的天然低共熔溶剂的水溶液中,水与天然低共熔溶剂的质量比为10-50%;
(3)所述的花色苷粗提液经固相萃取,得到花色苷纯化液,经浓缩干燥即可得到以飞燕草素-3-半乳糖苷、飞燕草素-3-阿拉伯糖苷和锦葵色素-3-阿拉伯糖苷为主要成分的花色苷。
本发明的天然低共熔溶剂对飞燕草素-3-半乳糖苷、飞燕草素-3-阿拉伯糖苷和锦葵色素-3-阿拉伯糖苷具有较强的选择性,可选择性地从蓝莓果渣中提取以飞燕草素-3-半乳糖苷、飞燕草素-3-阿拉伯糖苷和锦葵色素-3-阿拉伯糖苷为主要成分的花色苷。
优选的,所述的天然低共熔溶剂的水溶液中,水与天然低共熔溶剂的质量比为30-35%。
优选的,在制备天然低共熔溶剂的水溶液的过程中,采用75-85℃水浴加热,并不断搅拌,以避免天然低共熔溶剂局部变性。
优选的,步骤(1)中,避光条件下冷冻蓝莓果渣,在-15~-60℃下预冻12-24小时,然后真空冷冻干燥24~36小时。
优选的,步骤(2)中,天然低共熔溶剂的水溶液与蓝莓果渣粉末的液固比为50~70mL/g。
优选的,步骤(2)中,将天然低共熔溶剂的水溶液与蓝莓果渣粉末混合时,在30-50℃下水浴预热3-10min,以使蓝莓果渣粉末在天然低共熔溶剂的水溶液中扩散均匀。
优选的,步骤(2)中,超声功率为240-360W,超声提取时间为1-9min;水浴加热温度为65-85℃。
本发明还提供了所述的天然低共熔溶剂在保存花色苷中的应用,包括将花色苷溶解于天然低共熔溶剂的水溶液中。
本发明的天然低共熔溶剂可显著提升花色苷在高温、不同pH环境、不同光照条件下的稳定性,抑制花色苷的降解。
本发明的天然低共熔溶剂对飞燕草素-3-半乳糖苷、飞燕草素-3-阿拉伯糖苷和锦葵色素-3-阿拉伯糖苷均具有较强选择性,并且可以有效提高其稳定性,不仅可以克服传统提取溶剂的低效、污染环境和残留对人体健康的潜在危害等缺点,同时对提取目标物更具针对性,并且有效保护了提取过程中以及后续加工储存过程中目标物的稳定性,对产业提质增效,构建绿色经济和可持续发展型社会有重要意义。
与传统的酸化水溶液或酸化乙醇溶液作为提取溶剂相比,本发明的有益效果为:
(1)本发明的天然低共熔溶剂可以显著提高蓝莓果渣中飞燕草素-3-半乳糖苷、飞燕草素-3-阿拉伯糖苷和锦葵色素-3-阿拉伯糖苷的选择性和提取效率;
(2)本发明的天然低共熔溶剂显著提升了提取的花色苷在高温、不同pH环境、不同光照条件下的稳定性,抑制花色苷的降解,在作为提取方案基础上,还可同时作为提取花色苷的保存、保护方案;
(3)本发明的提取方法中用到的溶剂为经过优化筛选的天然低共熔溶剂,在提高提取效率的同时保证了提取绿色、安全、对环境无污染,并且成本低廉,适合规模化放大;
(4)相较于其他方法而言,本发明采用的方法操作简单、易于培训和使用,同时过程耗时短,能耗低。
附图说明
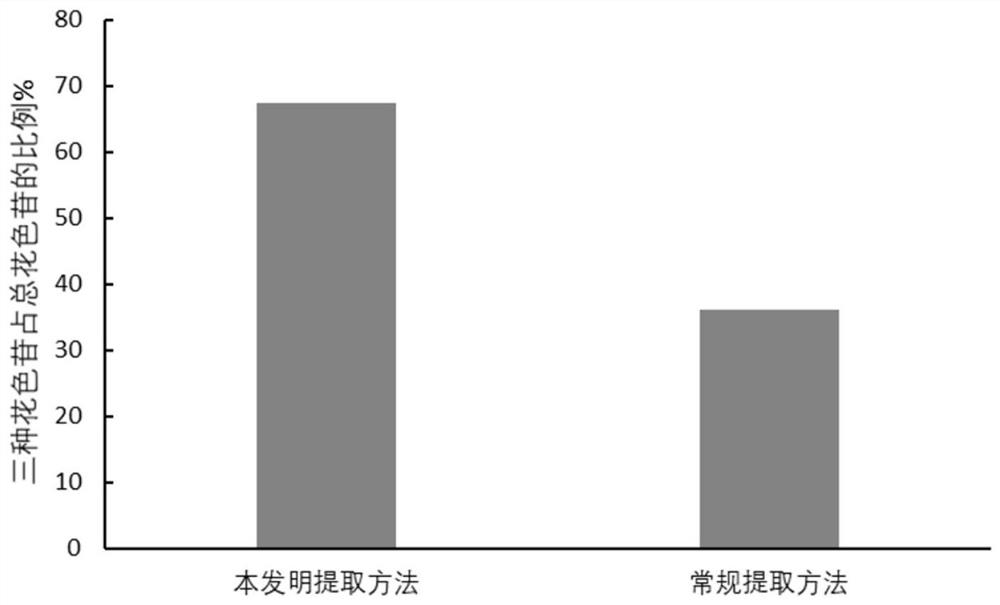
图1为不同提取方法提取蓝莓花色苷中飞燕草素-3-半乳糖苷/阿拉伯糖苷和锦葵色素-3-阿拉伯糖苷占总花色苷的比例比对比图;
图2为不同提取方法提取蓝莓花色苷中飞燕草素-3-半乳糖苷/阿拉伯糖苷和锦葵色素-3-阿拉伯糖苷的总量对比图;
图3为不同提取方法的溶剂中花色苷在各温度下的降解图;
图4为不同提取方法的溶剂中花色苷在个pH环境下的降解图;
图5为不同提取方法的溶剂中花色苷在不同光照环境下的降解图。
具体实施方式
实施例1
本实施例提供一种从蓝莓果渣中有较强选择性的同时提取飞燕草素-3-半乳糖苷/阿拉伯糖苷和锦葵色素-3-阿拉伯糖苷,并同时可以保护其稳定性的方法,包括如下步骤:
步骤(1):将鲜榨后的蓝莓果渣冷冻,且温度为-20℃预冻24小时,然后在大型冻干机中真空冷冻干燥36小时,破碎研磨,全程避光;
步骤(2):采用氯化胆碱作为氢键受体,采用草酸作为氢键供体,二者摩尔比为2:1,需采用水浴加热80℃并不停搅拌,避免局部变性,得到澄清透明且均一的液体(天然低共熔溶剂)后,加水量为30%(w/w,水与天然低共熔溶剂的质量比),与步骤(1)中的样品粉末混合,液固比为50mL/g,且需要在45℃水浴预热5min,使样品粉末在天然低共熔溶剂中扩散均匀;
步骤(3):在脉冲式超声破碎机的辅助下进行提取,超声功率在300W,超声提取时间为3min,循环水浴温度控制在73℃,经离心、收集上清液,得到以目标花色苷飞燕草素-3-半乳糖苷/阿拉伯糖苷和锦葵色素-3-阿拉伯糖苷为主要花色苷的粗提液,同时也可直接作为花色苷的原位保存手段;
步骤(4):经C18固相萃取柱吸附、解吸,纯化粗提液,即可得到飞燕草素-3-半乳糖苷/阿拉伯糖苷和锦葵色素-3-阿拉伯糖苷为主要成分的花色苷纯化液,经浓缩干燥即可得到目标产品。
实施例2
本实施例提供一种从蓝莓果渣中有较强选择性的同时提取飞燕草素-3-半乳糖苷/阿拉伯糖苷和锦葵色素-3-阿拉伯糖苷,并同时可以保护其稳定性的技术方案,包括如下步骤:
步骤(1):将鲜榨后的果渣冷冻,且温度为-40℃预冻24小时,然后在大型冻干机中真空冷冻干燥36小时,破碎研磨,全程避光;
步骤(2):采用氯化胆碱作为氢键受体,采用草酸作为氢键供体,摩尔比为1:1,需采用水浴加热80℃并不停搅拌,避免局部变性,得到澄清透明且均一的液体后,加水量为30%(w/w),与步骤(1)中的样品粉末混合,液固比为60mL/g,在45℃预热5min,使样品粉末在天然低共熔溶剂中扩散均匀;
步骤(3):在脉冲式超声破碎机的辅助下进行提取,超声功率在325W,超声提取时间为3min,循环水浴温度控制在76℃,经离心、收集上清液,得到以目标花色苷飞燕草素-3-半乳糖苷/阿拉伯糖苷和锦葵色素-3-阿拉伯糖苷为主要花色苷的粗提液,同时也可直接作为花色苷的原位保存手段;
步骤(4):经C18固相萃取柱吸附、解吸,纯化粗提液,即可得到飞燕草素-3-半乳糖苷/阿拉伯糖苷和锦葵色素-3-阿拉伯糖苷为主要成分的花色苷纯化液,经浓缩干燥即可得到目标产品。
实施例3
本实施例提供一种从蓝莓果渣中有较强选择性的同时提取飞燕草素-3-半乳糖苷/阿拉伯糖苷和锦葵色素-3-阿拉伯糖苷,并同时可以保护其稳定性的技术方案,包括如下步骤:
步骤(1):将鲜榨后的果渣冷冻,且温度为-60℃预冻24小时,然后在大型冻干机中真空冷冻干燥24小时,破碎研磨,全程避光;
步骤(2):采用氯化胆碱作为氢键受体,采用草酸作为氢键供体,摩尔比为1:2,需采用水浴加热80℃并不停搅拌,避免局部变性,得到澄清透明且均一的液体后,加水量为30%(w/w),与步骤(1)中的样品粉末混合,液固比为60mL/g,在40℃预热8min,使样品粉末在天然低共熔溶剂中扩散均匀;
步骤(3):在脉冲式超声破碎机的辅助下进行提取,超声功率在340W,超声提取时间为4min,循环水浴温度控制在78℃,经离心、收集上清液,得到以目标花色苷飞燕草素-3-半乳糖苷/阿拉伯糖苷和锦葵色素-3-阿拉伯糖苷为主要花色苷的粗提液,同时也可直接作为花色苷的原位保存手段;
步骤(4):经C18固相萃取柱吸附、解吸,纯化粗提液,即可得到飞燕草素-3-半乳糖苷/阿拉伯糖苷和锦葵色素-3-阿拉伯糖苷为主要成分的花色苷纯化液,经浓缩干燥即可得到目标产品。
实施例4
本实施例提供一种从蓝莓果渣中有较强选择性的同时提取飞燕草素-3-半乳糖苷/阿拉伯糖苷和锦葵色素-3-阿拉伯糖苷,并同时可以保护其稳定性的技术方案,包括如下步骤:
步骤(1):将鲜榨后的果渣冷冻,且温度为-60℃预冻24小时,然后在大型冻干机中真空冷冻干燥24小时,破碎研磨,全程避光;
步骤(2):采用氯化胆碱作为氢键受体,采用草酸作为氢键供体,摩尔比为1:1,需采用水浴加热80℃并不停搅拌,避免局部变性,得到澄清透明且均一的液体后,加水量为35%(w/w),与步骤(1)中的样品粉末混合,液固比为65mL/g,在45℃预热6min,使样品粉末在天然低共熔溶剂中扩散均匀;
步骤(3):在脉冲式超声破碎机的辅助下进行提取,超声功率在350W,超声提取时间为4min,循环水浴温度控制在80℃,经离心、收集上清液,得到以目标花色苷飞燕草素-3-半乳糖苷/阿拉伯糖苷和锦葵色素-3-阿拉伯糖苷为主要花色苷的粗提液,同时也可直接作为花色苷的原位保存手段;
步骤(4):经C18固相萃取柱吸附、解吸,纯化粗提液,即可得到飞燕草素-3-半乳糖苷/阿拉伯糖苷和锦葵色素-3-阿拉伯糖苷为主要成分的花色苷纯化液,经浓缩干燥即可得到目标产品。
为了验证本发明的技术效果,现以下述实验为例进行说明:
1、在不同的提取条件下对飞燕草素-3-半乳糖苷/阿拉伯糖苷和锦葵色素-3-阿拉伯糖苷(简称三种花色苷,下同)的提取效果进行比较。
将常规提取方法(溶剂为0.1%酸化乙醇(简记为ethanol),提取温度70℃,超声功率325W,提取时间4min,液固比60mL/g)与本发明的提取方法(溶剂为30%含水量(w/w)且摩尔比为1:1的氯化胆碱-草酸天然低共熔溶剂(简称ChOa),提取温度70℃,超声功率325W,提取时间4min,液固比60mL/g)分别对相同蓝莓果渣样品进行提取,结果如图1,图2所示。
由图1,图2可以看出,本发明的提取方法可以极大提升三种目标花色苷占总花色苷的比重,并且三种目标花色苷的含量是常规超声辅助提取方法的三倍以上。
2、在不同提取方法的溶剂中花色苷在不同温度、pH和光照环境下的降解对比。
将常规提取方法(溶剂为0.1%酸化乙醇(简记为ethanol),提取温度76℃,超声功率325W,提取时间3min,液固比60mL/g)与本发明的提取方法(溶剂为30%含水量(w/w)且摩尔比为1:1的氯化胆碱-草酸天然低共熔溶剂(简称ChOa),提取温度76℃,超声功率325W,提取时间3min,液固比60mL/g)分别对相同蓝莓果渣样品进行提取,得到提取液后,分别在不同温度(-4~80℃),不同pH(pH1~6),不同光照条件(避光、室内荧光灯管自然照明、夏日太阳光)进行稳定性测试,结果如图3、图4、图5所示。
由图3、图4、图5可以看出,本发明的提取方法采用的溶剂可以有效保护花色苷在高温、不同pH环境以及光照环境中的稳定性,其同样条件下的降解速率较传统酸化乙醇溶液被极大降低。因此本发明的提取方法中采用的溶剂可以有效降低提取过程中超声探头局部高温对花色苷造成的损失,同时,其作为提取后花色苷的保存溶液也具有极大优势。
以上所述的实施例对本发明的技术方案和有益效果进行了详细说明,应理解的是以上所述仅为本发明的具体实施例,并不用于限制本发明,凡在本发明的原则范围内所做的任何修改、补充和等同替换等,均应包含在本发明的保护范围之内。
- 一种天然低共熔溶剂在选择性提取花色苷以及保存花色苷中的应用
- 一种天然低共熔溶剂在选择性提取花色苷以及保存花色苷中的应用
