一种用于防治植物真菌病害的化合物及其制备方法
文献发布时间:2024-04-18 20:01:23
技术领域
本发明涉及一种防治植物真菌病害的化合物及其制备方法,属于农药和化学领域。
背景技术
琥珀酸脱氢酶(SDH)抑制剂通过作用于病原菌线粒体呼吸电子传递链上的复合体II(也称琥珀酸脱氢酶或琥珀酸泛醌还原酶)干扰呼吸电子传递链上琥珀酸脱氢酶来抑制线粒体功能,阻止其产生能量,抑制病原菌生长,最终导致其死亡,以达到防治病害的目的,例如3-(二氟甲基)-1-甲基-N-[2-(3,4,5-三氟苯基)苯基]-1H-吡唑-4-甲酰胺(通用名为氟唑菌酰胺)可用于防治多种植物病原真菌。SDH抑制剂因其高效、广谱的杀菌活性和相对较低的抗性风险,近年来已经成为最有发展前景的一类杀菌剂。
氟唑菌酰胺
色胺(Tryptamine),化学名为3-(2-胺乙基)吲哚,色胺系列衍生物由于其结构的特殊性使其在中枢神经系统方面有巨大的生理、药理特性,可形成了许多药物化合物的骨架,例如致幻剂麦角酰二乙胺(LSD)、抗疟原虫药螺吲哚酮(Yeung等人,2010,J MedChem.53:5155-5164),痛觉螺环己烷衍生物,以及法尼酯X受体拮抗剂氮杂卓并吲哆(azepinoindole)衍生物。之前文献报道了其在抗偏头痛方面的应用,例如舒马坦,利扎普坦等上市药物,也可用于合成长春胺、长春西汀等吲哚类生物碱。
基于色胺结构的衍生物如5-羟色胺,在植物中可以作为一种信号分子,通过调节植物体内活性氧的水平来调节植物的生长、发育以及对生物、非生物胁迫的响应。研究发现,5-羟色胺可以通过改变活性氧的水平以及茉莉酸乙烯信号转导来调节拟南芥根系的发育。在盐胁迫下,5-羟色胺可以通过降低过氧化氢和丙二醛的含量来提高的油菜的耐盐性。
基于色胺结构的衍生物如褪黑素(N-acetyl-5-methoxytryptamine),可用做保健品用于调节人类睡眠、视网膜生理、增强免疫和抗衰老等,在人类中的研究和应用较为成熟,且目前已经实现商业化。在植物中也参与生长调节、逆境胁迫和生物胁迫等重要生理过程。有研究表明褪黑素不仅对部分细菌病害和病毒病害有抑制作用,如由革兰氏阴性细菌黄单胞杆菌(Xanthomonasoryzaepv.oryzae)引起的水稻白叶枯病和由水稻矮缩病毒(Ricedwarfvirus)引起的水稻矮缩病。褪黑素对植物病原真菌也有抑制作用(CN114680114A)。
色胺本身是许多重要药物的化合物骨架,基于色胺结构的衍生物如5-羟色胺、褪黑素等也参与植物生长发育和逆境胁迫等重要生理过程,关于色胺及系列衍生物用于农用化学品,仅有部分文献报道用于防治部分细菌病害和病毒病害,针对常见经济作物植物病原真菌的防治方面的应用罕见文献报道。本发明通过将色胺与氟唑菌酰胺进行拼接并选取不同化学基团进行修饰,系统研究了化合物对植物病原真菌的防治作用,使其有望成为一类潜在的抑菌分子。
色胺及其衍生物
发明内容
本发明的第一个目的是提供一种化合物,该化合物是由色胺或其衍生物与氟唑菌酰胺进行拼接和结构修饰而得到,其结构式如下式(Ⅰ)所示:
其中,R
优选地,R
进一步优选地,R
本发明的第二个目的是提供一种式(Ⅰ)所示化合物的合成方法,该方法的合成路线如下:
在上述合成路线中,式II、式III、式IV、式V中的R
具体的合成步骤如下:
(1)在圆底烧瓶中加入N,N-二甲基甲酰胺,冰浴条件下,缓慢滴加三氯氧磷,滴加完毕后在0℃下继续反应0.5小时,将原料II溶于N,N-二甲基甲酰胺,缓慢滴入上述反应液中,在0℃下继续反应2小时,TLC监测反应直到反应完全;待反应完成后冰浴条件下向反应体系中加水淬灭反应,并2M NaOH调节pH至9,用乙酸乙酯萃取并合并有机相,干燥浓缩得到式III化合物;
(2)在N
(3)在N
(4)在N
(5)在N
本发明提供的化合物可用于防治植物真菌病害,所述植物真菌病害包括禾谷镰刀菌(Fusarium graminearum)、灰霉菌(Botrytis cinerea)、核盘菌(Sclerotiniasclerotiorum)、拟盘多毛孢(Pestalotiopsis)、桃褐腐病菌(Monilinia fructicola)、玉米小斑病菌(Bipolaris maydis)、立枯丝核菌(Rhizoctonia solani)、茶树链格孢病菌(Altermaria alternata)。
与现有技术相比,本发明具有以下优点:
本发明通过将已知的两类化合物进行结构拼接和修饰,提高了化合物对植物真菌病害的抑制活性,合成的化合物具有更多的修饰位点,这有利于化合物结构的进一步衍生化与多样化从而克服耐药性。该化合物既可单独使用,也可与其它化学农药组合、混配使用,能较大幅度提高农药药效、减少农药施用量。合成化合物所需的化学原料廉价易得,合成步骤相对简单,部分色胺衍生物中间体为已经商品化的产品,可降低投入成本、缩短研发周期。
附图说明
图1为化合物I-025的核磁共振谱图(氢谱)。
图2为化合物I-025的核磁共振谱图(碳谱)。
图3为化合物I-025的核磁共振谱图(氟谱)。
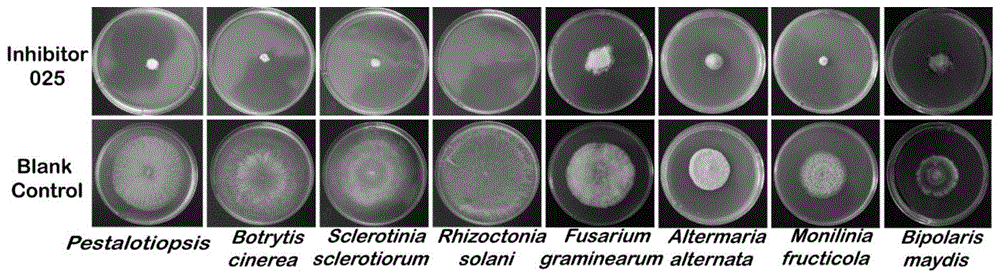
图4为200μM浓度下化合物I-025对8种常见经济作物真菌病害的抑制效果图。
图5为在100μM、50μM、25μM、12.5μM、6.25μM、3.125μM浓度下,化合物I-025对灰霉菌、核盘菌、立枯丝核菌3种真菌病害的抑制效果图。
图6为在100μM、400μM浓度下,化合物I-025对核盘菌侵染油菜叶片的抑制效果图。
图7为在100μM、200μM、400μM浓度下,化合物I-025对灰霉菌侵染番茄果实的抑制效果图。
具体实施方式
以下将通过具体实施例对本发明进行详细描述。但是本领域技术人员将会理解,下列实施方式和实施例仅用于说明本发明,而不应视为限制本发明的范围。基于本发明中的实施例,本领域普通技术人员在没有做出创造性劳动前提下所获得的所有其他实施例,都属于本发明保护的范围。实施例中如无特殊说明,使用的相关试剂均来源于商业渠道,所用的实验方法均为本领域常规实验方法。未注具体条件者,按照常规条件或制造商建议的条件进行。所用试剂或仪器未注明生产厂商者,均为可以通过市售购买获得的常规产品。
实施例1:化合物I-025的合成
(1)中间体(5,6-二氯-1H-吲哚-3-基)乙基胺的合成:
步骤a:Ⅲ-025中间体5,6-二氯吲哚-3-甲醛的合成:在N
步骤b:Ⅳ-025中间体的合成:在N
步骤c:Ⅴ-025中间体的合成:在N
(2)化合物I-025的合成:
步骤d:Ⅶ-025中间体的合成:在N
步骤e:I-025的合成:在N
N-(2-(5,6-dichloro-1H-indol-3-yl)ethyl)-1-methyl-3-(trifluoromethyl)-1H-pyrazole-4-car boxamide:
1
13
19
具体核磁共振谱见图1-3。
以上仅示出本发明其中一种具体化合物的合成工艺,通过以上相同的合成路线与原理,还可以合成其它一系列化合物,下表1为本发明合成的部分化合物
表1具体化合物种类及取代基
/>
实施例2化合物I-025对8种植物病害病原真菌的抑制活性测定
试验一、化合物对八种病原真菌的抑菌率测定
(1)植物病原真菌的培养:将病原真菌接种于PDA培养基上,置于25±0.1℃恒温培养箱中培养3-6天,菌丝长好后备用。
(2)离体抑制活性采用菌丝生长速率法测定:将供试化合物和对照药剂用DMSO(二甲基亚砜)配制成20mM的药液,随后将计算量的药液与PDA培养基配制成测试浓度。以DMSO作为空白对照,啶酰菌胺和氟唑菌酰胺为阳性对照。将培养基在9cm培养皿中制备成平板、每个处理三个重复,接种5mm菌饼后置于25±0.1℃的恒温培养箱中。待空白对照培养皿中的菌落直径长至6-9cm左右后,用十字交叉法测量各处理及对照的菌落直径。
抑菌率的计算:菌落增长直径(mm)=菌落测量直径(mm)-菌饼直径(mm);
菌丝生长抑制率(%)=[空白对照菌落增长直径(mm)-含药培养基上菌落增长直径(mm)]/空白对照菌落增长直径(mm)*100%。
其中,立枯丝核菌(Rhizoctonia solani):配置PDA固体培养基,然后培养基中加入含色胺结构的琥珀酸脱氢酶衍生物,使它的终浓度为200μM,刮取5mm纹枯菌菌块上的菌丝放置于培养基中间,室温放置培养2-3天,计算抑菌率,每组3个重复。
禾谷镰刀菌(Fusarium graminearum)、灰霉菌(Botrytis cinerea)、核盘菌(Sclerotinia sclerotiorum)、拟盘多毛孢(Pestalotiopsis)、桃褐腐病菌(Moniliniafructicola)、玉米小斑病菌(Bipolaris maydis)、茶树链格孢病菌(Altermariaalternata)等其它7种植物病原菌的测试方法,与以上立枯丝核菌(Rhizoctonia solani)的测试方法相同,不同的是,不同菌种的培养时间在3-7天不等。
化合物I-025、阳性对照对8种植物病害病原真菌的抑菌率结果见表1,其中的I-025抑菌效果见图4。从表1的结果可以看出,化合物I-025的抑菌活性普遍高于氟唑菌酰胺或褪黑素。
表1三种化合物对8种植物病害病原真菌的抑菌率
本实施例中涉及的马铃薯葡萄糖琼脂培养基PDA培养基配制:选取新鲜的马铃薯洗净去皮,再称取200g切成小块,加水煮烂(煮沸20-30分钟,能被玻璃棒戳破即可),用四层纱布过滤,加入20g D-glucose,搅拌均匀,稍冷却后再补足水分至1000mL,最后加15gAgar,高压灭菌115℃,20min。
试验二:化合物I-025对3种真菌病害的半数抑制浓度测定
抑制剂化合物I-025对灰霉菌(Botrytis cinerea)、核盘菌(Sclerotiniasclerotiorum)、立枯丝核菌(Rhizoctonia solani)3种真菌病害的抑制活性测定方法与实施案例3的测试方法相同,不同的是,供试化合物I-025药液与PDA培养基配制成100μM、50μM、25μM、12.5μM、6.25μM、3.125μM的测试浓度。计算抑制率,得到化合物I-025对灰霉菌、核盘菌、立枯丝核菌的半数抑制浓度分别为44.50±0.41μM、19.75±0.41μM、49.70±0.53μM。抑菌效果见图5。
试验三:化合物I-025对核盘菌真菌病害侵染油菜叶片的抑制效果测定
取新鲜采摘的油菜叶片洗净消毒,将浓度为100μM、400μM的化合物I-025溶液滴加在叶片中间,室温处理6-8小时后,用打孔器取8mm大小的核盘菌(Sclerotiniasclerotiorum)菌饼接种于叶片中央,25±0.1℃的恒温培养箱中培养2-3天,观测油菜叶片感染核盘菌的菌斑的大小,结果见图6。从图中可知,滴加I-025的叶片菌斑面积明显缩小,当化合物浓度为400μM时,叶片上基本没有菌斑。
试验四:化合物I-025对灰霉菌真菌病害侵染番茄果实的的抑制效果测定
在超市购买新鲜、大小均一的番茄果实洗净消毒晾干,用消毒的刀片在番茄表面划大小均一的十字形伤口,取抑制剂化合物I-025滴加到灰霉菌的孢子悬浮液中配制成100μM、200μM、400μM浓度的带药孢子悬浮液,取带药孢子悬浮液滴加到番茄表面的十字形伤口,25±0.1℃的恒温培养箱中培养2-3天,观测番茄表面感染灰霉菌的菌斑大小,结果见图7。从图中可知,化合物I-025能抑制灰霉菌对番茄果实的侵染且存在量效关系。
综上,本发明制备的化合物在体内和体外都对多种植物病原真菌表现了抑制活性,可用于制备新型杀菌剂,在提高病害防效方面具有重要意义。另外,由于化合物中的色胺结构具有更多的修饰位点,这有利于化合物结构的进一步衍生化与多样化,有利于克服耐药性。
- 一种2D-3D显示切换光学模组及其制备方法、显示装置
- 一种LED显示屏及LED显示屏模组
- 一种显示模组、显示装置及显示模组的制作方法
- 一种接收卡、数据存储调度方法及LED显示控制系统
- 一种LED显示模组控制系统及接收卡切换方法
