血中中性脂肪估计设备、血中中性脂肪估计方法以及程序
文献发布时间:2023-06-19 19:28:50
技术领域
本发明涉及血中中性脂肪估计设备、血中中性脂肪估计方法以及计算机程序。
背景技术
传统上,通过采集被检者的血液来测量血中中性脂肪是常见的。但是,在该方法中,需要将针或类似物侵入性地插入被检者的皮肤,给被检者造成心理或生理上的负担。作为非侵入性地估计血中中性脂肪的方法,专利文献1公开了通过用特定波长的光束照射指尖来估计血中中性脂肪的方法。
引用列表
专利文献
专利文献1:日本专利No.6241853
非专利文献
非专利文献1:Psychology Research and Behavior Management 2011:4 81-86,Summary of the clinical investigations E.S.Teck Complex March,20,2010要旨
非专利文献2:R.N.Chua,Y.W.Hau,C.M.Tiew and W.L.Hau,″Investigation ofAttention Deficit/Hyperactivity Disorder Assessment Using ElectroInterstitial Scan Based on Chronoamperometry Technique″,in IEEE Access,vol.7,pp.144679-144690,2019,doi:10.1109/ACCESS.2019.2938095.
非专利文献3:Maarek A.Electro interstitial scan system:assessment of10years of research and development.Med Devices(Auckl).2012;5:23-30.doi:10.2147/MDER.S29319
发明内容
技术问题
本发明旨在提供除了用特定波长的光束照射得到的脉波数据来非侵入性地准确地估计血中中性脂肪,还能够基于BMI、血压、心电图数据、生物阻抗等来估算血中中性脂肪的血中中性脂肪估计设备、血中中性脂肪估计方法以及计算机程序。
问题的解决方案
根据本发明的血中中性脂肪估计设备包括:信息获取单元,被配置为获取预定用户的属性信息和非侵入性生物信息;估计模型存储单元,被配置为存储血中中性脂肪估计模型;以及估计处理单元,被配置为,使用血中中性脂肪估计模型,基于预定用户的属性信息和/或非侵入性生物信息,计算预定用户的血中中性脂肪估计值。
该血中中性脂肪估计设备还包括:训练数据存储单元,被配置为存储训练数据集;以及学习处理单元,被配置为基于训练数据集通过机器学习来生成血中中性脂肪估计模型。
属性信息包括年龄和性别中的任意一个或组合,并且非侵入性生物信息包括BMI、血压、脉波数据、心电图数据和生物阻抗中的任意一个或组合。
训练数据集包括被检者的属性信息、非侵入性生物信息和血液测量的血中中性脂肪测量值。
血中中性脂肪估计值的对数与血中中性脂肪测量值的对数之间的相关系数等于或大于0.6。
估计处理单元计算血中中性脂肪风险估计值来代替血中中性脂肪估计值。
学习处理单元基于血液测量的血中中性脂肪测量值,向训练数据集提供表示血中中性脂肪风险的存在性的标签,并且当标签中具有血中中性脂肪风险的数据条数与不具有血中中性脂肪风险的数据条数之差等于或大于预定值时,学习处理单元增加训练数据集中的样本数据的条数来减小该差。
学习处理单元基于不同种类的训练数据集中的每一个训练数据集通过机器学习来生成第一血中中性脂肪风险估计模型和第二血中中性脂肪风险估计模型,并且估计处理单元使用第一血中中性脂肪风险估计模型和第二血中中性脂肪风险估计模型来计算预定用户的血中中性脂肪风险估计值。
该血中中性脂肪估计设备还包括生物信息估计单元,该生物信息估计单元被配置为估计生物信息中包括的BMI、血压、脉波数据、心电图数据和生物阻抗中的至少一个或多个生物信息,并且信息获取单元获取由生物信息估计单元估计的生物信息作为预定用户的生物信息。
一种非侵入性血中中性脂肪估计系统,包括:血中中性脂肪估计设备;以及被配置为测量非侵入性生物信息的生物信息测量设备。
根据本发明的血中中性脂肪估计方法包括:存储训练数据集的步骤,该训练数据集包括被检者的属性信息、非侵入性生物信息和血液测量的血中中性脂肪测量值;基于训练数据集通过机器学习来生成血中中性脂肪估计模型的步骤;以及使用血中中性脂肪估计模型,基于预定用户的属性信息和/或非侵入性生物信息,计算预定用户的血中中性脂肪估计值的步骤。
根据本发明的计算机程序使计算机执行:存储训练数据集的步骤,该训练数据集包括被检者的属性信息、非侵入性生物信息和血液测量的血中中性脂肪测量值;基于训练数据集通过机器学习来生成血中中性脂肪估计模型的步骤;以及使用血中中性脂肪估计模型,基于预定用户的属性信息和/或非侵入性生物信息,计算预定用户的血中中性脂肪估计值的步骤。
本发明的有益效果
根据本发明,可以使用非侵入性生物信息通过机器学习来极其准确地估计血中中性脂肪或血中中性脂肪风险。
附图说明
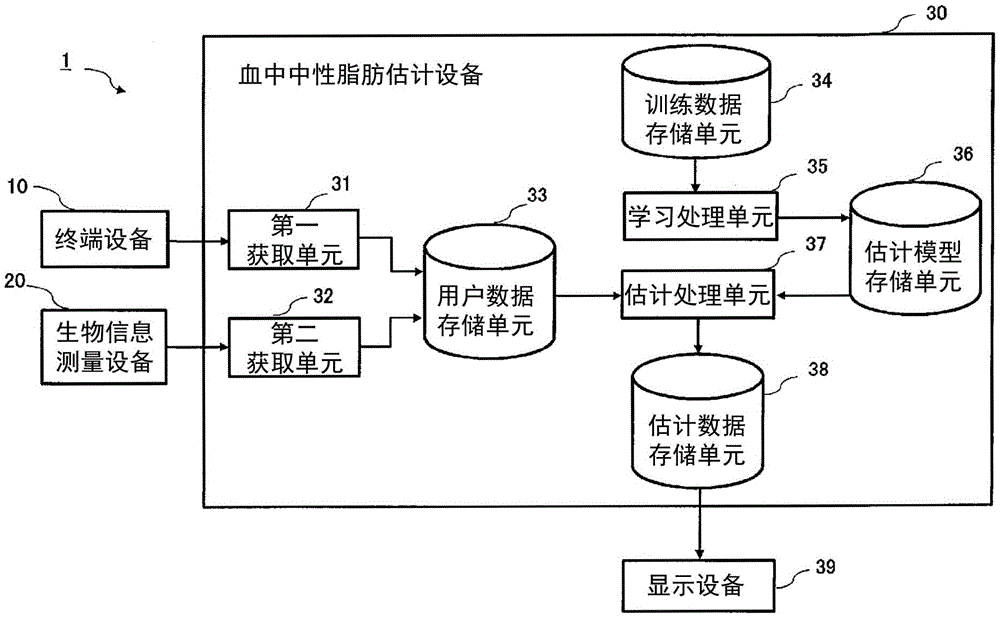
图1是示出了血中中性脂肪估计系统的示意性配置的框图。
图2是用于描述扫描电图(ESG)的图。
图3是血中中性脂肪估计设备的硬件配置图。
图4是示出了通过机器学习生成血中中性脂肪估计模型的执行过程的流程图。
图5是示出了用于血中中性脂肪估计的神经网络的分层结构。
图6是示出了血中中性脂肪估计处理的执行过程的流程图。
图7是示出了通过机器学习生成血中中性脂肪风险估计模型的执行过程的流程图。
图8示出了用于血中中性脂肪风险估计的第一神经网络的分层结构。
图9示出了用于血中中性脂肪风险估计的第二神经网络的分层结构。
图10是示出了血中中性脂肪风险估计处理的执行过程的流程图。
图11示出了示例2中的估计结果的ROC_AUC曲线。
图12示出了示例3中的估计结果的ROC_AUC曲线。
具体实施方式
下面将参照附图来描述实施例。注意,该实施例是示例性的并且本发明不限于以下描述的配置。
<设备功能>
下面,将参照图1至图6描述根据本实施例的血中中性脂肪估计系统1和血中中性脂肪估计设备30。图1是示出了根据本实施例的血中中性脂肪估计系统1的示意性配置的框图。血中中性脂肪估计系统1包括终端设备10、生物信息测量设备20、血中中性脂肪估计设备30和显示设备39。
“用户”是指使用血中中性脂肪估计系统来非侵入性地获得血中中性脂肪估计值或血中中性脂肪风险估计值的人。“被检者”是根据预定程序和协议提供诸如年龄或性别等属性信息、非侵入性生物信息、以及血液测量的血中中性脂肪测量值作为在血中中性脂肪估计系统中使用的训练数据集的人。
终端设备10可以是能够输入用户的属性信息(诸如姓名、ID、年龄或性别)并且可以通过有线或无线通信网络将输入信息输出到血中中性脂肪估计设备30的任何信息终端。终端设备10的示例包括便携式终端,其包括平板终端、智能手机和可穿戴终端,并且包括个人计算机(PC)。另外,也可以通过稍后描述的生物信息测量设备20来测量身高、体重等。
生物信息测量设备20测量用户的非侵入性生物信息。非侵入性生物信息是通过不需要将器械插入皮肤或身体的开口部分的方法而获取的生物信息。可以使用例如市售的身高计、体重计、血压计、脉搏血氧仪、脉波计、心电图机、阻抗测量仪或皮肤电测试仪来测量非侵入性生物信息。或者,可以使用能够同时测量脉波数据、心电图数据和生物阻抗的ES-TECK BC-3(Ryobi Systems株式会社)。这些设备可以测量非侵入性生物数据,不会给用户带来心理或生理上的负担。
在本发明实施例中,非侵入性生物信息包括身体质量指数(BMI)、血压、脉波数据、心电图数据、生物阻抗中的任意一个或组合。
BMI基于身高h[m]和体重w[kg]通过下式计算:
BMI=w/h
血压包括收缩压、舒张压、脉压和平均动脉血压中的任意一个或组合。
脉压通过下式计算。
脉压=收缩压-舒张压
平均动脉血压通过下式计算:
平均动脉血压=舒张压+脉压×1/3
通过使用脉波计或脉搏血氧仪用来自红色LED的红光(高达660nm)和来自IR LED的近红外光(高达905nm)照射诸如手指等突出的身体部位,并使用光电晶体管测量透射光,从而测量脉波数据。
脉波数据包括脉搏、弹性指数、外周血管阻力、加速度容积描记图、b/a、e/a、-d/a、光电容积描记图老化指数的Takazawa二阶导数、射血分数、LVET和重搏脉弹性指数(DEI)中的任意一个或组合。
弹性指数是通过将光电容积描记图中的高度除以从检测到收缩压峰值到检测到舒张压峰值的时间而获得的数值。外周血管阻力由“平均动脉血压”/“心输出量”×80来计算。重搏脉弹性指数(DEI)是舒张期血管弹性的指标,并且可以通过PWV测量设备进行测量。DEI在0.3至0.7是正常的,DEI在0.3或以下提示有高血压或动脉硬化的可能,而DEI在0.7或以上提示有急性焦虑症的可能。加速度容积描记图是光电容积描记图(PTG)的二阶导数(SDPTG)。加速度容积描记图由初始正波(a波)、初始负波(b波)、收缩中期再升高波(c波)、收缩晚期再下降波(d波)和舒张早期正波(e波)构成,而上述的b/a、e/a、-d/a是根据波高的比值计算出的。可以观察到,随着老化,b/a增大,c/a、d/a和e/a减小,因此血管的老化可以通过光电容积描记图老化指数(b-c-d-e)/a的Takazawa二阶导数来评估。射血分数是每次心跳时从心室转移的血液的比率,并且与光电容积描记图老化指数的二阶导数成正比。LVET是在主动脉瓣打开后左心室中的血液射出到主动脉的左心室射血时间。
心电图数据可以通过利用电极的心电描记法(ECG)或通过光电容积描记法(PPG)来测量。
心电图数据包括呼吸率、心率、心跳间距、心跳间距的标准差、MxDMn比、低频段功率谱、高频段功率谱、心率变化指标LF/HF、以及总功率中的任意一个或组合。心跳间距是心电图中从一个QRS波到下一QRS波的间距。MxDMn比是一个时间段内最长心跳间距与最短心跳间距的比,并且是心跳不规则的指标。总功率是功率谱在0到0.4Hz的频率(VLF、LF、HF)下测量两分钟的总功率的计算值。该值反映了整个自主神经活动以交感神经活动为主。
可以通过基于心电图计算功率谱密度来获取高频功率谱比(0.1875到0.50Hz;HF)、低频功率谱比(0.05到0.1875Hz;LF)、LF/HF比、以及极低频功率谱比(0到0.05Hz;VLF)。
生物阻抗(电导)例如可以通过在腿、手、左右前额六个部位处的电极中的两个电极之间生成小电流来测量。当电流在六个部位处的电极中的两个电极之间流动时,可以测量:(1)阳极/阴极电导(μS);(2)阴极/阳极电导(μS);(3)上述(1)中测量的电导与上述(2)中测量的电导之差(delta SCRA-SCRC);以及(4)电导率(μS/m)。此外,还可以同时测量肌肉质量、体脂量、总水分含量、相位角和电阻值。此外,可以测量右手与左手之间传导以及右前额与左前额之间传导的情况下的介电常数(μSi)。优选地,使用六个部位处的电极的22个传导模式来测量生物阻抗(电导)。
生物阻抗包括下述中的任意一个或组合:体脂量(kg)、体脂量(%)、去脂体重、去脂率、肌肉质量、总水分含量(kg)、总水分含量(%)、细胞内水分含量(%)、心输出量、1前额左侧-2左手/SCR A、1前额左侧-2左手/delta SCR C-SCR A、5左手-6左脚/delta SCR C-SCR A、13左脚-14右脚/SCR A、15右手-16前额左侧/delta SCR C-SCR A、15右手-16前额左侧SCR C、19右脚-20左手/delta SCR C-SCR A、ESG 2+4+15+17(μS/m)、ESG 6+13+19(%)、ESG 6+8+19+21(%)、ESG 6+8+19+21(μS/m)、ESG 9+10(μS/m)、ESG 9+10(%)、左脚电导、R(Ω)、相位角、前额路径的介电常数、前额路径电导率(9)、手到手路径的介电常数、手到手电导率(11、12)、以及单次输出量(心输出量/心率)。
SCR代表皮肤电导响应,而ESG代表扫描电图。ESG 2+4+15+17中的符号“+”表示贴在身体上并用于测量的电极。例如,ESG 2+4+15+17表示下述的平均值:当从左手传导至左前额时在左手处测量的电导值、当从右手传导至右前额时在右手处测量的电导值、当从右手传导至左前额时在右手处测量的电导值、以及当从左手传导至右前额时在左手处测量的电导值,如图2所示。非专利文献1中提供了这些电导值的详细描述。注意,在非专利文献2和3中描述了ESG(扫描电图)测量方法的细节。
值“1前额左侧-2左手/SCR A”是通过当电流在“1前额左侧”的阴极和“2左手”的阳极流动时的路径测量的电导(或电导率),而值“5左手-6左脚/delta SCR C-SCR A”是当“5左手”的阳极和“6左脚”的阴极之间进行传导时测量的电导值与在当“5左手”的阴极和“6左脚”的阳极之间进行传导时测量的电导值之差。
BMI和血压可以通过身高体重计和血压计来测量。
测量到的非侵入性生物信息通过有线或无线通信网络输出给血中中性脂肪估计设备30。生物信息测量设备20可以是固定式测量设备,也可以是诸如可穿戴终端等便携式测量设备。
血中中性脂肪估计设备30包括:第一获取单元31、第二获取单元32、用户数据存储单元33、训练数据存储单元34、学习处理单元35、估计模型存储单元36、估计处理单元37、以及估计数据存储单元38。第一获取单元31从终端设备10获取用户的属性信息。第二获取单元32从生物信息测量设备20获取用户的非侵入性生物信息。
用户数据存储单元33存储从第一获取单元31和第二获取单元32获取的用户的属性信息和非侵入性生物信息。
训练数据存储单元34存储多个训练数据集作为机器学习的训练数据集,每个训练数据集均由预先获取的多个被检者的属性信息、非侵入性生物体信息、以及通过血液检查获取的诸如血中中性脂肪的样本检查信息(测量值)组成。注意,样本检查信息还可以包括从血液、尿液、粪便等获取的检查信息。
学习处理单元35获取存储在训练数据存储单元34中的训练数据集,并使用训练数据集来生成血中中性脂肪估计模型。具体地,将获取的训练数据集归一化,通过神经网络(NN)、梯度提升(诸如XGBoost)、线性回归等的机器学习来学习属性信息、非侵入性生物信息与通过血液检查获得的血中中性脂肪之间的关系,并生成基于非侵入性生物信息来估计血中中性脂肪的估计模型。
估计模型存储单元36存储由学习处理单元35生成的血中中性脂肪估计模型。
非侵入性生物信息包括BMI、血压、脉波数据、心电图数据和生物阻抗中的任意一个或组合。
估计处理单元37使用学习处理单元35生成的估计模型,基于用户的属性信息和/或非侵入性生物信息来估计预定用户的血中中性脂肪。然后,血中中性脂肪估计值被存储在估计数据存储单元38中。
显示设备39可以显示血中中性脂肪估计值连同用户的属性信息和非侵入性生物信息。注意,这些数据可以显示在用户拥有的终端设备10上。
<设备硬件配置>
图3是血中中性脂肪估计设备30的硬件配置图。如图3所示,血中中性脂肪估计设备30被配置为包括一个或多个处理器301、存储器302、存储设备303、输入/输出端口304和通信端口305的计算机300。每个处理器301通过执行计算机程序来执行与根据本实施例的血中中性脂肪估计相关的处理。存储器302临时存储计算机程序和计算机程序的计算结果。存储设备303存储被配置为执行血中中性脂肪估计设备30的处理的计算机程序。存储设备303可以是任何计算机可读存储设备,例如可以是诸如磁盘、光盘、随机存取存储器、闪存、只读存储器等各种记录介质。输入/输出端口304执行从终端设备10和生物信息测量设备20输入信息以及向显示设备39输出血中中性脂肪估计值。通信端口305进行与未示出的信息终端(如其他计算机)的数据收发。可以通过无线通信方法和有线通信方法执行通信。另外,血中中性脂肪估计设备30可以由市售的台式PC或笔记本PC来实现,并且使用估计模型计算血中中性脂肪估计值的时间为数秒。
注意,上述第一获取单元31、第二获取单元32、学习处理单元35、估计处理单元37等在血中中性脂肪估计设备30的处理器301运行时发挥功能。
<通过机器学习生成血中中性脂肪估计模型>
图4是示出了通过机器学习生成血中中性脂肪估计模型的执行过程的流程图。
在步骤ST101处,学习处理单元35执行对输入数据(例如,上述训练数据集)的预处理。具体地,学习处理单元35将每个被检者的性别的属性信息转换为一位热码(One-hot)向量。此外,学习处理单元35通过yeo-johnson变换、boc-box变换等对除性别之外的属性信息、每个被检者的非侵入性生物信息、以及通过血液检查获得的血中中性脂肪测量值的对数进行归一化。
在步骤ST102处,学习处理单元35并行地执行通过线性回归、神经网络(NN)和梯度提升决策树的机器学习。注意,可以选择和使用线性回归、神经网络(NN)和梯度提升决策树中的任意一个或两个的组合。网格搜索可以用于梯度提升的超参数调整。
在通过梯度提升决策树的机器学习中可以使用诸如XGBoost、CatBoost和LightBGM等软件库。
在步骤ST103处,学习处理单元35还利用线性回归、神经网络(NN)和梯度提升决策树的学习结果来执行集成学习(岭回归)。注意,当在步骤ST102处选择线性回归、神经网络(NN)和梯度提升决策树中的任意一个时,在步骤ST103处的集成学习(岭回归)是不必要的。
学习处理单元35将上述学习处理生成的血中中性脂肪估计模型存储在估计模型存储单元36中。
例如,Python开源机器学习库Scikit-learn中提供的线性回归可以用于通过线性回归的机器学习。必要时可以通过主成分分析来减少维数。
注意,上述机器学习算法是示例性的并且本发明不限于此。
图5示出了用作估计模型的神经网络(NN)的结构。矩形表示执行数据转换的层组,并且圆角矩形表示输入/输出数据。“D”表示检查项目的数量。图5中的估计模型通过四个层组(编译A1到编译A3和编译B)按照D维、96维、96维、96维、一维的顺序转换数据。
如图5所示,编译A1到编译A3均包括执行全连接处理的全连接层“线性”、执行正则化的“内核正则化器”、和执行ReLU处理的“ReLU”层,而层组编译B包括全连接层“线性”和执行优化处理的“Adam”层。层组编译A1的全连接层的输入单元对应于输入层,层组编译B的输出单元对应于输出层,并且它们之间的每个单元对应于中间层(隐藏层)。中间层包括:用于将某个输入值限制为零并防止过度拟合的退出(dropout)层;以及用于在学习时对每个小批量(minibatch)执行归一化的批量归一化(BN)层。
当XGBoost用在通过梯度提升决策树的机器学习中时,计算通过血液检查获得的血中中性脂肪与血中中性脂肪估计值之间的残差,并调整XGBoost参数(max_depth、subsample、colsample_bytree和learning_rate)以最小化均方误差,从而生成估计模型。参数“max_depth”表示决策树的深度,参数“subsample”表示在每棵树上随机抽取的样本比率,参数“colsample_bytree”表示在每棵树上随机抽取的列的比率,而参数“learning_rate”表示学习率。在“max_depth”为1到10,“subsample”为0.1到1.0,“colsample_bytree”为0.3到1.0,以及“learning_rate”为0.1到0.7的范围下进行调整。
<使用血中中性脂肪估计模型的血中中性脂肪估计>
图6是示出了血中中性脂肪估计处理的执行过程的流程图。
在步骤ST201处,血中中性脂肪估计设备30的第一获取单元31从终端设备10获取用户的属性信息。在步骤ST202处,血中中性脂肪估计设备30的第二获取单元32获取用户的非侵入性生物信息。然后,将用户的属性信息和非侵入性生物信息存储在用户数据存储单元33中。接着,在步骤ST203处,估计处理单元37通过使用估计模型存储单元36中存储的血中中性脂肪估计模型来计算血中中性脂肪估计值。
在步骤ST204处,将计算出的血中中性脂肪估计值输出并存储在估计数据存储单元38中,并且在步骤ST205处,将血中中性脂肪估计值显示在诸如显示设备39的外部终端上。
<示例(血中中性脂肪估计)>
下面将描述本申请发明的实施例。然而,本发明不限于以下示例。
属性信息包括ID、姓名、年龄和性别中的任意一个或组合,并且非侵入性生物信息包括BMI、血压、脉波数据、心电图数据和生物阻抗中的任意一个或组合。作为BMI计算参考的身高和体重分别用身高计和体重计测量,而血压用血压计测量。脉波数据、心电图数据和生物阻抗由ES-TECK BC-3(Ryobi Systems株式会社)测量。注意,可以组合使用市售的脉波计、心电图机、阻抗测量设备和脉搏血氧仪来代替ES-TECK BC-3。上述非侵入性生物信息可以使用预定的可穿戴终端来获取。
通过在腿、手、左右前额六个部位处的电极中的两个电极之间生成小电流来测量生物阻抗(电导)。电压和电流分别为1.28V和200μA,并且在每秒的32毫秒中测量电导。使得电流在六个部位处的电极中的两个电极之间流动,以测量:(1)阳极/阴极电导(μS);(2)阴极/阳极电导(μS);(3)上述(1)中测量的电导与上述(2)中测量的电导之差(delta SCRA-SCRC);以及(4)电导率(μS/m)。
此外,还测量肌肉质量、体脂量、总水分含量、相位角和电阻值,并且测量在右手与左手之间传导和在右前额与左前额之间传导的情况下的介电常数(μSi)。
使用ES-TECK BC-3对每个被检者测量两分钟的脉波数据、心电图数据和生物阻抗。在测量时,将具有心电图、脉波计和脉搏血氧仪功能的设备安放在每个被检者的左手食指上,两个电极安放在前额上,并且当被检者坐在椅子上时手脚放在电极板上。
<学习模型1>
如图4所示,在学习模型1中,并行地执行通过线性回归、神经网络(NN)和梯度提升决策树(XGBoost)的机器学习,并利用学习结果来执行岭学习(岭回归)。
在这种情况下,下述数据被选择并被用作属性信息和非侵入性生物数据。(A)属性信息:性别和年龄;(B)非侵入性生物数据:BMI、血压、平均动脉血压、脉压、脉波数据、脉搏、弹性指数、左心室射血时间(LVET)、b/a、光容积描记老化指数的二阶导数、重搏脉弹性指数(DEI)、心电图数据、心率、MxDMn比值、LF/HF、生物阻抗、体脂量(kg)、体脂量(%)、肌肉质量、ESG 2+4+15+17(μS/m)、ESG 9+10(μS/m)、R(Ω)、心输出量和通过前额路径的电导率(9)。
ESG 9+10是在如图2所示部位处测量的阻抗值的平均值。单位[μS/m]是测量平均值的单位,并且单位[%]是将测量平均值换算到通常测量值的范围内获取的值。非侵入性生物数据还包括脉压/脉搏。
<示例1>
在示例1中,使用(1)属性信息;(2)由身高体重计、血压计、ES-TECK BC-3测量的非侵入性生物信息;以及(3)通过总共712名被检者在非侵入性生物信息测量的同一天执行的血液检查获得的血中中性脂肪训练数据集,通过上述学习模型1的机器学习生成血中中性脂肪估计模型。注意,在机器学习中使用通过血液检查获得的血中中性脂肪测量值的对数。
然后,通过计算与经由血液检查获得的血中中性脂肪测量值的对数之间的相关系数来确定血中中性脂肪估计模型的估计准确度。
结果,血中中性脂肪估计值与通过血液检查获得的血中中性脂肪测量值之间的误差的平均值、标准偏差和标准误差分别为12.4、53.7和4.03。通过血液检查获得的血中中性脂肪测量值的对数与基于血中中性脂肪估计模型的血中中性脂肪估计值的对数之间的相关系数为0.63。无相关性测试得到的结果p值小于0.001,因此由估计模型估计的血中中性脂肪对数值与通过血液检查获得的血中中性脂肪测量值之间存在相关性。
如上所述,通过基于包括身体质量指数(BMI)、血压、脉波数据、心电图数据和生物阻抗等的非侵入性生物数据通过机器学习生成中性脂肪估计模型,可以在不执行血液检查的情况下估计血中中性脂肪。
如下所述,即使当非侵入性生物数据中包含的数据条数有限的情况下,也可以确定“血中中性脂肪风险”,也就是血中中性脂肪水平是否正常。
<通过机器学习生成血中中性脂肪风险估计模型>
根据本发明,可以计算血中中性脂肪风险估计值来代替血中中性脂肪估计值。
图7是示出了通过机器学习生成血中中性脂肪风险估计模型的执行过程的流程图。
在步骤ST301处,学习处理单元35执行对输入数据(例如,上述训练数据集)的预处理。具体地,对于通过血液检查获得的血中中性脂肪测量值,学习处理单元35将低于15Omg/dL的血中中性脂肪转换为“0”(不存在风险),并且将等于或高于150mg/dL的血中中性脂肪转换为“1”(存在风险)。当被分类为“0”的被检者的数量和被分类为“1”的被检者的数量存在偏差和不平衡时,学习处理单元35可以将SMOTE(Chawla,NV.等人,2002)应用于学习数据以人工生成训练样本。具体地,可以基于血液测量的血中中性脂肪测量值,向每个输入数据(训练数据集)提供表示血中中性脂肪风险的存在性的标签(例如上述的“0”或“1”),并且当具有血中中性脂肪风险的标签(标签“1”)的数目与不具有血中中性脂肪风险的标签(标签“0”)的数目之差等于或大于预定值时,可以增加(生成)训练数据集中的样本数据的条数来减小该差。
在步骤ST302处,学习处理单元35并行执行(1)通过具有图8所示结构的第一神经网络(NN)的机器学习、或(2)通过具有图9所示结构的第二神经网络(NN)以及通过逻辑回归、梯度提升决策树和随机森林的机器学习。
在通过梯度提升决策树的机器学习中可以使用诸如XGBoost、CatBoost和LightBGM等软件库。
在步骤ST303处,学习处理单元35还利用通过逻辑回归、第二神经网络(NN)、梯度提升决策树和随机森林的机器学习的结果来执行集成学习。注意,当仅第一神经网络(NN)用于步骤ST302的机器学习时,步骤ST303处的集成学习(投票)是不必要的。
图8示出了用作血中中性脂肪风险估计模型的第一神经网络(NN)的结构。“D”表示检查项目的数量。第一神经网络(NN)的结构通过三个层组(编译A1、编译A2和编译B)按D维、96维、64维和一维的顺序转换数据。
编译A1和编译A2均包括执行全连接处理的全连接层“线性”、执行正则化的“内核正则化器”和执行ReLU处理的“ReLU”层,并且层组编译B包括执行全连接处理的全连接层“线性”和执行优化处理的“Adam”层。层组编译A1的全连接层的输入单元对应于输入层,层组编译B的输出单元对应于输出层,并且它们之间的每个单元对应于中间层(隐藏层)。中间层包括:将一些输入值限制为零并防止过度拟合的退出层,以及执行归一化并将数值传递给下一层的批量归一化(Batch_Normalization,简称BN)层。
图9示出了用作血中中性脂肪风险估计模型的第二神经网络(NN)的结构。“D”表示检查项目的数量。第二神经网络(NN)的结构通过四个层组(编译A1、编译A2、编译A3和编译B)按D维、64维、64维、64维和一维的顺序转换数据。
例如,Python开源机器学习库Scikit-learn中提供的Logistic Regression可以用于通过逻辑回归的机器学习中。必要时可以通过主成分分析来减少维数。将通过血液检查获得的血中中性脂肪风险与通过机器学习估计的血中中性脂肪风险估计值进行比较,并调整Logistic Regression(逻辑回归)的参数(C、正则化方法、max_iter和solber)以获得最大f1分数。参数“C”是决定正则化强度的权衡参数,并且该参数的值越大,正则化强度越弱。参数“正则化方法”是指选择L1正则化还是L2则化。参数“max_iter”是学习的最大迭代次数。参数“solber”选择能最小化交叉熵损失的收敛方法(例如,L-BFGS方法、Newton CG方法、liblinear、sag或saga)。注意,在下面的示例2中选择了liblinear方法。
注意,上述机器学习算法是示例性的并且本发明不限于此。
XGBoost、CatBoost和LightBGM等软件库可以用于通过梯度提升决策树的机器学习。将通过血液检查获得的血中中性脂肪风险测量值与通过机器学习获得的血中中性脂肪风险估计值进行比较,并调整XGBoost的参数(max_depth、subsample、colsample_bytree和learning_rate)以获得最大的f1分数。参数“max_depth”表示决策树的深度,参数“subsample”表示在每棵树上随机抽取的样本比率,参数“colsample_bytree”表示在每棵树上随机抽取的列的比率,而参数“learning_rate”表示学习率。在“max_depth”为1到10,“subsample”为0.3到0.7,“colsample_bytree”为0.3到1.0,以及“learning_rate”为0.1到0.9的范围下进行调整。
例如,Python开源机器学习库Scikit-learn中提供的Random Forest Classifier(随机森林分类器)可以用于通过随机森林的机器学习。将通过血液检查获得的血中中性脂肪风险测量值与通过机器学习获得的血中中性脂肪风险估计值进行比较,并调整随机森林分类器的参数(max_depth、max_features和n_estimators)以获得最大的f1分数。参数“max_depth”是决策树的深度,并且参数“max_features”指定每棵树的随机性。参数“n_estimators”是要建立的决策树的数量。但是,max_depth为None(无)或1到7之间的值,subsample为0.3到0.7之间的值,max_features理想地从“auto”、“sqrt”和“log”中选择,而n_estimators在10到1000的范围内调整。
<使用血中中性脂肪风险估计模型来估计血中中性脂肪风险>
如图10所示,在步骤ST401处,血中中性脂肪估计设备30的第一获取单元31从终端设备10获取用户的属性信息。在步骤ST402处,血中中性脂肪估计设备30的第二获取单元32获取用户的非侵入性生物信息。然后,将用户的属性信息和非侵入性生物信息存储在用户数据存储单元33中。然后在步骤ST403处,估计处理单元37通过使用存储在估计模型存储单元36中的血中中性脂肪风险估计模型来计算血中中性脂肪风险估计值,即用户属于类别0(不存在风险)或类别1(存在风险)的概率。在步骤ST404处,将计算出的血中中性脂肪风险估计值输出并存储在估计数据存储单元38中,并且在步骤ST405处,将血中中性脂肪风险估计值显示在诸如显示设备39的外部终端上。
<示例(血中中性脂肪风险估计)>
下面将描述血中中性脂肪风险估计的示例。但是,本发明中的血中中性脂肪风险估计的方式并不限定于以下示例。
属性信息包括ID、姓名、年龄和性别中的任意一个或组合,并且非侵入性生物信息包括BMI、血压、脉波数据、心电图数据和生物阻抗中的任意一个或组合。作为BMI计算参考的身高和体重分别用身高计和体重计测量,而血压用血压计测量。脉波数据、心电图数据和生物阻抗由ES-TECK BC-3(Ryobi Systems株式会社)测量。注意,可以组合使用市售的脉波计、心电图机、阻抗测量设备和脉搏血氧仪来代替ES-TECK BC-3。上述非侵入性生物信息可以使用预定的可穿戴终端来获取。
通过在脚、手、左右前额六个部位处的电极中的两个电极之间生成小电流来测量生物阻抗(电导)。电压和电流分别为1.28V和200μA,并且在每秒的32毫秒中测量电导。使得电流在六个部位处的电极中的两个电极之间流动,以测量:(1)阳极/阴极电导(μS);(2)阴极/阳极电导(μS);(3)上述(1)中测量的电导与上述(2)中测量的电导之差(delta SCRA-SCRC);以及(4)电导率(μS/m)。
此外,还测量肌肉质量、体脂量、总水分含量、相位角和电阻值,并且测量在右手与左手之间传导和在右前额与左前额之间传导的情况下的介电常数(μSi)。
使用ES-TECK BC-3对每个被检者测量两分钟的脉波数据、心电图数据和生物阻抗。在测量时,将具有心电图、脉波计和脉搏血氧仪功能的设备安放在每个被检者的左手食指上,两个电极安放在前额上,并且当被检者坐在椅子上时手脚放在电极板上。
<学习模型2>
在学习模型2中,执行具有图8所示结构的第一神经网络(NN)的机器学习。在这种情况下,下述数据被选择并被用作非侵入性生物数据。(A)属性信息:年龄;(B)非侵入性生物数据:BMI、血压、收缩压、脉压、脉波数据、脉搏、生物阻抗、去脂体重(kg)、总水分含量(%)、13左脚-14右脚/SCRA、ESG 6+13+19(%)。
<学习模型3>
在学习模型3中,并行执行通过逻辑回归、梯度提升和随机森林的机器学习与通过图9中所示的第二神经网络的机器学习,并且通过执行关于学习结果的投票的集成学习,生成血中中性脂肪风险估计模型。在这种情况下,下述数据被选择并被用作非侵入性生物数据。注意,与上述学习模型2不同,学习模型3不需要被检者的属性信息。(B)非侵入性生物数据:BMI、血压、收缩压、舒张压、脉波数据、弹性指数、LVET、脉搏、生物阻抗、体脂量(kg)、去脂率(%)、肌肉质量、总水分含量(%)、R(Ω)、心输出量、13左脚-14右脚/SCRA、EGS9+10(μS/m)。
<示例2>
在示例2中,通过使用(1)属性信息;(2)由身高体重计、血压计、ES-TECK BC-3测量的非侵入性生物信息;以及(3)321名被检者在非侵入性生物信息测量的同一天执行的血液检查获得的血中中性脂肪的训练数据集,通过上述学习模型2的机器学习生成血中中性脂肪风险估计模型。
然后,使用ROC_AUC曲线,针对估计结果评估血中中性脂肪风险估计模型的估计准确度。结果,ROC_AUC为0.80,表示分类非常好。示例2中的估计结果的ROC_AUC曲线如图11所示。
<示例3>
在示例3中,通过使用(1)属性信息;(2)由身高体重计、血压计、ES-TECK BC-3测量的非侵入性生物信息;以及(3)通过总共712名被检者在非侵入性生物信息测量的同一天执行的血液检查获得的血中中性脂肪的训练数据集,通过上述学习模型3的机器学习生成血中中性脂肪风险估计模型。
然后,使用ROC_AUC曲线,针对估计结果评估血中中性脂肪风险估计模型的估计准确度。结果,ROC_AUC为0.77,其超过0.7,表示分类良好。示例3中的估计结果的ROC_AUC曲线如图12所示。
(变形)
在上述实施方式中,使用学习模型2或学习模型3来估计血中中性脂肪风险,但也可以使用多种学习模型来估计血中中性脂肪风险。
因此,与使用一种学习模型估计血中中性脂肪风险相比,可以以更高的准确度估计血中中性脂肪风险。
在上述实施例和示例中,当BMI用于学习模型数据集时,在某些情况下估计准确度提高,因此可以在血中中性脂肪估计设备中提供被配置为估计BMI的功能组件。
BMI通常不是通过可穿戴终端等获取的,而是基于用户输入的身高和体重来计算出的。然而,当估计BMI时,可以仅通过获取生物信息来获取上述血中中性脂肪风险,这提高了用户的便利性。
BMI估计不限于特定方法,但是例如,已知BMI与用户的腹部区域(预定位置)的倾斜度相关。因此,例如,可以在用户的腹部区域设置预定加速度传感器(或者可以将包含加速度传感器的腕带式可穿戴终端等放置在腹部区域),并且可以通过基于加速度传感器输出的数据计算腹部区域的倾斜度来估计BMI。
与上面的描述类似,可以使用包含脉波传感器或血氧水平传感器的腕带式可穿戴终端等来估计脉波数据。
与上面的描述类似,可以使用腕带式可穿戴终端等来估计血压。由于已知血压与由心跳通过动脉传递的脉波的速度相关,因此可以使用被配置为测量由心跳通过动脉传递的脉波的速度的预定传感器来估计血压。
与上面的描述类似,可以使用腕带式可穿戴终端等来估计心电图数据。例如,可以基于从与腕带式可穿戴终端的显示表面相反侧的表面上设置的电极以及该显示表面那侧上设置的电极获取的数据,来估计心电图数据。具体地,可以基于当其上安装有腕带式可穿戴终端的手(例如左手)的手腕接触设置在相反表面上的电极以及与所安装的手相反的手(例如,右手)的指尖接触设置在显示表面那侧的电极时获取的数据,来估计心电图数据。
与上面的描述类似,可以使用包括各种电极的腕带式可穿戴终端等来估计生物阻抗。例如,可以基于使用腕带式可穿戴终端等从胸部区域和手腕获取的生物信息来估计生物阻抗。
注意,可以将可穿戴终端可获取的生物信息和上述估计目标生物信息作为教师数据,使用利用各种机器学习算法生成的分类器,来估计上述估计目标生物信息(BMI、血压、脉波数据、心电图数据和生物阻抗中的至少一个或多个生物信息)。
在这种情况下,上述第二获取单元可以获取估计生物信息。
(其他)
例如,上述一系列处理可以由硬件或软件来执行。换言之,上述功能配置仅是示例性的并且不被具体限制。具体地,在信息处理系统中提供执行整个系列的上述处理的功能就足够了,而使用哪些功能块来实现所述功能并不具体限于上述示例。功能块存在的位置并不具体限于图1中的那些,而是可以是可选的。例如,服务器的功能块可以转移到另一终端或设备。可以将另一终端或设备的功能块转移到服务器等。每个功能块可以仅由硬件、仅由软件、或由它们的组合来配置。
当一系列处理由软件执行时,从网络或记录介质将构成软件的计算机程序安装到计算机等上。计算机可以是结合在专用硬件中的计算机。备选地,计算机可以是能够利用安装在其上的各种计算机程序执行各种功能的计算机,诸如服务器或通用智能手机或个人计算机。
包括这样的计算机程序的记录介质不仅被配置为未示出的与设备主体分开分发以向用户等提供计算机程序的可移动介质,而且也可以被配置为例如预先结合在设备主体中并提供给用户等的记录介质。计算机程序可以通过网络分发,并且因此记录介质可以安装在计算机上或是从计算机可访问的,该计算机连接到或可连接到网络。
注意,在本说明书中,代表记录在记录介质中的计算机程序的步骤不仅包括根据顺序以时间顺序的方式执行的处理,而且还包括不一定以时间顺序处理的而是并行或单独执行的处理。在本说明书中,系统术语是指包括多个设备、多个单元等的整个设备的术语。
附图标记列表
1 血中中性脂肪估计系统
10终端设备
20生物信息测量设备
30血中中性脂肪估计设备
31第一获取单元
32第二获取单元
33用户数据存储单元
34训练数据存储单元
35学习处理单元
36估计模型存储单元
37估计处理单元
38估计数据存储单元
39示设备
300 计算机
301 处理器
302 存储器
303 存储设备
304 输入/输出端口
305 通信端口。
- 血中中性脂肪减少组合物
- 餐后血中中性脂肪的上升抑制剂以及含有其的食品
