卡铂在制备预防或治疗多发性硬化症药物中的应用
文献发布时间:2024-01-17 01:19:37
技术领域
本发明属于生物医药技术领域,尤其涉及卡铂在制备预防或治疗多发性硬化症药物中的应用。
背景技术
多发性硬化(Multiple sclerosis,MS)是一种中枢神经系统(Central NervousSystem,CNS)的自身免疫性疾病。其特征是局部淋巴细胞浸润、髓鞘破裂、星形胶质细胞增殖、小胶质细胞活化和神经变性。MS的分子机制很复杂,人们普遍认为自身反应性T细胞在疾病的发展中起着关键作用。目前,美国至少批准了19种疾病修饰疗法(DMT)用于治疗多发性硬化症,所有这些疗法都可以通过发挥免疫抑制或免疫调节作用在一定程度上降低其复发率。然而,目前的药物仅对一些MS患者有效,对继发性进展性MS没有明显治疗作用。此外,这些治疗的长期效果与并发症相关,也会引起一些严重的副反应。因此,迫切需要开发一种新的、有效的治疗药物。实验性自身免疫性脑脊髓炎(experimental autoimmuneencephalomyelitis,EAE)是研究MS发病机制和开发新疗法的最佳动物模型。
卡铂(carboplatin,CA)是一种静脉给药的铂类配合物和烷基化剂,用作治疗各种癌症的化疗剂,主要是卵巢癌、头颈癌和肺癌。卡铂和顺铂作为烷基化剂,导致DNA链之间和链内的交联,导致DNA、RNA和蛋白质合成受到抑制,并触发程序性细胞死亡,主要发生在快速分裂的细胞中。1989年,卡铂在美国被批准用于癌症化疗。然而,关于卡铂在免疫系统中的调节功能的报道很少。因此,卡铂是否对MS有治疗作用尚不清楚。
发明内容
本发明所要解决的技术问题是提供一种卡铂在制备预防或治疗多发性硬化症药物中的应用,为多发性硬化症的治疗和预防提供方向。
本发明为解决上述技术问题而采用的技术方案是提供一种卡铂在制备预防或治疗多发性硬化症药物中的应用。
进一步地,所述多发性硬化症包括:局部淋巴细胞浸润、髓鞘破裂、星形胶质细胞增殖、小胶质细胞活化和神经变性。
进一步地,所述药物抑制T细胞增殖,并促进活化的T细胞和髓鞘少突胶质细胞糖蛋白特异性T细胞凋亡。
进一步地,所述药物包括所述卡铂及药学上可接受的载体。
进一步地,所述药物在预防多发性硬化症时,每隔两天口服一次,并控制卡铂的用量为30mg/kg-100mg/kg。
本发明对比现有技术有如下的有益效果:本发明研究了卡铂对EAE神经病理学的影响。研究发现,口服卡铂可以减轻EAE的总体临床症状,减少脊髓炎症和脱髓鞘现象。此外,卡铂处理组EAE小鼠外周组织中T细胞的比例和数量明显降低。同时,质谱数据分析也表明对照组和卡铂处理组EAE小鼠的脾细胞中的差异表达蛋白主要与凋亡调控途径有关。体外细胞实验数据表明卡铂抑制活化T细胞的增殖并诱导其凋亡。本发明的数据表明卡铂可安全有效地应用于MS治疗药物中。
附图说明
图1表明卡铂治疗减轻EAE小鼠的临床症状;
图2表明卡铂治疗减少了CNS中致病性T细胞的浸润;
图3表明卡铂治疗减少了EAE小鼠外周T细胞数量;
图4表明卡铂治疗增强了EAE期间的凋亡信号;
图5表明卡铂介导活化T细胞凋亡;
图6表明卡铂增强EAE小鼠中MOG特异性T细胞凋亡。
具体实施方式
下面结合附图和实施例对本发明作进一步的描述。
本发明试图评估口服卡铂是否可以用于改善EAE的病情。卡铂治疗降低了EAE小鼠的脊髓炎症、脱髓鞘和疾病评分。此外,卡铂治疗组的EAE小鼠的脾脏和引流淋巴结中的致病性T细胞(尤其是Th-1和Th-17)的数量和比例明显减少。蛋白质组差异富集分析表明,卡铂处理组脾细胞所表达的与凋亡信号相关蛋白发生显著变化。CFSE实验结果显示卡铂显著抑制T细胞增殖。最后,体外实验证明卡铂可以促进活化的T细胞和髓鞘少突胶质细胞糖蛋白(简称MOG)特异性T细胞凋亡。研究结果表明卡铂在EAE的发生和发展中起着保护作用,并且为治疗MS的新药设计成为可能。
以下详细公开实验、检测、理论分析。
一、实验中涉及的材料(动物模型)与本领域通用的实验和检测方法
1.动物模型
雄性C57BL/6小鼠购自江苏集萃药康生物科技股份有限公司(南京,中国)。所用C57BL/6小鼠为8-10周龄,饲养于同济大学实验动物中心SPF级实验室,自由食用水和饲料。所有实验均获得批准,并按照同济大学的动物保护委员会的指导进行。
2.方法:建立小鼠EAE模型及药物治疗
C57BL/6小鼠(8-10周)皮下注射200μg完全溶于完全弗氏佐剂并包含有热灭活结核杆菌(H37Ra,5mg/ml,BD Diagnostics)的MOG
3.方法:组织病理和免疫组织化学分析
每只小鼠深度麻醉后0.9%NaCl心脏灌流去除各器官中的外周血,4%(w/v)多聚甲醛灌流进行固定。取腰髓组织样品置于4%多聚甲醛溶液,4℃固定过夜。石蜡包埋后H&E染色分析炎症浸润,快蓝染色分析脊髓脱髓鞘,Image-Pro软件进行统计分析。
4.方法:中枢神经系统浸润细胞分离和分析
脑和脊髓用预冷的组织匀浆器进行匀浆,70μm细胞滤网过滤收集至15ml离心管中,500g 4℃离心10min获得细胞,然后将细胞重悬在8ml 37%Percoll中。在15ml离心管中先轻轻加入4ml 70%Percoll,瞬时离心去除离心管壁上残留的70%Percoll,避免与后面加入的37%Percoll互溶;沿着管壁缓缓加入37%Percoll细胞悬液,避免破坏界面层。780g25℃密度梯度离心25min,收集位于37/70%Percoll界面处的细胞,进行分析。
5.方法:细胞染色和流式分析
脾脏细胞和引流淋巴结细胞进行表面染色,FITC-CD4、APC-CD8、APC-B220和FITC-CD11b在4℃避光染色30分钟,洗涤,然后用1×PBS重悬。脾脏细胞,引流淋巴结细胞,或CNS浸润细胞用PMA(50ng/ml;Sigma-Aldrich)、ionomycin(750ng/ml;Sigma-Aldrich)和brefeldin A(5μg/ml;Sigma-Aldrich)37℃刺激5小时。细胞表面标记CD4用抗体4℃避光染色30min,然后细胞用固定通透液重悬,分别进行胞内IL-17A(BioLegend,506904,1:100)和IFN-γ(BioLegend,505810,1:100)染色。流式分析为BD FACS Verse系统,并用Flow JoV10软件进行分析。
6.方法:ELISA检测外周血中炎症因子表达
卡铂(100mg/kg体重)或溶媒(无菌水)处理小鼠构建EAE模型。在建模第10天时,从眼眶静脉血中收集全血约150μl。眼眶静脉血在室温静置30分钟。30分钟后,4℃下以4000rpm离心10分钟,仔细收集上清,尽可能不要吸到下方的沉淀,获得血清。根据制造商的说明,使用特定的ELISA试剂盒(eBioscience)测量血清中IL-17A和IFN-γ的浓度。
7.方法:T细胞增殖实验
用10mM羧基荧光素二乙酸琥珀酰亚胺酯(CFSE)标记脾细胞,然后接种至96孔板中,加入200μL包含10%FBS、2mML-谷氨酰胺和50μMβ-巯基乙醇的RPMI1640完全培养基进行培养,加入anti-CD3(2μg/ml;BD Pharmingen)和anti-CD28(2μg/ml;BD Pharmingen)抗体激活细胞。各种浓度的卡铂同时加入,培养48小时。收集细胞,流式细胞术检测CFSE荧光。
8.方法:T细胞凋亡实验
在含有2μg/ml anti-CD28抗体和2μg/ml anti-CD3抗体的RPMI1640完全培养基中以5×10
9.方法:LC-MS/MS分析
用400μl尿素裂解缓冲液(8M尿素,100mM Tris-HCl pH8.0)、4μl蛋白酶抑制剂(Pierce
10.方法:统计学分析
EAE小鼠处理组间统计学差异用two-way ANOVA test分析,其他数据统计用Student’s t-test分析,数据表示为mean±SEM,P<0.05被认为有统计学意义。
实验1对应方法:建立小鼠EAE诱导模型及药物治疗;组织病理和免疫组织化学分析;
实验2对应方法:中枢神经系统浸润细胞分离和分析;
实验3对应方法:细胞染色和流式分析;ELISA检测外周血中炎症因子表达;
实验4对应方法:LC-MS/MS分析;
实验5对应方法:T细胞增殖实验;T细胞凋亡实验。
二、实验及结果
实验1卡铂改善EAE小鼠的临床症状
为了评估卡铂是否对多发性硬化症有治疗作用,本发明通过MOG
低剂量卡铂口服给药不能改善EAE的严重程度。在30mg/kg时,卡铂延迟了EAE的发作,并降低了EAE缓解期间的临床评分(图1A)。100mg/kg卡铂的治疗也延迟了EAE的发作,并显著降低了其严重程度和累积临床评分(图1A)。本发明发现,每隔两天口服卡铂也可以延缓EAE的发作,缓解EAE的症状,且药效更好(图1B)。有趣的是,在发病后(第12天)给予卡铂(100mg/kg,口服)仍能降低EAE的严重程度,这表明CA除了预防作用之外,还有治疗作用。
图1中:(A-C)通过MOG
实验2卡铂减少EAE小鼠中枢神经系统中白细胞浸润和神经病变
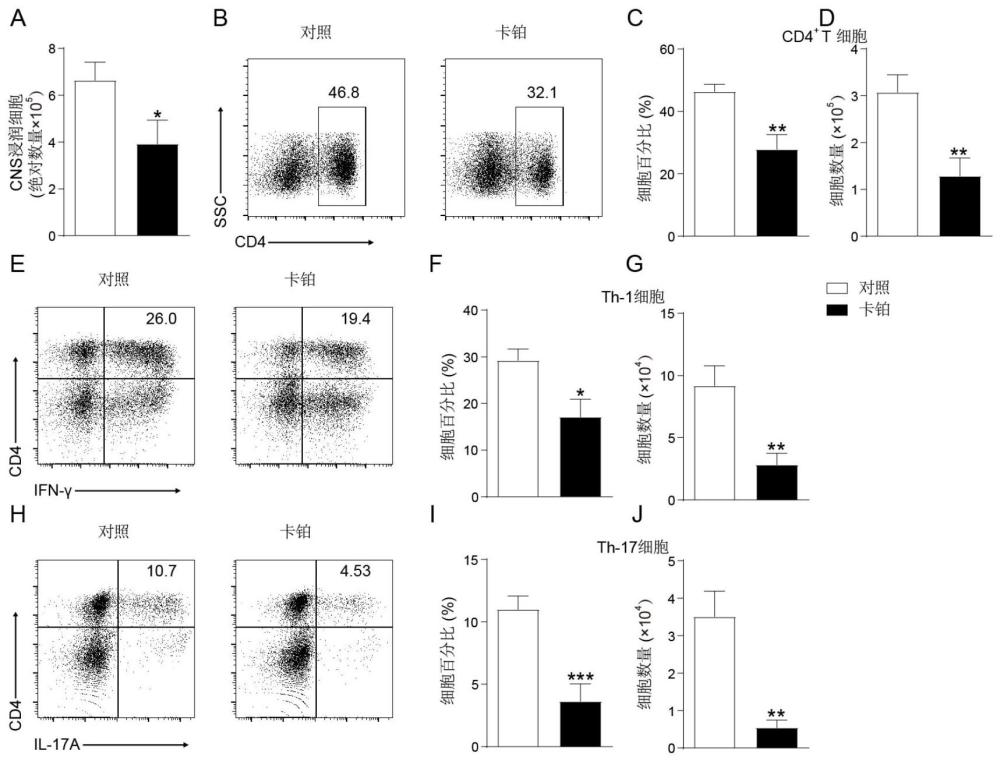
EAE小鼠发病过程中伴随着CNS(脑和脊髓)的炎性细胞浸润及髓鞘损伤,在发病高峰期现象最明显,其中腰髓的白质部分现象最为突出。因此,本发明选取卡铂给药组和无菌水对照组EAE小鼠,在发病最高峰(第17天)时取脊髓切片进行病理组织检测,确定卡铂给药是否能减少EAE小鼠CNS病灶部位炎性细胞的浸润和减轻髓鞘损伤。同时,本发明选取健康的C57BL/6小鼠(naive小鼠)作为没有炎性细胞浸润和髓鞘损伤的阴性对照。与对照组相比,卡铂导致脊髓白细胞浸润显著减少(图1D,1F)。与对照组相比,快蓝染色还显示卡铂处理的EAE小鼠的脱髓鞘较少(图1E,1G)。免疫后第17天,通过流式细胞术分析对CNS白细胞浸润进行定量。结果证实了卡铂治疗后EAE小鼠CNS中CD4+T细胞积聚减少(图2A-D)。产生IL-17A的Th17细胞和产生IFN-γ的Th1细胞是EAE的主要致病性T效应细胞。因此,本发明量化了CNS浸润中Th1和Th17细胞的数量。卡铂治疗后,IFN-γ+CD4+T细胞(Th1细胞)和IL-17A+CD4+T细胞(Th17细胞)的百分比和数量显著降低(图2E-J)。上述这些数据表明卡铂治疗可显著降低EAE的严重程度,减少CNS炎症和脱髓鞘。
图2中:(A)在免疫后第17天,用37/70%Percoll从对照组或卡铂组(100mg/kg,从第3天开始)EAE小鼠的大脑和脊髓中分离总CNS浸润,并通过流式细胞术定量总浸润的数量。(B,E,H)用卡铂(100mg/kg,从第3天开始)或无菌水处理的EAE小鼠的CNS中CD4+T细胞、Th-1细胞和Th-17细胞的代表性FACS图。(C,F,I)通过GraphPad Prism 8软件对CNS中IFN-γ和IL-17A的细胞内染色进行FACS分析的统计数据。(D,G,J)CD4+T细胞、Th-1细胞和Th-17细胞的细胞数统计。数据为平均值±SEM(每组n=7-8),统计测试采用Student's t test,与对照组相比,*p<0.05,**p<0.01,***p<0.001。
实验3卡铂降低EAE小鼠外周CD4+T和CD8+T细胞
MS是由外周免疫系统的免疫细胞引起的自身免疫性疾病;T细胞、B细胞和单核细胞参与了MS的发病机制。为了检测卡铂是否影响基础免疫应答,从对照组和卡铂处理组的EAE小鼠脾脏中收集白细胞,并通过流式细胞术分析脾白细胞中CD4+T细胞、CD8+T细胞、B细胞和CD11b+细胞的比例。表面染色显示,卡铂处理显著降低了脾脏中CD4+T细胞和CD8+T细胞的比例,而不影响B细胞和CD11b+细胞群体(图3A顶部两行,C和G)。
接下来,本发明用细胞内细胞因子染色检测脾脏中Th-1和Th-17细胞的数量。研究发现,在卡铂处理的EAE小鼠中,CD4+群体中Th-1和Th-17细胞的比例数量显著减少(图3A底行,D和H)。对引流淋巴结中的免疫细胞进行相同分析,本发明也获得了类似的结果(图3B、E、F、I和J)。
最后,在卡铂治疗的EAE小鼠中,血清中的细胞因子IFN-γ和IL-17A的分泌显著减少(图3K和L)。
图3中:(A-B)免疫后第10天,从卡铂(100mg/kg,口服,从第3天开始)或无菌水处理的EAE动物的脾脏(A)和引流淋巴结(dLN)(B)分离白细胞,并用表面染色和流式细胞术分析CD4+T细胞、CD8+T细胞、B细胞(B220+)和CD11b+细胞的百分比。Th-1和Th-17细胞通过胞内染色流式分析CD4阳性细胞中IFN-γ和IL-17A的比例。(C-J)A和B的统计分析。数据表示平均值±SEM(n=9)。与对照组相比,*p<0.05,**p<0.01,***p<0.01(Student's t test)。(K-L)从用100mg/kg卡铂或相同体积的水处理的EAE小鼠收集血清,分析其中的细胞因子IFN-γ和IL-17A的分泌量。数据为平均值±SEM(n=9-13)。与对照组相比,*p<0.05(Student'sttest)。
实验4卡铂治疗增强EAE期间的凋亡通路信号
为了探讨卡铂在EAE发病机制中的作用,本发明对分别用无菌水和卡比处理的EAE小鼠(免疫第10天)的脾细胞进行了质谱分析。卡铂处理后,表达差异蛋白质主要影响凋亡信号通路调节、蛋白质稳定性调节、细胞杀伤和细胞周期负调节的生物学功能(图4A和B)。KEGG分析显示卡铂主要通过凋亡、抗原处理和呈递等影响EAE进展。其中,与抗原处理和呈现相关的蛋白质(例如,Hsp90ab1、Canx、Hsp90aa1、Pdia3和Hspa8)和凋亡(例如,Ybx3、Runx3、Rps7和Hsph1)在卡铂处理后显著下调(图4C和D)。
图4中:(A-B)通过GO富集分析(A)和网络分析(B)按功能对EAE小鼠的对照组和卡铂组的比较蛋白质组分析进行分类。(C-D)KEGG富集分析(C)和KEGG热图(D)显示免疫后第10天EAE小鼠的对照组和卡铂(100mg/kg,从第3天开始)组脾细胞的总蛋白显著富集的信号通路。
实验5卡铂抑制T细胞增殖并促进T细胞凋亡
实验3的脾细胞和淋巴细胞的表面染色结果表明,卡铂治疗后,外周免疫组织中T细胞的频率显著降低。同时,质谱数据分析也表明差异表达蛋白主要与凋亡调控有关。因此推测卡铂可能影响T细胞的增殖或凋亡。为了验证这一假设,本发明利用小鼠脾细胞进行了体外细胞增殖或凋亡实验。在卡铂存在下,用抗小鼠CD3和抗小鼠CD28的抗体活化从野生型小鼠分离得到的脾细胞48小时。如图5A所示,卡铂剂量依赖性抑制T细胞抗原刺激的细胞增殖。
接下来,在卡铂(3μM和10μM)处理不同持续时间(24-72小时)后,用annexin V和7-AAD染色检测凋亡细胞比例。体外实验表明卡铂增强了CD4+和CD8+T细胞群的凋亡(图5B-G)。
本发明同时测试了卡铂对MOG特异性T细胞的影响。在免疫后第10天从EAE小鼠中分离脾细胞,并在卡铂的存在下用MOG(20μg/ml)在体外重刺激,用FACS测量CD4+和CD8+T亚群中的凋亡(图6)。卡铂处理显著促进MOG特异性CD4+和CD8+T细胞的凋亡。上述这些数据都表明了卡铂诱导了T细胞凋亡(图6A-F)。
图5中:(A)分离野生型小鼠的脾细胞,用2μg/ml抗小鼠CD3和2μg/ml抗小鼠CD28抗体活化细胞;用CFSE染色评估细胞增殖。(B-C)经卡铂处理的CD4+(B)或CD8+(C)T细胞凋亡的代表性FACS图。(D-E)B和C中的凋亡统计分析。数据来自三个独立实验(平均值±SEM)。与对照组相比,*p<0.05,***p<0.001(two-way ANOVA)。
图6中:(A-B)免疫后第10天从EAE小鼠分离脾细胞,并用MOG35-55(20μg/ml)再刺激。用卡铂处理细胞24、48或72小时,通过流式细胞术检测CD4+(A)或CD8+(B)T细胞的凋亡情况。(C-D)A和B的统计分析。数据来自三次独立的实验(平均值±SEM)。与对照组相比,*p<0.05,***p<0.001(two-way ANOVA)。
三、实验后的讨论和小结
多发性硬化(Multiple sclerosis,MS)是一种慢性神经系统疾病,具有潜在的破坏性和长期并发症。实验性自身免疫性脑脊髓炎(experimental autoimmuneencephalomyelitis,EAE)是一种CD4+T细胞介导的中枢神经系统脱髓鞘疾病,常被用作人类MS的动物模型。激活的CD4+T细胞从外周迁移到中枢神经系统,在那里通过分泌细胞因子和趋化因子启动炎症反应级联。CD8+T细胞也参与了EAE的发病机制。在MS病变中检测到的CD8+T淋巴细胞表现出活化和克隆扩增细胞的特征,支持了这些细胞积极参与观察到的损伤的概念。已有研究表明,髓磷脂反应性CD8+T细胞直接引发轴突损失,而神经元损伤已被发现与CD8+T细胞浸润的程度相关。因此,诱导T细胞凋亡可能有助于改善EAE。
凋亡是大多数多细胞动物生长和存活的先决条件,并确保组织稳态的维持。它在免疫学中的矛盾作用可以通过以下事实来说明:这个过程不仅有助于平衡功能,而且会产生有害影响,包括组织损伤。使用EAE模型的实验表明,细胞死亡影响浸润淋巴细胞和CNS驻留细胞,并有助于轴突损伤和炎症的消退。研究报告称,醋酸格拉替雷和干扰素β等药物通过诱导外周T细胞凋亡来治疗MS。同样,本发明的数据表明卡铂降低了脾脏和引流淋巴结中CD4+T细胞的比例。可能是由于外周T细胞凋亡的增加,因此浸润CNS的CD4+T细胞的数量也减少。此外,本发明的体外实验数据也表明卡铂诱导了脾细胞中CD4+T细胞和CD8+T细胞凋亡。
细胞凋亡可能由线粒体途径、内质网应激途径或死亡受体介导的外源性途径触发。在这些途径中,线粒体途径可被线粒体中的caspase级联和Bcl-2家族成员激活。Bcl-2家族包含多种促凋亡和抗凋亡蛋白,它们是“内在”通路的关键组成部分。有文献报道卡铂处理显著降低Bcl-2蛋白的表达,并以时间依赖性方式诱导Raji细胞凋亡。本发明的质谱数据显示,对照组和卡铂治疗组之间脾细胞中的差异表达的蛋白主要与凋亡信号的调控有关。因此,本发明推测卡铂促进T细胞凋亡也可能是受到Bcl-2家族调控。
总之,本发明证明卡铂通过抑制EAE小鼠外周组织中致病性T细胞的数量来减轻EAE的临床和组织病理学症状。此外,本发明的结果表明卡铂抑制T细胞增殖并促进T细胞凋亡。本发明的研究表明卡铂是治疗MS的潜在治疗剂。
虽然本发明已以较佳实施例揭示如上,然其并非用以限定本发明,任何本领域技术人员,在不脱离本发明的精神和范围内,当可作些许的修改和完善,因此本发明的保护范围当以权利要求书所界定的为准。
- 金络合物在制备预防和/或治疗多发性硬化症的药物中的应用
- 金络合物在制备预防和/或治疗多发性硬化症的药物中的应用
