乳剂组合物及其在预防和/或治疗由辐射引起的皮肤损伤中的用途
文献发布时间:2024-04-18 19:44:28
技术领域
本发明涉及呈适用于外用施用的形式的药物组合物的领域。更具体地,本发明涉及包含血管收缩剂诸如溴莫尼定或其盐的药物组合物;以及这样的组合物,其用作药物,更具体地用于预防和/或治疗皮肤辐射损伤。
可能损害皮肤的辐射类型包括紫外线(UV),包括可导致晒伤的UVA和UVB;可见光范围内的射线;红外辐射(IR);电离辐射,诸如X射线和α、β或γ辐射;以及由质子构成的辐射。
背景技术
辐射暴露对组织的第一类影响之一是红斑,即,一种导致血管扩张和皮肤变红的炎症反应。这种反应在暴露于UV后大约6-8小时可见并且在36-48小时后消失。
已知将高选择性α2-肾上腺素能受体激动剂真皮应用于面部借助直接皮肤血管收缩来减轻红斑。皮肤血管收缩的主要特征是苍白;通过减小真皮中的小动脉和小血管的直径,其导致血流量立即减小,从而特别是产生皮肤颜色的降低。
因此,
更具体地,溴莫尼定已知是一种高选择性α2-肾上腺素能受体激动剂。溴莫尼定对α2-肾上腺素能受体的选择性比α1-肾上腺素能受体高1,000倍。
已经显示溴莫尼定可用于治疗由痤疮性酒渣鼻引起的红斑并且已经被提出用于其他皮肤障碍。参见例如专利申请US10/853585、专利申请US10/626037和专利申请US 12/193098。
溴莫尼定(酒石酸盐)具有适用于外用施用的化学稳定性和提供不同配制选择的溶解度特征。
例如,我们知道专利文献WO 2015013709描述了通过使用酒石酸溴莫尼定减轻和/或抑制辐射诱发的皮肤增生,通过外用施用,例如以乳剂的形式,其浓度为按重量计0.01%-5%,优选按重量计0.1%-2%。例如,其披露了一种组合物,所述组合物包含具有基于PVM/MA、乙醇和聚二甲基硅氧烷的乙酯共聚物的醇相;基于PVP/PA共聚物的水相;和包含oleth-20、椰油酰胺MEA和硬脂醇聚醚-16的油相。此类配制品中乙醇的存在使其特别不适合用于治疗辐射诱发的皮炎,因为它会在皮肤受损的患者中引起刺痛和烧灼感。
我们还知道,专利文献US20110224216描述了一种治疗诱发性红斑的方法,例如,通过物理程序,诸如激光辐射、UV辐射、射频、放疗、发光二极管,通过外用施用特别是呈乳膏形式的组合物,所述组合物特别地包含酒石酸溴莫尼定、PEG-300和PEG-6硬脂酸酯。
此外,我们知道文献WO 2012075319描述了一种用于治疗酒渣鼻和酒渣鼻相关症状的基于羟甲唑啉的组合物,所述组合物另外含有丁基羟基甲苯、PEG、二醇、PEG-32硬脂酸酯、鲸蜡硬脂醇和油醇。
为治疗目的而设计的外用产品通常由活性成分和赋形剂组成。在配制过程中,对于盖仑制剂形式的稳定性及其质地、局部耐受性和患者依从性,赋形剂的选择对于通过使活性成分可溶并且优化其皮肤渗透来保证药物的功效而言是至关重要的。除了优化这些单独元素中的每一种之外,一个复杂且相辅的挑战是鉴定这些关键因素的最佳平衡,以提供满足患者、医疗保健专业人员调节身体的需求的产品。
通常难以用包括盐在内的离子化活性剂产生释放和皮肤储库,因为它们倾向于不太容易渗透角质层(主要由脂质构成的屏障)。此外,此类活性剂由于其在水中的溶解性而倾向于从活组织中被快速清除。
溴莫尼定实际上是一种亲水性分子并且因此难以渗透脂质角质层。
另一方面,一旦跨过角质层,溴莫尼定进入亲水性介质(表皮,尤其是颗粒层和基底层,并且然后是真皮),并且然后被消除,从而降低血管收缩的有效性。
因此,由皮肤形成的屏障的结构对获得设计用于皮肤应用的外用配制品提出了真正的挑战,所述外用配制品允许活性血管收缩剂通过外脂质层而不在下层亲水层中被快速消除,从而在16小时或甚至24小时的时间段内产生快速、持续且延长的血管收缩作用。
此外,所用的活性血管收缩剂的浓度不得太高,因为这然后将在全身水平上造成显著且潜在有害的暴露风险。
另外,旨在用于外用应用的组合物中的某些化合物可能引起副作用,所述副作用可能限制它们的使用并且因此限制它们的有效性。例如,某些活性剂具有引起刺激的主要缺点,这可能导致产品耐受性差。这进而可能就患者而言导致对治疗的不依从性和对所述治疗不满意。
为此,以对羟基苯甲酸甲酯、丙二醇、卡波姆、苯氧基乙醇、丙三醇、二氧化钛、氢氧化钠和纯化水为其基质的
目前需要开发新的组合物,使得有可能限制与辐射相关的效应并且特别是通过放疗治疗癌症的副作用。
辐射性皮炎(或辐射诱发的皮炎)产生的病变使患者感到疼痛和忧虑并且可能导致暂时或永久中止治疗。
然而,对于急性辐射性皮炎的治疗尚无一致意见。已经提出了许多不同的解决方案,目前还没有被所有人接受的足够满意度水平。
对于急性1级辐射性皮炎,在辐射时段后几小时应用的润肤剂(诸如
然而,重要的是注意,该选项要求不在所述时段前应用这些产品,以避免组织等效物效应(bolus effect)(辐射剂量的局部增加)和增加的烧伤风险。
提供了一些更具体的用于辐射性皮炎病变的产品,诸如基于透明质酸的乳膏、
所述时段结束后还应应用局部外用皮质类固醇(诸如
在急性辐射性皮炎的情况下,如果放疗科医师认为暂时中断放疗治疗的继续是有必要或优选的,则可以将其暂时中断,这取决于治疗的进展和治疗的优先项。
已经描述了使用一种外用血管收缩剂(肾上腺素)来预防接受放疗的乳腺癌患者的辐射性皮炎(James F.Cleary等人,Significant suppression of radiationdermatitis in breast cancer patients using a topically applied adrenergicvasoconstrictor,Radiation Oncology,2017)。
然而,此类产品是一种临时的基于醇的挥发性制剂,需要在即将放疗治疗之前、最多20分钟之前应用。
此外,其效果是有限的,最值得注意的是因为其作用持续时间极短。因此,在所讨论的研究中,仅50%的患者显示出显著的益处。
在这些患者已经发现难以耐受的癌症治疗中,副作用可能是限制性的并且可能干扰最佳治疗过程。因此,确实需要新的有效配制品,其使得有可能产生强有力且延长的保护效果并且从而显著地减轻放疗治疗的皮肤副作用。
因此,需要开发新的配制品,其目的在于随着时间的推移,在皮肤中产生强有力的、延长的、受控的血流减少,限于应用部位,并且克服上面提及的在接受辐射的患者、特别是用放疗治疗的癌症患者的耐受性、有效性和依从性方面的缺点。
技术问题
考虑到上述情况,本发明提出要解决的一个问题在于开发一种优化的外用配制品,所述外用配制品基于已充分确立的血管收缩剂,诸如酒石酸溴莫尼定,并且目的在于改善血管收缩剂在预防和显著减轻由辐射引起的主要皮肤副作用方面的活性的持续时间和效力,最值得注意的是在通过放疗的癌症治疗中。
所获得的优点
申请人开发了一种新的外用组合物,所述外用组合物通过使血管收缩剂在真皮和表皮中的生物利用度超过12-14小时来改善血管收缩的持续时间和效力,以保护皮肤免受由辐射引起的损伤并且更特别地免受放疗治疗的皮肤副作用,同时避免对放疗射线的任何干扰,很可能降低它们对被治疗肿瘤或辐射场的有效性。
已经开发了复杂且难以提供的含有低分子量(低于150g/mol并且优选低于100g/mol)极性溶剂和较高分子量(高于150g/mol,优选在350-650g/mol之间)极性溶剂的组合,以便在皮肤表面上和角质层的上层中产生酒石酸溴莫尼定储库。然而,亲水性化合物储库的形成比亲脂性药剂更复杂得多,因为极性化合物不像亲脂性化合物那样容易分布在角质层中。另外,亲水性化合物本身在活组织中更游离地分布并且通过血液循环进入下面的局部血管系统中而被去除。因此,必须鉴定最佳且复杂的组成平衡,以调节变量,诸如热力学、残留表面溶解度、在角质层中的溶解度、在活组织中的渗透和持久性(牵引效应/溶剂拖曳)。
除了上述参数之外,在开发根据本发明的组合物时,还考虑了对产生可接受的剂型和成品重要的因素。根据本发明的组合物集中于最佳溶剂系统,其促进真皮施用并且提供足够的物理、化学和微生物稳定性,以及适当的局部耐受性和美容优雅性。
由申请人由此提出的优化外用组合物改善了血管收缩过程的持续时间(从至少14小时到24小时的时间段)以及其能力,但是没有中断辐射通过皮肤的过程并且因此避免了其功效的降低。
根据本发明的组合物将允许在角质层中产生活性极性血管收缩剂储库,这种现象通常只有亲脂性分子诸如皮质类固醇才能获得,极性分子通常被血流快速“洗出”。这允许在皮肤中的持久性以及因此在每次再次应用时最大且快速的效果。这种动力学允许最大的预防效率并且为患者和放疗科医师提供了使用灵活性。
特别适用于放疗治疗的优化组合物有助于促进患者的依从性并且使抗癌治疗的有效性最大化。
此外,申请人由此开发的新外用配制品耐受性良好,因为与现有技术的组合物相比,其刺激性非常小或根本没有刺激性,具有改善的皮肤渗透和增加的酒石酸溴莫尼定溶解度。
最后,所开发的根据本发明的药物组合物的制备也是经济、容易且快速的。
技术方案
该问题的解决方案的第一目的是一种具有水基质的呈适用于外用施用的形式的组合物,所述组合物在基于溶剂的相中包含血管收缩剂,所述组合物呈包含液晶的乳剂、优选油包水或水包油、更优选水包油的形式,并且所述血管收缩剂选自溴莫尼定或其盐,所述基于溶剂的相包含:
-聚乙二醇与丙二醇的组合;
-亲水性成膜剂,所述亲水性成膜剂选自聚乙烯吡咯烷酮/乙酸乙烯酯共聚物、呈非交联、交联或乙酸酯形式的聚乙烯吡咯烷酮(PVP),单独或组合使用,优选聚乙烯吡咯烷酮/乙酸乙烯酯共聚物作为亲水性成膜剂;
-甘油;
-乳化剂,所述乳化剂选自PEG-75硬脂酸酯和单硬脂酸甘油酯的组合以及聚氧乙烯-20脱水山梨醇单硬脂酸酯(聚山梨醇酯-60)和鲸蜡硬脂醇的组合;
-油酸或油醇,优选油醇;和
-油相,所述油相适用于获得包含液晶的乳剂、优选油包水或水包油、更优选水包油。第二目的是根据本发明的组合物,其用作药物。
附图说明
通过阅读关于附图的以下描述和非限制性实施方法,将更好地理解本发明和源自本发明的优点,在所述附图中:
图1表示使用
图2表示使用
图3表示在实施例5并且特别是表14的背景下进行的方法条件下,使用参考组合物19-0155-0090P/F3,用不同组合物获得的粘度测量结果。
图4表示用不同W/O乳剂组合物19.0155-0083/F1(基于Gelot-64)、19.0155-0087/F1(基于Gelot-64)和19.0155.0086A/F1(基于Polawax)获得的皮肤美白得分。
图5表示用不同乳剂组合物19-0155.0091/F1(基于Polawax)、19-0155.0089/F1(基于Brij)和19-0155-0090/F1(基于Gelot)获得的皮肤美白得分。
图6示出了用不同的活性(包含酒石酸溴莫尼定)或非活性(仅包含媒介物)水包油乳剂获得的皮肤美白得分。
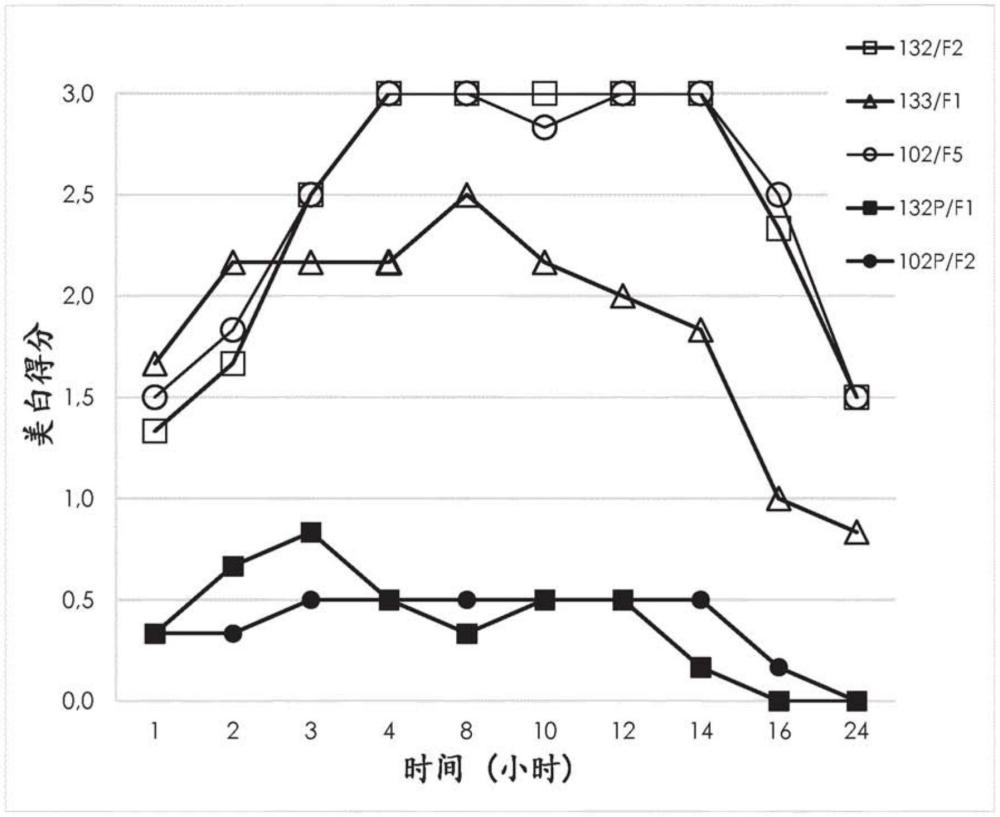
图7表示用不同的活性(包含酒石酸溴莫尼定,19-0155-0102/F5)或非活性(仅包含媒介物,19.0155-0102P/F2)水包油乳剂组合物获得的皮肤美白得分。
图8表示用不同的活性(包含酒石酸溴莫尼定)或非活性(仅包含媒介物)水包油乳剂组合物获得的平均红斑得分。
图9表示参考血管收缩剂产品获得的皮肤美白得分。
图10表示用改良的MIRVASO组合物(1.5%w/w酒石酸溴莫尼定)(19-0155-0098/F1)、去甲肾上腺素溶液和
具体实施方式
本发明涉及一种具有水基质的呈适用于外用施用的形式的组合物,所述组合物包含血管收缩剂。
根据本发明的外用组合物的特征在于所述外用组合物呈具有液晶的乳剂、优选油包水或水包油、更优选水包油的形式。
液晶是分子的无限聚集体,其大大提高了溶解度并且促进了乳化。
从微观结构的角度来看,亲水性非离子乳化剂与脂族脂肪醇的组合通过产生被层状相包围的液晶而在乳剂的连续相中导致特定组织。层状相的普遍存在与过量的一种或多种脂肪醇有关。
液晶配制品作为外用组合物的媒介物具有几个优点,包括:
-修复皮肤屏障;
-向皮肤递送水分;
-优异的耐受性;
-改善某些活性剂的皮肤释放。
根据本发明的外用组合物的特征在于所述外用组合物在溶剂相中包含选自溴莫尼定或其盐的血管收缩剂,所述溶剂相包含:
-聚乙二醇与丙二醇的组合;
-亲水性成膜剂,所述亲水性成膜剂选自聚乙烯吡咯烷酮/乙酸乙烯酯共聚物(KOLLIDON VA
-甘油;
-乳化剂,所述乳化剂选自PEG-75硬脂酸酯和单硬脂酸甘油酯的组合以及聚氧乙烯-20脱水山梨醇单硬脂酸酯(聚山梨醇酯-60)和鲸蜡硬脂醇的组合;
-油酸或油醇,优选油醇;
-和油相,所述油相适用于获得包含液晶的乳剂、优选油包水或水包油、更优选水包油。
术语“盐或药学上可接受的盐”是指感兴趣的化合物的那些盐,其对于哺乳动物的外用使用是安全且有效的并且具有希望的生物活性。药学上可接受的盐包括指定化合物中存在的酸或碱基团的盐。药学上可接受的酸加成盐包括但不限于以下:盐酸盐、氢溴酸盐、氢碘酸盐、硝酸盐、硫酸盐、硫酸氢盐、磷酸盐、酸式磷酸盐、异烟酸盐、乙酸盐、乳酸盐、水杨酸盐、柠檬酸盐、酒石酸盐、泛酸盐、酒石酸氢盐、抗坏血酸盐、琥珀酸盐、马来酸盐、龙胆酸盐、富马酸盐、葡萄糖酸盐、葡萄糖醛酸盐、糖酸盐、甲酸盐、苯甲酸盐、谷氨酸盐、甲磺酸盐、乙磺酸酯、苯磺酸盐、对甲苯磺酸盐和双羟萘酸盐(即,1,1'-甲苯基-双-(2-羟基-3-萘甲酸盐))。用于本发明的某些化合物可以与各种氨基酸形成药学上可接受的盐。合适的碱盐包括但不限于铝、钙、锂、镁、钾、钠、锌和二乙醇胺的盐。关于药学上可接受的盐的综述,参见Berge等人,66J.PHARM.SCI.1-19(1977)。在本发明上下文中,术语“水合物”是指感兴趣的化合物或其药学上可接受的盐,其进一步包含化学计量或非化学计量量的通过非共价分子间力与其结合的水。
优选地,用于根据本发明的组合物中的溴莫尼定是酒石酸溴莫尼定,但是从油包水或水包油乳剂配制品的稳定性角度来看,盐形式存在挑战。
确实,盐可以与非离子表面活性剂和聚合物相互作用并且降低它们的水溶性,并且因此损害半固体配制品的物理稳定性。相反,活性剂的盐水形式产生相对高的水溶性并且有利地允许设计和评价基于水性的配制品,所述配制品可以在感觉和局部耐受性方面提供改善的性能。
优选使用浓度为占组合物总重量的按重量计在0.15%与3.00%之间的溴莫尼定或其盐、优选酒石酸溴莫尼定以实现功效和在应用后长达24小时的改善的作用持续时间,同时防止任何全身暴露的风险。
优选地,根据本发明的组合物包含浓度为占组合物总重量的按重量计在0.50%与2.50%之间、优选在0.75%与1.50%w/w之间、更优选在1.00%与1.50%w/w之间、甚至更优选1.00%或1.50%w/w的溴莫尼定或其盐,优选酒石酸溴莫尼定。
溴莫尼定、优选酒石酸溴莫尼定的浓度以及由此应用的剂量有利地根据应用的位点进行调整。
确实,脚和手上的由皮肤形成的屏障比头皮上的更厚,特别是在待穿过的角质层方面,并且身体的其余部分并且特别是胸部具有中等厚度。因此,对于相同的剂量,与在身体其余部位使用的浓度(例如,在胸部的浓度为0.75%-1.5%w/w或甚至在脚和手上的浓度为例如1.5-3%w/w)相比,在头皮上优选使用的浓度有利地更低,例如在0.15%-0.5%w/w的范围内。
优选地,根据本发明的由液晶构成的油包水或水包油乳剂的油相包含单独或组合使用的鲸蜡醇和硬脂醇,和/或单独或组合使用的椰子/棕榈仁的饱和辛酸和癸酸脂肪酸与植物源丙三醇的甘油三酯(Miglyon 812N)和聚丙二醇(PPG)-11硬脂基醚(Arlamol PS11E-LQ-[RB])。
优选地,油相包含鲸蜡醇和硬脂醇的组合。
根据本发明的包含液晶的油包水或水包油乳剂组合物的油相优选包含组合使用的鲸蜡醇、硬脂醇和油醇,其浓度为占组合物总重量的按重量计在1%与15%之间、优选在2.5%与10%之间。
优选地,油相包含椰子/棕榈仁的饱和辛酸和癸酸脂肪酸与植物源丙三醇的甘油三酯和PPG-11硬脂基醚的组合。
根据本发明的具有液晶的油包水或水包油乳剂组合物的油相优选包含椰子/棕榈仁的饱和辛酸和癸酸脂肪酸和植物源丙三醇的甘油三酯和PPG-11硬脂基醚的组合,其浓度为占组合物总重量的按重量计在5%与10%之间。
根据本发明的外用组合物的特征在于所述外用组合物包含聚乙二醇(PEG)与丙二醇(PG)的组合。
虽然低分子量聚乙二醇(PEG)通常用于外用产品,主要是因为它们通常是许多类型活性成分的有效溶剂,但就外用施用而言,它们不一定是最有效的赋形剂。
这主要与它们的高极性和分子量有关,所述高极性和分子量限制了它们通过皮肤的吸收。这些特性限制了溶剂将活性剂携带(牵引)到皮肤中的潜力。这通常在溶剂在皮肤下溶解并且将溶解的溶质输送到皮肤中时发生。
另外,PEG的高溶解能力可能导致对于外用施用的次优热力学,并且在以高浓度使用的情况下,通常与挥发性组分诸如水的蒸发相关的产物转化不能用于增强在皮肤中的释放。从整体来看,这些特性可能降低递送效率,尽管高浓度也是可能的;大部分应用剂量的外用药剂保留在皮肤表面上或通过接触转移流失到周围环境中。
增加的递送效率,即应用剂量的分数,可以限制增加剂量以达到真皮递送的目标水平的需要和使用高PEG浓度的需要。
还显示PEG的渗透和穿透取决于它们的分子量。
然而,在根据本发明的油包水或水包油乳剂组合物中,PEG对于外用配制品是必需的。
通过限制刺激潜力、消除极性杂质并且因此减少赋形剂与活性剂(酒石酸溴莫尼定)之间的相互作用和随后的活性剂分解,优选使用高达PEG-600的小分子量PEG,诸如PEG-200、PEG-300、PEG-400或PEG-400SR,更优选PEG-400并且甚至更优选PEG-400SR,有益地促进了根据本发明的油包水或水包油乳剂组合物的稳定性和耐受性。
尽管PEG-400或PEG-400SR由于其分子量和高极性(低分配系数)而具有相对低的到角质层中的渗透,但是根据本发明的油包水或水包油乳剂组合物中优选使用的PEG降低了活性剂在皮肤表面上和角质层的上层中的沉淀的速率(对于表面溶解而言)。这有利于延长酒石酸溴莫尼定向活皮肤层中并且特别是向酒石酸溴莫尼定的靶位点所在的真皮丛的血管中的施用。PEG-400或PEG-400SR具有足够的溶解度,以促进在溶液中的酒石酸溴莫尼定更好地保留在皮肤表面上和角质层的上层中。
优选地,根据本发明的组合物包含浓度为占组合物总重量的按重量计在1%至20%之间、优选在5%与15%之间、更优选10%的PEG。
丙二醇(PG,1,2-丙二醇)是一种透明、无色、吸湿性的液体,其广泛用作各种肠胃外和非肠胃外药物配制品中的溶剂和防腐剂。
PG已知是比甘油更好的通用溶剂,并且溶解多种多样的材料,包括皮质类固醇、酚类、巴比妥类、酚类、巴比妥类、维生素(A和D)、大多数生物碱和许多局部麻醉剂。
然而,在酒石酸溴莫尼定的情况下,PG具有甘油50%的溶解能力。
作为抗细菌剂,PG的作用与乙醇相似;然而,其防霉菌作用稍差,其特征与甘油可比较。
PG还展现出挥发性:尽管当应用到皮肤上时或至少在应用后37小时内,应用剂量的一部分蒸发,但更大得多的一部分渗透角质层并且渗透到皮肤的深层中。
PG相对快速地渗透角质层以及其挥发性可能耗尽其溶剂的残留媒介物,增加媒介物中活性剂的热力学活性,并且因此改变扩散的驱动力。另外,PG的渗透和穿透也可能破坏角质层中的脂质屏障并且从而降低扩散阻力。
因此,PG在皮肤渗透和穿透方面具有有利的物理化学特性并且通过皮肤吸收。因此,易于被PG溶解的溶质(即,高的溶剂/媒介物亲和力)可以通过溶剂抗性机制或牵引效应而受益于改善的皮肤渗透。
即使各种化合物的数据在文献中被描述为表明药学上相关的化合物的真皮递送可以被PG增强,但对于本领域的技术人员来说,当其在复杂的溶剂体系中使用以获得有效、稳定且药学上可接受的根据本发明的外用组合物时,在稳定性、活性剂(尤其与酒石酸溴莫尼定)的渗透效率和耐受性方面预测这些特征不是显而易见的。
毋庸置疑,PG已知比大多数活性剂更快地知渗透皮肤,并且因此,活性剂在皮肤表面上的沉淀将限制其作用持续时间。
另外,所用PG的体内浓度通常限制在约20%w/w或更低,以避免局部刺激反应和全身毒性问题。
由于溶解度和其他媒介物相关的变量,不容易预测在根据本发明的外用组合物中选择使用PG作为溶剂和渗透增强剂。
优选地,根据本发明的组合物包含浓度为占组合物总重量的按重量计在5%与40%之间、优选在10%与30%之间、更优选在15%与25%之间并且甚至更优选20%的PG。
在根据本发明的油包水或水包油乳剂组合物的背景下,控制PEG:PG的比率是特别有益的。
过高浓度的PEG与PG组合(高于50%w/w)对酒石酸溴莫尼定的血管收缩强度有负面影响。
根据一个优选的实施方案,PEG和PG以1:1至1:5、优选1:2的比率使用。
优选地,根据本发明的组合物包含浓度为占组合物总重量的按重量计10%的聚乙二醇(PEG)与浓度为占组合物总重量的按重量计20%的丙二醇(PG)的组合。
根据本发明的外用组合物的特征在于所述外用组合物包含亲水性成膜剂,所述亲水性成膜剂选自呈非交联、交联或乙酸酯形式的聚乙烯吡咯烷酮/乙酸乙烯酯共聚物(PVP),单独或组合使用。
优选地,根据本发明的组合物由以下构成:单独或组合使用的亲水性成膜剂,其浓度为占组合物总重量的按重量计在0.1%与1.5%之间、优选在0.25%与1.4%之间、更优选在0.5%与1.3%之间、甚至更优选在0.75%与1.25%之间、甚至更优选1%。
优选地,根据本发明的外用组合物包含聚乙烯吡咯烷酮/乙酸乙烯酯共聚物(KOLLIDON VA
优选地,根据本发明的组合物包含浓度为占组合物总重量的按重量计在0.1%与1.5%之间、优选在0.25%与1.4%之间、更优选在0.5%与1.3%之间、甚至更优选在0.75%与1.25%之间、甚至更优选1%的聚乙烯吡咯烷酮/乙酸乙烯酯共聚物(KOLLIDON VA
根据本发明的外用组合物的特征在于所述外用组合物进一步包含甘油。
甘油(丙三醇)是一种众所周知的可以增加水在角质层中的保留并且改善水合作用的保湿剂。
甘油也是已知的并且用于支持皮肤屏障的正常功能,促进皮肤弹性和可塑性,改善皮肤光滑度并且提供抗刺激作用。甘油实际上能够将水从表皮和大气吸引到角质层中。
由于其相对高的极性,甘油对皮肤的渗透程度和深度与丙二醇不同,但可以在角质层的亲水性区域中积聚并且形成储库,并且增加水含量。
甘油与角质层的相互作用、其在皮肤中的分布以及其对酒石酸溴莫尼定的相对高的溶解度(是丙二醇的两倍)提供了改善的皮肤的施用和延长的皮肤渗透而不会在皮肤表面造成粘性的优点。
优选地,根据本发明的组合物包含浓度为占组合物总重量的按重量计在1%与20%之间、优选在2%与15%之间、更优选在3%与10%之间、甚至更优选4%的甘油。
以特别有利的方式,PG和甘油的组合改善了活性剂、优选酒石酸溴莫尼定在角质层中的分布。
根据本发明的外用组合物的特征在于所述外用组合物进一步包含乳化剂,所述乳化剂选自PEG-75硬脂酸酯和单硬脂酸甘油酯的组合以及聚氧乙烯-20脱水山梨醇单硬脂酸酯(聚山梨醇酯-60)和鲸蜡硬脂醇的组合,优选PEG-75硬脂酸酯和单硬脂酸甘油酯(Gelot64)的组合。
根据一个优选的实施方案,根据本发明的组合物包含PEG-75硬脂酸酯和单硬脂酸甘油酯(Gelot 64)的组合,其含有熔点在46℃与66℃之间的脂肪成分。
考虑到制造过程,乳化后最重要的步骤是冷却阶段,所述乳化在约65℃±5℃的温度下进行。温度的降低导致脂肪成分在达到其转变温度时结晶。
在冷却阶段,脂肪乳化剂/助乳化剂被组织在油滴周围。亲脂性助乳化剂主要保留在油滴中,而亲水性乳化剂和两亲性脂肪脂族醇保留在乳剂的油滴与连续水相之间的界面处。
优选地,根据本发明的组合物包含浓度为占组合物总重量的按重量计在1%与10%之间、优选在2%与7%之间、更优选在3%与5%之间、甚至更优选3%w/w的乳化剂(例如,GELOT
根据本发明的外用组合物的特征在于所述外用组合物进一步包含油酸或油醇,优选油醇(KOLLICREAM
优选地,根据本发明的组合物包含浓度为占组合物总重量的按重量计在0.1%至7%之间、优选在1%与5%之间、更优选2.5%的油酸或油醇。
优选地,根据本发明的外用组合物进一步包含黄原胶作为胶凝剂。
优选地,根据本发明的组合物包含浓度为占组合物总重量的按重量计在0.1%与1.5%之间的黄原胶,优选在0.2%与1%之间、更优选分别在0.2%-0.5%之间的黄原胶。
因此,除了其他非挥发性溶剂PG和PEG之外,黄原胶和聚乙烯吡咯烷酮/乙酸乙烯酯共聚物(KOLLIDON VA
优选地,根据本发明的外用组合物进一步包含天然或合成抗氧化剂或自由基清除剂。
所述抗氧化剂优选选自丁基羟基茴香醚(BHA)、DL-生育酚、丁基羟基甲苯(BHT)、丙醛、抗坏血酸棕榈酸酯或谷胱甘肽,单独或混合使用,优选BHA和/或DL-生育酚。
根据本发明的油包水或水包油乳剂组合物中优选使用浓度为占组合物总重量的按重量计在0.01%与4.0%之间、更优选在0.1%与1.0%之间、甚至更优选0.1%的抗氧化剂,例如0.1%w/w的BHA和/或0.1%w/w的DL-生育酚。
优选地,根据本发明的外用组合物进一步包含对羟基苯甲酸酯,所述对羟基苯甲酸酯选自对羟基苯甲酸甲酯、对羟基苯甲酸丙酯或对羟基苯甲酸异丙酯,单独或组合使用。
优选地,根据本发明的组合物包含浓度为占组合物总重量的按重量计在0.01%至0.5%之间、优选在0.1%与0.4%之间、更优选0.3%的单独或组合使用的对羟基苯甲酸酯。
优选地,根据本发明的组合物进一步包含优选浓度在0.15%与1.5%之间、更优选在0.4%与1.25%之间、甚至更优选在0.5%与1.1%之间、甚至更优选1%w/w的苯氧基乙醇;优选浓度在0.05%与0.5%之间、更优选在0.1%与0.3%之间、甚至更优选0.2%w/w的苯甲酸钠;优选浓度在0.1%与1%之间、更优选在0.25%与0.75%之间、甚至更优选0.5%w/w的作为替代防腐剂的苯乙醇;和/或优选浓度为0.2%w/w的EDTA作为螯合剂,其有助于组合物的保存和稳定性。
更优选地,所述组合物包含组合使用的苯氧基乙醇、苯甲酸钠、苯乙醇和EDTA。
将亲水性溶剂相与具有吸湿性、保湿性和皮肤调理特性的溶剂(包括PG和甘油)结合改善了酒石酸溴莫尼定在角质层中的溶解度并且增加其中的水含量。
抗氧化剂的掺入有益地改善了活性剂和油相的稳定性。
此外,所用的油相已被选择为利于乳剂形成、物理稳定性和所希望的微观结构的实现,并且有助于皮肤递送,同时呈现适当的感官性能。
因此,根据本发明的油包水或水包油乳剂组合物允许改善和延长酒石酸溴莫尼定的皮肤递送,并且满足患者的需要,具有足够和延长的局部血管收缩以及优越的表皮和真皮保护以免受活性氧物质和炎性介质的影响。
根据本发明的此类组合物易于应用并且可以应用于潜在受刺激的皮肤。
它们提供了快速干燥,在皮肤上残留最少。
根据本发明的外用组合物的pH在3.5.0与6.5之间、优选在4.0与5.5之间、更优选为4.5。
根据本发明的油包水或水包油乳剂组合物被设计成含有相对高量的二醇,例如20%PG和10%PEG-400。如此相对高浓度的这些组分不一定支持微观结构的稳定性和维持,因为它们可能破坏界面并且溶解乳化剂和助乳化剂。另外,添加相对高浓度的活性盐酒石酸溴莫尼定呈现了界面和乳剂的物理不稳定的可能性。
然而,这些特性使得有可能获得油包水或水包油、优选水包油乳剂组合物,所述组合物具有高密度的小油滴和液晶,从而改善了这些结构的表面积并且增加了活性剂向角质层中的渗透。
本发明的另一个目的涉及用作药物的根据本发明的油包水或水包油、优选水包油乳剂组合物。
优选地,根据本发明的油包水或水包油乳剂组合物用于预防和/或治疗由辐射引起的损伤,无论此类辐射是光子还是质子并且无论它是天然的、治疗性的还是偶然的,包括紫外(UV)辐射(包括可能导致晒伤的UVA和UVB辐射)、可见光范围内的辐射、红外(IR)辐射、或电离辐射诸如X射线和α、β、γ辐射或质子束。
更优选地,根据本发明的油包水或水包油乳剂组合物用于预防和/或治疗由辐射引起的皮炎,值得注意的是在放疗治疗中,例如通过X射线。
实施例
现将用以下实施例来说明本发明:
方法
通过向各种溶剂中添加过量的药物物质并且将样品在室温下在连续搅拌下在密封容器中储存24小时来制备饱和方法。
通过磁力搅拌器搅拌大多数样品;然而,在粘性样品(例如,纯甘油)的情况下,使用旋转混合器搅拌样品。调节旋转混合器的速度以确保样品的适当混合,并且这通常涉及较慢的旋转速度。
平衡期后,将样品离心或过滤,并且使用Thermo Scientific Dionex U3000UPLC-UV系统定量酒石酸溴莫尼定。下面描述了色谱条件:·柱:Sunfire C18 150mm x4.6mm,3.5μm
·柱温:40℃
·注射体积:5μl
·流速:0.8ml/分钟
·UV监测:246nm
结果
每种独立使用的溶剂的溶解度饱和结果总结在表1中。
表1:
*再注入后T+72小时观察到的峰降解
**再注入后T+24小时观察到的峰降解。
***进行的目视溶解度。由于观察到高溶解度,因此未进行UPLC-UV分析。
****产品专题:
结论
根据获得的结果,DMSO看起来是酒石酸溴莫尼定的优良溶剂。即使在添加8.5%w/w酒石酸溴莫尼定后也没有达到饱和。
水看起来是第二好的溶剂;活性剂的盐形式很可能利于其在水中的溶解度。
然后,按降序是甘油(GLY)、glucam、丙二醇(PG)和PEG-400。
对于其他溶剂观察到的溶解度显著更低并且没有提供令人满意的酒石酸溴莫尼定的溶解度结果。
有趣的是,对于酒石酸溴莫尼定而言,众所周知的溶剂诸如Transcutol和DMI看起来远不如甘油或丙二醇有效。
方法
如实施例1中所述制备、培养和测量饱和溶液。
结果
不同溶剂混合物的溶解度饱和结果总结在表2中。
表2:
结论
如所预期的,非水性溶剂混合物看起来具有比含水混合物更低的溶解能力。
然而,根据由此获得的结果,与水性混合物PG/PEG-400/GLY/PVP/水(20:10:5:1:40)相比,含有PG/PEG400/GLY/PVP(20:10:5:1)的非挥发性混合物看起来能够溶解大约22%的活性剂。这表明水性凝胶的非挥发性极性组分可能具有一定的溶解皮肤表面上和角质层中的酒石酸溴莫尼定到残留配制品中的能力,即使在水蒸发之后也是如此。
如果使用浓度为1%或1.5%的酒石酸溴莫尼定,则在应用之前,活性剂在主要配制品的水性溶剂相中可以分别为约30%或50%的饱和度。然而,当配制品应用于皮肤表面时,水将相对快速地蒸发。
因此,所获得的结果在配制品的物理稳定性方面看起来是有利的,但在常规皮肤分布方面不一定是有利的,并且热力学活性将相对低。
如表3所述制备溶剂组合。为了便于评价,向每种混合物中添加0.1%酒石酸溴莫尼定。将样品在环境温度、40℃和50℃下储存1个月,并且取样间隔T=0和T=1个月。
表3:
表4总结了本研究中产生的相容性数据。
表4:
根据获得的结果,平均值在99.36%与101.45%之间,并且相对标准偏差小于1%。
不含Glucam E20的溶剂混合物显示出最有利的稳定性特征,并且
不含Glucam E20的溶剂共混物显示出最有利的稳定性特征,而甘油看起来改善了稳定性。当Glucam E10以5%的浓度包含在组合物中时,酒石酸溴莫尼定的稳定性得到改善。酒石酸溴莫尼定测量值倾向于随着Glucam浓度的增加而降低。M8(在水中的30%Transcutol)获得了最稳定的溶剂混合物,然后是M1(在水中的10%DMSO、5%Glucam E10和5%甘油)。
获得的数据表明,使用Glucam E10和E20会增加酒石酸溴莫尼定不稳定性的风险。另一方面,transcutol、DMSO和甘油显示出可接受的相容性特征。
制备不同组合物并且评价它们的短期物理稳定性。
使用离心和更定量快速的筛选工具
多样品
根据澄清率和不稳定性指数、沉降和颗粒浮选率、残余浊度、分离相(液体或固体)的体积、沉积物固结或脱水对分层(demixing)现象进行量化。
下表5-8中提到的组合物的稳定性使用标准化
表5:19-0155.0045(水包油乳剂;基于BRIJ/ARLAMOL;活性剂)
表6:19-0155.0065P(水包油乳剂;Brij/Arlamol基质;媒介物)
表7:19-0155.0090/F1(水包油乳剂,Gelot 64基质)
表8:19-0155.0091(水包油乳剂,Polawax基质)
用
此类初步结果表明,配制品19-0155.0045(具有Brij/Arlamol基质的水包油乳剂)是最不稳定的,并且比仅包含媒介物(没有活性剂酒石酸溴莫尼定)的等效组合物(19-0155.0065P)更不稳定。
该数据表明,活性物质酒石酸溴莫尼定在该组合物中具有去稳定作用,这可能是由于其盐水的形式。
另一方面,包含由Gelot 64(19-0155.0090)和Polawax(19-0155.0091)制成的活性物质的其他组合物令人惊讶地显示出类似于媒介物19-0155.0065P的物理稳定性。
使用
表9:使用
RT-室温
LC-液晶
N/A-不适用
表10:使用
LC-液晶
表11:使用
LC-液晶
获得的额外结果示出在图2中。
常规目视观察结果和用
从基于BRIJ/ARLAMOL的组合物中可以得到有益的观察结果:
媒介物(19-0155.0070P/F1)比包含活性剂酒石酸溴莫尼定的相同组合物(19-0155.CR2.0044A/F1)更稳定;
10%w/w PEG-400的添加增加了所有包含活性剂的测试组合物(19-0155.0076/F2和19-0155.0089/F1与19-0155.CR2.0044A/F1)的稳定性;
黄原胶的添加也增加了稳定性,并且组合物19-0155.0089/F1比组合物19-0155.0076/F2稍微更稳定(在40℃下储存3个月后显示出渗出物并且显示出稍微更高的不稳定指数)。
两种基于Gelot 64的乳剂(19-0155-0083/F1和19-0155-0087/F1)显示出良好的稳定性,即使没有有益地包含黄原胶作为稳定剂也是如此,并且给出了最好的结果。
使用基于Gelot 64的组合物(19-0155.0087/F1)作为参考,用下表12中详述的组合物,在类似的附加分析中也测试了聚合物的添加。
表12:使用
LC-液晶
获得的额外结果表明,与参考配制品19-0155.0087/F1相比,黄原胶(0.2%w/w)的添加大幅增加了乳剂19-0155.0103/F1的稳定性。
另一方面,诸如SEPINEO
表13中配制的媒介物用于评估相异的不同制造方法步骤对组合物外观和稳定性的影响。下面还描述了此类媒介物在外观、pH和粘度方面的初始特征。
表13:媒介物原型19-0155-0090P/F3的组成和组合物19-0155-0090P/F3的物理参数
不同方法变化获得的结果描述在表14中。
表14:使用基础组合物19-0155-0090P评估的方法变量的总结
粘度方面的结果示出在图3中。
特别是对下文所述的“反絮凝器”和“Croda”方法进行了对比测试。
“反絮凝器”方法使用反絮凝或分散叶片,而“Croda”方法在整个制造过程中使用桨叶搅拌器。
“反絮凝器”方法
阶段A:
所用设备:烧杯:600ml;搅拌类型:反絮凝或分散叶片
步骤1:称量并且向烧杯中添加水、PG和PEG-400。
加热至70℃,并且用反絮凝或分散叶片混合,直至均匀。
步骤2:称量并且向步骤1中获得的混合物中添加KOLLIDON。用反絮凝或分散叶片混合,直至均匀。
步骤3:将预先分散在甘油中的黄原胶添加到步骤2中获得的混合物中。
步骤4:当步骤3中获得的混合物的含量均匀时,称重并且添加对羟基苯甲酸甲酯。
步骤5:在乳化前不超过20分钟,将苯氧基乙醇引入步骤4中获得的混合物中。
阶段B:
所用设备:另一个烧杯;搅拌类型:磁棒
步骤6:称重并且添加构成脂肪相的所有赋形剂。加热至70℃并且混合直至均匀。
乳化阶段:
搅拌类型:反絮凝或分散叶片
步骤7:在70℃下,将步骤6中获得的阶段B混合物倒入步骤5中获得的阶段A混合物中,同时以500rpm混合10分钟。
冷却步骤:
搅拌类型:反絮凝或分散叶片
步骤8:从热板中取出步骤7中获得的混合物,允许冷却至35℃,同时以200-300rpm搅拌。
步骤9:在30℃与35℃之间,配制品的粘度增加,并且使用抹刀从烧杯壁上除去产物。
步骤10:一旦在步骤9中获得的混合物是均匀的,就使用10%柠檬酸溶液调节至大约pH4.5-5。
步骤11:一旦pH被调节,就使用反絮凝/分散叶片在大约200rpm下混合20分钟。
步骤12:一旦步骤11完成,就用水(适量)完成。
“Croda”方法
阶段A:
所用设备:烧杯:600ml;搅拌类型:桨叶搅拌器。
步骤1:称量并且向烧杯中添加水和对羟基苯甲酸甲酯。
加热至70℃,并且用桨叶搅拌器混合,直至均匀。
步骤2:称量并且向步骤1中获得的混合物中添加KOLLIDON。用桨叶搅拌器搅拌直至均匀。
步骤3:在65℃下将预先分散在甘油中的黄原胶添加到步骤2中获得的混合物中。
阶段B:
所用设备:另一个烧杯;搅拌类型:磁棒
步骤4:称重并且添加构成脂肪相的所有赋形剂。加热至70℃并且混合直至均匀。
乳化阶段:
搅拌类型:Ultra Turrax
步骤5:在70℃下,将步骤4中获得的阶段B混合物倒入步骤3中获得的阶段A混合物中,同时以11,500rpm混合2分钟。
冷却步骤:
搅拌类型:桨叶搅拌器(带孔)
步骤6:从热板中取出步骤5中获得的混合物,允许冷却至35℃,同时以200-300rpm搅拌。
步骤7:在冷却时,将PG和PEG-400引入到步骤6中获得的混合物中。
步骤8:在35℃-40℃下,称重并且向步骤7中获得的混合物中添加苯氧基乙醇。
步骤9:在大约30℃下,配制品的粘度增加,并且使用抹刀从烧杯壁上除去产物。
步骤10:一旦在步骤9中获得的混合物是均匀的,就使用10%柠檬酸溶液调节至大约pH4.5-5。
步骤11:一旦pH被调节,就使用桨叶振动器在大约200rpm下混合30分钟。
步骤12:一旦步骤11完成,就用水(适量)完成。
用“反絮凝器”方法的参比配方获得了最佳结果。
对于配制品19-0155-0090P/F3,用该方法获得了适当的粘度和高密度的单分散液晶/层状凝胶相。
在这些条件下获得的微观结构对于药物递送是最有效的,因为液滴和液晶/层状凝胶相小且密度高。
此类微观结构使液晶/层状凝胶相的比表面积最大化,以促进活性剂转移到皮肤中并且从而在血管收缩强度和延长的血管收缩持续时间方面改善血管收缩。
因此,液滴尺寸受到所用方法的影响,并且与“反絮凝器”方法相比,“Croda”方法倾向于在更大程度上减小液滴尺寸。这很可能是由于在乳化过程中使用了高剪切混合器以及随后使用了桨叶搅拌器。
冷却速率也被鉴定为是重要的变量,并且环境空气冷却产生了所进行的测试的最令人满意的结果。
因此,可以通过该测试得出几种其他观察结果:
苯氧基乙醇应优选在乳化步骤之后引入。
如果活性相(包含活性剂)是在乳化后引入的,则不应将其加热。
微观结构受到二醇去除的显著影响,并且在“反絮凝器”和“Croda”方法的情况下液滴尺寸和液晶/层状凝胶相尺寸不同。
在“反絮凝器”方法中掺入1%w/w聚二甲基硅氧烷(配方0090P/F10)看起来消除了在摩擦/应用配制品时观察到的皂洗/美白效果。
当使用反絮凝器方法制造时,这种微小配制变化看起来不会显著影响微观结构。
使用如下所述的体内血管收缩方案三重测试每种组合物。
在上午8点,使用外置活塞式移液器(positive displacement pipette)将60微升的每种组合物以随机盲法的方式一次应用到上胸部的用塑料O型环限定的10cm2表面积上。
应用后,然后进行30秒的按摩期和10分钟的产品的应用后干燥期。
在应用后1、2、3、4、8、10、12、14、16和24小时测量在0至3(3=最大值)的常规标度上的美白得分。
评价两种基于Gelot 64的乳剂(上述表10)和一种基于Polawax NF的乳剂(上述表11)。
皮肤美白结果示出在图4中。
所有测试的乳剂都产生相似的作用起效。
Polawax NF乳剂(19-0155,0086A/F1)产生了比基于Gelot 64的组合物(19-0155-0083/F1和19-0155-0087/F1)略微更好的总体特征。应注意,组合物19-0155.0086A/F1还含有油醇(KOLLICREAM OA,2,5%)和KOLLIDON VA-64,两者都改善和延长了局部应用的活性剂的皮肤施用。
基于Gelot-64的组合物(19-0155-0083/F1)不含任何聚合物或油醇,而基于Gelot64的组合物19-0155-0087/F1含有KOLLIDON VA-64和油醇。与基于Polawax的配方相比,两种基于Gelot 64的组合物都显示出优异的物理稳定性。
基于这些结果,看起来黄原胶和KOLLIDON VA 64加上油醇的组合改善了活性剂的皮肤施用,同时提供了所希望的物理稳定性。
因此,此类水包油乳剂在皮肤美白的起效、强度和持续时间方面表现出改善的性能特征。
因此测试了不同的配制品,并且结果分为两组:O/W乳剂[水包油](Gelot 64,表14)和O/W乳剂(Polawax,表15)。此外,测试的配制品均包含黄原胶,黄原胶在稳定性方面具有优势。
表14:Gelot 64乳膏19.0155-0090/F1的组成
LC-液晶
表15:Polawax组合物19-0155.0091/F1
LC-液晶
W/O乳剂(Polawax、Brij和Gelot概念)的皮肤美白结果呈现在图5中,基于3次重复的平均值。
Polawax乳剂(19-0155.0091/F1)在4与10小时之间实现了最高的皮肤美白,得分为3。对于Gelot乳剂(19.0155-0090/F1),观察到类似但略低的强度特征。
基于Brij的组合物显示出一些不稳定性(尽管存在0.2%黄原胶)并且被认为是不令人满意的。
下表17和18描述了测试的基于Gelot 64和Polawax的乳剂的组成和物理稳定性数据。
表17:使用体内血管收缩模型测试的Gelot 64乳剂的详细组成
LC-液晶
表18:使用体内血管收缩模型测试的Polawax NF乳剂的详细组成
LC-液晶
如此使用的基于Gelot的组合物是Gelot 64乳剂(19-0155-0090/F1和19.0155-0103/F1)的优化形式,而Polawax乳剂是Polawax乳剂(19-0155.0091/F1)的优化变体。
使用如先前所述的体内血管收缩方案三重测试每种组合物。
由此获得的结果示出在图6中。根据这些结果,包含1.5%w/w酒石酸溴莫尼定的配制品产生指示血管收缩的高水平的延长皮肤美白。
测试的基于Gelot的乳剂实现了最大的美白性能,但性能略低于基于Polawax 19-0155-0133/F1的乳剂。该配方含有与其他测试组合物和其他活性Polawax配方(19-0155-0132/F2)完全相同浓度的活性剂。唯一的区别是组合物19-0155-0133/F1含有1.0%w/w生育酚,而19-0155-0132/F2含有0.1%w/w生育酚。
基于Gelot 64(19-0155-0102/F5)和Polawax(19-0155-0132/F2)的乳剂配制品产生了相似的血管收缩特征。血管收缩程度相似,应用后约1-1.5,并且约4小时后为最大值。血管收缩强度保持在大约3.0直到应用后14小时,并且在24小时后降至1.0-1.5。
例如,图7示出了活性配制品19-0155-0102/F5和相应媒介物19-0155-0102P/F2的平均皮肤美白特征±标准偏差,并且还证明了血管收缩测试的优异再现性。
使用UV诱导的红斑模型评价表19中列出的包含酒石酸溴莫尼定和媒介物的活性组合物。
使用如下所指定的方案应用组合物。其涉及在UV辐照前的晚上和UV辐照前2小时对三名健康志愿者进行应用。
在实验前24小时确定每个受试者的单独最小红斑剂量(MED)。在每个受试者的背侧躯干上还标示出九个小区域,将组合物以5mg/cm2的剂量应用于这些区域。施用UV并且等同于1x MED、2x MED(2MED)和3x MED(3MED)。
在辐照后24小时,使用研究者红斑得分并且使用色差色度计得到实验读数。
表19:
图8中总结了每种组合物的平均红斑得分。
与媒介物相比,含有1.5%酒石酸溴莫尼定的活性组合物证明了红斑得分显著降低。当1.5%w/w酒石酸溴莫尼定与抗氧化剂组合使用时,观察到在抗红斑效果方面的额外益处。BHA和α-生育酚用作模型抗氧化剂,其浓度为0.1%和1%w/w。含有1%BHA或1%α-生育酚的配制品显示出最有效力的抗红斑作用并且有效抑制了2MED。配方19-0155.0102/F5(液晶乳剂O/W Gelot 64)产生最强的抗红斑作用。
使用已知诱发皮肤美白/血管收缩的参考药物测试皮肤美白(血管收缩)模型。用以下进行最初研究:
·
·丙酸氯倍他索乳膏,0.05%w/w
·如由Fahl(Effect of topical vasoconstrictor exposure upontumoricidal radiotherapy.Int J Cancer;135(4):981-988,2014)使用并且与由Cleary等人(Significant suppression of radiation dermatitis in breast cancerpatients using a topically applied adrenergic vasoconstrictor.RadiationOncology,2017)使用的配制品相似的盐酸去甲肾上腺素溶液(在70:30乙醇:水中82mg/ml)。
皮肤美白模型允许根据皮肤美白的起效、强度和持续时间来区分由在不同配制品中应用的几种活性剂引起的皮肤美白能力。
该模型在配制品筛选阶段具有足够的再现性和鉴别性能。
丙酸氯倍他索乳膏已被选为皮肤美白涉及的明确产品/活性剂。事实上,使用这种血管收缩作用评估外用皮质类固醇的有效性和体内生物等效性(1997FDA指南,https://www.fda.gov/media/70931/download)。
去甲肾上腺素(norepinephrine)(降肾上腺素(noradrenaline))溶液在应用后1小时产生快速和中度的皮肤美白;然而,在4小时的观察间隔后,效果开始消退。10小时后美白为0.5或更低,并且仅16小时后恢复到观察起始点。虽然最初的效果是有希望的,但效果的持续时间和强度不足。
与极性去甲肾上腺素分子及其水性乙醇媒介物相反,丙酸氯倍他索乳膏展现出缓慢的作用起效,从2小时起逐渐增加,在14小时与16小时之间达到2.0的峰值美白得分。从16小时开始,美白迅速降低,并且在24小时恢复到起始点。氯倍他索美白的较慢的作用起效可能与活性剂的物理化学特征有关,由此与亲水性更大的去甲肾上腺素相比,其亲脂性的性质导致储库的形成和在活表皮中更有限的分布。同样重要的是注意,丙酸氯倍他索和去甲肾上腺素的血管收缩药效机制也不同。
因此,用高剂量1.5%w/w酒石酸溴莫尼定(19-0155-0098/F1)制备改良的MIRVASO配制品。进行该评价以评估在类似于MIRVASO的媒介物中增加剂量对皮肤美白的影响。
图10中示出了两种配方的相应皮肤美白结果。也包括去甲肾上腺素溶液和可商购的
与可商购的
然而,皮肤美白的强度没有持续如所希望的延长的时间段来解决根据本发明的技术问题。
这种性能限制也与MIRVASO媒介物不适合辐射性皮炎相关。如先前所提到的,MIRVASO媒介物中二氧化钛颗粒的存在将干扰和破坏与所用高能电磁波相关的辐射剂量。
- 硫酸钙晶须或其组合物在制备皮肤促渗剂中的用途
- 水凝胶组合物及其在预防和/或治疗由辐射引起的皮肤损伤中的用途
- 水凝胶组合物及其在预防和/或治疗由辐射引起的皮肤损伤中的用途
