一种基于适配体-多巴胺印迹限域的多种金属离子同时检测的电化学传感器及其应用
文献发布时间:2024-04-18 20:01:55
技术领域
本发明涉及食品安全检测技术领域,尤其涉及一种基于适配体-多巴胺印迹限域的多种金属离子同时检测的电化学传感器及其应用。
背景技术
铅、镉、汞、砷是广泛分布于水产及其制品中的重金属污染物,具有普遍性、高毒性、生物蓄积性、隐蔽性、持久性等特点,易在食用者体内形成累积毒性造成严重的食品安全隐患。由于已经引起了世界许多地区的严重健康问题,受到高度关注。目前重金属的检测的标准方法多以原子吸收法(AAS)、原子荧光法(AFS)、电感耦合等离子体质谱法(ICP-MS)等大型仪器法为主,然而,基于仪器的分析需要非常昂贵的设备、训练有素的操作员,检测成本较高,因此,无法满足食品安全快速检测的社会需求。现有的重金属速测方法主要以比色速测方法和溶出伏安法为主,难以在兼具特异性和pH耐受性的同时实现多种重金属的同步检测。
发明内容
针对现有技术的不足,本发明提供了一种基于适配体-多巴胺印迹限域的多种金属离子同时检测的电化学传感器及其应用。本发明实现了铅离子、镉离子、汞离子、砷离子检测超灵敏和高选择性测定的需求,对在食品安全领域的实际应用方面具有重要意义。
本发明的技术方案如下:
一种基于适配体-多巴胺印迹限域的多种金属离子同时检测的电化学传感器,所述电化学传感器包括巯基修饰的适配体、多巴胺印迹层。
进一步地,所述适配体包括铅适配体、镉适配体、汞适配体、砷适配体中的一种或多种;所述铅适配体的序列如SEQ No.1所示;所述镉适配体的序列如SEQNo.2所示;所述汞适配体的序列如SEQ No.3所示;所述砷适配体的序列如SEQNo.4所示。
进一步地,所述电化学传感器的制备方法,包括如下步骤:
(1)将适配体溶液与缓冲溶液混合后,加入还原剂溶液反应,得到打开二硫键的适配体溶液;
(2)将打开二硫键的适配体溶液滴加在电极表面,静置反应、清洗、干燥;
(3)将电极浸入封闭液中,静置反应、清洗、干燥;
(4)再将电极浸渍入金属离子溶液中进行孵育,清洗、干燥;
(5)滴加多巴胺溶液,聚合,洗脱,得到电化学传感器。
进一步地,步骤(1)中,所述适配体溶液中包含铅适配体、镉适配体、汞适配体、砷适配体,铅适配体的浓度为5-10μmol/L,镉适配体的浓度为5-7.5μmol/L,汞适配体的浓度为5-7.5μmol/L,砷适配体的浓度为5-7.5μmol/L;所述缓冲溶液为三羟甲基氨基甲烷醋酸盐溶液,浓度为5-100mmol/L;所述适配体溶液与缓冲溶液的体积比为1:9-10;所述还原剂溶液为盐酸三(2-羧乙基)膦溶液,浓度为3-10mmol/L;所述还原剂溶液与适配体溶液的体积比为9-10:1,所述反应的温度为20-30℃,时间为2-3h。
进一步地,步骤(2)中,所述电极为丝网印刷金电极,所述反应的温度为20-30℃,时间为30-40min;所述打开二硫键的适配体溶液的体积为5-10μL。
进一步地,步骤(3)中,所述封闭液为巯基己醇溶液,浓度为1-2mmol/L,所述反应的温度为20-30℃,时间为30-40min。
进一步地,步骤(4)中,所述金属离子包括铅离子、镉离子、汞离子、砷离子;所述金属离子溶液中金属离子的浓度为10-20ppm;所述孵育的温度为20-30℃,时间为20-90min。
进一步地,步骤(5)中,所述多巴胺溶液的浓度为0.5-10mmol/L,体积为50-100μL;所述聚合为电聚合,所述电聚合是在-0.5V到0.5V的电位下以45-55mV/s的速率进行电聚合,扫描2-4个循环;所述洗脱的洗脱液为乙二胺四乙酸溶液,浓度为5-20mmol/L,时间为40-90min。
进一步地,所述电化学传感器的应用,所述电化学传感器用于食品中金属离子的检测。
进一步地,所述金属离子包括铅离子、镉离子、汞离子、砷离子中的一种或多种。
本发明有益的技术效果在于:
本发明首次利用适配体-多巴胺印迹限域构建了铅(II)离子、镉(II)离子、汞(II)离子、砷(ⅡI)离子响应的生物传感器,通过提供不同的适配体,结合铅(II)离子、镉(II)离子、汞(II)离子、砷(ⅡI)离子,电聚合多巴胺后,再利用EDTA与靶标离子的螯合作用进行洗脱,洗脱后在工作电极表面原来金属离子所在的区域可以形成不同的适配体-多巴胺印迹限域空腔,进而提高电化学传感器的pH耐受性。采用适配体结合表面多巴胺印迹限域识别技术能提高重金属表面印迹聚合物的识别能力,具有高特异高灵敏的重金属快速检测能力,同时能很好地解决多种重金属的同步检测等难题,满足食品安全快速检测的社会需求,因此本发明所制备的基于适配体-多巴胺印迹限域的四种金属离子同时检测的电化学传感器在提高适配体检测性能方面有重要意义。
本发明在丝网印刷金电极表面构建适配体-多巴胺印迹限域聚合物,可用于铅(II)离子、镉(II)离子、汞(II)离子、砷(Ⅲ)离子的检测中,同时,能够增强适配体电化学传感器的pH耐受性,通过实验室筛选出的铅离子适配体、镉适配体、汞适配体、砷适配体和多巴胺为材料,通过金硫键和电聚合的方法形成印迹限域,实现了铅离子、镉离子、汞离子、砷离子检测超灵敏和高选择性测定的需求,在不形成适配体-多巴胺印迹限域聚合物的情况下,pH耐受性较差,当形成适配体-多巴胺印迹限域聚合物时,pH耐受性较好,且针对铅(II)离子、镉(II)离子、汞(II)离子、砷(Ⅲ)离子也表现出良好的特异性。最后,也将该传感器用于鱿鱼丝中的铅离子、镉离子、汞离子、砷离子检测,检测结果与国标中的方法所得到的结果类似,证明了该传感器的优良性能。所构建的检测方法具有操作简单、选择性和特异性高等优点,对在食品安全领域的实际应用方面具有重要意义。
附图说明
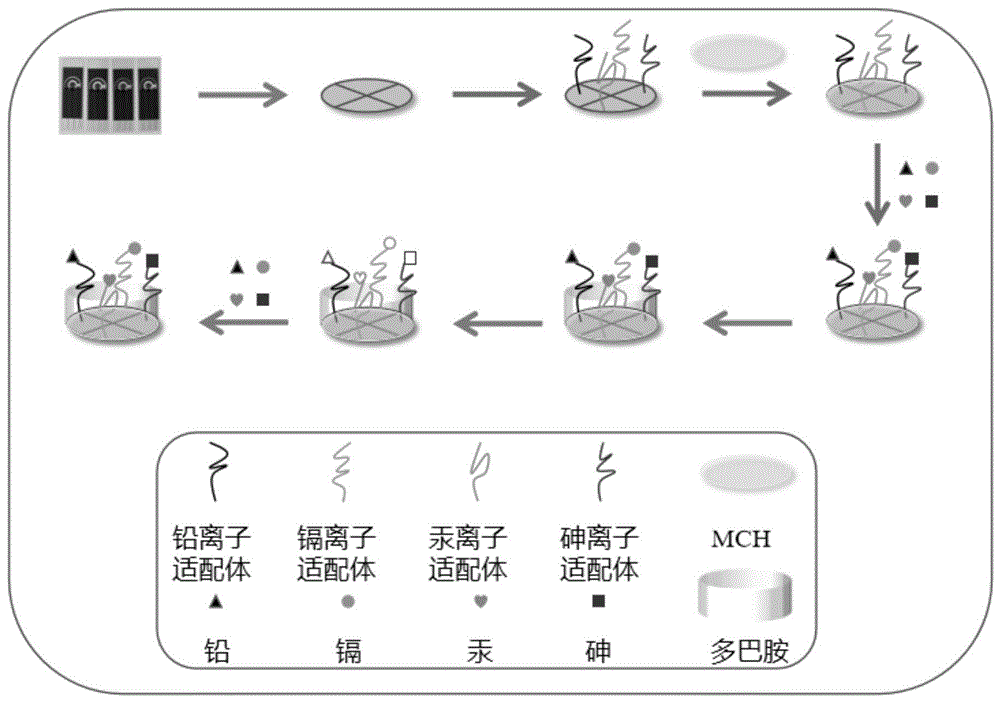
图1为本发明基于适配体-多巴胺印迹限域的四种金属离子同时检测的电化学传感器原理图。
图2为本发明实施例1所制备的电化学传感器在不同铅离子浓度条件下的标准曲线和对铅离子特异性测试图。
图中:A、不同铅离子浓度条件下的标准曲线;B、电化学传感器对铅离子及其他多种离子检测结果图。
图3为本发明实施例1所制备的电化学传感器在不同镉离子浓度条件下的标准曲线和对镉离子特异性测试图。
图中:A、不同镉离子浓度条件下的标准曲线;B、电化学传感器对镉离子及其他多种离子检测结果图。
图4为本发明实施例1所制备的电化学传感器在不同汞离子浓度条件下的标准曲线和对汞离子特异性测试图。
图中:A、不同汞离子浓度条件下的标准曲线;B、电化学传感器对汞离子及其他多种离子检测结果图。
图5为本发明实施例1制备的电化学传感器在不同砷离子浓度条件下的标准曲线和对砷离子特异性测试图。
图中:A、不同砷离子浓度条件下的标准曲线;B、电化学传感器对砷离子及其他多种离子检测结果图。
图6为本发明实施例1所制备的电化学传感器与对比例1所制备的非多巴胺印迹限域的适配体电化学传感器在不同pH条件下的电流响应值的结果图。
图中:A、本发明实施例1所制备的电化学传感器和对比例1所制备的非多巴胺印迹限域的适配体电化学传感器在不同pH条件下对Pb(II)的电流响应值;B、本发明实施例1所制备的电化学传感器和对比例1所制备的非多巴胺印迹限域的适配体电化学传感器在不同pH条件下对Cd(II)的电流响应值;C、本发明实施例1所制备的电化学传感器和对比例1所制备的非多巴胺印迹限域的适配体电化学传感器在不同pH条件下对Hg(II)的电流响应值;D、发明实施例1所制备的电化学传感器和对比例1所制备的非多巴胺印迹限域的适配体电化学传感器在不同pH条件下对As(Ⅲ)的电流响应值。
具体实施方式
下面结合附图和实施例,对本发明进行具体描述。
下述实施例中的基于适配体-多巴胺印迹限域对重金属离子检测的原理如图1所示。将铅离子适配体、镉适配体、汞适配体、砷适配体通过金硫键连接在丝网印刷金电极表面,然后多巴胺通过电聚合的方法在丝网印刷金电极表面形成印迹限域,在没有适配体-多巴胺印迹限域的情况下,电化学传感器的pH耐受性较差,当有适配体-多巴胺印迹限域时,电化学传感器的pH耐受性较好。且电化学响应由重金属离子浓度决定的,重金属离子浓度越高,电流响应越明显,因此,可以通过测定电化学中的电流响应值来实现对重金属离子的测定。
电化学传感器的制备方法,包括如下步骤:
(1)取10μL适配体溶液(适配体溶液中,铅适配体的浓度为5-10μmol/L,镉适配体的浓度为5-7.5μmol/L,汞适配体的浓度为5-7.5μmol/L,砷适配体的浓度为5-7.5μmol/L)与90-100μL的5-100mmol/L三羟甲基氨基甲烷醋酸盐溶液混合后,使用PCR变性退火,具体程序为:95℃加热变性10min,降温至4℃下退火10min;再加入90-100μL的3-10mmol/L盐酸三(2-羧乙基)膦溶液(TCEP),20-30℃反应2-3h,得到打开二硫键的适配体溶液;
(2)将5-10μL打开二硫键的适配体溶液滴加在丝网印刷金电极表面,20-30℃静置反应30-40min;然后使用超纯水沿着电极表面缓慢冲洗使得水流缓慢流下,氮气吹干10~20s;
(3)将电极浸入1-2mmol/L巯基己醇溶液中,20-30℃静置反应30-40min、然后使用超纯水沿着电极表面缓慢冲洗使得水流缓慢流下,氮气吹干10~20s;
(4)再将电极浸入10-20ppm铅离子、10-20ppm镉离子、10-20ppm汞离子、10-20ppm砷离子的溶液中于20-30℃孵育20-90min,然后使用超纯水沿着电极表面缓慢冲洗使得水流缓慢流下,氮气吹干10~20s;
(5)再滴加50-100μL的0.5-10mmol/L多巴胺溶液,在-0.5V到0.5V的电位下以45-55mV/s的速率进行电聚合,扫描2-4个循环,每个循环1-2min;然后用5-20mmol/L乙二胺四乙酸溶液洗脱40-90min,得到电化学传感器。
实施例1:
一种基于适配体-多巴胺印迹限域的多种金属离子同时检测的电化学传感器,其制备方法包括以下步骤:
(1)取10μL适配体溶液(适配体溶液中,铅适配体的浓度为7.5μmol/L,镉适配体的浓度为5μmol/L,汞适配体的浓度为5μmol/L,砷适配体的浓度为5μmol/L)与90μL的10mmol/L三羟甲基氨基甲烷醋酸盐溶液混合后,使用PCR变性退火,具体程序为:95℃加热变性10min,降温至4℃下退火10min;再加入100μL的3mmol/L TCEP,25℃反应3h;
(2)将5μL打开二硫键的适配体溶液滴加在丝网印刷金电极表面,25℃静置反应30min;然后使用超纯水沿着电极表面缓慢冲洗使得水流缓慢流下,氮气吹干15s;
(3)将电极浸入1mmol/L巯基己醇溶液中,25℃静置反应30min,然后使用超纯水沿着电极侧壁缓慢冲洗使得水流缓慢流下,氮气吹干15s;
(4)再将电极浸入10ppm铅离子、10ppm镉离子、10ppm汞离子、10ppm砷离子的溶液中25℃孵育30min,然后使用超纯水沿着电极侧壁缓慢冲洗使得水流缓慢流下,氮气吹干15s;
(5)再滴加50μL的1mmol/L多巴胺溶液,在-0.5V到0.5V的电位下以50mV/s的速率进行电聚合,扫描2个循环,每个循环1min;然后用5mmol/L乙二胺四乙酸溶液洗脱60min,得到电化学传感器。
实施例2:
一种基于适配体-多巴胺印迹限域的多种金属离子同时检测的电化学传感器,其制备方法包括以下步骤:
(1)取10μL适配体溶液(适配体溶液中,铅适配体的浓度为5μmol/L,镉适配体的浓度为7.5μmol/L,汞适配体的浓度为7.5μmol/L,砷适配体的浓度为7.5μmol/L)与95μL的100mmol/L三羟甲基氨基甲烷醋酸盐溶液混合后,使用PCR变性退火,具体程序为:95℃加热变性10min,降温至4℃下退火10min;再加入90μL的10mmol/L TCEP,20℃反应3h,得到打开二硫键的适配体溶液;
(2)将7.5μL打开二硫键的适配体溶液滴加在丝网印刷金电极表面,20℃静置反应40min;然后使用超纯水沿着电极表面缓慢冲洗使得水流缓慢流下,氮气吹干20s;
(3)将电极浸入1.5mmol/L巯基己醇溶液中,20℃静置反应40min、然后使用超纯水沿着电极表面缓慢冲洗使得水流缓慢流下,氮气吹干20s;
(4)再将电极浸入15ppm铅离子、15ppm镉离子、15ppm汞离子、15ppm砷离子的溶液中20℃孵育90min,然后使用超纯水沿着电极表面缓慢冲洗使得水流缓慢流下,氮气吹干20s;
(5)再滴加75μL的10mmol/L多巴胺溶液,在-0.5V到0.5V的电位下以45mV/s的速率进行电聚合,扫描3个循环,每个循环1.5min;然后用20mmol/L乙二胺四乙酸溶液洗脱40min,得到电化学传感器。
实施例3:
一种基于适配体-多巴胺印迹限域的多种金属离子同时检测的电化学传感器,其制备方法包括以下步骤:
(1)取10μL适配体溶液(适配体溶液中,铅适配体的浓度为10μmol/L,镉适配体的浓度为5μmol/L,汞适配体的浓度为5μmol/L,砷适配体的浓度为5μmol/L)与100μL的5mmol/L三羟甲基氨基甲烷醋酸盐溶液混合后,使用PCR变性退火,具体程序为:95℃加热变性10min,降温至4℃下退火10min;再加入95μL的5mmol/L TCEP,30℃反应2h,得到打开二硫键的适配体溶液;
(2)将10μL打开二硫键的适配体溶液滴加在丝网印刷金电极表面,30℃静置反应30min;然后使用超纯水沿着电极表面缓慢冲洗使得水流缓慢流下,氮气吹干10s;
(3)将电极浸入2mmol/L巯基己醇溶液中,30℃静置反应30min、然后使用超纯水沿着电极表面缓慢冲洗使得水流缓慢流下,氮气吹干10s;
(4)再将电极浸入含有20ppm铅离子、20ppm镉离子、20ppm汞离子、20ppm砷离子的金属离子溶液中30℃孵育20min,然后使用超纯水沿着电极表面缓慢冲洗使得水流缓慢流下,氮气吹干10s;
(5)再滴加100μL的0.5mmol/L多巴胺溶液,在-0.5V到0.5V的电位下以55mV/s的速率进行电聚合,扫描4个循环,每个循环2min;然后用10mmol/L乙二胺四乙酸溶液洗脱看90min,得到电化学传感器。
对比例1:
一种非多巴胺印迹限域的适配体电化学传感器,其制备方法包括以下步骤:
(1)取10μL适配体溶液(适配体溶液中,铅适配体的浓度为7.5μmol/L,镉适配体的浓度为5μmol/L,汞适配体的浓度为5μmol/L,砷适配体的浓度为5μmol/L)与90μL的10mmol/L三羟甲基氨基甲烷醋酸盐溶液混合后,使用PCR变性退火,具体程序为:95℃加热变性10min,降温至4℃下退火10min;再加入100μL的3mmol/L TCEP,25℃反应3h;
(2)将5μL打开二硫键的适配体溶液滴加在丝网印刷金电极表面,25℃静置反应30min;然后使用超纯水沿着电极表面缓慢冲洗使得水流缓慢流下,氮气吹干15s;
(3)将电极浸入1mmol/L巯基己醇溶液中,25℃静置反应30min,然后使用超纯水沿着电极侧壁缓慢冲洗使得水流缓慢流下,氮气吹干15s,得到非多巴胺印迹限域的适配体电化学传感器。
测试例:
(1)构建标准曲线:
以已知浓度的铅(II)离子、镉(II)离子、汞(II)离子、砷(Ⅲ)离子溶液制备标准曲线,所述已知浓度的金属离子溶液的浓度分别为0μg/L、0.01μg/L、0.05μg/L、0.1μg/L、0.5μg/L、1μg/L;将已知浓度的金属离子溶液滴加在本发明实施例1所制备的电化学传感器表面,25℃反应30min,用差分脉冲伏安法(DPV)检测峰高,得到电流响应值与金属离子浓度的标准曲线,铅(II)离子、镉(II)离子、汞(II)离子、砷(Ⅲ)离子的标准曲线分别如图2A、3A、4A、5A所示。从图中可以得出,标准曲线(X表示浓度,Y表示电流响应值)为:铅离子:Y=5.41X+4.19,R
(2)特异性测试:
特异性是生物传感器最重要的特性之一,为了验证本发明所制备的电化学传感器的特异性,使用本发明实施例1所制备的电化学传感器检测其对Pb
(3)稳定性测试:
稳定性是生物传感器最重要的特征之一,为了验证本发明所制备的电化学传感器的稳定性,使用本发明实施例1所制备的电化学传感器与对比例1所制备的非多巴胺印迹限域的适配体电化学传感器检测其在不同pH条件下的稳定性,结果用电流响应差值(ΔI)表示ΔI=I
(4)实际样品重金属含量及加标回收率测试:
用本发明实施例1所制备的电化学传感器和电感耦合等离子体质谱法对市售鱿鱼丝样品中的Pb
样品前处理:根据GB5009.17-2021的试样消解方法(微波消解法)对市售鱿鱼丝样品进行前处理,得到待测样品。
取5μL待测样品滴加在本发明实施例1所制备的电化学传感器表面或通过电感耦合等离子体质谱法检测样品中Pb
表1.本发明实施例1所制备的电化学传感器与电感耦合等离子体质谱法对鱿鱼丝样品中重金属离子的检测结果比较
从表1可以看出,两种方法检测得到的重金属离子的含量结果一致,无明显差异,且电化学传感器对Pb
以上所述仅是本发明的优选实施方式,本发明不限于以上实施例。可以理解,本领域技术人员在不脱离本发明的精神和构思的前提下直接导出或联想到的其他改进和变化,均应认为包含在本发明的保护范围之内。
