基于脉管化模式的诊断、预测、确定预后、监测或分期疾病的方法
文献发布时间:2023-06-19 09:52:39
相关申请的交叉引用
根据35 U.S.C.§119(a),本申请要求于2018年7月3日提交的标题为“A METHODFOR DIAGNOSING DISEASE BASED UPON ANALYSIS OF VASCULARIZATION PATTERNS”的临时申请第62/693,852的优先权,并主张其优先权,其全部内容通过引用合并于此。
技术领域
本说明书涉及一种疾病检测和预测的方法。更具体地,本说明书涉及一种应用人工智能算法来分析脉管结构并检测受试体(subject)是否患有疾病、预测受试体是否可能患有疾病、确定受试体的预后、监测疾病或对疾病分期的方法。
背景技术
在美国,癌症和中风分别是第二大和第五大死亡原因。大约38.5%的人口将在一生中被诊断出患有癌症,且大约16.7%的人口将在其一生中经历中风。仅在美国,癌症就造成了1,470亿美元的经济负担,并且仅在美国中风就造成了750亿美元的经济负担。鉴于美国代表的世界人口不到5%,因此全球影响可能会大很多倍。
众所周知,癌症的早期发现是影响患者长期预后的最重要因素之一。确实,早期发现癌症可以使生存率提高三倍。不幸的是,有几种癌症难以被检测到,直到后期,此时直接影响生存率的症状才会出现。但是,即使是更容易发现的癌症,目前的癌症筛查测试也存在问题。当前的癌症筛查测试是侵入性的、费时的,并且有时是不准确的。
同样,对中风的快速、准确诊断对于最大程度地提高治疗效果和最大程度地减少脑损伤至关重要。为了预防性治疗并显著降低中风风险,识别有中风风险的患者至关重要。当前的中风筛查测试也具有与上述癌症筛查测试相同的缺点。
脉管系统渗透到所有生物的组织中,为生物的细胞提供营养。在患病的组织中,脉管结构与健康组织中的脉管结构有很大不同。例如,存在癌症的组织的脉管结构将与没有癌症的组织的脉管结构有很大不同。在另一个示例中,处于中风风险的受试体的大脑中的组织的脉管结构将与健康受试体的大脑中的组织的脉管结构明显不同。
已经开发出某些方法,这些方法使用机器学习算法从肿瘤组织的图像中检测癌症。但是,这些方法对检测早期阶段的癌症可能不够灵敏。为了疾病诊断的目的,也已经开发出分析各种血管属性的某些方法。这些血管属性不包括可以量化生物体代谢的代谢比例指数。这些方法中的某些方法不应用机器学习,而是将血管属性与来自健康受试体的现有血管属性图集进行比较。其余已开发的方法未应用机器学习算法来训练模型以检测疾病的存在。因此,需要开发一种更快、更灵敏、更准确且侵入性更小的方法来检测受试体是否患有疾病,预测受试体是否可能患病,确定受试体的预后,监测疾病和对疾病分期。
发明内容
通常,本说明书中描述的主题的一个方面体现在用于检测脉管系统疾病的方法中。该方法包括获得脉管系统的图像。该方法包括从获得的图像中提取血管测量值。该方法包括基于提取的血管测量值确定所获得的图像中的脉管系统的特征。该方法包括将人工智能算法应用于所确定的特征以确定脉管系统中是否存在疾病。
这些和其他实施例可以包括以下特征中的一个或多个。可以自动提取血管测量值。该疾病可以包括癌症、脑血管疾病(例如中风、短暂性脑缺血发作)、心血管疾病、其他血管疾病、眼病或皮肤病。该疾病可以是以下中的至少一种:肿瘤、中风、短暂性脑缺血发作、糖尿病、动脉粥样硬化、高血压(例如心脏、肾脏或门静脉)、周围静脉疾病、动脉瘤、肺栓塞、颈动脉疾病、慢性静脉供血不足、先天性血管畸形、深静脉血栓形成、纤维肌发育异常、肾动脉狭窄、淋巴水肿、肠系膜动脉疾病、术后血栓形成综合征、血栓形成、血管炎、血管性痴呆、类风湿关节炎、系统性红斑狼疮、肺气肿、炎性肠病、子宫息肉、先兆子痫和神经纤维瘤病。血管测量值可以来自多个血管。所提取的血管测量值可以包括血管名称、血管半径、血管长度、血管的三维坐标、血管子代的数量或下游血管尖端的数量中的至少一个。
特征可以是量化脉管系统的生理学以便随后应用于疾病的检测、诊断、监测或预测的任何值。计算这些特征可能涉及使用异度缩放定律来量化生理与脉管系统功能和/或分形分析之间的关系。特征可以根据以下中的至少一项来确定:比例指数、非对称比例指数、曲折度、曲率、微脉管密度、血管直径、血管长度、血管体积、血管表面积、分支角度、分支频率、分支点数、血管尖端数、血管环数、分层分形维数、Hausdorff维数、腔隙度维数和广义分形维数。机器学习算法可以应用于基于脉管结构特征来训练模型。
该方法可以包括应用特征选择来选择与疾病的诊断最相关的脉管结构特征。该方法可以包括应用特征提取来选择与疾病的诊断最相关的脉管结构特征。
在本说明书中描述的主题的一个方面体现在用于检测脉管系统疾病的计算机程序中。该程序可以包括用于确定脉管系统的特征的模块。所确定的特征可以包括脉管网络比例指数、脉管非对称比例指数、脉管曲折度、脉管曲率和脉管微脉管密度中的至少一项。该程序可以包括用于将人工智能算法应用于确定特征以确定脉管系统中是否存在疾病的模块。
附图说明
通过检查以下附图和详细描述,本发明的其他系统、方法,特征和优点对于本领域的普通技术人员将是或将变得显而易见。旨在将所有这样的附加系统、方法、特征和优点包括在本说明书中,在本发明的范围内,并由所附权利要求书保护。附图中所示的组成部分不必按比例绘制,并且可以被夸大以更好地说明本发明的重要特征。在附图中,贯穿不同的视图,相同的参考数字表示相同的部分,其中:
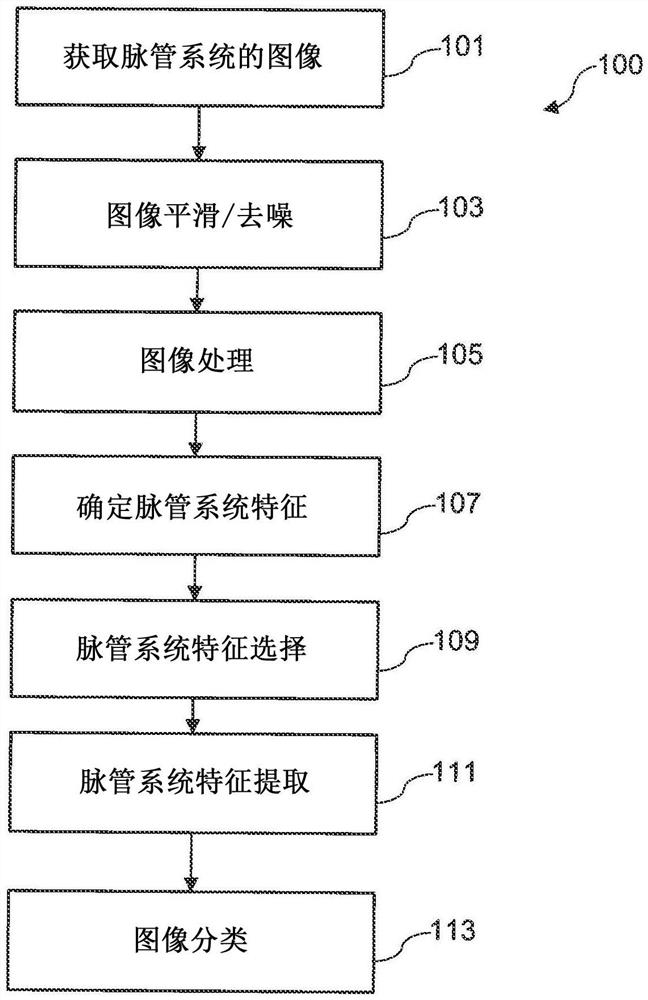
图1是根据本发明的一方面的用于疾病检测的过程的流程图。
图2是根据本发明的一方面的用于实现图1中的疾病检测过程的系统。
图3A至图3L示出根据本发明的一方面的机器学习结果的样本图。
图4A示出根据本发明的一方面的基于分布的比例指数对数回归的机器学习结果的样本图。
图4B示出根据本发明的一方面的基于回归的比例指数对数回归的机器学习结果的样本图。
图5A示出根据本发明的一方面在缺血性中风发作之后来自脑脉管系统的径向指数(a)的基于保守性计算的分布的样本图。
图5B示出根据本发明的一方面在缺血性中风发作之后来自脑脉管系统的长度比例指数(b)的基于保守性计算的分布的样本图。
图5C示出根据本发明的一方面在缺血性中风发作之后来自脑脉管系统的径向指数(a)的基于分布的计算。
图5D示出根据本发明的一方面在缺血性中风发作之后来自脑脉管系统的长度比例指数(b)的基于分布的计算。
图5E示出根据本发明的一方面的来自缺血性中风的径向指数(a)的基于分层平均的计算。
图5F示出根据本发明的一方面的来自缺血性中风的长度比例指数(b)的基于分层平均的计算。
图5G示出根据本发明的一方面的来自缺血性中风的径向指数(a)的基于比率的计算结果的样本图。
图5H示出根据本发明的一方面的来自缺血性中风的长度比例指数(b)的基于比率的计算结果的样本图。
图5I示出根据本发明一方面的来自缺血性中风的径向指数(a)的基于回归的计算。
图5J示出根据本发明的一方面的来自缺血性中风的长度比例指数(b)的基于回归的计算。
图6A示出根据本发明一方面的来自非中风脑脉管系统(非缺血性半球)的径向指数(a)的基于保守性计算结果的样本图。
图6B示出根据本发明一方面的来自非中风脑脉管系统(非缺血性半球)的长度比例指数(b)的基于保守性计算结果的样本图。
图6C示出根据本发明一方面的来自非中风脑脉管系统(非缺血性半球)的径向指数(a)的基于分布的计算。
图6D示出根据本发明一方面的来自非中风脑脉管系统(非缺血性半球)的长度比例指数(b)的基于分布的计算。
图6E示出根据本发明的一方面的来自非中风脑脉管系统(非缺血性半球)的径向指数(a)的基于分层平均的计算。
图6F示出根据本发明的一方面的来自非中风脑脉管系统(非缺血性半球)的长度比例指数(b)的基于分层平均的计算。
图6G示出根据本发明的一方面的来自非中风脑脉管系统(非缺血性半球)的径向指数(a)的基于比率的计算结果的样本图。
图6H示出根据本发明的一方面的来自非中风脑脉管系统(非缺血性半球)的长度比例指数(b)的基于比率的结果的样本图。
图6I示出根据本发明一方面的来自非中风脑脉管系统(非缺血性半球)的径向指数(a)的基于回归的计算。
图6J示出根据本发明的一方面的来自非中风脑脉管系统(非缺血性半球)的长度比例指数(b)的基于回归的计算。
图7示出根据本发明的一方面的通过从脉管系统分析来检测缺血性中风的对数回归程序和朴素贝叶斯分类器的准确度的表。
图8A示出样本图,其中根据本发明的一方面的基于血管半径与长度的平均比与血管子代的平均数量的分析,使用正则对数回归来对非中风和缺血性中风脉管系统的几次扫描进行分类。
图8B示出样本图,其中根据本发明的一方面的基于血管半径与长度的平均比与下游血管尖端平均数量的分析,使用朴素贝叶斯分类器来对非中风和缺血性中风脉管系统的几次扫描进行分类。
图9A示出根据本发明的一方面的非中风脉管系统的完成的Angicart++处理图像。
图9B示出根据本发明的一方面的来自梗塞周围中风区域的脑脉管系统的三维微CT扫描的Angicart++的处理图像。
图9C示出根据本发明一方面的缺血性中风脉管系统的完成的Angicart++处理图像。
图10A示出根据本发明的一方面的在梗塞周围区域中来自中风后脉管系统的径向指数(a)的基于保守性计算的分布的样本图。
图10B示出根据本发明的一方面的在梗塞周围区域中来自中风后脉管系统的长度比例指数(b)的基于保守性计算的分布的样本图。
图10C示出根据本发明的一方面的在梗塞周围区域中来自中风后脉管系统的径向指数(a)的基于分布的计算结果的样本图。
图10D示出根据本发明的一方面的在大脑的梗塞周围区域中来自脉管系统的长度比例指数(b)的基于分布的计算结果的样本图。
图10E示出根据本发明的一方面的在梗塞周围区域中来自风后脉管系统的径向指数(a)的基于分层平均的计算。
图10F示出根据本发明的一方面的在梗塞周围区域中来自中风后脉管系统的长度比例指数(b)的基于分层平均的计算。
图10G示出根据本发明的一方面的在梗塞周围区域中来自中风后脉管系统的径向指数(a)的基于比率的计算的分布。
图10H示出根据本发明的一方面的在梗塞周围区域中来自中风后脉管系统的长度比例指数(b)的基于比率的计算的分布。
图10I示出根据本发明的一方面的在梗塞周围区域中来自中风后脉管系统的径向指数(a)的基于回归的计算。
图10J示出根据本发明的一方面的在梗塞周围区域中来自中风后脉管系统的长度比例指数(b)的基于回归的计算。
图11A至图11E示出根据本发明的一方面的样本输出Angicart++数据文件。
图12A至图12E示出根据本发明的一方面的样本输出Angicart++数据文件。
图13A至图13C示出根据本发明的一方面的样本输出Angicart++数据文件。
图14A至图14F示出根据本发明的一方面在预处理之后的样本脉管系统图像。
图15A至图15F示出根据本发明的一方面在预处理之后的样本脉管系统图像。
图16A至图16C示出根据本发明的一方面在预处理之后的样本脉管系统图像。
具体实施方式
本文公开使用人工智能算法检测脉管系统疾病的方法、计算机程序和系统。更具体地,本公开涉及基于数学模型和脉管系统的机器学习的自动化疾病检测和疾病预测。本公开提供非侵入性早期疾病检测,其使用基于生物学原理的数学模型来量化脉管系统的结构,并且可以实施机器学习以确定组织是否患病。可以有把握地预测这种疾病检测的准确性以及疾病的进展。
在美国和全世界,死亡的主要原因之一是癌症。至关重要的是,在有机会扩散之前以及在成功治疗的可能性达到最高时尽早发现癌症。不幸的是,某些癌症天生就难以检测直到后期。这些癌症包括最致命的癌症,例如肝癌、脑癌、卵巢癌和肺癌。验证癌症存在的常规方法是通过活检,其固有地是侵入性的并且过度损害周围组织。肿瘤脉管系统的数学模型与非侵入性医学成像技术相结合,可以实现更有效和侵入性更小的癌症检测。数学模型可以是或包括以下任何一种:机器学习算法、机器学习方法、模型、公式和算法。
随着癌性肿瘤的生长,肿瘤周围的脉管系统也必须生长,以为肿瘤提供越来越多的氧气和相关营养。癌症的非常早期以血管新生为特征,血管新生是新血管的形成。肿瘤细胞发出化学信号,触发周围肿瘤血管的快速和高度不规则生长。因此,肿瘤脉管系统的结构与健康脉管系统的结构有很大不同。
健康的脉管系统表现出自相似性,这是一种特性,在任何给定的放大倍率下,较小的物体在结构上都与整个物体相似。因此,在整个脉管网络(即脉管系统)中,父血管与子血管的半径或长度之比是相似的。
相反,由于肿瘤细胞发出的化学信号触发肿瘤周围血管的快速和高度不规则生长,因此肿瘤脉管系统几乎没有或没有自相似性。血管的半径和长度之比非常不规则,每个父分支分裂成许多子血管。健康的脉管系统和患病的脉管系统之间的这种根本区别可以允许疾病的早期检测而没有与常规过程相关的上述缺点。
同样,发生血管新生以从缺血性中风、出血性中风、轻度中风和短暂性脑缺血发作(TIA)恢复中向大脑组织输送氧气和营养。由于上述条件,血管内皮生长因子(VEGF)水平增加。反过来,这会触发大脑梗塞区域周围血管的快速且高度不规则的生长。健康的脉管系统和患病的脉管系统之间的根本区别也可以允许早期发现或预测此类疾病。动脉硬化是上述神经系统疾病以及其他脉管疾病如心脏病发作和周围脉管疾病发作的重要先兆。在有动脉粥样硬化斑块积聚在血管中的患者中,发生血管新生以补偿血流减少。因此,血管测量值可用于确定脉管系统中是否存在疾病。另外,血管测量值可用于预测脉管系统中疾病的发作。
诸如West、Brown和Enquist(WBE)模型的数学模型使用基本生物学原理量化和预测脉管网络的结构。各种脉管系统的数学模型优先考虑不同的生物学原理:脉管系统充满空间,使脉管网络遍布生物体,从而氧气可以扩散到所有细胞,而脉管系统旨在最大程度地减少由阻抗(例如分支交界处的波反射)引起的能量损失。这些模型假定在同一层次级别内的所有血管都是等效的。血管层次结构的确定如下:未连接到任何具有较大半径的血管(即未连接到任何父血管)的血管在网络中的层次级别为0。与该血管相连的半径较小的血管的层次级别为1。随后的血管以这种方式被分配给血管层次级别,并依次编号更大。
血管的半径和长度遵循幂律。因此,可以计算出不同级别的脉管网络的半径与长度之比。本公开可以利用计算比例指数的五种方法中的至少一种,特别是从诸如基于分布、基于回归和基于分层平均的整个网络特征中得出的三种,以及从诸如基于保守性和基于比率的局部分支交界特征中得出的两种。
处理受试体的脉管系统的医学图像。医学图像可以是任何器官或脉管系统的一部分。受试体可以是人或动物。提取脉管系统的定量和/或定性血管数据。使用这些数据,计算某些可量化的脉管系统特性。然后将人工智能算法应用于检测、预测、诊断、确定预后、监测或分期疾病。人工智能算法可以包括但不限于机器学习算法。该疾病可以是癌症、中风、短暂性脑缺血发作、糖尿病、动脉粥样硬化、高血压心脏病、动脉瘤、外周动脉疾病、肺栓塞或血管性痴呆。
现在参考图1,其是用于检测、预测、诊断、确定预后、监测和分期脉管系统疾病的过程100的流程图。在一些实施例中,过程100可以由关于图2所讨论的系统200执行和/或实现。在其他实施例中,过程100可以由计算机程序的一个或多个模块执行和/或实现。
脉管系统可包括多个血管。可以首先获得脉管系统的图像(101)。可以使用任何非侵入性成像技术来获得图像,例如磁共振成像(MRI)、磁共振血管造影(MRA)、计算机断层扫描(CT)、CT血管造影(CTA)、微型CT、X射线、X射线血管造影、功能性MRI或PET。可以在成像过程之前向动物或人施用造影剂,其可以包括基于碘的造影剂和基于钆的造影剂,从而可以在所得扫描中清楚地看到脉管系统。造影剂可以口服、灌肠给药或注入血管。但是,根据各种实施例,可以互换地使用其他非侵入性成像技术。
如果这些图像本质上是三维图像,则扫描将包含一堆二维图像。例如,然后这些二维图像中的每一个可以被转换为.png图像。然而,根据各种实施例,其他图像格式可以互换使用。然后可以将图像堆栈转换为灰度格式。
图像堆栈可以经历图像平滑和/或去噪,以将图像堆栈转换为预处理图像(103)。图14A至图14F、图15A至图15F和图16A至图16C示出通过实验获得的预处理后的样本脉管系统图像。进行降噪是为了消除图像堆栈中的噪声。可以使用局部均值(LM)技术来执行图像平滑和去噪。在其他实施例中,可以使用非局部均值(NLM)技术来执行图像平滑和去噪。然而,根据各种实施例,可以互换地执行图像平滑和/或去噪的其他技术。例如,可以使用一个或多个软件程序来执行图像平滑和/或去噪。
在图像平滑和/或去噪过程中,图像堆栈中的每个像素的强度值可以被其相邻像素的平均强度值代替。可以保存包含三维图像的预处理图像的堆栈的文件夹,以准备进行图像处理。例如,可以保存包含一堆预处理过的.png图像的文件夹,以准备以后进行图像处理。
然后,可以对预处理图像堆栈进行图像处理(105)。图像处理和分割可以由一个或多个软件程序执行,以从预处理图像的堆栈中提取血管测量值。例如,图像处理可以由作为开源软件程序的Angicart++执行。然而,根据各种实施例,能够处理预处理图像的堆栈的其他软件程序可以互换使用。图9A示出通过实验获得的非中风脑脉管系统的完成的Angicart++处理图像。图9B示出通过实验获得的梗塞周围区域中风脉管系统的完成的Angicart++处理图像。图9C示出通过实验获得的缺血性半球中风脉管系统的完成的Angicart++处理图像。
所提取的血管测量值可以包含脉管系统内每个血管的测量结果。在前面的示例中,可以在Angicart++源代码中更改目录以指向.png图像的正确文件夹。然后,Angicart++会输出包含血管测量值的制表符分隔值(TSV)文件。
对于脉管系统内的每个血管,可以进行各种血管测量值以形成血管数据。各种血管测量值可包括以下数据标准中的至少一项:血管名称、血管半径、血管长度、血管体积、血管连接到的半径较大的血管(例如父血管)的名称,血管数量、血管相连到的半径较小的血管(例如子代血管)的数量,子代血管的名称,血管起点的三维坐标或血管终点的三维坐标。图11A至图11E、图12A至图12E和图13A至图13C示出通过实验获得的样本输出Angicart++数据文件。
在一些实施例中,然后可以将血管数据转换为纯文本文件并保存为纯文本文件。然后可以将纯文本文件导入到一个或多个软件程序中,以便根据血管数据计算血管特征。例如,纯文本文件可以导入到MATLAB中并保存为变量。一个或多个软件程序可以读取纯文本文件并为文件的每一列创建变量。例如,MATLAB可以读取纯文本文件并为文件的每一列创建变量。一个或多个软件程序可以使用tdfread读取纯文本文件。可以创建具有多个行和多个列的空矩阵,并用血管测量值填充。行的数量可以等于血管的数量,列的数量可以等于不同血管测量值的数量。在其他实施例中,行的数量可以等于不同血管测量值的数量,并且列的数量可以等于血管的数量。
可以基于提取的血管测量值确定脉管系统的特征(107)。脉管系统的特征可以包括从脉管系统内的每个血管计算出的平均值、中值和标准差。
对于脉管系统中的每个分支交界(branching junction),可以使用以下公式计算对称比例因子:
公式1:
公式2:
在上述公式中,自由基比例因子由β表示,而长度比例因子由γ表示。在上述公式中,下标表示血管的分支级别。例如,r
对于脉管系统中的每个分支交界,可以使用以下公式计算不对称比例因子:
公式3:,γ
公式4:γ
公式5:β
公式6:β
可以计算两个不同的代谢比例指数。第一指数可以使用血管半径测量值,并且第二指数可以使用血管长度测量值。
为了计算基于保守性的比例指数和基于比率的比例指数,可以执行以下三个步骤。首先,对于脉管系统中的每个血管,可以将血管的长度和半径保存为变量。其次,一个或多个软件程序可以在数据文件中定位父血管的测量值。第三,可以将父血管的长度、半径和血管子代的数量保存为变量。
对于脉管系统中的每个分支交界,可以计算基于保守性的比例指数。使用牛顿法,可以针对径向指数(a)和长度比例指数(b)求解以下公式:
公式7:
公式8:
在上述公式中,r
对于脉管系统中的每个分支交界,可以使用以下公式计算基于比率的比例指数:
公式9:a=-log
公式10:b=-log
然后可以计算脉管系统中的每个血管的基于比率的比例指数的平均值、中值和标准差。图5G示出通过实验获得的来自中风后脉管系统(缺血性半球)的径向指数(a)的基于比率的计算结果的样本图。图6G示出通过实验获得的来自非中风脑脉管系统(非缺血性半球)的径向指数(a)的基于比率的计算结果的样本图。图10G示出通过实验获得的来自中风后脉管系统(梗塞周围)的径向指数(a)的基于比率的计算的分布。图5H示出通过实验获得的来自中风后脉管系统(缺血性半球)的长度比例指数(b)的基于比率的计算结果的样本图。图6H示出通过实验获得的来自非中风脑脉管系统(非缺血性半球)的长度比例指数(b)的基于比率计算结果的样本图。图10H示出通过实验获得的在梗塞周围区域中来自中风后脉管系统的长度比例指数(b)的基于比率的计算的分布。
对于脉管系统中的每个血管,可以记录血管的半径和长度。半径和长度可以归类为脉管系统的分支层次。然后可以为每个仓(bin)计算基于比率的比例指数。然后可以计算脉管系统中每个血管的分层平均比例指数的平均值、中值和标准差。图5E示出通过实验获得的来自缺血性中风的径向指数(a)的基于分层平均的计算。图6E示出通过实验获得的来自非中风脑脉管系统(非缺血性半球)的径向指数(a)的基于分层平均的计算。图10E示出通过实验获得的在梗塞周围中来自中风后脉管系统的径向指数(a)的基于分层平均的计算。图5F示出通过实验获得的来自缺血性中风的长度比例指数(b)的基于分层平均的计算。图6F示出通过实验获得的来自非中风脑脉管系统(非缺血性半球)的长度比例指数(b)的基于分层平均的计算。图10F示出通过实验获得的在梗塞周围区域中来自中风后脉管系统的长度比例指数(b)的基于分层平均的计算。
对于基于分布的比例指数和基于回归的比例指数,这些仓可以是等距的间隔,范围从集合中的最小数据到最大数据。仓的数量可以近似等于脉管系统中血管的数量的平方根。
可以使用以下公式计算基于分布的比例指数a和b:
公式11:
公式12:
在上述公式中,N代表脉管系统中血管的数量,r
图5D示出通过实验获得的在缺血性中风发作之后来自脑脉管系统的长度比例指数(b)的基于分布的计算。图6D示出通过实验获得的来自非中风脑脉管系统(非缺血性半球)的长度比例指数(b)的基于分布的计算结果的样本图。图10D示出通过实验获得的在大脑的梗塞周围区域中来自脉管系统的长度比例指数(b)的基于分布的计算结果的样本图。
基于回归的比例指数是基于以下理论的:任何血管的半径和长度均与下游血管尖端的数量成比例。基于径向回归的比例指数可以是血管半径与下游血管尖端数量的对数-对数图中最佳拟合线的斜率。基于长度分布的比例指数可以是血管长度与下游血管尖端数量的对数-对数图中在最佳拟合线的斜率。图4B示出基于回归的比例指数对数回归的机器学习结果的样本图。图5I示出通过实验获得的来自缺血性中风的径向指数(a)的基于回归的计算。图6I示出通过实验获得的来自非中风脑脉管系统(非缺血性半球)的径向指数(a)的基于回归的计算。图10I示出通过实验获得的在梗塞周围区域中来自中风后脉管系统的径向指数(a)的基于回归的计算。图5J示出通过实验获得的来自缺血性中风的长度比例指数(b)的基于回归的计算。图6J示出通过实验获得的来自非中风脑脉管系统(非缺血性半球)的长度比例指数(b)的基于回归的计算。图10J示出通过实验获得的在梗塞周围区域中来自中风后脉管系统的长度比例指数(b)的基于回归的计算。
整个脉管系统的不对称比例指数可以使用以下公式计算:
公式13:
对于脉管网络中的每个血管,可以使用距离度量方法通过将血管段的弧长除以血管段的起点和终点之间的直线距离来计算曲折度值。可替代地,可以使用拐点计数方法来计算曲折度,其被计算为:(拐点的数量+1)倍(距离度量曲折度)。可替代地,可以使用角度总和度量(SOAM)来计算曲折度,其中,沿采样的空间曲线对血管的曲率求和,并通过血管的弧长对其进行归一化。在其他实施例中,可以使用其他方法来计算曲折度。可以为脉管系统中的每个血管计算平均值、中值和标准差曲折度度量。
总毛细血管容积可以通过将直径小于10μm的网络中每个血管的容积相加而得出。然后可以通过将总毛细血管体积除以三维医学图像的总体积来计算毛细血管密度度量。可以计算直径小于10μm的网络中每个血管的总表面积,并将其除以三维医学图像的总表面积。在其他实施例中,可以为直径大于10μm的血管计算这些值。
对于以下7个脉管特征中的每个附加特征,可以计算整个脉管系统中每个血管的均值、中值和标准差:
1.血管直径
2.血管长度
3.分支角度
4.计算每个血管的分支频率为
5.血管尖端的数量
6.血管子代的数量
7.动脉或静脉分支点的数量
8.层次分形维数的计算公式为:
脉管系统中环的总数,当血管分裂成多个子代血管时会发生,其中一些会聚到同一子血管中。
分支点的总数可以被计数并除以脉管系统的总体积,该分支点的总数被定义为脉管系统中血管分裂成两个或多个血管子代的位置。
血管尖端的总数可以被计数并除以脉管系统的总体积,该血管尖端的总数被定义为脉管系统中没有血管子代的位置。
分形分析测量受试体填充可用空间并从缩放定律得出的程度。分形分析可用于量化脉管系统的不规则性。这是医学图像分类和诊断中的重要特征。分形分析的类型可以包括分别用于计算Hausdorff分形维数、腔隙度维数和多分形维数的盒计数分析、腔隙度分析和多重分形分析。开源分形分析软件FracLAC可用于计算这些不同类型的分形维数。
Hausdorff维数的计算方法如下。对于脉管系统的三维图像,计数覆盖脉管系统所需的边长为s的立方体N(s)的数量。针对多个边长s计数立方体N(s)的数量。然后可以通过绘制log(N(s))对
腔隙度维数测量分形如何填充空间并可以量化旋转不变性和异质性。具有更多或更大间隙的图案对应于更高的腔隙度值。可以使用二维或三维盒计数算法来覆盖不同边长s的盒中的整个脉管系统图像。对每个盒中的像素数计数。令μ
公式14:
多分形分析表明,如果图案以某些方式失真,图案是如何表现的。首先使用盒计数算法用二维或三维盒覆盖图像,并记录每个盒中的像素数。出现在盒j中的多个像素x的概率P随着盒大小s变化到某个指数a。广义分形维数D
公式15:
公式16:
公式17:
公式18:P
可以编辑由每个脉管系统图像的血管特征组成的数据集。每个数据集包含两个独立的血管特征的两列,并且第三列指示疾病状态(0=无疾病,1=患病)。
然后可以选择脉管系统的特征(109)。可以使用弹性网算法执行特征选择,以从原始数据集中选择最突出的特征。弹性网算法可以是选择相关变量组的正则回归算法。可以使用LASSO(最小绝对收缩和选择算子),使用以下公式估算弹性网:
公式19:
公式20:
在上述公式中,X是定量血管特征x
弹性网可以在一个或多个软件程序中实现。例如,弹性网可以使用内置的LASSO函数在MATLAB中实现,该函数利用a,X和y,其中X是包含血管特征的矩阵,其中行代表每个血管并且每列代表其中一个血管特征。另外,y是二进制分类标签向量,其中y的每个元素代表X的行,其中1表示患病的脉管系统,而0表示未患病的脉管系统。内置的LASSO函数可以在矩阵β中输出回归系数,并输出矩阵F,矩阵F列出每个列向量具有多少个特征并且每个中的λ个,其中F用于查找数据集的最突出特征和使用的λ。最后,可以对数据进行排序,以根据突出特征的幅度按降序对突出特征的系数进行排序。
在其他实施例中,可以在特征选择中使用LASSO或岭回归算法。LASSO可以在一个或多个软件程序中实现。例如,可以使用内置的LASSO函数在MATLAB中实现LASSO。岭回归可以类似地由一个或多个软件程序实现。例如,根据各种实施例,可以在MATLAB中实现岭回归。根据各种实施例,能够实现LASSO和/或岭回归的其他软件程序可以互换使用。
然后,脉管系统的特征可以进行提取(111)。可以使用主成分分析(PCA)进行特征提取。PCA找到数据的甚至更低维度的表示形式,该表示形式保留突出且线性不相关的特征。
可以在一个或多个软件程序中实现PCA。例如,PCA可以在MATLAB中实现。PCA代码以矩阵X中的弹性网的突出特征作为输入。使用内置的奇异值分解(SVD)函数,代码执行X的SVD,并使用SVD中的“u”输出前几个主成分(PC),使用SVD中的“v”创建投影矩阵,并使用SVD中的“s”表示每个主成分的方差。
数据集可以随机分为训练集(58%)和测试集(42%)。可替代地,数据集一次可以包含两个以上的血管特征,并且可以分为训练集(85%)和测试集(15%)。
然后可以对脉管图像进行分类(113)。训练数据集可以用于训练机器学习算法。例如,机器学习算法可以是二元对数回归模型和二元朴素贝叶斯分类器模型(图3A至图3L示出机器学习结果的样本图)。然而,根据各种实施例,适合于执行该方法的其他机器学习算法可以互换使用。一些实施例可以包括多变量(例如,两个以上)的假设。二变量对数回归模型可以在MATLAB中实现,并且可以学习以下公式:
公式21:
在上述公式中,
公式22:J(θ)=-∑
为了训练模型,可以通过根据以下公式相对θ取J(θ)的导数来最小化上述代价函数:
公式23:
二元朴素贝叶斯分类器模型可以是概率分类器,其根据以下公式应用条件概率的贝叶斯定理:
公式24:
在上述公式中,P(c|x)是给定预测变量x的类别c的后验概率,其中P(c)是类别c的先验概率。给定类别c的预测变量x的概率由P(x|c)表示。给定类别c的预测变量x的先验概率由P(x)表示。
在图1的上述步骤中,诸如朴素贝叶斯分类器的算法可以使用诸如内置朴素贝叶斯分类器fitcnb的算法在一个或多个软件程序(诸如MATLAB)中实现。然后可以测试模型。根据测试集的特征,这些模型将脉管系统图像分类为患病或未患病。然后可以将模型的预测与测试集的实际结果进行比较。然后,可以将模型的准确度确定为正确分类除以做出的总分类的比率。图7示出通过从脉管系统分析来检测缺血性中风的对数回归程序和朴素贝叶斯分类器的准确度的表。
在其他实施例中,可以应用替代的人工智能算法。替代的人工智能算法可以是机器学习算法,包括但不限于:人工神经网络、卷积神经网络、递归神经网络、决策树、支持向量机、替代贝叶斯算法、聚类算法、深度学习和基于实例的算法。在一些实施例中,可以实施多级分类方案而不是单级分类方案。在一些实施例中,可以使用曲线下面积(AUC)、接收器工作特性(ROC)或交叉验证来执行机器学习模型的测试。
图2示出用于执行用于检测脉管系统中的疾病的方法/过程的系统200。例如,系统200可以执行关于图1公开的过程100。系统可以包括计算设备201。系统可以包括网络203和/或服务器205。服务器205可以具有处理器207和/或存储器209。不同的组件,例如计算设备201和服务器205,可以通过网络203彼此互连。
计算设备201可具有加载在计算设备201上的一个或多个软件程序211,用于执行用于检测脉管系统中的疾病的方法。计算设备201可以从服务器205下载一个或多个软件程序211。计算设备201包括处理器213和存储器215。计算设备201可以包括用于访问网络203的网络访问设备217。计算设备201可以包括用户界面219,该用户界面219从诸如医学从业者或研究者的用户接收输入。然而,根据各种实施例,计算设备201可以从其他类型的用户接收输入。
一个或多个软件程序211可以存储在存储器215中。在其他实施例中,一个或多个软件程序211可以位于服务器205上,或者可以通过网络203获得。存储器215可以存储要在处理器213上执行的指令,并且可以包括一个或多个RAM或其他易失性或非易失性存储器。存储器215可以是非暂时性存储器或数据存储设备,例如硬盘驱动器、固态磁盘驱动器、混合磁盘驱动器或其他适当的数据存储,并且可以进一步存储机器可读指令,这些指令可以由处理器213加载和执行。
一个或多个软件程序211可以包括与用户界面219的接口和/或交互。用户界面219可以包括能够接收用户输入的任何设备,例如按钮、键盘、鼠标、表盘、麦克风、图形用户界面或触摸屏以及任何能够输出的设备,例如显示器、扬声器或可刷新的盲文显示器。用户界面219允许用户与一个或多个软件程序211通信。例如,用户可能能够向一个或多个软件程序211提供数据,例如用户输入,和/或通过用户界面219从一个或多个软件程序211接收反馈。
网络访问设备217可以包括通信端口或信道,例如USB端口、Wi-Fi单元、
计算设备201可以获得脉管系统的图像(参见图1的101)。计算设备201可以经由用户在计算设备201上上传、下载或以其他方式获取图像来获得图像。处理器213可以对图像执行图像平滑和/或去噪(参见图1的103)。可以使用位于计算设备201的存储器215中的一个或多个软件程序211来执行图像平滑和/或去噪。在其他实施例中,可以使用位于服务器205上或可通过网络203获得的一个或多个软件程序211来执行图像平滑和/或去噪。在一些实施例中,图像平滑和/或去噪可以由用户经由用户界面219启动。在其他实施例中,图像平滑和/或去噪可以由计算设备201自动启动。
处理器213可以对图像执行图像处理(参见图1的105)。可以使用位于计算设备201的存储器215中的一个或多个软件程序211来执行图像处理。在其他实施例中,可以使用位于服务器205上或可通过网络203获得的一个或多个软件程序211来执行图像处理。在一些实施例中,图像处理可以由用户经由用户界面219启动。在其他实施例中,图像处理可以由计算设备201自动启动。
处理器213可以确定脉管系统的脉管特征(参见图1的107)。可以使用位于计算设备201的存储器215中的算法来执行脉管特征的确定。在一些实施例中,算法可以是位于计算设备201的存储器215中的一个或多个软件程序211的一部分。在其他实施例中,可以使用位于服务器205上或可通过网络203获得的算法来执行脉管系统特征的确定。在一些实施例中,算法可以是位于服务器205上或可通过网络203获得的一个或多个软件程序211的一部分。在一些实施例中,脉管系统特征的确定可以由用户经由用户界面219启动。在其他实施例中,脉管系统特征的确定可以由计算设备201自动启动。
处理器213可以选择脉管系统的特征(参见图1的109)。可以使用位于计算设备201的存储器215中的算法来执行脉管特征的选择。在一些实施例中,算法可以是位于计算设备201的存储器215中的一个或多个软件程序211的一部分。在其他实施例中,可以使用位于服务器205上或可通过网络203获得的算法来执行脉管系统特征的选择。在一些实施例中,算法可以是位于服务器205上或可通过网络203获得的一个或多个软件程序211的一部分。在一些实施例中,脉管系统特征的选择可以由用户经由用户界面219启动。在其他实施例中,脉管系统特征的选择可以由计算设备201自动启动。
处理器213可以从脉管系统中提取特征(参见图1的111)。可以使用位于计算设备201的存储器215中的一个或多个软件程序211来执行脉管系统的特征的提取。在其他实施例中,可以使用位于服务器205上或可通过网络203获得的一个或多个软件程序211来执行脉管系统的特征的提取。在一些实施例中,脉管系统的特征的提取可以由用户经由用户界面219启动。在其他实施例中,脉管系统的特征的提取可以由计算设备201自动启动。
处理器213可以对脉管系统的图像进行分类(参见图1的113)。可以使用位于计算设备201的存储器215中的算法来执行脉管系统图像的分类。在一些实施例中,算法可以是位于计算设备201的存储器215中的一个或多个软件程序211的一部分。在其他实施例中,可以使用位于服务器205上或可通过网络203获得的算法来执行脉管系统图像的分类。在一些实施例中,算法可以是位于服务器205上或通过可网络203获得的一个或多个软件程序211的一部分。在一些实施例中,脉管系统图像的分类可以由用户经由用户界面219启动。在其他实施例中,脉管系统图像的分类可以由计算设备201自动启动。
本发明的中风数据
对小鼠脑脉管系统进行了19次微CT扫描。19次微CT扫描中有8次是健康/非缺血性脉管系统。在诱发性缺血性中风(血栓性中风)发作后7天,十九次微CT扫描中有十一次是脉管系统的。来自三只不同小鼠的微CT扫描包括来自脑缺血半球、脑梗塞周围区域和脑非缺血半球的脉管系统成像。图14A至图14F、图15A至图15F和图16A至图16C示出通过实验获得的预处理之后的样本脉管系统图像。
然后可以使用Angicart++从脉管系统的成像中提取测量数据。更具体地,可以使用Angicart++从脉管系统的成像中提取八个定性和定量特征。图9A示出通过实验获得的非中风脉管系统的完成的Angicart++处理图像。图9B示出通过实验获得的梗塞周围中风的完成的Angicart++处理图像。图9C示出通过实验获得的中风脉管系统的完成的Angicart++处理图像。
对于每个图像,可以通过以0.005为增量在各种阈值下进行测试来计算体素尺寸并且可以确定最佳阈值。对于网络中的每个血管,可以提取血管名称、血管半径、血管长度、血管体积、血管父代、血管子代的数量以及下游血管尖端的数量。图8A示出样本图,其中基于血管半径与长度的平均比与血管子代的平均数量的分析,使用正则对数回归来对非中风和缺血性中风脉管系统的几次扫描进行分类。图8B示出样本图,其中基于血管半径与长度的平均比与下游血管尖端平均数量的分析,使用朴素贝叶斯分类器来对非中风和缺血性中风脉管系统的几次扫描进行分类。图11A至图11E、图12A至图12E和图13A至图13C示出通过实验获得的样本输出Angicart++数据文件。
MATLAB程序可以自动计算和绘制比例指数,以及其他统计信息,例如平均值、中值、标准差、95%置信区间和未调整的R
图5C示出通过实验获得的在缺血性中风发作之后来自脑脉管系统的径向指数(a)的基于分布的计算。图6C示出通过实验获得的来自非中风脑脉管系统(非缺血性半球)的径向指数(a)的基于分布的计算结果的样本图。图10C示出通过实验获得的在梗塞周围中来自中风后脉管系统的径向指数(a)的基于分布的计算结果的样本图。图5D示出通过实验获得的缺血性中风发作之后来自脑脉管系统的长度比例指数(b)的基于分布的计算。图6D示出通过实验获得的来自非中风脑脉管系统(非缺血性半球)的长度比例指数(b)的基于分布的计算结果的样本图。图10D示出通过实验获得的在大脑的梗塞周围区域中来自脉管系统的长度比例指数(b)的基于分布的计算结果的样本图。
图5G示出通过实验获得的来自缺血性中风的径向指数(a)的基于比率的计算结果的样本图。图6G示出通过实验获得的来自非中风脑脉管系统(非缺血性半球)径向指数(a)的基于比率的计算结果的样本图。图10G示出通过实验获得的在梗塞周围中来自中风后脉管系统的径向指数(a)的基于比率的计算的分布。图5H示出通过实验获得的来自缺血性中风的长度比例指数(b)的基于比率的计算结果的样本图。图6H示出通过实验获得的来自非中风脑脉管系统(非缺血性半球)的长度比例指数(b)的基于比率的计算结果的样本图。图10H示出通过实验获得的在梗塞周围区域中来自中风后脉管系统的长度比例指数(b)的基于比率的计算的分布。
图5I示出通过实验获得的来自缺血性中风的径向指数(a)的基于回归的计算。图6I示出通过实验获得的来自非中风脑脉管系统(非缺血性半球)的径向指数(a)的基于回归的计算。图10I示出通过实验获得的在梗塞周围区域中来自中风后脉管系统的径向指数(a)的基于回归的计算。图5J示出通过实验获得的来自缺血性中风的长度比例指数(b)的基于回归的计算。图6J示出通过实验获得的来自非中风脑脉管系统(非缺血性半球)的长度比例指数(b)的基于回归的计算。图10J示出通过实验获得的在梗塞周围区域中来自中风后脉管系统的长度比例指数(b)的基于回归的计算。
包含定量数据(例如比例指数)的数据集可以随机分为训练集和测试集。例如,数据集可以随机分为训练集(64%)和测试集(36%)。对数回归和朴素贝叶斯分类器程序可能正在使用训练集进行训练。然后,程序可以根据测试集预测中风的发生,然后可以记录测试的准确性。图3A至图3L示出该实验的机器学习结果的样本图。
对数回归是在检测缺血性中风的发生中测试的两种机器学习算法中最准确的方法,平均测试准确性为74.6%。朴素贝叶斯分类器的平均测试准确度为59.7%。这是提高对缺血性中风的准确诊断的重要步骤,使用常规方法(Tyan等,2014)正确诊断出缺血性中风的几率只有31%。通过通知医生治疗病人以防止未来中风的发作,本文的公开内容可潜在地挽救许多生命并显著降低医疗成本。图7示出通过从脉管系统分析来检测缺血性中风的对数回归程序和朴素贝叶斯分类器的准确度的表。
上述结果的局限性包括仅获得了十九次脉管成像的微CT扫描。这减少了训练机器学习模型的数据点。可能至少需要数百张图像(微CT扫描)才能训练和测试机器学习模型。错误的潜在来源可能包括Angicart++处理的图像噪声。
在另一实施例中,由于中风恢复脉管系统包含环,因此可以计算出扭转以量化脉管系统的弯曲度。在另一实施例中,为了获得更多的数据点来训练和测试机器学习模型,可以获得中风恢复脉管系统的更多成像,大约数百张图像。另外,在另一实施例中,可以实现神经网络以改善机器学习模型。
应当理解,尽管通过参考特定实施例突出了本说明书的各方面,但是本领域技术人员将容易理解,这些公开的实施例仅是本文公开主题的原理的说明。因此,应当理解,所公开的主题绝不限于本文所述的特定方法、方案和/或试剂等。这样,在不脱离本说明书的精神的情况下,可以根据本文的教导对所公开的主题进行各种修改或改变或替代配置。最后,本文所使用的术语仅出于描述特定实施例的目的,并不旨在限制本文所公开的系统、装置和方法的范围,该范围仅由权利要求书来定义。因此,系统、装置和方法不限于精确地如所示出和描述的那样。
本文描述系统、装置和方法的某些实施例,包括发明人已知的用于执行该系统的最佳模式。当然,这些描述的实施例的变型对于本领域普通技术人员而言,在阅读了前面的描述之后将变得显而易见。发明人期望熟练的技术人员适当地采用这样的变型,并且发明人希望以不同于本文具体描述的方式来实践的系统、装置和方法。因此,系统、装置和方法包括适用法律所允许的所附权利要求中记载的主题的所有修改和等同物。而且,除非本文另外指出或与上下文明显矛盾,否则上述实施例在其所有可能的变化中的任何组合都被系统、装置和方法所涵盖。
系统、装置和方法的替代实施例、元件或步骤的分组不应解释为限制。每个小组成员可以单独引用或要求保护,也可以与本文中公开的其他小组成员进行任意组合。预期出于方便和/或可专利性的原因,组中的一个或多个成员可以包括在组中或从中删除。当发生任何这样的包含或删除时,说明书被认为包含经修改的小组,从而满足所附权利要求中使用的所有马库什小组的书面描述。
除非另有说明,否则在本发明说明书和权利要求书中使用的表示特征、项目、数量、参数、特性、术语等的所有数字在所有情况下均应理解为由术语“约”修饰。如本文所用,术语“约”是指如此限定的特征、项目、数量、参数、特性或术语涵盖可以变化但仍能够执行本文所讨论的期望操作或过程的近似值。
除非本文另外指出或与上下文明显矛盾,否则在描述系统、装置和方法的上下文中使用的术语“一”、“一个”、“该”和类似指代物(特别是在以下权利要求的上下文中)应解释为涵盖单数和复数。除非本文另外指出或与上下文明显矛盾,否则本文描述的所有方法可以以任何合适的顺序执行。本文提供的任何和所有示例或示例性语言(例如,“诸如”)的使用仅旨在更好地阐明系统、装置和方法,并且不对另外要求保护的系统、装置和方法的范围构成限制。本说明书中的任何语言都不应被解释为表示对系统、装置和方法的实践必不可少的任何未要求保护的要素。
- 基于脉管化模式的诊断、预测、确定预后、监测或分期疾病的方法
- 用于诊断、预后和治疗监测基于神经性、神经退行性和炎症的疾病的方法
