用于二尖瓣的经导管锚固组件、二尖瓣和相关方法
文献发布时间:2023-06-19 11:57:35
技术领域
本发明大致涉及一种微创地植入瓣膜在心脏中的医疗组件、一种用于置换天然心脏瓣膜的新型瓣膜以及一种用于定位和限制瓣膜的锚固装置。本发明还涉及医疗组件的部件和瓣膜的植入方法。更具体地,本发明涉及一种新型的经导管的瓣膜、经导管的瓣膜裙、锚固装置、锚固件递送系统和瓣膜递送装置,以及涉及用于血管内植入瓣膜以跨二尖瓣以置换天然二尖瓣的功能的这种组件的方法。
背景技术
经导管的瓣膜已被证明用于置换天然心脏瓣膜,如主动脉瓣和肺动脉瓣,是安全和有效的。置换二尖瓣的确定性较低,因为经导管二尖瓣置换(TMVR)的初始临床试验已经面临由二尖瓣疾病的临床和解剖复杂性带来的重大挑战。
二尖瓣疾病,主要引起二尖瓣反流(MR),由瓣膜的原发性退变(如粘液瘤样变性、心内膜炎、风湿性疾病、先天性疾病或其他原因)或不完全小叶接合(继发性或“功能性”二尖瓣反流)引起,二尖瓣环扩张和/或继发于左心室扩张和乳头肌移位的二尖瓣小叶栓系(mitral leaflet tethering)的结合可发生不完全小叶接合。MR增加左心房压,引起肺充血,从而导致充血性心力衰竭的症状和体征,即外周水肿、端坐呼吸、夜间阵发性呼吸困难和进行性劳累性呼吸困难。此外,MR加剧左心室功能不全,降低存活率。由于许多患有MR的患者有明显的共病和高手术风险,开发治疗MR的微创(即经导管)方法是重要的。
最初开发的经导管技术具有重要的局限性,因为它们修复但不置换二尖瓣。例如,经导管的瓣环成形术装置[Arto(MVRx,Inc.,San Mateo,CA,USA);Cardioband(EdwardsLifesciences,Irvine,CA,USA);Carillon(Cardiac Dimensions,Kirkland,WA,USA);Millipede(Boston Scientific,Marlborough,MA,USA);Mitral Loop Cerclage(Tau-PNUMedical Co,Ltd.Pusan,Korean);Mitralign(Mitralign,Inc.,Tewksbury,MA,USA)]通过直接或间接缩小二尖瓣环的尺寸,使二尖瓣小叶更完全地接合,模拟外科瓣环成形术。尽管如此,这些技术受到不确定的再现性和无法处理小叶栓系或异常的限制。相反,MitraClip修复系统(Abbott Vascular,Abbott Park,Illinois,USA)或Pascal系统(EdwardsLifesciences)可以通过将小叶折叠在一起,复制手术Alfieri缝合来治疗小叶异常。尽管MitraClip系统是FDA批准的,对许多患者有效,但仍有相当数量的患者(>10%)在MitraClip后复发MR,许多患者由于解剖限制而无法接受MitraClip。类似地,人工腱索疗法(artificial chordal therapies)[NeoChord DS1000(NeoChord,Inc.,St.Louis Park,Minnesota,USA);Harpoon TSD-5and V-chordal(Edwards LifeSciences)]目前仅限于非常特殊的解剖结构(例如孤立的小叶脱垂)。
经导管二尖瓣置换术(TMVR)不受解剖限制,少数患者有复发性MR。然而,基于它们锚固到二尖瓣的方式,当前技术仍具有局限性和缺点。锚固在二尖瓣小叶上,Fortis瓣膜(Edward Lifesciences)的血栓形成率不可接受。同样固定在天然小叶上的Tiara瓣膜(Neovasc,Richmond,BC,Canada)已经成功植入,没有同样的血栓形成问题。同样,直接与二尖瓣环接合的CardiAQ(Edwards Lifesciences),用“小翼(winglets)”穿刺环和小叶的NaviGate(NaviGate Cardiac Structures,Lake Forest,CA,USA),以其“沙漏(hour-glass)”形状接合瓣环的Cephea(Abbott Vascular),以及通过“类似软木塞(champagnecork-like)”效应与瓣环接合的Intrepid瓣膜(Medtronic,Minneapolis,Minnesota,USA),都是在没有血栓问题的情况下植入的。
然而,由于这些装置直接锚固到二尖瓣环,它们在不同程度上限制了二尖瓣环运动的自由度。限制这种自由度可能会导致左心室功能障碍。例如,一项将经导管二尖瓣修复(使用Abbott Vascular的MitraClip装置)与心脏直视手术进行比较的研究表明,与心脏直视手术相比,二尖瓣环运动明显较低,作者认为这是与经导管修复相比心脏直视手术后左心室射血分数(LVEF)较低的一个因素。类似地,一项比较柔性和刚性二尖瓣瓣环成形术环的研究发现,刚性环的LVEF显著降低,这比柔性环更能限制二尖瓣环的运动。因此,通过限制二尖瓣环,这些装置可能对左心室功能产生有害影响。
类似地,使用对接系统的TMVR装置可能通过限制二尖瓣环运动而降低左心室功能。特别是,Caisson(LivaNova,PLC,London,England)、HighLife(HighLife SAS,Paris,France)、Mvalve(Boston Scientific)和Sapien M3(Edwards Lifesciences)瓣膜都使用对接系统将经导管假体固定到二尖瓣环。
除了约束二尖瓣环之外,这些装置还引起左心室流出道(LVOT)阻塞的风险,当瓣膜支撑物(valve prop)打开二尖瓣前小叶时发生这种阻塞,从而产生LVOT流出的固定阻塞。这是TMVR装置在心室小、肥大(女性更常见)或二尖瓣环钙化患者中的一个特别限制。
为了减轻这些担忧和限制,Tendyne瓣膜(Abbott Vascular)具有较低的LVOT阻塞风险,并且不像其他TMVR装置那样限制二尖瓣环。Tendyne之所以能做到这一点,是因为瓣膜通过附着在心外膜系绳上的腱索锚固。因此,它不需要刚性固定到二尖瓣环,并且该瓣膜的狭窄的环内部分不将前二尖瓣小叶推入LVOT至与其它瓣膜相同的程度。Tendyne的问题是它需要经心尖进入(左心室切口),这可能会损害某些患者的左心室功能。
Alta瓣膜(4C Medical Therapies)避免了经心尖进入,也不限制二尖瓣环或诱导LVOT阻塞,Alta瓣膜(4C Medical Therapies)包括一个固定在适当位置的上环形瓣膜,在左心房有一个大的、灵活的球笼。然而,目前尚不清楚这种球笼是否会引起心房异常,如纤维化,从而导致心房颤动和/或心房收缩功能丧失。此外,天然二尖瓣小叶的持续功能可能会导致流动干扰,从而改变假体小叶的功能。
因此,在相关领域中仍然期望提供一种用于放置在二尖瓣环上的经导管的瓣膜,其可以在没有经心尖进入的情况下递送,其具有最小的LVOT阻塞风险,通过不锚固到心房或二尖瓣环而允许正常的心房和二尖瓣环功能,并且在手术过程中可完全重新定位和取出。
发明内容
本文提出了一种医疗组件,其微创地植入二尖瓣,以替换天然二尖瓣的功能。本文公开的方法经由经间隔通路植入二尖瓣,并且瓣膜(其可以是内环形的(intra-annular)或上环形的(supra-annular))锚固至室间隔,从而避免二尖瓣环锚固和约束,并且同时最小化LVOT阻塞的风险。因此,有益的是,系统的任何部分都不需要外科开胸和经心尖进入植入。
在一个方面,该系统包括经股静脉的经房间隔引导件和经间隔穿插针,其允许穿过房间隔以将圈套器鞘管递送到左心室中,同时将圈套器递送到左心室中邻近室间隔。
该系统还包括经颈静脉的经室间隔引导件和射频交叉线,其允许穿过室间隔,接着将线引入定位在左心室中的圈套器鞘管。通过经房间隔引导件将线体外化,形成线环,线从经颈引导件外侧延伸至经股引导件外侧。一个交换导管被推进到线环上,射频线被交换成更大更硬的线。
在一个方面,所述系统包括在所述线环上前进的顺行或逆行的锚固件递送鞘管,以及附接到构造成接受系绳的锚固帽的顺行或逆行的室间隔锚固件。所述系绳被配置成附连到一个或多个绳索,并且所述系绳附连到经导管的瓣膜。
根据各个方面,室间隔锚固件可由通过室间隔元件连接的右心室盘和左心室盘构成,并且这些中的每一个可由任何金属合金构成,例如但不限于镍钛诺、不锈钢、钛或钴铬合金。锚固件的每个元件可覆盖有合成材料,例如但不限于聚四氟乙烯(PTFE)或聚对苯二甲酸乙二醇酯(PET),或生物膜,例如但不限于牛或猪的心包组织。
锚固帽也由任何金属合金构成,并连接到室间隔锚固件的左心室盘上。对于逆行的室间隔锚固件(从室间隔的左心室侧递送),锚固帽的近端限定了一个内部的“阴”螺纹,该螺纹接受递送线缆远端的“阳”螺纹。在一个方面中,递送线缆保持附接到锚固帽并且用于引导系绳直到系绳的对接环与锚固件连接。最后,可以从锚固帽拧下递送线缆并将其移除。
对于顺行的室间隔锚固件(从室间隔的右心室侧递送),锚固帽是线环的导管。右心室盘具有限定内部的“阴”螺纹的线缆连接件,该内部的“阴”螺纹接受顺行的递送线缆的远端的“阳”螺纹。顺行的递送线缆还用作用于线环的导管,使得线在经股鞘管的外部开始,经过室间隔锚固件的锚固帽,穿过附连到间隔锚固件的右心室侧的递送线缆,并且离开经颈鞘管。延伸穿过锚固帽的线环引导系绳,直到系绳的对接环与锚固件连接。在连接之后,可以移除线环,并且可以旋松顺行的递送线缆,从而完全展开室间隔锚固件,其中系绳连接至锚固帽。
在一个方面,系绳具有连接到至少一个对接环臂的对接环,对接环臂具有限定在对接环臂的近端处的孔眼。每个孔眼连接到系绳杆的远端,系绳杆通过钩连接到孔眼。所述系绳杆由任何金属合金构成,并且所述系绳杆的近端连接到绳索。在一个方面,系绳的对接环在锚固帽上前进,压下锚固帽的突出的锁定臂。在另一个方面,对接环到达锚固帽的端部,从而允许突出的锁定臂推出,从而将对接环锁定在适当位置,并因此将系绳锁定在适当位置。在另一个方面,即使在被锁定就位之后,系绳也可以自由地绕着锚固帽的纵向轴线旋转,而不影响锚固帽或锚固螺钉的位置。为了收回,瓣膜递送导管在锁定臂上翻转,从而压下锁定臂,并允许取回系绳的对接环。
在一个方面,该系统包括被配置为将瓣膜连接和/或固定到室间隔的系绳,并且经导管的瓣膜包括集成到顶缘或底缘的本体罩住的瓣膜小叶。
在一个方面,所述经导管的瓣膜是自膨胀的并且由镍钛诺组成,并且覆盖有合成材料,例如但不限于聚四氟乙烯(PTFE)或聚对苯二甲酸乙二醇酯(PET),或者覆盖有生物膜,例如但不限于牛或猪的心包组织。
根据一个方面,经导管的心脏瓣膜的小叶由但不限于牛、马或猪的心包组织组成。在另一个方面,经导管的心脏瓣膜在展开部位处覆盖有直径大于瓣环的膜,使得使用中膜基本上覆盖二尖瓣环。
内环形式的经导管的瓣膜的框架从圆柱形状开始,圆柱的底部在瓣环处或低于瓣环,并且圆柱的顶部延伸到心房中。由激光切割或成形的镍钛诺制成的、由一个或多个线延伸部构成的顶缘从圆柱体的顶部延伸。这些延伸部被成形为例如但不限于线、弧、钩、圆、椭圆、正弦曲线或三条或更多条边的多边形的形状。顶缘的延伸部,如瓣膜的本体,覆盖有和/或连接有合成膜或生物膜。顶缘垂直于瓣膜本体,或者可以向心房底弯曲,呈凸形或凹形曲线。为了在顶缘向心房底弯曲时促进密封,覆盖织物由编织或针织织物组成,这允许“拉伸性”,提高顺应心房底构形的能力。
在上环形式的经导管的瓣膜中,框架从位于左心房底部的底缘开始。底缘由一个或多个由激光切割或成形的镍钛诺制成的线延伸部构成。这些延伸部被成形为例如但不限于线、弧、钩、圆、椭圆、正弦曲线或三条或更多条边的多边形的形状。底缘的延伸部分,如瓣膜的本体,覆盖和/或连接有合成膜或生物膜。底缘垂直于经导管的瓣膜本体,或者可以向心房底弯曲,呈凸形或凹形曲线。当底缘向心房底弯曲时,为了便于密封,覆盖织物由编织或针织织物组成,这允许“拉伸性”,提高了顺应心房底构形的能力。容纳瓣膜小叶的圆柱体从底缘延伸到左心房。
在一个方面,邻近瓣膜的圆柱体的顶部,沿瓣膜本体的内部或外部纵向延伸的是一个或多个导管,其形状为圆柱体,其横截面是圆形、椭圆形、抛物线或双曲线的任何部分,或者采取具有平的基部和顶部的多面体的形状,所述基部和顶部具有三条或更多条边的多边形的形状。这些导管由覆盖瓣膜本体的膜构成,或者可以由但不限于不锈钢、镍钛诺或其它金属合金制成。所述一个或多个导管是中空的并且容纳附接到至少一个系绳的至少一个绳索,并且每个导管附接到瓣膜的心房表面附近的可拆卸的锁定件。
可拆卸的锁定件将经导管的瓣膜牢固地固定到锚固系统,该锚固系统包括连接到室间隔锚固件的系绳,该室间隔锚固件牢固地附接到室间隔。在一个方面,系绳经由锚固帽连接到室间隔锚固件,并且至少一根绳索从系绳延伸穿过裙本体的至少一个导管。因此,通过导管将经导管瓣膜穿到到绳索上,使得经导管瓣膜与绳索滑动地相互作用。在另一个方面,绳索的近端附接到缝线,该缝线在心脏外部延伸以供使用者接近。
该系统还包括至少一个心房定位杆,该心房定位杆的近端附接至递送系统,并且其远端可逆地连接至可拆卸的锁定件,该可拆卸的锁定件附接至经导管的瓣膜本体的导管的近端。缝线和/或绳索穿过定位杆的内部管腔,从而定位杆推动或拉动经导管的瓣膜本体,从而将不同的力和弯曲施加到相关的顶缘或底缘,允许与心房底并置。在另一个方面,定位杆的旋转和/或定位杆的内部元件的推动或拉动导致可拆卸的锁定件接合绳索和/或缝线,将绳索和/或缝线固定到经导管的瓣膜本体,保持顶缘或底缘到心房底的力和弯曲,以及固定经导管的瓣膜的位置。
还提供了相关的植入方法。通过查验以下附图和详细描述,对于本领域技术人员而言,微创地植入心脏中的医疗装置和系统的其它装置、方法、系统、特征和优点将是或将变得显而易见的。所有这样的额外的装置、方法、系统、特征和优点都包括在本说明书中,并且在微创性地植入心脏中并且由所附权利要求保护的医疗组件的范围内。
附图说明
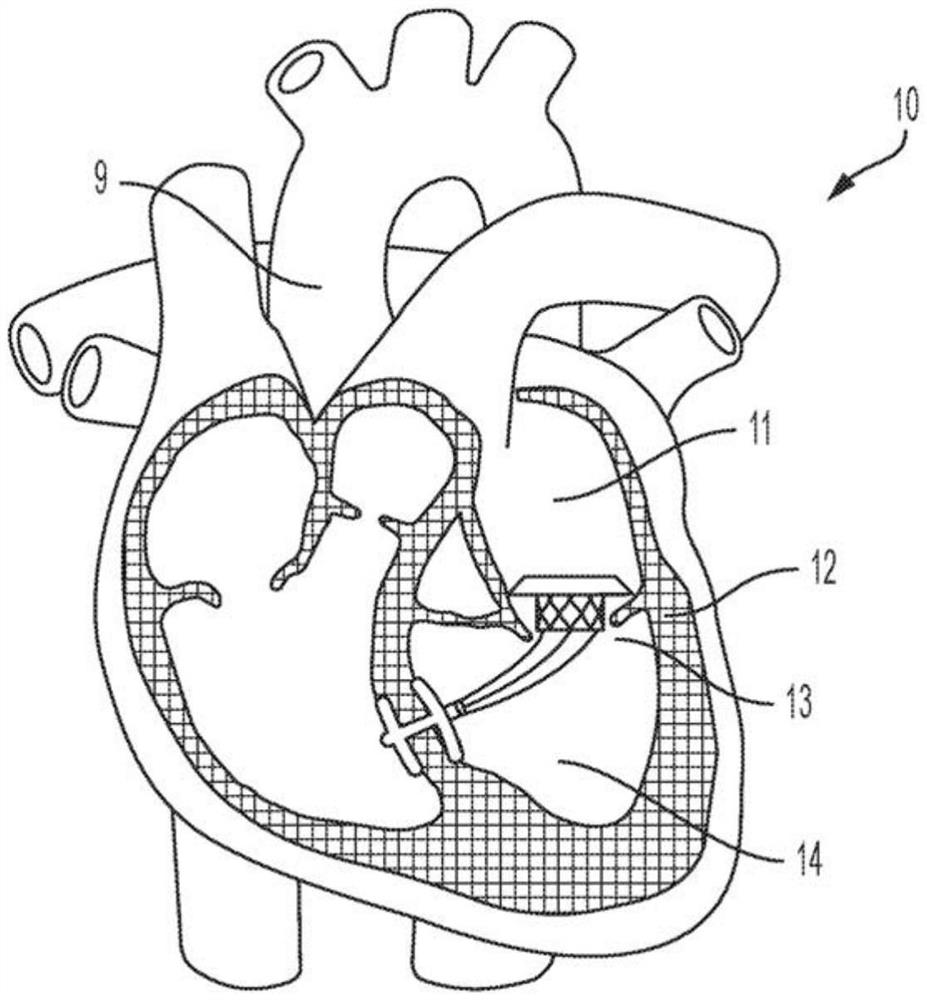
图1是根据一个方面的心脏的剖视图,其示出了定位在心脏中的本申请的经导管的瓣膜系统;
图2是用于将系绳锚固到室间隔的逆行的锚固件的立体图;
图3是用于将系绳锚固到心壁的逆行的锚固件的递送线缆的立体图;
图4是用于将经导管的瓣膜锚固到逆行的锚固件的系绳的立体图;
图5是逆行的锚固组件的立体图,包括用于将经导管的瓣膜连接到锚固件的系绳,连接到用于将系绳锚固到室间隔的锚固件,其中锚固件的LV盘连接到递送线缆。
图6是用于将经导管的瓣膜锚固到锚固件的顺行的锚固件的递送线缆的立体图;
图7是用于将系绳锚固到室间隔的顺行的锚固件的立体图;
图8是用于将经导管的瓣膜锚固到顺行的锚固件的系绳的立体图;
图9是顺行的锚固组件的立体图,所述顺行的锚固组件包括用于将经导管的瓣膜连接到锚固件的系绳,连接到用于将系绳锚固到室间隔的锚固件,其中锚固件的RV盘连接到递送线缆和导线贯穿组件;
图10A和图10B是内环形瓣膜的侧视图和顶部透视图,该内环形瓣膜由连接到具有集成的瓣膜小叶的经导管的瓣膜本体的顶缘构成;
图11A和图11B是瓣膜的透视图和俯视图,该瓣膜包括连接到具有集成的瓣膜小叶的经导管的瓣膜本体的顶缘;
图12是具有瓣膜的经导管的瓣膜的侧视图,其中顶缘的一个边缘从凹形构造过渡到凸形构造;
图13A是连接到心房定位杆和绳索的经导管的瓣膜本体的放大侧视图;
图13B是锁定系统的放大侧视图;
图14A是锁定系统的立体图;
图14B是锁定系统的立体剖视图;
图15A是用于经导管瓣膜本体定位在非锁定位置的锁定系统的截面侧视图;
图15B是用于经导管的瓣膜本体定位在锁定位置的锁定系统的截面侧视图;
图16A是处于锁定位置的锁定系统的局部剖视图;
图16B是锁定系统的立体图;
图17A-17F是按顺序步骤示出的具有锚固螺钉和配置成用于接收连接环和系绳系统的锚固帽的锚固件的立体图。
图18A是正在进行的经间隔穿刺和室间隔交叉引导件就位的透视图;
图18B是经间隔穿刺后圈套器定位在左心室中的透视图;
图19A是圈套器接收室间隔交叉线的透视图;
图19B是室间隔交叉导管穿过间隔前进的透视图;
图19C是室间隔交叉导管穿过间隔前进的放大透视图;
图20A是室间隔交叉导管前进到经间隔引导件的透视图;
图20B是室间隔交叉线被交换为0.035"线的透视图;
图21A是逆行的锚固件递送鞘管在0.035"轨线上向室间隔推进的透视图;
图21B是逆行的锚固件递送鞘管跨室间隔定位的透视图,其中逆行的锚固件递送鞘管的末端在右心室中,且逆行的锚固件定位在鞘管内侧;
图22A是逆行的锚固件的右心室盘被展开的透视图;
图22B是逆行的锚固件的左心室盘被展开且取回0.035"轨线的透视图;
图23是完全展开准备接收经导管的瓣膜的逆行的锚固件的透视图;
图24A是顺行的锚固件递送鞘管在0.035"轨线上穿过间隔前进的透视图;
图24B是顺行的锚固件递送鞘管的跨室间隔定位的透视图,其中顺行的锚固件递送鞘管的末端在左心室中,并且顺行的锚固件定位在鞘管内侧;
图25A是顺行的锚固件的左心室盘被展开的透视图;
图25B是顺行的锚固件的右心室盘被展开的透视图;
图26A是顺行的锚固件递送线缆被拧松并移除的透视图;
图26B是顺行的锚固件递送线缆被移除而0.035"轨线保持在适当位置的透视图;
图26C是经间隔引导件被移除的透视图,其中0.035"轨线留在适当位置,用于接收经导管的瓣膜,以在对接件上前进到顺行的锚固件上;
图27A是瓣膜递送系统接近锚固件的透视图;
图27B是系绳连接到锚固件的锚固帽上的透视图;
图28A是瓣膜递送引导件部分撤回的透视图,并且瓣膜的内环形部分被暴露;
图28B是瓣膜递送引导件完全撤回的透视图,在心房定位杆仍然连接到经导管的瓣膜本体的情况下暴露左心房中的瓣膜的顶缘;
图28C是完全暴露的瓣膜的放大透视图,其中心房定位杆仍然连接到经导管的瓣膜本体;
图29A是心房锁定接合件和心房定位杆撤回的透视图,只留下连接到经导管的瓣膜的本体的缝线;
图29B是心房锁定件接合和心房定位杆撤回的放大透视图,只留下连接到经导管的瓣膜的本体的缝线;
图29C是瓣膜展开和瓣膜递送系统从人体撤回的透视图,留下连接到经导管的瓣膜的本体的缝线通过瓣膜递送鞘管离开人体;
图30A是缝线切割器经由瓣膜递送鞘管被推进到刚好在经导管的瓣膜的顶缘上方的透视图;
图30B是在瓣膜顶缘上方切割缝线后瓣膜完全展开的透视图;
图30C是具有根据本发明另一方面的二尖瓣的图30A的透视图;
图30D是图30B的透视图,其中二尖瓣如图30C所示;
图31A和图31B是上环形瓣膜的侧视图和顶部透视图,该上环形瓣膜包括连接到具有集成的瓣膜小叶的经导管的瓣膜本体的顶缘;
图32A是根据本发明的另一方面的具有锚固螺钉和锚固帽的锚固件的分解图,该锚固帽构造成用于接收连接环和系绳系统;
图32B是图32A的锚固系统的侧视图,其中连接环在锚固帽上前进并锁定就位;
图32C是图32B的侧视图,其中递送线缆与系统分离;
图33A是具有根据本发明另一方面的稳定件的图32的锚固件的立体图;
图33B是图32的锚固螺钉的端部平面图。
具体实施方式
通过参考下面的详细描述、实施例和权利要求以及它们的前面和下面的描述,可以更容易地理解本发明。在公开和描述本系统、装置和/或方法之前,应当理解,除非另有说明,本发明不限于所公开的特定系统、装置和/或方法,因为它们当然可以变化。还应理解,本文所使用的术语仅用于描述详细的方面,而不旨在进行限制。
提供本发明的以下描述作为本发明的最佳的、当前已知的方面的可行教导。相关领域的技术人员将认识到,对所描述的方面进行许多改变,同时仍然获得本发明的有益结果。同样清楚的是,通过选择本发明的一些特征而不利用其它特征来获得本发明的一些想要的益处。因此,本领域的技术人员将认识到,对本发明的许多修改和调整是可能的,并且在某些情况下甚至可以是想要的,并且是本发明的一部分。因此,提供以下描述是为了说明本发明的原理,而不是限制本发明的原理。
本文所用的单数形式“一”(“a”,“an”)和“所述”(“the”)包括复数指代,除非上下文另有明确规定。因此,例如,对一“系绳”的引用包括具有两个或更多个系绳的方面,除非上下文另外清楚地指示。
范围在本文中表示为从“约”一个特定值和/或到“约”另一个特定值。当表达这样的范围时,另一个方面包括从一个特定值和/或到另一个特定值。类似地,当通过使用先行词“约”将值表示为近似值时,应理解该特定值形成另一个方面。将进一步理解,每个范围的端点相对于另一个端点并且独立于另一个端点都是显著的。
如本文所使用的,术语“可选的”或“可选地”是指随后描述的事件或情况可以发生或可以不发生,并且该描述包括所述事件或情况发生的实例和不发生的实例。本文所用的“流体”是指自由流动的任何物质,包括液体、气体和等离子体。本文所用的“流体连通”是指允许物质在相关部件之间自由流动的任何连接或相对定位。本文所用的“远侧”是指应用方向,“近侧”是指装置使用者的方向。
本申请涉及微创地植入心脏中的医疗装置和系统、以及植入这些装置和系统的方法。更特别地,本申请涉及用于在血管内将逆行或顺行的锚固件22或49引入并锚固至室间隔20,并将瓣膜66(见图10A和图10B、图11A和图11B)植入在心脏中系于逆行或顺行的锚固件(retrograde or antegrade anchor)22或49以置换天然二尖瓣的装置、方法和系统。此外,系绳组件与锚固件22或49配合将瓣膜66或156连接到锚固件22或49。此外,瓣膜66包括用于连接到瓣膜本体68的顶缘67或底缘157,使得瓣膜经由顶缘67或底缘157顺应相应的心房底,以防止假体的瓣周反流。根据本文的公开内容,锚固件独立于系绳和经导管的瓣膜而被植入。
图2-5中所示的逆行的锚固组件44的部件包括具有锚固帽27的锚固件22和允许递送系绳36的递送线缆32。锚固帽27连接到左心室盘26,左心室盘26经由间隔连接件24连接到右心室盘23。递送线缆32可移除地连接到锚固帽27。如图所示,间隔连接件24被尺寸化和构造成横跨室间隔。然而,可选地,间隔连接件24可以具有不同的尺寸(根据室间隔的厚度更长或更短),并采用横截面为圆、椭圆、抛物线或双曲线的任何部分的圆柱形状,或者采用具有平的基部和顶部的多面体形状,所述基部和顶部具有三条或更多条边的多边形形状。间隔连接件可由任何已知的金属合金构成,包括但不限于不锈钢、镍钛诺、钛、钴铬或其它金属合金。在另一个方面,间隔连接件24的金属合金可涂覆有生物组织,例如牛、羊、猪或马的心包,或涂覆有可促进愈合和限制炎症的抗炎药物的任何组合。右心室盘和左心室盘可以由任何已知的金属合金构成,包括但不限于不锈钢、镍钛诺、钛、钴-铬或其它金属合金。另外,右心室盘和左心室盘可以采用圆、椭圆、抛物线或双曲线的任何部分的形状,或者采用具有三条或更多条边的多边形形状。右心室盘和左心室盘可覆盖有但不限于由聚碳酸酯、聚氨酯、聚酯、膨胀聚四氟乙烯(ePTFE)、聚对苯二甲酸乙二醇酯(PET)、硅酮、天然或合成橡胶或其组合组成的类别的合成材料。右心室盘和左心室盘也可以覆盖有成年或幼年的牛、羊、马或猪的心包。在另一方面,锚固件22具有沿其右心室盘和左心室盘定位的锚固元件(未示出)。这些锚固元件允许固定到室间隔,但不一定用于主要的固定机构。
使用中,通过相对室间隔20的右心室表面17移去右心室盘23的鞘管,然后暴露间隔连接件24,接着相对室间隔20的左心室表面16移去左心室盘26的鞘管,从而将逆行的锚固件22固定到室间隔上。通过重新给左心室盘26、然后间隔连接件24、最后右心室盘23装上鞘管,逆行的锚固件被安全地从心壁移除,或被重新定位,或被完全移除。
锚固帽27包括从锚固帽27径向向外延伸的至少一个锁定臂29。锁定臂29被尺寸化和构造成用于将系绳36的一部分(下面描述)可释放地固定到锚固帽27。所述至少一个锁定臂29在第一锁定位置和第二解锁位置之间运动,在所述第一锁定位置中,锁定构件29远离锚固帽27的本体延伸第一距离,在所述第二解锁位置中,锁定构件29远离锚固帽27延伸第二距离,所述第二距离小于所述第一距离。锚固帽27包括至少一个偏置构件(未示出),例如弹簧,其构造成将每个锁定臂29推动到第一锁定位置。如图所示,提供了多个锁定臂29,这些锁定臂绕着锚固帽27的圆周等距地间隔开,尽管可以设想锁定臂29不必等距地间隔开。
现在参照图3,递送线缆32包括柔性递送线33,柔性递送线33具有定位在递送线33的远端上或形成在递送线33的远端中的带螺纹的远端部分34。递送线由(但不限于)不锈钢、镍钛诺或其它金属合金构成,具有或不具有亲水涂层,或具有或不具有聚合物涂层,例如聚四氟乙烯(PTFE)。带螺纹的远端部分34被尺寸化和构造成选择性地接合形成在限定于锚固帽27的近端31中的腔中的互补螺纹,见图2和图5。使用中,带螺纹的远端部分34前进到(例如旋入)锚固帽27的近端31中,以将锚固帽27连接到柔线33的远端。如下文更全面地描述地,带螺纹的远端部分34从锚固件22的近端旋出,从而将柔线33从锚固件22分离。
根据本公开的另一方面,如图17A-17F所示,示出了锚固组件91。锚固件91包括锚固轴92和顺行的锚固件49,尽管逆行的锚固件22可以互换在该锚固组件91中。如图所示,顺行的锚固件49从锚固件基部94向远侧延伸。锚固件基部94限定至少一个或多个如图所示的锚固凸缘96和其间的凹陷区域97。锚固轴92包括图17B中所示的至少一个或如图所示的多个锁定构件98。锁定构件98例如通过弹簧(未示出)从锚固轴92径向向外偏置。锚固连接件99和连接件杆101与锚固轴92配合以连接到顺行的锚固件49。锚固连接件101限定至少一个或如图所示的多个孔1020,孔1020被配置为用于接收锚固凸缘96。因此,锚固连接件99和连接件杆101匹配地连接到锚固轴92,从而向内推动锁定构件98。孔100和凸缘96的配合使锚固连接件101和锚固件基部94成为一体。
在已植入顺行的锚固件49之后,施加系绳环102以越过连接件杆101和锚固连接件99,并邻接顺行的锚固件49的近端。系绳环102包括大致圆柱形的远侧的第一部分103和直径大于第一部分103的近侧的第二部分104。如图17E和图17F所示,第二部分104限定至少一个或如图所示的多个孔106,孔106构造成用于接收系绳杆108。如图17D所示,移除锚固连接件99和连接件杆101。锁定构件98被径向向外推动,以接合系绳环102的第二部分104,从而将系绳环102锁定在锚固件基部94上。系绳杆108如上文所述操作以与经导管的瓣膜66或156配合。
图6-9所示的顺行的锚固组件63的部件包括具有锚固帽58和递送线缆连接件51的锚固件49、以及允许递送系绳36的递送线缆46。锚固帽58连接到左心室盘57,左心室盘57经由间隔连接件56连接到右心室盘54。递送线缆46通过其螺纹端52可拆卸地连接到递送线缆连接件51。如图所示,间隔连接件56被尺寸化和构造成横跨室间隔。然而,可选地,间隔连接件56可以具有不同的尺寸(根据室间隔的厚度更长或更短),并采用横截面为圆、椭圆、抛物线或双曲线的任何部分的圆柱形状,或者采用具有平的基部和顶部的多面体形状,所述基部和顶部具有三条或更多条边的多边形形状。间隔连接件可由任何已知的金属合金构成,包括但不限于不锈钢、镍钛诺、钛、钴铬或其它金属合金。在另一方面,间隔连接件56的金属合金可涂覆有生物组织,例如牛、羊、猪或马的心包,或涂覆有可促进愈合和限制炎症的抗炎药物的任何组合。右心室盘和左心室盘可以由任何已知的金属合金构成,包括但不限于不锈钢、镍钛诺、钛、钴-铬或其它金属合金。另外,右心室盘和左心室盘可以采用圆、椭圆、抛物线或双曲线的任何部分的形状,或者采用具有三条或更多条边的多边形形状。右心室盘和左心室盘可覆盖有但不限于由聚碳酸酯、聚氨酯、聚酯、膨胀聚四氟乙烯(ePTFE)、聚对苯二甲酸乙二醇酯(PET)、硅酮、天然或合成橡胶或其组合组成的类别的合成材料。右心室盘和左心室盘也可以覆盖有成年或幼年的牛、羊、马或猪的心包。在另一方面,锚固件49具有沿着其右心室盘和左心室盘定位的锚固元件(未示出)。这些锚固元件允许固定到室间隔,但不一定用于主要的固定机构。
使用中,通过相对室间隔20的左心室表面16移去左心室盘57的鞘管,然后暴露间隔连接件56,接着相对室间隔20的右心室表面17移去右心室盘54的鞘管,从而将顺行的锚固件49固定到室间隔。通过重新给右心室盘54、然后间隔连接件56、最后左心室盘57装上鞘管,将顺行的锚固件安全地从心壁移除,以重新定位或完全移除。
锚固帽58包括从锚固帽58径向向外延伸的至少一个锁定臂61。锁定臂61被尺寸化和构造成用于将系绳36的一部分(下面描述)可释放地固定到锚固帽58。所述至少一个锁定臂61在第一锁定位置和第二解锁位置之间运动,在所述第一锁定位置中,锁定构件61远离锚固帽58的本体延伸第一距离,在所述第二解锁位置中,锁定构件61远离锚固帽58延伸第二距离,所述第二距离小于所述第一距离。锚固帽58包括至少一个偏置构件(未示出),例如弹簧,其构造成将每个锁定臂61推动到第一锁定位置。如图所示,提供了多个锁定臂61,这些锁定臂61围绕锚固帽58的圆周等距地间隔开,尽管可以设想锁定臂61不必等距地间隔开。
现在参照图6,递送线缆46包括柔性递送线47,柔性递送线47具有定位在递送线47的远端上或形成在递送线47的远端中的带螺纹的远端部分48。递送线缆46具有可容纳线轨的中心通道(未示出)。递送线由(但不限于)不锈钢、镍钛诺或其它金属合金构成,具有或不具有亲水涂层,或具有或不具有聚合物涂层,例如聚四氟乙烯(PTFE)。带螺纹的远端部分48被尺寸化和构造成选择性地接合形成在限定于递送线缆连接件51的近端52中限定的腔中的互补螺纹,见图7和图9。使用中,带螺纹的远端部分48前进到(例如旋入)递送线缆连接件51的近端52中,以将递送线缆连接件51连接到柔线47的远端。如下文更全面地描述地,带螺纹的远端部分48从递送线缆连接件51的近端旋出,从而将柔线47从锚固件49分离。
根据本公开的另一方面,如图17A-F所示,示出了环状锚固组件91。环状锚固组件91包括连接到锚固轴92的锚固件基部94(根据其它方面代替锚固帽58)并且融合到顺行的锚固件49的其余部分,尽管该环状锚固组件91可以包括连接到锚固轴92的锚固件基部94(代替如图2所示的锚固帽27),融合到逆行的锚固件22的其余部分。如图所示,顺行的锚固件49从锚固件基部94向远侧延伸。锚固件基部94限定至少一个或多个如图所示的锚固凸缘96和其间的凹陷区域97。锚固轴92包括如图17B中所示延伸的至少一个或如图所示的多个锁定构件98。锁定构件98例如通过弹簧(未示出)从锚固轴92径向向外偏置。锚固连接件99和连接件杆101在延伸穿过锚固轴92和螺纹端52(如图9所示)的线轨64上行进,其中连接到连接件杆101的锚固连接件99与锚固轴92配合。锚固连接件99限定至少一个或如图所示的多个孔100,孔100被配置为用于接收锚固凸缘96。因此,锚固连接件99和连接件杆101匹配地连接到锚固轴92,从而向内推动锁定构件98。配合的孔100和凸缘96使锚固连接件99和锚固件基部94成为一体。在通过锁定构件98固定系绳环102之后,移除锚固连接件99和连接件杆101,留下延伸穿过附接至锚固件基部94的锚固轴92的线轨64。对于融合到逆行的锚固件22的锚固组件91,锚固连接件99和连接件杆101在递送线缆32上行进,递送线缆32在移除锚固连接件99和连接件杆101之后保留。
图32A-C和图33示出了环状锚固组件的另一个方面。锚固组件91还包括柔性连接件170,其可以由诸如金属或金属合金的合适材料形成,在锚固件基部94和锚固轴92之间延伸。如图所示,柔性连接件170为螺旋构造,但也可设想其它构造。固定到锚固轴92的底部的是从锚固轴92径向向外延伸的至少一个或如图所示的三个锁定臂98。臂98例如由任何金属或金属合金形成。锁定臂98被径向向内推动,但被偏置到所示的位置。因此,当系绳环202定位成与锁定构件98接合时,锁定构件98与系绳环202配合,并且锚固组件91的柔性连接件使得系绳能够保持与要植入的瓣膜轴向对准(例如,平行于室间隔),特别是当锚固螺钉93被植入时。
为了植入锚固螺钉93,预加载在递送线缆232上的扭矩驱动器(未示出)与锚固件基部94配合,并允许螺钉旋转并由此驱动到组织中。一旦完全植入,扭矩驱动器被移除,留下连接到递送线缆232的锚固组件91。在递送线缆232上,经由系绳杆208(经由孔206附接到系绳环202)连接到系绳的系绳环202在锚固轴92上前进。系绳环202在锁定臂98上前进,从而向内按压锁定臂98。一旦系绳环202的近端已经在锁定臂98下方经过,锁定臂98向外弹出,从而将系绳环202限制在适当位置,防止系绳环202被附连到系绳杆208上的系绳无意中移动。最后,旋转递送线缆232,使得“阴”螺纹234从由锚固轴92的螺纹腔限定的螺纹分开。
这些图中所示的锚固组件91还包括稳定件172,以稳定锚固件并限制或防止从系绳传递的张力引起的运动,例如旋转运动,并提供牵引力以限制或防止螺旋锚固件93无意中旋转而与它所植入的组织脱开。可以提供至少一个稳定件172。如图32所示,示出了八个稳定件172,图33示出了三个。如图32所示,稳定件172从锚固件的纵向轴线径向向外延伸。稳定件172被配置为具有非线性构造。可以设想其他构造。图33所示的稳定件172还从锚固件纵向轴线径向向外延伸,并沿水平轴线以锐角(例如45度)延伸。该角度通常面向螺旋锚固件93的相反方向。稳定件通常是线性的,但也可设想其它构造。例如,当插入到室间隔中时,稳定件172将在与锚固螺钉植入相反的方向上推动并可能进入组织中,以防止锚固螺钉93意外退出。
在由顺行的锚固件49或逆行的锚固件22组成的环状锚固组件植入后,将系绳环102施加在连接件杆101和锚固连接件99上,并邻接融合到顺行的锚固件49或逆行的锚固件22的锚固件基部94。系绳环102包括大致圆柱形的远侧的第一部分和直径大于第一部分103的近侧的第二部分104。如图17E和图17F所示,第二部分104限定至少一个或如图所示的多个孔106,孔106被配置为用于接收系绳杆108。如图17D所示,移除锚固连接件99和连接件杆101。锁定构件98被径向向外推动,以接合系绳环102的第二部分104,从而将系绳环102锁定在锚固件基部94上。系绳杆108如上所述地操作以与经导管的心脏瓣膜66或156配合。
当柔线33连接到逆行的锚固件22时,柔线用作将系绳36推进到逆行的锚固件22的导轨。对于顺行的锚固件49,通过进入锚固帽58的远端62、经由螺纹端52离开递送线缆连接件51、穿过递送线缆46的中心通道,线轨64用作系绳36到顺行的锚固件49的导轨。系绳36包括可旋转地连接到对接环43的一个或多个系绳杆38。系绳杆38连接到由对接环臂42限定的孔眼41,如图4所示。系绳36在递送线缆33的柔线32上前进(在逆行的锚固件的情况下)或者在线轨64上前进(在顺行的锚固件的情况下),并且系绳36的对接环43将锚固帽27或58的至少一个锁定臂29或61压到第二解锁位置。当锁定臂29或61处于第二位置时,系绳36分别在锚固帽27或58上的锁定臂29或61上前进,直到对接环43邻接和/或邻近锚固帽27的远端28或锚固帽58的远端59。此时,锚固帽27或58的偏置构件将至少一个锁定臂29或61推动到第一锁定位置,从而将对接环43可释放地连接到逆行的锚固件22或顺行的锚固件49,因此也将系绳36的其余部分可释放地连接到逆行的锚固件22或顺行的锚固件49。
在一个方面,当连接到逆行的锚固件22或顺行的锚固件49时,系绳36绕锚固件的纵向轴线旋转一个完整的360度。可选地,在另一方面,通过系绳36的一部分与至少一个锁定臂29或61的相互作用,系绳36可被约束到较小的旋转角度。
如图4所示,在一个方面,系绳36包括连接到对接环43的至少一个对接环臂42、以及连接到对接环臂42的至少一个系绳杆38。如图所示,对接环臂42的远端牢固地连接到对接环43或与对接环43一体地形成。如图所示,至少一个对接环臂包括多个对接环臂42。如图所示,多个对接环臂42围绕对接环的圆周等距地间隔开,尽管可以设想对接环臂42不必等距地间隔开。孔眼41由对接环臂42限定。系绳杆38包括被配置用于与孔眼41配合的系绳杆钩39。
每个对接环臂42的近端可旋转地连接到相应的系绳杆38的远端如图所示,。系绳杆钩39由系绳杆38限定,并且连接到每个系绳杆38的远端或者与每个系绳杆38的远端一体地形成。在另一方面,孔眼41和系绳杆钩39被尺寸化和构造为使得系绳杆钩39插入孔眼41中,以将系绳杆38牢固地、可旋转地连接到对接环43。使用中,每个系绳杆钩39绕孔眼41的圆周旋转。如图4所示,每个系绳杆的近端连接到绳索37。系绳杆38和系绳杆钩39可以由任何金属合金构成。
现在参考图18A和18B,线轨递送系统由经房间隔引导件118和经室间隔引导件111组成。经房间隔引导件118经由经股鞘管117插入到股静脉中,并且引导件118具有近端毂119,经间隔穿刺针121通过近端毂119被引入,并且该针121通过引导件的远端扩张器122离开经间隔引导件121。经室间隔引导件111经由经颈鞘管109被插入颈静脉,并经由导线116被引导至右心室18。经室间隔引导件111具有可偏转远侧末端114,该可偏转远侧末端114由附接到引导件的近侧手柄112的偏转旋钮113控制,并且该远端可朝向室间隔20的右心室表面17偏转。
现在参考图21A和图21B,逆行的锚固件递送鞘管131越过线轨64进入经房间隔引导件118的近端毂119,并离开经间隔引导件的远端120。扩张器133穿过逆行的锚固件递送鞘管131的远端132,所述扩张器133越过线轨64并进入室间隔20的左心室表面16,直到其离开室间隔20的右心室表面17。一旦穿过,移除扩张器133,将逆行的锚固件递送鞘管的远端132留在右心室18中,以允许逆行的锚固件22的递送。
现在参考图24A和24B,顺行的锚固件递送鞘管134越过线轨64进入经室间隔引导件111的近端手柄112,并离开经间隔引导件的远端114。扩张器137穿过顺行的锚固件递送鞘管134的远端136,所述扩张器137越过线轨64并进入室间隔20的右心室表面17,直到其离开室间隔20的左心室表面16。一旦穿过,移除扩张器137,将顺行的锚固件递送鞘管的远端136留在左心室14中,以允许顺行的锚固件49的递送。
如图所示,在图18A中,鞘管109被配置为接收经室间隔引导件111,并且鞘管117被配置为接收经房间隔引导件118。鞘管109与经室间隔引导件111流体连通,并且鞘管117与经房间隔引导件118流体连通,使得诸如肝素化盐水等流体通过鞘管109围绕经室间隔引导件111并且通过鞘管117围绕经室间隔引导件118。
如18A中所示,J线116经由鞘管109引入并且由使用者血管内引导到右心室18中。在J线116上,将经室间隔引导件111推进到鞘管109中,并由使用者在血管内引导到右心室18中。一旦在右心室18中,J线116被移除,并且引导末端114由经室间隔引导件111的近侧手柄112的偏转旋钮113偏转,直到引导末端114邻近室间隔20的右心室表面17。
如18A所示,J线(未示出)经由鞘管117引入并且由使用者血管内引导进入右心房19。在该J线上,经房间隔引导件118由使用者进行血管内引导,直到其处于右心房19中,其中扩张器122延伸出引导件的远侧末端120。然后,J线被移除,并且经间隔穿刺针121被推进通过经房间隔引导件118的近端毂119,直到穿刺针接近扩张器122的端部。接下来,撤回并旋转经房间隔引导件118的近端毂119,直到延伸出远侧末端120的扩张器122推抵房间隔21。使用荧光镜和超声心动描记引导,经间隔穿刺针121前进穿过房间隔21进入左心房11,随后推进扩张器122和经房间隔引导件118的远侧末端120。一旦远侧末端120位于左心房11中,扩张器122和经间隔穿刺针121都从经房间隔引导件118的近侧毂119撤回。
如图18B所示,圈套器鞘管123被引入到经房间隔引导件118的近端毂119中,直到圈套器鞘管123离开引导件118的远侧末端120,从左心房11前进到左心室14中。圈套器124经由圈套器鞘管123前进到左心室14中,直到圈套器124邻近室间隔20的左心室表面16。
如图19A所示,连接到射频发生器126或电烙器系统(未示出)的射频线127经由经室间隔引导件111的近端手柄112前进,直到线127离开经室间隔引导件111的远端114,并穿过室间隔20进入左心室14,随后由圈套器124捕获线127。如图19B所示,圈套器124将线127拉入经房间隔引导件118中,直到线离开引导件118的近端毂119。接下来,在线127的从经室间隔引导件111的近端手柄112延伸的部分上,微导管128在线127上前进穿过室间隔120。图19C示出了微导管128的放大视图,其中远端扩张器129在线127上前进穿过室间隔20。
如图20A所示,微导管128在线127上前进,直到其进入经房间隔引导件118的远侧末端120。一旦微导管128在经房间隔引导件118内几厘米或更多厘米,则通过拉出经房间隔引导件118的近端毂119来移除线127。如图20B所示,更大和更硬的J线64经由微导管128前进通过经室间隔引导件111,直到J线64离开微导管128(定位在经房间隔引导件118内部),并最终离开引导件118的近端毂119。
如在[0018]中所述以及在图21A和图21B中所示,一旦逆行的锚固件鞘管131被定位在右心室18中邻近右心室表面17,则逆行的锚固件22通过逆行的锚固件鞘管131邻近线材64并且定位在远侧末端132处。
如图22A所示,逆行的锚固件鞘管131的远侧末端132首先缩回,直到其位于左心室14中邻近左心室表面16。当远侧末端132缩回时,逆行的锚固件22的自膨胀右心室盘23展开,邻接室间隔20的右心室表面17,并且间隔连接件24暴露在室间隔20中。如图22B所示,随着远侧末端132进一步缩回,自膨胀左心室盘26展开,邻接室间隔20的左心室表面16。接下来,从经房间隔引导件118的近端毂119移除逆行的锚固件鞘管131,并且通过从经室间隔引导件111的近端手柄112拉动J线64来移除J线64。
如图23所示,经房间隔导引件118已经通过经股鞘管117被拉出体外,将逆行的锚固件22留在适当位置,并且仍然连接到递送线缆32的柔线33。
如在[0019]中所述以及在图24A和24B中所示,一旦顺行的锚固件鞘管134被定位在左心室14中邻近左心室表面16,则顺行的锚固件49在线64上前进通过顺行的锚固件鞘管134并且定位在远侧末端136处。
如图25A所示,首先将远侧末端136缩回,直到其位于右心室18中邻近右心室表面17。当远侧末端136缩回时,顺行的锚固件49的自膨胀左心室盘57展开,邻接室间隔20的左心室表面16,并且间隔连接件56暴露在室间隔20中。如图25B所示,随着远侧末端136进一步缩回,自膨胀右心室盘54展开,邻接室间隔20的右心室表面17。接下来,从经室间隔引导件111的近侧手柄112移除顺行的锚固件鞘管134。
如图26A-B所示,将递送线缆46旋松,使得其远侧螺纹端48与递送连接件51分离,从而允许移除递送线缆46的柔线47。如图26C所示,经房间隔引导件118已经通过经股鞘管117被拉出体外,将顺行的锚固件49留在适当位置,其中线64穿过它。
如图10A、10B、11A、11B所示,系统10包括经导管的心脏瓣膜66,该经导管的心脏瓣膜66具有沿经导管的心脏瓣膜66的上端周向延伸的心房密封裙顶缘67。经导管的心脏瓣膜66包括经导管的瓣膜本体68(图示为大致圆柱形)和心房密封裙顶缘67,心房密封裙顶缘67构造成顺应左心房底12,如图所示。如本文所述,经导管的心脏瓣膜66通过系绳36连接到逆行的锚固件22或顺行的锚固件49。当锚固件22或49固定到室间隔20时,融合或以其他方式连接到系绳36的系绳杆38的绳索37将经导管的心脏瓣膜66连接到锚固件22或49。
如图1所示,经导管的心脏瓣膜66被尺寸化和结构成位于左心房11和左心室14之间的二尖瓣中。经导管的心脏瓣膜66与瓣膜小叶77预组装(图11A、11B)。这是示例性的。因此,然后,通过略微变化,这些装置、系统和方法可通过静脉结构在血管内放置,所述静脉结构包括但不限于颈内静脉、锁骨下静脉、锁骨下静脉或股静脉。
经导管的心脏瓣膜66是自膨胀的(即,瓣膜是可压缩的,使得它适合通过系统1的导管),并且由镍钛诺组成,但是也可以包含由(但不限于)不锈钢、镍钛诺或其它金属合金制成的元件。在另一方面,经导管的心脏瓣膜具有小于或近似等于二尖瓣环的展开部位13处的环的较小直径,从而减少对二尖瓣环的约束。
如图31A和图31B所示,经导管的心脏瓣膜66的替代实施例是经导管的心脏瓣膜156。与具有心房密封裙顶缘67的经导管的心脏瓣膜66相比,经导管的心脏瓣膜156具有心房密封裙底缘157,该心房密封裙底缘157连接到经导管的瓣膜本体68的底部,而不是如经导管的心脏瓣膜66中的顶部。心房密封裙底缘157顺应心房底12,并且经导管的心脏瓣膜157的经导管的瓣膜本体68延伸到左心房11中,由此最小化与天然二尖瓣小叶的相互作用,进一步降低LVOT阻塞的风险。
如图10A和图10B、图11A和图11B以及图31A和图31B所示,在经导管的心脏瓣膜66或156中限定至少一个导管74。每个导管被尺寸化和形状化成使得绳索37的一部分(在近端处附接到缝线148)延伸通过导管74,从而将系绳36连接到经导管的心脏瓣膜66或156,允许自由运动,直到瓣膜66或156被锁定就位。在另一方面,经导管的瓣膜66或156具有沿其外径定位的锚固元件(未示出)。这些锚固元件允许固定到二尖瓣环和/或小叶上,但不必用作主要的固定机构。
至少一根绳索37连接到系绳36的系绳杆38,并且绳索37的近侧部分连接到缝线148。在一个方面,绳索可以是坚固但柔性的绳索,例如但不限于,膨胀聚四氟乙烯(ePTFE)或超高分子量聚乙烯(UHMWPE,UHMW)绳索。在下面更全面地描述地,在使用中,绳索37的中心部分(在远端和近端之间)延伸通过和/或连接到经导管的瓣膜66或156,以将裙相对于二尖瓣环保持在想要的位置。
图11A和图11B还示出了经导管的瓣膜66。经导管的瓣膜66具有从经导管的瓣膜本体68径向向内延伸的小叶77。小叶77由牛、马或猪的心包小叶组成。类似于任何常规瓣膜的功能,缝合到经导管的瓣膜本体68的内部的小叶77在心脏舒张期间(心脏舒张)打开,允许血液从左心房11进入左心室14,并且在心脏收缩期间(心脏收缩)关闭,防止血液从右心室或左心室分别回流到右心房或左心房。
如图10A和图10B、图11A和图11B以及图31A和图31B所示,由经导管的瓣膜本体68和心房密封裙顶缘67或心房密封裙底缘157限定的经导管的心脏瓣膜66或156包括膜状材料,并且心房密封裙顶缘67或心房密封裙底缘157的直径大于展开部位处的环。例如,心房密封裙顶缘67或心房密封裙底缘157可具有大于二尖瓣环的直径的直径。在另一个方面,经导管的心脏瓣膜由但不限于由聚碳酸酯、聚氨酯、聚酯、膨胀聚四氟乙烯(ePTFE)、聚对苯二甲酸乙二醇酯(PET)、硅酮、天然或合成橡胶或其组合组成的类别的合成材料形成。经导管的心脏瓣膜66或156也可以覆盖有成年或幼年的牛、羊、马或猪的心包。可选地,心房密封裙顶缘67或心房密封裙底缘157的至少一部分可由替代材料形成,例如但不限于聚氨酯泡沫或其它聚合物。
在另一方面,经导管的心脏瓣膜66或156的至少一部分沿其长度具有一个或多个固定构件(未示出),从而允许进一步固定到左心房底和/或二尖瓣环的心房侧上的其它部分,防止经导管的心脏瓣膜66或156迁移到近侧的左心房11中,从而防止假体不稳定(例如摇摆)和瓣周反流。
经导管的心脏瓣膜66或156至少包括经导管的瓣膜本体68和心房密封裙顶缘67或心房密封裙底缘157。如图所示,经导管的瓣膜本体68是圆柱体并且具有可变长度和直径。其选择性地由激光切割或模制的镍钛诺组成,但也可包含任何其它金属合金的元件,且可沿其圆周或长度的任何部分覆盖上述生物膜或合成材料。如图所示,顶缘67或底缘157从经导管的瓣膜本体68径向向外并向下延伸,形成基本上凹入的顶缘,其中凹部面向左心房底11。在经导管的心脏瓣膜66的情况下,顶缘67或底缘157围绕经导管的瓣膜本体68的上端周向地延伸,或者在经导管的心脏瓣膜156的情况下,顶缘67或底缘157围绕经导管的瓣膜本体68的下端周向地延伸。
提供至少一个或示出的多个柔性延伸构件69,并且该延伸构件69可以例如但不限于由激光切割或模制的镍钛诺构成,该延伸构件69通过延伸构件基部71附接至裙本体的顶部并且终止于延伸构件末端72。在一个或多个延伸构件69之间是垂直于相邻延伸构件69延伸的弹性密封膜73。如图10A和图10B所示,延伸构件69可径向向外且基本线性地延伸,但这是示例性的。如图11A、11B、31A和图31B所示,延伸构件可以是非线性的并且大致是U形的。如图所示,密封膜73围绕顶缘67或底缘157周向地延伸。它也可以仅延伸圆周的一部分。经导管的瓣膜本体68包括多个支撑件78,支撑件78类似于顶缘67或底缘157的延伸构件69,例如可由激光切割或模制的镍钛诺组成,但不限于此。如图所示,支撑件78形成网格状构造,但也可设想其它构造,包括但不限于垂直延伸的支撑件。
密封构件73由如上所述的生物组织或合成织物构成。在一个方面,合成织物是编织的或针织的,允许顺应心房底构形所需的“拉伸性”。在图10A和图10B、图31A和图31B中,延伸构件69经由延伸构件基部71附接到经导管的瓣膜本体68,并且延伸构件末端72向下弯曲,由此防止围绕二尖瓣环的反流。这种构造需要通过一个或多个心房定位杆147施加向下的力,所述一个或多个心房定位杆147附接到一个或多个导管74,并且通过一个或多个可拆卸的锁定件83(图14A-B、15A-B、16A-B)锁定到位,所述可拆卸的锁定件83集成在如本文所述的导管74的心房端部内。
图30A-30D示出了作为天然二尖瓣替换物的瓣膜的放置。图30A和图30B示出了具有心房密封裙顶缘67的瓣膜,图30C和图30D示出了具有心房密封裙底缘157的瓣膜。具有底部密封裙157的二尖瓣定位在这些图中所示的心房底12上方。将该瓣膜与上述系绳一起使用防止瓣膜的实质性的竖直或浮动运动。
根据上述方法,逆行的锚固件22或顺行的锚固件49由逆行的锚固件递送鞘管131或顺行的锚固件递送鞘管134引入并固定至室间隔20。锚固帽27或58以及递送线缆33(用于逆行的锚固件)或线轨64(用于顺行的锚固件)保持在心脏内并且准备接收上述系绳36。
现在参考图27A和图27B,并且如上所述,系绳36在递送线缆32的递送线33(未示出)或线轨64上前进通过以递送引导件141的形式示出的经导管的心脏瓣膜递送系统。通过将对接环43连接到锚固帽27或58,系绳36锁定到锚固帽27或58上。从系绳杆38延伸的至少一根绳索37连接到至少一个系绳杆38。至少一根绳索37在近侧连接到至少一根缝线148,缝线148经由递送引导件141的中心管腔151延伸到体外。一旦系绳被锁定到锚固帽27或58,引导件141如图27B所示缩回,留下植入的锚固件22或49、系绳36、绳索37和从植入部位延伸的缝线。如图27A-B、28A-B所示,同一引导件141递送系绳36和经导管的心脏瓣膜66或156两者。
现在参考图27A-B和图28A-B,示出了用于在想要的展开部位13处定位和展开经导管的心脏瓣膜66或156的经导管的心脏瓣膜递送系统139。经导管的瓣膜递送系统139包括经导管的瓣膜递送引导件141、鼻锥体146、经导管的瓣膜展开旋钮142和至少一个心房定位杆147。经导管的瓣膜递送引导件141具有远端144、相对的近端的瓣膜展开旋钮142和在其间延伸的内部引导管腔143。内部引导管腔143被尺寸化和构造成使得经导管的瓣膜66或156和其它系统部件选择性地且可移除地插入其中。经导管的瓣膜递送引导件141的至少一部分是柔性的,使得经导管的瓣膜递送引导件141的远端处的末端144定位成经过展开部位13并进入左心室14中。
经导管的瓣膜展开旋钮142连接到经导管的瓣膜递送引导件141的近端。经导管的瓣膜展开旋钮142限定与内部引导管腔143流体连通的中心通道151。因此,心房定位杆147、导线64和/或至少一个缝线148可延伸穿过中心通道151并进入内部引导管腔143。如图所示,经导管的展开旋钮142是可旋转的并且被构造成使得旋钮142在第一方向上的旋转导致经导管的瓣膜递送引导件141的围绕经导管的瓣膜66或156的远侧末端144缩回,从而允许经导管的瓣膜66或156扩张。鼻锥体146可以是任何常规鼻锥体,其连接到经导管的瓣膜递送引导件141并构造成将经导管的瓣膜66或156引导到展开部位13。
参照图27A-B、28B-C和图29A,至少一个心房定位杆147具有远端153、近端150和在它们之间延伸的内部杆管腔149,内部杆管腔被尺寸化和构造成使得缝线148和/或绳索37的一部分插入其中。心房定位杆147的至少一部分是柔性的,使得心房定位杆的远端153可定位在展开部位13处或邻近展开部位13。
至少一个定位杆147连接到导管74。如图13A和图13B所示,每个导管74包含可拆卸的锁定件83,锁定件83被配置为牢固地附接至少一根绳索37。因此,绳索37牢固地附连至系绳36的系绳杆38,系绳36连接至锚固帽27或58,锚固帽27或58通过逆行的锚固件22或顺行的锚固件49的心室盘和间隔连接件固定至室间隔20,并且可拆卸的锁定件83将绳索37牢固地附连在例如左心房中。
参考图13A、13B、14A、14B、15A、15B、16A和图16B,锁定系统82包括可拆卸的锁定件83,锁定件83集成在导管74内,导管74附接至第一通道海波管(gateway hypotube)84和第二收回的海波管(retracting hypotube)86。在可拆卸的锁定件83内是一个锁定夹87。现在参照图30A,系统10还包括缝线切割器154,缝线切割器154被尺寸化和配置成穿过递送鞘管117以切割至少一条缝线148(如图30B所示)。
使用中,系统10通过放置室间锚固件22或49并使系绳36与锚固件22或49对接,利用经导管方法来植入经导管的心脏瓣膜66或156。如图27A所示,将经导管的瓣膜系统139插入线64或递送线缆32的柔线33上并插入心脏9的一部分。随着经导管的瓣膜递送引导件141(经导管的瓣膜66或156预加载到远端144中)被插入到心脏中,缝线148的至少一部分也被预加载并穿过至少一个导管74,并且随着经导管的瓣膜递送引导件141前进,缝线148和绳索37的至少一部分沿经导管的瓣膜递送引导件141的内部引导管腔143延伸并在近侧超出该内部引导管腔143。因此,至少一根绳索37的一部分延伸通过并超过经导管的瓣膜递送引导件141的远端144,并且至少一根缝线148的一部分延伸通过并超过经导管的瓣膜递送引导件141。在经导管的瓣膜66或156预载到远端144中的情况下,经导管的瓣膜递送引导件141定位成使得经导管的瓣膜递送引导件141的远端144通过展开部位13并进入左心室14中。
将经导管的瓣膜66或156预加载到经导管的瓣膜递送引导件141的远端144中,用于定位在展开部位13处。如图所示,缝线148与经导管的瓣膜66或156预组装,使得每个缝线148穿过经导管的瓣膜66或156的至少一个导管74,如图11A-B和图31A-B所示。当经导管的瓣膜66或156和经导管的瓣膜递送引导件141的远端144作为一个单元前进并接近展开部位时,缝线148的端部和绳索37的一部分将穿过限定在经导管的瓣膜66或156中的导管74。这样,经导管的瓣膜66或156可沿着至少一根绳的长度移动,直到到达想要的展开部位13。也就是说,经导管的瓣膜在绳索37上自由浮动,直到由可拆卸的锁定件83锁定就位。
当经导管的瓣膜66或156处于想要的展开部位13时,利用经导管的瓣膜展开旋钮142来至少部分地撤回围绕经导管的瓣膜66或156的递送引导件141。在引导件141不限制经导管的瓣膜66或156的情况下,瓣膜66或156膨胀到其完全的、不受限制的尺寸。可选地,因为经导管的瓣膜的位置是可调节的,所以可使用经导管的瓣膜展开旋钮142来折叠经导管的瓣膜66或156,从而允许重新定位到想要的展开部位。
预加载在经导管的递送引导件141中的心房定位杆147然后在每个缝线148上前进,使得每个缝线的一部分在内部杆管腔149内延伸,并且每个缝线的一部分延伸超过定位杆147的近端150。参照图28B和图29A,定位杆147然后前进通过经导管的瓣膜引导件141,并且绳索37的一部分由杆147的内部杆管腔149接收,并且定位杆的远端153(可拆卸的锁定件83附接到其上)邻近于经导管的瓣膜66或156。定位杆147由使用者向下推动,直到密封裙相对于二尖瓣环处于想要的位置。
经导管的瓣膜66或156在系绳36上,直到达到想要的瓣膜66或156位置。在实现想要的瓣膜位置之后,至少一个心房定位杆147将经导管的瓣膜66或156推动到适当位置,并且经由可拆卸的锁定件83(位于每个导管74内并连接到每个定位杆147的端部)锁定到适当位置。可重新定位或收回经导管的瓣膜66或156,直到延伸通过每个心房定位杆147的缝线148释放为止。
如图28B所示,示出了经导管的瓣膜66或156在左心房11内的定位,使得经导管的瓣膜66顶缘67或经导管的瓣膜156底缘157顺应左心房底12的构形。经由经导管的瓣膜递送系统端144,医师推进一个或多个心房定位杆147,使得经导管的瓣膜66或156在一个或多个绳索37上平移,所述一个或多个绳索延伸通过由经导管的瓣膜本体68限定的一个或多个导管74。如图28B所示,一旦经导管的顶缘67或底缘157接触心房底12,则一个或多个延伸构件69根据局部解剖结构不同地挠曲。因为每个心房定位杆147以不同的力被推动,所以精确的张紧量是可以实现的,并且因此延伸构件69或多或少地弯曲,以促进经导管的瓣膜顶缘67或底缘157顺应围绕心房底12的整个周边,从而限制通过二尖瓣口的反流。
图12示出了经导管的瓣膜顶缘67从凹形到凸形的转换(对于底缘157可以发生相同的顺应变化)。当通过附接至延伸构件69的延伸构件基部71的心房定位杆147将瓣膜向下推至心房底12时,延伸构件末端72向上弯曲,顺应凸形的心房底解剖结构。经导管的瓣膜66(在图12中从左到右示出)或经导管的瓣膜156(未示出)的进一步向远侧的运动进一步改变顶缘67或底缘157的形状,因为顶缘67或底缘157被心房定位杆147向下推动(图28B)。
现在参照图15A和图15B,拉动收回的海波管86导致锁定夹87收回,锁定夹87向下推动锁定舌片88,并与绳索37接合。更具体地,第二海波管86被收回,并且由于其连接到锁定夹87,第二海波管86也收回锁定夹87。在收回时,锁定夹87接触第一通道海波管84的接触点89,从而断开锁定夹87,允许移除第二海波管86。一旦收回的海波管86被拉动,通道海波管84的内臂向内弹开,允许通道海波管被移除。第一通道海波管84是有益的,因为它能够在第二海波管86收回时锁定绳索37。然后移除通道海波管84,将锁定夹87留在经导管的瓣膜66或156的导管74内。图16A示出了完全接合的锁定件的剖视图。根据一个方面,定位杆147可与通道海波管集成或可移除地连接到通道海波管。图16B示出了完全接合的锁定件的完整视图。
如图30A所示,在经导管的瓣膜牢固地顺应至心房底12的情况下,缝线切割器154在缝线148上前进并到达经导管的瓣膜顶缘67。缝线切割器154在可拆卸的锁定件83上方切割并释放每个缝线148的远端。然后将缝线148和缝线切割器154从心脏9移除。
在一个方面,在切割缝线148之前,可取回或重新定位经导管的瓣膜66或156。例如,如果确定要移除或重新定位经导管的瓣膜,则将心房定位杆147定位在每个缝线上,使得缝线的一部分在内部杆管腔149中。当定位杆的远端153邻近于可拆卸的锁定件83或与可拆卸的锁定件83接触时,使通道海波管84前进并且收回的海波管86将可拆卸的锁定件连接到定位杆的远端,从而将锁定件从绳索37解锁。随着每个绳索的解锁,瓣膜可从展开部位13移除和/或重新定位在展开部位13中。
在另一个方面,经导管的瓣膜66或156在瓣膜展开后数天至数周重新定位和/或移除。在这方面,不切割缝线,而是绕线轴或其它缠绕装置缠绕。然后将该装置附接至瓣膜66的经导管的瓣膜顶缘67,或附接至瓣膜156的经导管的瓣膜本体68。在瓣膜展开和手术完成几天后,可以重新捕获线轴/缠绕装置,从而允许展开和收回缝线。然后将心房定位杆147定位在每个缝线上,使得缝线的一部分在内部杆管腔149中。当定位杆的远端153邻近于可拆卸的锁定件83或与可拆卸的锁定件83接触时,使通道海波管84前进并且收回的海波管86将可拆卸的锁定件连接到定位杆的远端,从而将锁定件从绳索37解锁。随着每个绳索的解锁,瓣膜从展开部位13移除和/或重新定位在展开部位13中。
尽管在以上说明书中公开了本发明的几个方面,但是本领域技术人员可以理解,受益于前述说明书和相关附图中呈现的教示,许多修改和其他方面都包括在本发明中。因此应当理解,本发明不限于以上公开的特定方面,并且许多修改和其他方面旨在被包括在所附权利要求的范围内。此外,尽管本文以及随后的权利要求书中采用了特定术语,但是它们仅以一般性和描述性意义使用,而不是为了限制所描述的发明。
- 用于二尖瓣的经导管锚固组件、二尖瓣和相关方法
- 用于在双孔二尖瓣中经导管二尖瓣置换的装置
