微生物标志物在脑梗死诊断和治疗效果评价中的应用
文献发布时间:2023-06-19 09:36:59
技术领域
本申请属于生物医学领域,涉及微生物标志物在脑梗死诊断和治疗效果评价中的应用。
背景技术
脑梗死又称缺血性卒中,是脑血管疾病中发生率最高的疾病之一,资料调查显示,脑梗死的发生率、致残率以及病死率都非常高,对患者的生活质量造成严重影响。脑梗死是由脑血液供应障碍引起的一种脑血管疾病,以腔隙性梗阻最为常见。脑梗死的最主要特征是发病急、发作前多伴有高血压病史或情志刺激,头晕,走路不稳,四肢乏力,在脑梗死发作时经常发生严重的意识障碍、感觉和运动功能障碍,神经退行性疾病,甚至碎死(Sober,S.,M.Laan,T.Annilo,MicroRNAs miR-124and miR-135a are potential regulators of themineralocorticoid receptor gene(NR3C2)expression.Biochem Biophys Res Commun,2010.391(1):727-32.),发生中等面积梗死时,常表现为突发、位置固定的剧烈跳痛,多伴有频繁的呕吐恶心感,有些还会伴发失语症。据报道,由于脑梗死的高发病率和死亡率,已成为全世界范围内导致残疾和死亡的主要原因(Liu,J.,Y.Zhu,et al.Association ofcarotid atherosclerosis andrecurrent cerebral infarction in the Chinesepopulation:a meta-analysis.Neuropsychiatr DisTreat,2017.13:527-533.)。据2015年世界卫生组织统计,世界范围内平均每225s就有一个人因为脑梗死死亡,就是在医疗相对最先进的美国,脑梗死死亡人数也约占各类死亡总数的5.6%,脑梗死不仅严重影响患者的生活质量,而且给社会和家庭带来巨大的负担和压力。遗传因素和不良生活习惯是发生脑梗死的两个主要原因。另外脑梗死的复发率极高,且短时间内复发的危险性更大更难治疗。
他汀类药物(3-羟基-3-甲基戊二酞辅酶A还原酶抑制剂)最初作为调脂类药物被纳入缺血性脑卒中的二级预防用药,广泛应用于临床,但随着研究的深入发现其在缺血性脑卒中治疗中的作用不止于此。
肠道微生物群是一个复杂的社区,有助于维持动态代谢生态平衡。肠道微生物组宿主超过100种细菌种类,编码150倍于人类基因组的基因[2276,277]。最新研究表明,肠道微生物群的变化可能影响大脑的生理,行为和认知功能。肠道微生物群可以影响神经回路和与应激反应相关的行为。肠道微生物群不仅通过神经系统(肠-脑的神经解剖学途径)而且通过内分泌系统,免疫系统和代谢系统对大脑产生影响。研究肠道菌群、他汀类药物和脑梗死之间的相关性,为脑梗死预防用药的策略提供新的思路和实验依据。
发明内容
本发明的目的在于提供一种用于脑梗死诊断和治疗效果评价的微生物标志物,所述微生物标志物来源于粪便,通过检测粪便中的微生物标志物来进行脑梗死诊断和治疗效果的评价无创、快速、灵敏。
为了实现上述目的,本发明采用了如下技术方案:
本发明的第一方面提供了一种与他汀类药物治疗相关的微生物标志物,所述微生物标志物为Vampirovibrio。
进一步,所述他汀类药物为阿托伐他汀。
本发明的第二方面提供了本发明第一方面所述的微生物标志物在制备脑梗死诊断或治疗效果评价产品中的应用。
进一步,所述产品包括检测所述微生物标志物丰度的试剂。
进一步,所述试剂包括定量样品中微生物标志物的靶核酸的试剂,和/或定量样品中微生物标志物的靶蛋白的试剂。
进一步,所述定量样品中微生物标志物的核酸的试剂包括特异性性扩增所述靶核酸的引物,或特异性识别所述靶核酸的探针;所述定量样品中微生物标志物的靶蛋白的试剂包括特异性结合靶蛋白的抗体。
进一步,所述样品来源于粪便。
本发明的第三方面提供了一种用于脑梗死诊断或治疗效果评价的产品,所述产品包括检测本发明第一方面所述的微生物标志物的丰度的试剂。
进一步,检测微生物标志物的丰度的方法包括宏基因组测序、16S测序、qPCR定量、免疫检测中的任意一种或多种。
本发明的第四方面提供了本发明第一方面所述的微生物标志物在制备治疗或预防脑梗死的药物中的应用。
进一步,所述药物包括所述微生物标志物的抑制剂。
进一步,所述抑制剂降低所述微生物标志物的丰度。
本发明的优点和有益效果:
本发明通过比较脑梗死以及用药后的样本中的肠道菌群的丰度,首次发现了肠道菌属Vampirovibrio与他汀类药物治疗脑梗死相关,为辅助诊断他汀类药物的治疗效果以及治疗脑梗死提供了一种手段。
附图说明
图1是Vampirovibrio在不同样本中的丰度图;
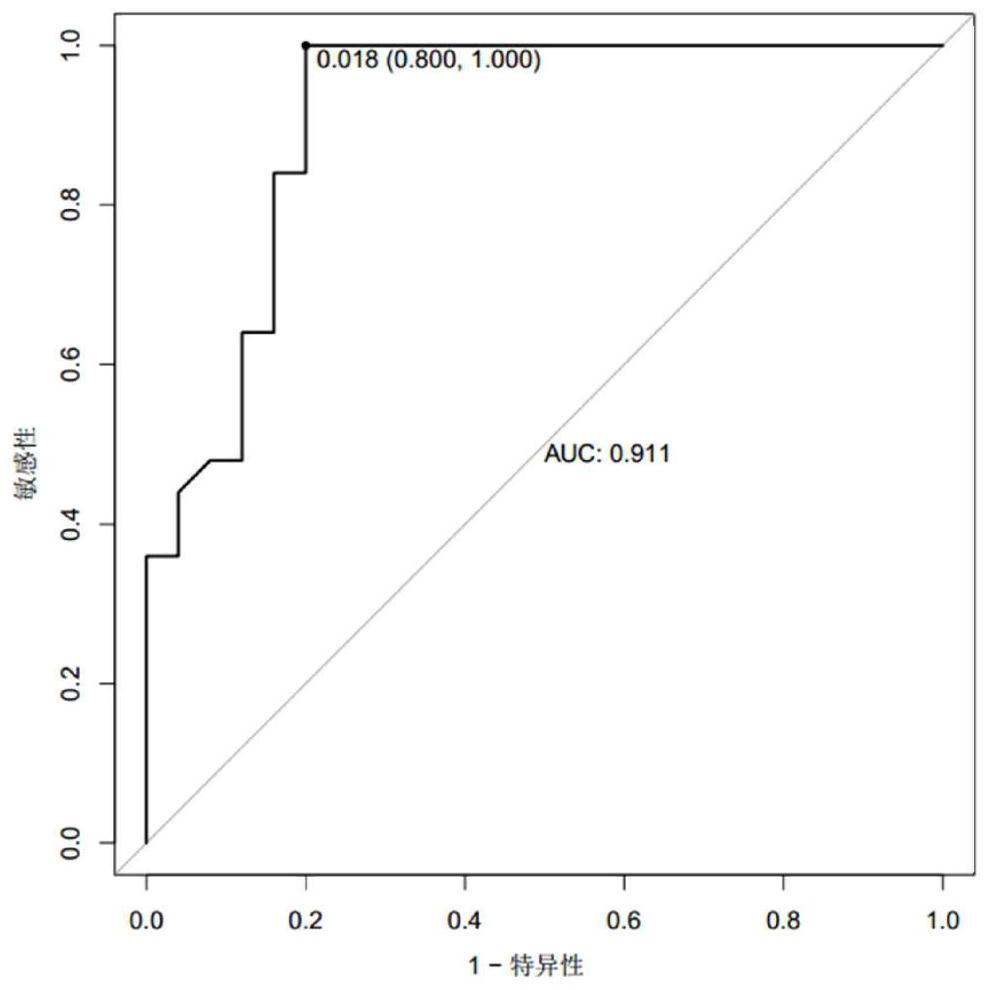
图2是Vampirovibrio作为检测变量的ROC曲线图;
图3是FMT移植实验结果图;其中图A是mNSS评分图;图B是跑轮实验图;图C是粘附物移除实验中接触时间检测图;图D是粘附物移除实验中接触时间检测图。
具体实施方式
本发明通过对脑梗死组与他汀治疗组的样本进行微生物测序,发现与脑梗死他汀类药物治疗相关的肠道菌群,同时通过粪便移植技术证实了肠道菌群可以改善神经行为学,降低脑梗死体积,从而起到治疗脑梗死的作用。
基于此,本发明提供了微生物标志物在制备脑梗死诊断或辅助药物治疗效果评价产品中的应用,所述产品包括检测微生物标志物丰度的试剂。所述试剂可以是本领域的任何常规的试剂,只要可以检测微生物标志物的丰度即可。在本发明的具体实施方式中,所述微生物标志物为Vampirovibrio。
本申请所用的术语“丰度”是指生物样品中目标微生物的数量的量度。“丰度”也被称为“负载”。一般通过分子方法,典型地通过例如荧光原位杂交(FISH)、定量聚合酶链反应(qPCR)或PCR/焦磷酸测序测定所述目标微生物的16S rRNA基因拷贝数,进行细菌定量。生物样品内目标核酸序列丰度的定量可能是绝对的或相对的。“相对定量”通常是基于一个或多个内部参考基因,即来自参考菌株的16S rRNA基因,比如使用通用引物并且将目标核酸序列的丰度表达为总细菌16S rRNA基因拷贝的百分比或通过大肠杆菌16S rRNA基因拷贝归一化而测定的总细菌。“绝对定量”通过与DNA标准进行比较或通过DNA浓度归一化来给出目标分子的确切数目。
术语“定量水平”可以是浓度(每单位体积的DNA量)、每细胞数量的DNA量或基因拷贝数、循环阈值(Ct值)或其任何数学变换。
一般来讲,生物标志物都具有有用性,作为生物标志物的有用性是指分子标志物识别感兴趣的目标条件的有效程度,换句话说,所述参数允许辨别属于不同种群组的对象的有效程度,例如疾病与非疾病组或不同疾病表型。这被称为测试的“有效性”或“性能”。
本申请所用的术语“ROC曲线”或“接受者操作特性曲线”是指展示二元分类器系统的性能随着其辨别阈值的变化的图形曲线。通过在各种阈值设置下绘制真阳性率对假阳性率的曲线来创建该曲线。真阳性率也被称为灵敏度。假阳性率计算为1-特异性。因此,ROC曲线是一系列截断值范围内的真阳性率对假阳性率(灵敏度vs(1-特异性))的图形显示以及选择最佳截断值进行临床使用的方式。将准确度表示为ROC曲线下面积(AUC),为比较测试性能提供了有用的参数。接近1的AUC表示该测试高度灵敏并且具有高度特异性,而AUC接近0.5则表明该测试既不灵敏也不具有特异性。
当涉及测试样品与对照样品或参考样品之间的差异时,术语“显著的”或“统计学显著的”涉及在使用适当的统计分析时,各组相同的概率小于5%(例如p<0.05)的情况。换句话说,在完全随机基础上获得相同结果的概率在100次尝试中少于5次。本领域技术人员知道如何选择适当的统计分析。典型地,基于所研究的变量是否具有正态分布(例如通过用Kolmogorov-Smirnov检验)和是否存在同方差性(例如用Levene检验)来确定适当的统计分析。优选地,在存在正态分布和同方差性的情况下,使用参数模型比如t检验或ANOVA检验;并且在这两个要求中的至少一个要求未达到的情况下,通常使用非参数模型,比如MannWhitney U检验或Kruskal-Wallis检验。
作为可选择的实施方式,检测微生物标志物丰度的试剂包括定量样品中微生物标志物的靶核酸的试剂。所述试剂可基于使用核酸分子的已知方法来发挥其功能:如PCR、如Southern杂交、Northern杂交、点杂交、荧光原位杂交(FISH)、DNA微阵列、ASO法、高通量测序平台等。
作为一种可选择的实施方式,检测微生物标志物的方法是测序的方法,所述测序方法是包括但不限于第二代测序方法或第三代测序方法。进行测序的手段并不受特别限制,通过二代或者三代测序的方法进行测序,可以实现快速高效的测序。作为具体的实施方式,所述测序方法是通过选自Hiseq2000、SOLiD、454、和单分子测序装置的至少一种进行的。由此,能够利用这些测序装置的高通量、深度测序的特点,从而有利于对后续测序数据进行分析,尤其是进行统计学检验时的精确性和准确度。
本领域技术人员知晓,当进一步扩大样本量时,利用本领域公知的样本检测和计算方法,可以得出每种生物标志物在样本中的正常含量值区间(绝对数值)。可以将检测得到的生物标志物含量的绝对值与正常含量值进行比较,任选地,还可以结合统计学方法,以得出脑梗死的治疗效果等。
作为另外一种可选择的实施方式,检测微生物标志物丰度的试剂包括定量样品中微生物标志物的靶蛋白的试剂。所述试剂可基于使用检测蛋白的已知方法来发挥其功能:如夹心免疫测定,例如夹心ELISA,其中使用识别生物标志物上不同表位的两种抗体进行该生物标志物的检测;放射免疫测定(RIA)、直接、间接或对比酶联免疫吸附测定(ELISA)、酶免疫测定(EIA)、荧光免疫测定(FIA)、蛋白质印迹法、免疫沉淀法和基于任何颗粒的免疫测定(如使用金颗粒、银颗粒或乳胶颗粒、磁性颗粒或量子点)。可例如在微量滴定板或条的形式中实施免疫法。
根据本发明的免疫法可基于,例如,以下方法中的任一种。
免疫沉淀法是最简单的免疫测定方法;这种方法测量沉淀物的量,在试剂抗体已与样本一起孵育并与其中存在的靶抗原反应以形成不溶性团聚体之后形成所述沉淀。免疫沉淀反应可以是定性的或是定量的。
在颗粒免疫测定中,多种抗体与该颗粒连接,且所述颗粒能够同时结合很多抗原分子。这大大地加速了可见反应的速度。这允许生物标志物的快速且灵敏的检测。
在免疫比浊法(immunonephelometry)中,抗体和生物标志物上的靶抗原的相互作用引起免疫复合物的形成,所述免疫复合物太小而不能沉淀。但是,这些复合物将散射入射光,这可使用比浊计来测量。可在反应的几分钟之内测定抗原(即生物标志物)的浓度。
放射免疫测定(RIA)法使用放射性同位素例如I125来标记抗原或抗体。所使用的同位素发射γ射线,通常在除去非结合的(游离的)放射性标记之后测量所述射线。与其它的免疫测定相比较,RIA的主要优势在于更高的灵敏度、容易的信号检测和确认的、快速的测定。主要的劣势在于由放射物的使用引起的健康和安全风险和与维护许可放射物安全和处理程序相关的时间和费用。出于该原因,在常规临床实验室实践中,RIA已很大程度上被酶免疫测定所取代。
酶免疫测定(EIA)发展为放射免疫测定(RIA)的替代物。这些方法使用酶来标记抗体或靶抗原。EIA的灵敏度接近RIA的灵敏度,且不存在由放射性同位素引起的危险。用于检测的最广泛使用的EIA方法之一是酶联免疫吸附测定(ELISA)。ELISA方法可使用两种抗体,其一对于靶抗原是特异性的,而另一与酶偶联,酶底物的添加引起化学发光信号或荧光信号的产生。
荧光免疫测定(FIA)指使用荧光标记或酶标记的免疫测定,所述荧光标记或酶标记作用在底物上以形成荧光产物。荧光测量固有地比色(分光光度法的)测量更加灵敏。因此,FIA方法具有比利用吸收(光密度)测量的EIA方法更高的分析灵敏度。
化学发光免疫测定使用化学发光标记,当其被化学能激发时产生光;使用光检测器测量发射。
因此,可使用熟知的方法进行根据本发明的免疫法。在本发明的微生物标志物的检测中可使用任何直接(如使用传感器芯片)或间接的方法。
在本发明中,可以使用任何结构、尺寸、免疫球蛋白类别、起源等的抗体或其片段,只要它结合靶蛋白质即可。本发明的检测产品中包括的抗体或其片段可以是单克隆的或多克隆的。抗体片段指保留抗体对抗原的结合活性的抗体一部分(部分片段)或含有抗体一部分的肽。抗体片段可以包括F(ab′)
抗体可以通过本领域技术人员公知的方法来获得。标记物与抗体或其片段的结合可以通过本领域普遍知道的方法来实施。
作为依照本发明的检测产品的样品,可以使用例如自活检患者获得的固体样品或流体。样品不受特别限制,只要它适于本发明的测定;例如,它可以包括组织、血液、血浆、血清、淋巴液、尿液、浆膜腔液、脊髓液、滑液、房水、泪液、唾液、粪便或其级分或经过处理的材料。
在本发明的具体实施方案中,所述样品来源于粪便。
下面结合附图和实施例对本发明作进一步详细的说明。以下实施例仅用于说明本发明而不用于限制本发明的范围。实施例中未注明具体条件的实验方法,通常按照常规条件,或按照制造厂商所建议的条件。
实施例1与脑梗死相关的生物标志物
1.实验动物
特定无病原体等级的成年雄性C57BL/6小鼠(体重23.0至26.0g,8至12周龄)购自北京维通利华。所有C57BL/6小鼠都饲养在无特定病原体的条件下,具有相对恒定的湿度(60%±5%)和温度(22℃±3℃),光照时间为12h/黑暗时间为12h,所有的动物都是可以自由饮食和喝水。通过电凝法建立小鼠局灶性皮层脑梗死模型,将小鼠随机分为两组,对照组(pMCAO,25只)和用药组(25只)。
2.药物干预:阿托伐他汀(美国辉瑞公司)以2mg/ml的浓度溶于0.9%的生理盐水中。通过灌胃给予该药物20mg/kg/d。脑梗死组用等体积的生理盐水处理。用药1天后收集小鼠的粪便样本;同时检测小鼠的行为学特征以及脑梗死体积。
3.16S rRNA基因测序
使用DNA提取试剂盒自样本中提取细菌DNA,操作步骤按说明书进行。
DNA样品被接收后,对样品进行检测;检测合格的样品构建文库:回收目的Amplicon片段,用T4 DNA Polymerase、Klenow DNA Polymerase和T4 PNK将打断形成的粘性末端修复成平末端,再通过3'端加碱基“A”,使得DNA片段能与3'端带有“T”碱基的特殊接头连接;或者设计合成含有测序接头的双Index融合引物,以基因组DNA为模板,进行融合引物PCR,磁珠筛选目的Amplicon片段,最后,用合格的文库进行cluster制备和测序。
4.数据分析
用下机得到的数据进行相应的生物信息分析。下机数据经过数据过滤,滤除低质量的reads,剩余高质量的Clean data方可用于后期分析;通过reads之间的Overlap关系将reads拼接成Tags;在给定的相似度下将Tags聚成OTU,然后通过OTU与数据库比对,对OTU进行物种注释;基于OTU和物种注释结果进行样品物种复杂度分析以及组间物种差异分析。
4.1数据处理
在进行数据处理过滤时,使用内部撰写的程序对原始的测序数据进行如下处理,获得Clean Data,具体步骤如下:
1)采取按窗口去低质量的方法,具体操作如下:设置30bp为窗口长度,如果窗口平均质量值低于20,从窗口开始截除read末端序列,移除最终read长度低于原始read长度75%的reads;
2)去除接头污染reads(默认adapter序列与read序列有15bp的overlap,设置为15bp,允许错配数为3);
3)去除含N的reads;
4)去除低复杂度reads(默认reads中某个碱基连续出现的长度≥10,设置10bp)。
如果样品通过barcode合并建库,得到Clean Data后,利用barcode序列通过内部撰写的程序对样品进行拆分。barcode序列与测序reads比对允许的错配个数为0bp。
4.2序列拼接
序列拼接使用软件FLASH(Fast Length Adjustment of Short reads,v1.2.11),利用重叠关系将双末端测序得到的成对reads组装成一条序列,得到高变区的Tags。拼接条件如下:
1)最小匹配长度15bp;
2)重叠区域允许错配率为0.1。去除没有overlap关系的reads。Paired End Reads通过reads之间的overlap关系拼接成Tags。
4.3物种分类和丰度分析
将经过上述处理的Clean Tags进行OTU聚类,然后通过对OTU注释完成OTU的物种分类。
利用软件USEARCH(v7.0.1090)将拼接好的Tags聚类为OTU。其主要步骤如下:
1)利用UPARSE在97%相似度下进行聚类,得到OTU的代表序列;
2)利用UCHIME(v4.2.40)将PCR扩增产生的嵌合体从OTU代表序列中去除;16S和ITS采取和已有的嵌合体数据库进行比对的方法去除嵌合体。18S采取Denovo的方法去除嵌合体16S嵌合体数据库:gold database(v20110519)ITS嵌合体数据库:UNITE(v20140703),分为ITS全长,ITS1和ITS2,按测序区域进行选择。
3)使用usearch_global方法将所有Tags比对回OTU代表序列,得到每个样品在每个OTU的丰度统计表。得到OTU代表序列后,通过RDP classifer(v2.2)软件将OTU代表序列与数据库有比对进行物种注释,置信度阈值设置为1。其中,对注释结果进行如下过滤:
去除没有注释结果的OTU;
去除注释结果不属于分析项目中的物种。例如,样品为细菌16S,如果OTU注释上古菌则去除。剩余的OTU方可用于后期分析。
比对数据库:16S(包括细菌与古菌):Greengene(默认):V201305;RDP:Release9201203
4)物种差异分析
运用生物信息学分析方法分析物种差异分析根据得到的群落丰度数据,检测不同组(或样本)微生物群落表现出的丰度差异。物种差异性分析的内容包括:组间差异显著性检验、Lefse多级物种差异判别分析。本项目使用组间差异显著性检验进行差异物种的筛选。
组间差异显著性检验根据得到的群落丰度数据,运用严格的统计学方法可以检测不同组(样本)微生物群落中表现出的丰富度差异的物种,进行假设性检验,评估观察到的差异的显著性。分析可选择域、界、门、纲、目、科、属、种、OTU等不同分类水平。
1)Wilcox秩和检验(Wilcoxon rank-sum test),也叫曼-惠特尼U检验(Mann-Whitney U test),是两组独立样本非参数检验的一种方法。其原假设为两组独立样本来自的两总体分布无显著差异,通过对两组样本平均秩的研究来实现判断两总体的分布是否存在差异,该分析可以对两组样本的物种进行显著性差异分析,并对P值进行多种方法的校正。
2)多重检验校正,即对P值进行多重检验校正方法为"fdr"。
3)双尾检验,用于指定所求置信区间的类型,选择双尾检验(求置信区间)。
4)CI计算方法,即计算置信区间的方法,方法为DP:Welch’s confidenceinverted。置信度选择:0.95。
运用DP的方法计算影响大小(effect size),即mean1-mean2;运用Welch T检验的方法计算置信区间,筛选标准FDR<0.05。
5)根据差异菌群的丰度,绘制受试者工作特征曲线(ROC),计算二项精确置信空间,分析差异菌群的诊断效能。
5、结果
1)行为学检测结果显示,相比对照组,用药后小鼠的mNSS评分降低,Rotarod跑轮时间增加,粘附物移除实验中接触时间及移除时间降低;同时脑梗死的体积降低。
2)生物信息学分析结果显示,与模型组相比,Vampirovibrio在用药组中呈现显著性差异(图1),Vampirovibrio在脑梗组中的平均丰度为0.04903516,在用药组中的丰度为0.00470556。
3)诊断效能结果显示,Vampirovibrio作为检测指标的曲线下面积为0.911,截断值为0.018,该点的敏感性为1.000,特异性为0.800(图2),具有较高的敏感性和特异性。
实施例2粪便移植实验(FMT)
在无菌条件下收集阿托伐他汀治疗的小鼠的粪便材料,将供体小鼠的粪便(0.1g)混合并悬浮在1ml无菌PBS中。使用台式涡流(Vortex-Genie 2,Science Industries,美国)将混合物混合15s,室温800g离心3min后,取上清液500μL经口灌胃给PMCAO小鼠(n=12)。新鲜粪便制备于粪便移植当天,于灌胃前15min内完成。测定FMT小鼠的神经行为,并与pMCAO组(n=12)进行比较。
结果如图3所示,粪便移植后,改善了小鼠的神经行为学,降低了mNSS评分(图3A),增加了Rotarod跑轮时间(图3B),降低粘附物移除实验中接触时间(图3C)及移除时间(图3D)。
上述实施例的说明只是用于理解本发明的方法及其核心思想。应当指出,对于本领域的普通技术人员来说,在不脱离本发明原理的前提下,还可以对本发明进行若干改进和修饰,这些改进和修饰也将落入本发明权利要求的保护范围内。
- 微生物标志物在脑梗死诊断和治疗效果评价中的应用
- 真菌微生物组作为标志物在制备治疗筛查和肺癌诊断中的应用
