一种HPV特异性miR-34、miR-199和miR-199的四重荧光检测试剂盒
文献发布时间:2023-06-19 19:28:50
技术领域
本申请涉及生物医学检测技术领域,尤其是涉及一种HPV特异性miR-34、miR-199和miR-199的四重荧光检测试剂盒。
背景技术
人乳头瘤病毒(Human Papillomavirus,简称HPV)是一种嗜上皮性病毒,有高度的特异性。根据致病力强弱,HPV被分为高危型和低危型两种,“是否能致癌”是危险度大小的主要标志。全世界每年宫颈癌的新发病例大约有500,000,是除乳腺癌之外威胁女性生命健康的第二大恶性肿瘤。HPV和宫颈癌的病因学关系已经明确,从HPV感染到宫颈癌发生需要较长时间,在此期间通过检测可以了解是否感染HPV,早发现早治疗,从而有效预防宫颈癌的发生。
目前人乳头瘤病毒的分型检测经过多年的发张已经比较成熟的,大部分的检测方法都是,通过设计多种不同分型的HPV的引物与探针,然后通过PCR进行检测,例如在在公开号为CN107488747A和CN102994647A的专利中都是通过上述的方法进行测试;但是上述的测试方法均需要通过阴道取脱落的宫颈细胞,这是一种侵入式的采样,因而对很多未成年、未婚或者胆小的女性而言,以会有较大的不适和恐惧感。
根据已有的研究表明,miR-34、miR-145和miR-199的表达量与人乳头瘤病毒HPV的感染是呈负相关的,因而血清中miR-34、miR-145和miR-199的浓度可以用来评价HPV病毒活动对宫颈细胞造成的损伤,从而推断出是否存在HPV感染。这三种microRNA都可以作为一种新的生物学指标应用于临床检测,具有重要的临床意义;但是目前并没有系统的通过特异性病毒的表达量来判定宫颈细胞损伤的相关研究。
目前关于miR-34、miR-145和miR-199的检测方法也都是通过PCR检测进行,主要有染料法和探针法,目前这两种方法都是通过加入的标准化内参Ct值进行相对定量的方法,无法准确定量出具体的分子拷贝数,检测下限和灵敏性都不可知。而且目前已有的方法都是单通道单色检测,每种microRNA需要单独一管进行PCR,检测效率低下。
针对上述相关技术,发明人认为人乳头瘤特异性病毒存在检测灵敏度不高和检测效率低的缺陷。
发明内容
为了提高人乳头瘤病毒特异性miR-34、miR-145和miR-199检测灵敏度和检测效率,本申请提供一种HPV特异性miR-34、miR-199和miR-199的四重荧光检测试剂盒。
本申请提供的一种HPV特异性miR-34、miR-199和miR-199的四重荧光检测试剂盒,采用如下的技术方案:
一种HPV特异性miR-34、miR-199和miR-199的四重荧光检测试剂盒,包括以下引物和探针:
miR-34茎环法逆转录引物如序列1所示,具体为:TACGCTACATTGACGCCATTCGATGCATTAACGCCGGATCAGCTAGCGATTGAC,
检测miR-34的荧光探针如序列2所示,具体为:CGATCATCGGTAGCTCGATCGAGC,
检测miR-34的上游引物如序列3所示,具体为:CAGTTAGCCTAGACTGCATC,
检测miR-34的下游引物如序列4所示,具体为:TCGATGCCAATCGTTACG;
miR-145茎环法逆转录引物如序列5所示,具体为:TCGATTGCCTAGCTGCAGTCGAAATGCTTCGGACGAACGTACGATCTGTGCAT,
检测miR-145的荧光探针如序列6所示,具体为:GTATAGAATTGCCATTGTACTCAG,
检测miR-145上游引物如序列7所示,具体为:GCTTACTAATCAGTATGTG,
检测miR-145下游引物如序列8所示,具体为:CTACGTAACCGTACGT;
miR-199茎环法逆转录引物如序列9所示,具体为:TAGCTTGAACTGGCCAATGGATGCATTCCAGGTGCTAAGGTACTGAC,
检测miR-199的荧光探针如序列10所示,具体为:CTGATTCCAGTCAAGTCAATGAGTC,
检测miR-199上游引物如序列11所示,具体为:TGCAATCCGATTCGTCATG,
检测miR-199下游引物如序列12所示,具体为:GTCAAGTTCCGATCGGC。
通过采用上述技术方案,本发明的三种特异性病毒microRNA采用茎环法进行逆转录,其特异性更强,成本更低,同时为四重荧光定量PCR提供了可能。本申请的针对不同的特异性病毒设计了三套引物和三种不同的荧光探针,同时进行荧光定量PCR检测,其相互不干扰,一管反应可以获得三个特异性病毒的结果,在提高了检测灵敏度的同时大幅度提升了检测的效率。同时可以通过三种特异性病毒的表达量可以更精准的判定宫颈细胞的损伤程度,提高检测效果。
作为优选,所述的人乳头瘤病毒特异性miR-34、miR-199和miR-199的四重荧光定量PCR检测试剂盒中还包括有内参的引物和探针,
内参的茎环法逆转录引物如序列13所示,具体为:ATCCATGGCTTAGCAGGTAGCTAGTCGAATGCTAGTCAGTCGATGTAAGC,
检测内参的荧光探针如序列14所示,具体为:TGCATCGATACATGTACTAGTAATG,
内参的上游引物如序列15所示,具体为:GTCTACTTAGTATCGTCT,
内参的下游引物如序列16所示,具体为:CAGTTCGATCAGTAAG。
通过采用上述技术方案,在本本申请中的试剂盒加入标准化内参,既可以有效监控假阴性的存在,还可以通过内参Ct值校正不同血清样本microRNA提取过程和PCR过程中产生的实验操作误差,对实验结果的重复性和稳定性有明显改善。
作为优选,所述的试剂盒中还包括有定量的参考品和标准化内参:
miR-34的定量参考品序列如序列17所示,具体为:ACTAGTTGCATGGTAAATCGTGCATCCCAGCGATAAGTGGATTGGTTCAGCGGTGCTGTACA;
miR-145的定量参考品序列如序列18所示,具体为:CGATGTAATAGCTATGGGCTGCTCTTATCCTGATCGATCGATTTACAAACTAGTGCTAGGCG;
miR-199的定量参考品如序列19所示,具体为:CAGTCAGTCGATGGATAGTCATCTTCACACCGTGTTATCGATCGGACGTAGCGTAGTCAGC;
标准化内参序列如序列20所示,具体为:
UCAGUGGAUCGUGUCAGUUGGAC。
通过采用上述技术方案,通过定量参考品可以进一步提升检测的灵敏度,从而更好的实现对人乳头瘤特异性病毒的检测。
所述的HPV特异性miR-34、miR-199和miR-199的四重荧光检测试剂盒的检测方法,包括以下步骤:
S1将人的血清或血浆进行microRNA进行提取,得到microRNA;
S2将提取的microRNA与逆转录引物混合物进行逆转录,获得cDNA;
S3将逆转录cDNA与探针引物混合物以及上游引物混合物和下游引物混合物进行PCR荧光检测,即可在不同的通道分别获得miR-34、miR-199和miR-199和内参扩增曲线;
其中:逆转录引物混合物为miR-34茎环法逆转录引物、miR-199茎环法逆转录引物、miR-199茎环法逆转录引物和内参茎环法逆转录引物组成的混合物;
探针引物混合物为miR-34的探针引物、miR-199的探针引物、miR-199的探针引物和内参的探针引物组成的混合物;
上游引物混合物为miR-34的上游引物、miR-199的上游引物、miR-199的上游引物和内参的上游引物组成的混合物;
下游引物混合物为miR-34的下游引物、miR-199的下游引物、miR-199的下游引物和内参的下游引物组成的混合物。
综上所述,本申请包括以下至少一种有益技术效果:
1.在本申请中三种人乳头瘤病毒特异性microRNA逆转录使用的是发夹茎环法,其产物为一种稳定的发夹结构,特异性结合小分子microRNA,排除长链RNA干扰,因而其特异性更强,成本较低,同时为四重荧光定量PCR提供了可能。本申请中的四重荧光定量PCR在同一个反应管中同时加入miR-34,miR-145、miR-199和内参的四套引物和四种不同荧光的探针,同时进行荧光定量PCR互不干扰,一管反应可以获得四个结果,在保证检测灵敏度的条件下,提升了检测效率。
2.本申请中提供的miR-34,miR-145、miR-199定量参考品,能够绘制标准曲线并且定量标本中的拷贝数浓度,比目前的相对定量方法准确度更高。
3.本申请的试剂盒通过外加标准化内参,既可以有效监控假阴性的存在,还可以通过内参Ct值校正不同血清样本microRNA提取过程和PCR过程中产生的实验操作误差,对实验结果的重复性和稳定性有明显改善。
附图说明
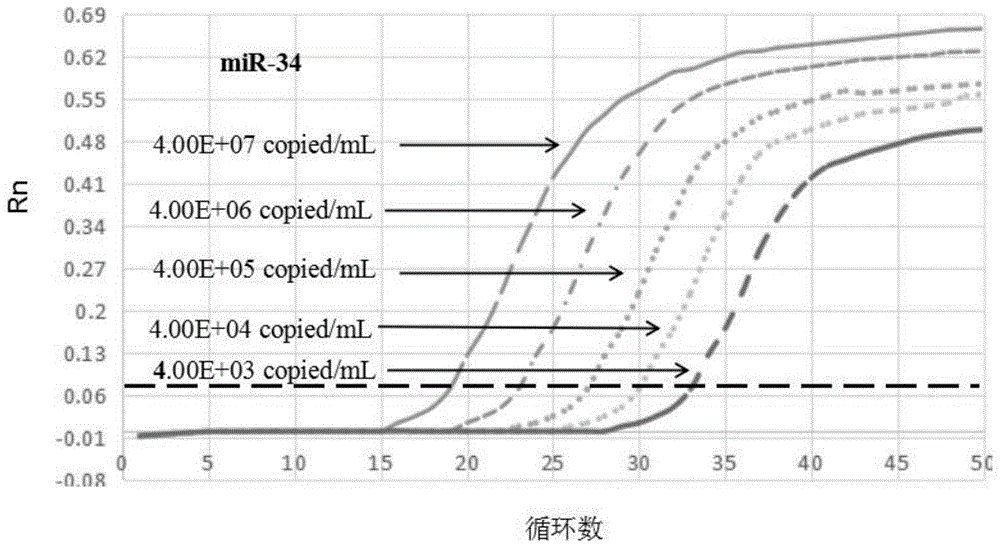
图1是本申请中miR-34不同浓度的定量参考品的扩增曲线。
图2是本申请中miR-145不同浓度的定量参考品的扩增曲线。
图3是本申请中miR-199不同浓度的定量参考品的扩增曲线。
图4是本申请中健康女性的miR-34的PCR扩增曲线。
图5是本申请中健康女性的miR-145的PCR扩增曲线。
图6是本申请中健康女性的miR-194的PCR扩增曲线。
图7是本申请中HPV阳性女性的miR-34的PCR扩增曲线。
图8是本申请中HPV阳性女性的miR-145的PCR扩增曲线。
图9是本申请中HPV阳性女性的miR-194的PCR扩增曲线。
具体实施方式
本申请中的四重荧光定量PCR检测试剂盒的引物和探针序列如表1所示:
表1本申请中的序列信息
实施例1 .microRNA提取
(1)取200μl血清/血浆加入1.5ml离心管,每管加入0.5ml的Trizol试剂,枪头反复吹打混匀直至蛋白完全溶解,每管加入的内参至其终浓度为0.2nm,混匀,冰浴放置15分钟;
(2)每管加入100μl预冷氯仿,振荡混匀;
(3)4℃,12000g离心15min,转移上清,加入等体积预冷酚/氯仿(1:1),振荡混匀,4°C,14000g离心10min;
(4)转移上清,加入等体积预冷氯仿,振荡混匀,4°C,14000g离心15min;
(5)转移上清,加入等体积异丙醇以及糖原(终浓度为200μg/ml),振荡混匀,4°C,16000g离心30min;
(6)小心倾倒上清,用1ml 70%乙醇洗涤沉淀一次,4°C,16000g离心10min;
(7)弃上清,待乙醇挥发后,加入10μlDEPC水溶解,置于-80°C中保存备用。
实施例2.microRNA逆转录和四重荧光定量PCR
1、microRNA逆转录
配制反应液:如表2所示:
表2
备注:逆转录引物混合液为miR-34、miR-145、miR-199和内参逆转录引物组成混合物,三者的浓度均为10μM。
miRNA反应混合物、逆转录引物混合液和BSA加入到的PCR薄壁管中;接着将取提取好的microRNA加入上述混合液中,吹打混匀;然后放入PCR仪进行逆转录,条件为:42℃ 30分钟,70℃5分钟;获得的cDNA置冰盒中。
2、四重荧光定量PCR
配制反应液:如表3所示:
表3
备注:探针引物混合液为miR-34、miR-145、miR-199和内参探针引物组成混合物,三者的浓度均为2μM;上游引物和下游引物混合物中,三者的浓度均为4μM。
取2×PCR混合液、2探针引物混合液、上游引物和下游引物的混合物5μL和去离子水10μL加入0.2mL的8联PCR管中。每管加入5μL逆转录好的cDNA,混匀。将PCR反应管放入荧光定量PCR扩增仪,按对应顺序设置待测样本名称及定量参考品浓度;荧光检测通道的选择:通过软件选择FAM通道检测miR-34,选择HEX检测内参,选择VIC检测miR-145,选在Cy5检测miR-199,荧光定量PCR反应条件为:95℃3分钟,进入循环:95℃12秒,60℃30秒(检测荧光),运行45-50个循环结束。反应结束后,仪器自动保存结果。在相应的通道,可以利用仪器自带的软件进行自动分析(也可以手动调节基线的开始值、结束值以及阈值线值进行分析),然后记录样本Ct值和定值结果。扩增曲线与阈值线的交点,称为Ct(即cyclethreshold,指PCR反应管内的荧光信号达到设定的阈值时,所经历的循环数值)。
实施例3
标准曲线的绘制:
根据miR-34、miR-145、miR-199定量参考品(序列可见表4)分别稀释成5个梯度的浓度,按照上述方法进行PCR扩增测试,其扩增曲线分别如图1~3所示,根据扩增曲线进行记录样本Ct值和定值结果,分别得到其标准曲线方程。
表4
测试:
测试5例HPV阴性且身体健康的女性的血清样品,按照上述的方法进行PCR扩增测试,miR-34、miR-145、miR-199的扩增曲线分别如图4~6所示。
测试5例HPV阳性女性患者且宫颈上皮内瘤变(CIN)Ⅱ~Ⅲ患者的血清样品,按照上述的方法进行PCR扩增测试,miR-34、miR-145、miR-199的扩增曲线分别如图7~9所示。
从图1~3可以看出,根据定量参考品的浓度不同,其曲线根据浓度会有相应的变化。PCR的软件可以自动求得各样本的定值结果;最后通过内参Ct值校正结果(校准浓度=检测浓度/2
从图4~6可以看出,测试5例HPV阴性且身体健康的女性的血清样品,按照上述的方法进行PCR扩增测试,miR-34、miR-145、miR-199的扩增曲线分别如图4~6所示,从图上的数据可以看出,其均是大于400copies/mL,显示为阴性。
从图4~6可以看出,测试5例HPV阳性女性患者且宫颈上皮内瘤变(CIN)Ⅱ~Ⅲ患者的血清样品,从图上的数据可以看出,其均是小于400copies/mL,其对应的HPV也是阳性的,因而可以看出HPV阳性与上述特异性的microRNA呈现负相关的情况。
根据上述的结构,miR-34、miR-145、miR-199的在判定宫颈细胞损伤是有潜在的应用的。
以上均为本申请的较佳实施例,并非依此限制本申请的保护范围,故:凡依本申请的结构、形状、原理所做的等效变化,均应涵盖于本申请的保护范围之内。
- 一种CVA2特异性引物、实时荧光检测试剂盒及其用途
- 乙型肝炎病毒miR-3和人肝脏特异性miR-122三重荧光定量PCR检测试剂盒
- 一种用于检测假单胞菌属细菌的特征性核苷酸序列及其特异性引物、试剂盒和检测方法
- 一种用于特异性检测HPV18的RPA荧光定量引物对、探针及试剂盒
- 一种用于特异性检测HPV18的RPA荧光定量引物对、探针及试剂盒
