肿瘤解聚剂、制备方法、用途、乳腺肿瘤治疗方法、卵巢肿瘤治疗方法
文献发布时间:2023-06-23 06:30:03
技术领域
本发明涉及生物材料技术领域,尤其涉及一种肿瘤解聚剂、制备方法、用途、乳腺肿瘤治疗方法、卵巢肿瘤治疗方法。
背景技术
乳腺癌和卵巢癌是常见的妇科癌症。乳腺癌是乳腺上皮细胞在多种致癌因子的作用下,发生增殖失控的现象。疾病早期常表现为乳房肿块、乳头溢液、腋窝淋巴结肿大等症状,晚期可因癌细胞发生远处转移,出现多器官病变,直接威胁患者的生命。卵巢癌是卵巢肿瘤的一种恶性肿瘤,是指生长在卵巢上的恶性肿瘤,其中90%~95%为卵巢原发性的癌,另外5%~10%为其它部位原发的癌转移到卵巢。由于卵巢癌早期缺少症状,即使有症状也不特异,筛查的作用又有限,因此早期诊断比较困难,就诊时60%~70%已为晚期,而晚期病例又疗效不佳。因此,虽然卵巢癌的发病率低于宫颈癌和子宫内膜癌居妇科恶性肿瘤的第三位,但死亡率却超过宫颈癌及子宫内膜癌之和,高居妇科癌症首位,是严重威胁妇女健康的最大疾患。
乳腺癌的治疗方法包括化学药物治疗、内分泌治疗、靶向治疗、手术治疗、放射治疗等。其中,手术治疗是乳腺癌患者的首选治疗方案,只有在全身情况差、主要脏器有严重疾病、老年体弱不能耐受等情况下,不采取手术治疗。放射治疗一般与手术治疗、化学药物治疗搭配使用。然而,上述治疗均存在并发症。对于手术治疗而言,其并发症包括皮瓣下积血、皮缘坏死、皮下积液、上肢淋巴水肿等。对于化学药物治疗而言,其并发症包括恶心、呕吐、骨髓抑制、心脏毒性、严重脱发、口腔黏膜出血、免疫力低下等。对于放射治疗而言,其并发症包括皮肤损伤、皮下组织纤维化、乳房纤维化、放射性肺炎等。
卵巢癌的治疗方法包括手术治疗、化学药物治疗、放射治疗、免疫治疗等。其中,手术治疗是卵巢癌患者的首选治疗方案,化学药物治疗是辅助治疗手段。然而,上述治疗均存在一些并发症。例如,采用手术治疗卵巢癌,容易出现术后感染、出血、深部静脉血栓形成、肠粘连、肠梗阻等。
目前针对相关技术中存在的治疗风险大、有并发症等问题,尚未提出有效的解决方案。
因此,本领域需要开发一种有效治疗乳腺肿瘤、卵巢肿瘤的药物,降低患者的痛苦。
发明内容
本发明的目的是针对现有技术中的不足,提供一种肿瘤解聚剂、制备方法、用途、乳腺肿瘤治疗方法、卵巢肿瘤治疗方法,以解决相关技术中存在的治疗风险大、有并发症等问题。
为实现上述目的,本发明采取的技术方案是:
本发明的第一方面,提供一种肿瘤解聚剂,所述的肿瘤解聚剂包括LDH/EDTA层状双氢氧化物材料。
在其中的一些实施例中,所述肿瘤解聚剂为口服制剂。
在其中的一些实施例中,所述肿瘤解聚剂还包括混合溶液。
在其中的一些实施例中,所述肿瘤解聚剂用于治疗乳腺肿瘤。
在其中的一些实施例中,所述肿瘤解聚剂用于治疗卵巢肿瘤。
在其中的一些实施例中,所述肿瘤解聚剂为液体制剂。
在其中的一些实施例中,所述肿瘤解聚剂为混悬液。
在其中的一些实施例中,所述LDH/EDTA层状双氢氧化物的质量为0.1g~1g。
在其中的一些实施例中,所述LDH/EDTA层状双氢氧化物材料的浓度为0.001g/mL~0.1g/mL。
在其中的一些实施例中,所述混合溶液的体积为1mL~1000mL。
在其中的一些实施例中,所述混合溶液为无菌磷酸盐缓冲液或生理盐水。
本发明的第二方面,提供一种肿瘤解聚剂的制备方法,用于制备如第一方面所述的肿瘤解聚剂,其特征在于,所述的方法包括:
将所述的LDH/EDTA层状双氢氧化物材料和无菌磷酸盐缓冲液或生理盐水混合,得到所述肿瘤解聚剂。
本发明的第三方面,提供一种如第一方面所述的肿瘤解聚剂在制备治疗乳腺肿瘤药物中的用途。
在其中的一些实施例中,所述LDH/EDTA层状双氢氧化物材料的用量为0.1g/次。
在其中的一些实施例中,给药周期为每个工作日一次、连续至少四周。
本发明的第四方面,提供一种乳腺肿瘤治疗方法,所述治疗方法包括:
将如第一方面所述的肿瘤解聚剂湿敷于乳腺部位。
本发明的第五方面,提供一种如第一方面所述的肿瘤解聚剂在制备治疗卵巢肿瘤药物中的用途。
在其中的一些实施例中,所述LDH/EDTA层状双氢氧化物材料的用量为0.5g/次~1g/次。
在其中的一些实施例中,给药周期为腹腔镜指导下给药一次。
本发明的第六方面,提供一种卵巢肿瘤治疗方法,所述治疗方法包括:
将如第一方面所述的肿瘤解聚剂灌注于卵巢。
本发明采用以上技术方案,与现有技术相比,具有如下技术效果:
本发明提供一种肿瘤解聚剂,所述肿瘤解聚剂通过简单的湿敷即可发挥对乳腺肿瘤的有效治疗以及通过简单的灌注即可发挥对卵巢肿瘤的有效治疗,本发明所述的肿瘤解聚剂直接在作用于乳腺或卵巢,能够有效发挥对乳腺肿瘤或卵巢肿瘤的靶向治疗,降低全身副作用,生物安全性较好,无须进行手术,后遗症少,降低患者的痛苦。
附图说明
图1为本发明实施例2乳腺破溃处湿敷治疗图,其中,图1a为本发明实施例2未治疗前图像,图1b为本发明实施例2治疗18天后图像,图1c为本发明实施例2的治疗34天后图像。
图2为本发明实施例3的乳腺破溃处湿敷治疗图,其中,图2a为本发明实施例3的未治疗前图像,图2b为本发明实施例3的治疗4天后图像,图2c为本发明实施例3的治疗25天后图像。
图3为本发明实施例5的灌注前后的腹腔镜图像。
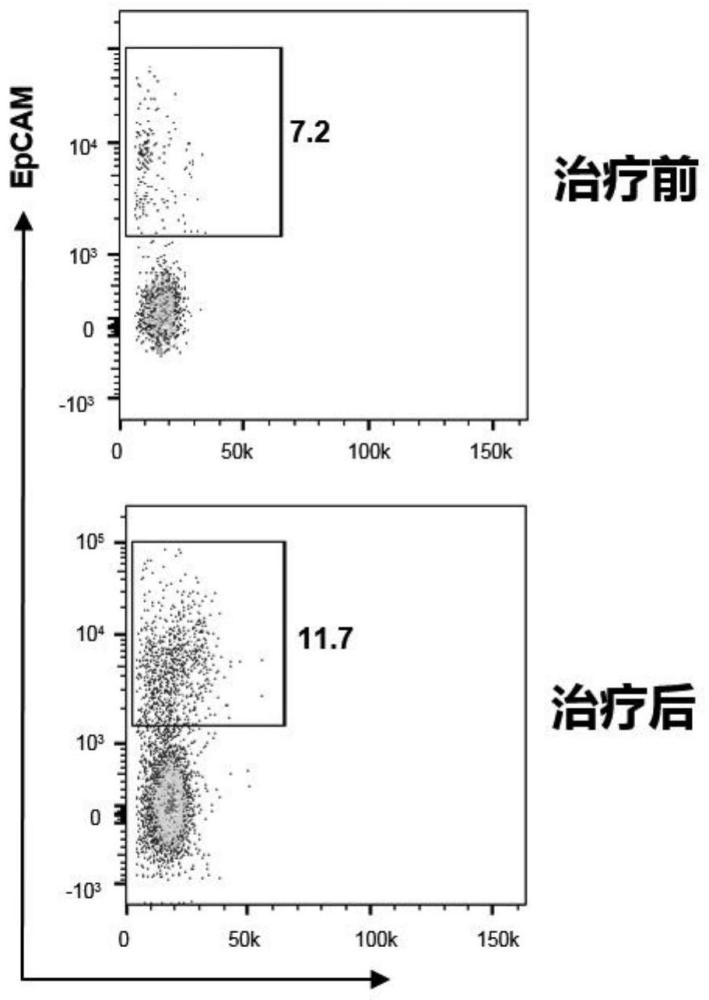
图4是本发明实施例6的治疗前后EpCAM的强度示意图。
具体实施方式
为了使本申请的目的、技术方案及优点更加清楚明白,以下结合附图及实施例,对本申请进行描述和说明。应当理解,此处所描述的具体实施例仅仅用以解释本申请,并不用于限定本申请。基于本申请提供的实施例,本领域普通技术人员在没有作出创造性劳动的前提下所获得的所有其他实施例,都属于本申请保护的范围。
下面结合具体实施例,进一步阐述本发明。应理解,以下具体实施例以本技术方案为前提,给出了详细的实施方式和具体操作过程,但本发明的保护范围并不限于本实施例。
在本发明中,LDH材料组成选用对机体相对安全的锌铝离子。为了保证LDH持续粘附在肿瘤细胞表面从而破坏细胞连接,避免LDH被细胞摄取到细胞内发挥螯合作用,本发明制备了颗粒尺寸在0.8μm左右的带正电性的LDH。实际上,所得LDH/EDTA层状双氢氧化物材料的颗粒尺寸也在0.8μm左右,其为带强正电性。
在本发明中,LDH材料具有更强的pH敏感性,可在肿瘤微酸环境中响应性释放EDTA。
在其中的一些实施例中,采用均相碱液法制备LDH材料,该工艺更加简单稳定。具体地,将溶有锌源(锌金属盐)和铝源(铝金属盐)、六次亚甲基四胺(HMT)以及氯化钠的混合溶液置于120℃油浴锅中,于氩气保护气氛下回流油浴2小时后,再加入乙二胺四乙酸二钠盐置换层间阴离子,制备负载EDTA的LDH,标记为LDH/EDTA。其中,油浴锅的温度可为80℃,回流油浴的时间可为22小时。其中,EDTA通过阴离子交换大量地插入LDH层间,后续可在微酸的机体环境下(pH 6.5)释放。
在其中的一些实施例中,乙二胺四乙酸二钠盐和锌源的质量比可为1.2g:0.594g。锌源优选选自硝酸锌等。铝源优选选自硝酸铝等。其中,锌源和铝源的摩尔比可为2:1。硝酸钠和锌源的质量比可为594:85。环六亚甲基四胺和锌源的质量比可为99:117。
以上所述LDH/EDTA的合成反应中,均需要在氩气和氦气等保护气氛下进行,避免空气中二氧化碳进入体系中,形成碳酸根离子插入LDH层间并难以置换出。
在本发明中,LDH/EDTA材料体系制备完后用水过滤清洗三次,并冷干后粉末均保存在4℃冰箱内,后续现用现配置按浓度分散到无菌磷酸盐缓冲液或生理盐水中。该材料体系LDH/EDTA对机体的主要组织和血液指标无明显的急性或慢性的病理毒性和异常,具有较好的系统体内安全性。
本发明中,LDH/EDTA材料体系由于大尺寸无法进入细胞,并表面带有正电性,可持续吸附在负电性的细胞膜表面,在肿瘤偏酸的微环境中释放EDTA来螯合钙离子,抑制钙离子依赖的相关蛋白表达,从而破坏细胞连接使贴壁细胞大量脱落。并且重要的是,这些脱落的分散细胞依旧被材料体系紧紧包裹,抑制其着壁转移的能力。
实施例1肿瘤解聚剂
(一)实验方法
LDH/EDTA层状双氢氧化物材料的制备过程如下:
称取一定量的Zn(NO3)2·6H2O(0.594g)、Al(NO3)3·9H2O(0.375g)、NaNO3(0.085g)和环六亚甲基四胺(HMT)(0.702g)溶于150mL的去离子水中,在高纯氩气氛保护下磁力搅拌20min排出空气,然后将该溶液移至120℃油浴锅中搅拌,在高纯氩作为保护气的条件下回流,100min后,缓慢加入Na2H2EDTA溶液(1.2mg溶于50mL去离子水中),100℃继续反应22h,最后将沉淀物过滤收集并用去离子水充分清洗,得到LDH/EDTA,并最终冷冻干燥,获得的粉末保存在4℃冰箱里。
肿瘤解聚剂的制备过程如下:
将0.1g的LDH/EDTA层状双氢氧化物材料加入至1mL~100mL无菌PBS缓冲液中超声混匀,以形成白色混悬液。
实施例2
考察实施例1的肿瘤解聚剂在治疗乳腺肿瘤方面的效果
实验方法
(一)患者筛选标准
患者的入组标准如下:
(1)晚期乳腺癌患者,其它治疗手段疗效不佳;
(2)局部复发和转移,堵塞管腔;
(3)CT、MRI评分、辅助检查诊断及病理诊断明确为乳腺癌;
(4)年龄18周岁以上;
(5)无严重心、肝、肾等重要脏器疾病;
(6)患者依从性好,愿意配合进行临床试验。
患者的排除标准如下:
(1)患者有严重合并症如营养不良、恶液质、腹水等肿瘤终末期;
(2)患者有凝血因子障碍等血液性疾病基础;
(3)妊娠或哺乳期妇女;
(4)患者同时患有多器官肿瘤或有严重未控制的内科疾病或急性感染者;
(5)患者不能理解研究目的或不同意研究的要求;
(6)不具备法律能力或法律能力受限制;
(7)研究者判断依从性不好,不能配合进行样本采集;
(8)任何病史,据研究者判断可能干扰试验结果或增加患者风险。
(二)实施方案
给药剂量为0.1g/次,给药体系为1mL~100mL/次,给药周期为每个工作日一次、连续至少四周;
在湿敷前,将LDH/EDTA层状双氢氧化物材料稀释于无菌磷酸缓冲盐溶液以形成肿瘤解聚剂。
(三)临床评估标准
(1)血常规、血栓弹力图、肝肾功能、电解质、心肺功能、肿瘤标志物及血液金属物指标检测提示治疗是否安全;
(2)收集患者治疗后局部分泌物,评估接受肿瘤解聚剂处理后脱落细胞种类及数量;
(3)对患者治疗前后进行局部增强磁共振检查,评估患者前后肿块大小。
实验结果
患者刘某某将肿瘤解聚剂溶液10ml湿敷于乳腺部位,给药剂量为0.1g/次。
图1是乳腺破溃处湿敷治疗图。如图1a所示,可见乳腺部位化脓破溃。如图1b~1c所示,治疗后化脓区域缩小、患处收敛,治疗后新生肉芽组织增多。
由上可知,在湿敷肿瘤解聚剂可以有效缓解破溃症状,且患者主诉治疗过程无灼热感、刺激感,治疗过程舒适、无其他不良反应。
实施例3
考察实施例1的肿瘤解聚剂在在治疗乳腺肿瘤方面的效果
实验方法
本实施例的实验方法同实施例2基本相同。
实验结果
患者宋某某将肿瘤解聚剂溶液10ml湿敷于乳腺部位,给药剂量为0.1g/次。
图2是乳腺破溃处湿敷治疗图。如图2a所示,可见乳腺部位化脓破溃。如图2b~2c所示,治疗3天后化脓区域缩小、患处收敛,治疗后新生肉芽组织增多。
由上可知,在湿敷肿瘤解聚剂可以有效缓解破溃症状,且患者主诉治疗过程无灼热感、刺激感,治疗过程舒适、无其他不良反应。
实施例4
肿瘤解聚剂
(一)实验方法
LDH/EDTA层状双氢氧化物材料的制备过程如下:
称取一定量的Zn(NO3)2·6H2O(0.594g)、Al(NO3)3·9H2O(0.375g)、NaNO3(0.085g)和环六亚甲基四胺(HMT)(0.702g)溶于150mL的去离子水中,在高纯氩气氛保护下磁力搅拌20min排出空气,然后将该溶液移至120℃油浴锅中搅拌,在高纯氩作为保护气的条件下回流,100min后,缓慢加入Na2H2EDTA溶液(1.2mg溶于50mL去离子水中),100℃继续反应22h,最后将沉淀物过滤收集并用去离子水充分清洗,得到LDH/EDTA,并最终冷冻干燥,获得的粉末保存在4℃冰箱里。
肿瘤解聚剂的制备过程如下:
将0.1g的LDH/EDTA层状双氢氧化物材料加入至1mL~10mL无菌PBS缓冲液中超声混匀,以形成白色混悬液。
实施例5
考察实施例4的肿瘤解聚剂在治疗卵巢肿瘤方面的效果
实验方法
(一)患者筛选标准
患者的入组标准如下:
(1)晚期卵巢癌伴腹腔、盆腔广泛转移患者,其它治疗手段疗效不佳;
(2)CT、MRI评分、辅助检查诊断及病理诊断明确为卵巢癌;
(3)年龄18周岁以上;
(4)无严重心、肝、肾等重要脏器疾病;
(5)患者依从性好,愿意配合进行临床试验。
患者的排除标准如下:
(1)患者有严重合并症如营养不良、恶液质、腹水等肿瘤终末期;
(2)患者有凝血因子障碍等血液性疾病基础;
(3)妊娠或哺乳期妇女;
(4)患者同时患有多器官肿瘤或有严重未控制的内科疾病或急性感染者;
(5)患者不能理解研究目的或不同意研究的要求;
(6)不具备法律能力或法律能力受限制;
(7)研究者判断依从性不好,不能配合进行样本采集;
(8)任何病史,据研究者判断可能干扰试验结果或增加患者风险。
(二)实施方案
给药剂量为0.5g/次~1g/次,给药体系为100mL~1000mL/次,给药周期为腹腔镜指导下给药一次;
在灌注前,将LDH/EDTA层状双氢氧化物材料稀释于无菌磷酸缓冲盐溶液以形成肿瘤解聚剂。
(三)临床评估标准
(1)血常规、血栓弹力图、肝肾功能、电解质、心肺功能、肿瘤标志物及血液金属物指标检测提示治疗是否安全;
(2)收集患者治疗后排泄物或局部分泌物,评估接受肿瘤解聚剂处理后脱落细胞种类及数量;
(3)对患者治疗前后进行局部增强磁共振检查,评估患者前后肿块大小。
实验结果
在无菌操作台将LDH/EDTA层状双氢氧化物材料放置缓冲液中进行超声,以使肿瘤解聚剂呈混悬液;患者孙某某躺卧于手术台;施术者于腹腔镜镜下将肿瘤解聚剂灌注于该患者的卵巢中。肿瘤解聚剂溶液500ml,给药剂量为0.5g/次。
图3是该患者灌注前后的腹腔镜图。如图3所示,盆腔腹腔广泛转移,有大量腹水,其他治疗均无法耐受。如图3所示,卵巢癌患者治疗后转移病灶肉眼可见完全剥落,患者手术后生命体征平稳,未见明显并发症,腹水消退。
在1周后检测肿瘤标记物CA125,其数值由治疗前770降至120,生活能够自理,饮食恢复正常。
由上可知,在腹腔镜指导下进行局部灌注治疗可以有效缓解腹水症状。
实施例6
考察实施例4的肿瘤解聚剂在治疗卵巢肿瘤方面的效果
实验方法
本实施例的实验方法同实施例5基本相同。
实验结果
在无菌操作台将LDH/EDTA层状双氢氧化物材料放置缓冲液中进行超声,以使肿瘤解聚剂呈混悬液;患者吴某某躺卧于手术台;施术者于腹腔镜镜下将肿瘤解聚剂灌注于该患者的卵巢中。肿瘤解聚剂溶液500ml,给药剂量为0.5g/次。
在灌注治疗前后收集患者的引流液,基于流式细胞术,对比治疗前后脱落细胞表达肿瘤细胞标志物EpCAM的强度。如图4所示,治疗后引流液中脱落细胞表面表达EpCAM的强度显著增强。
由上可知,在腹腔镜指导下进行局部灌注治疗可以有效缓解腹水症状,且基于患者治疗后的引流液组织分析可见大量肿瘤细胞脱落。
以上所述仅为本发明较佳的实施例,并非因此限制本发明的实施方式及保护范围,对于本领域技术人员而言,应当能够意识到凡运用本发明说明书及图示内容所作出的等同替换和显而易见的变化所得到的方案,均应当包含在本发明的保护范围内。
- 适用于肿瘤患者的营养治疗型配方及制备方法、用途
- 一类五元六元杂环化合物及其制备方法和治疗肿瘤的用途
- 一种以四苯乙烯吲哚衍生物为光敏剂的纳米复合材料及制备方法和在肿瘤治疗方面的应用
- 配合肿瘤手术治疗的复合益生菌菌剂、其制备方法及用途
- 一种用于肿瘤血管靶向治疗的疏水剂及其制备方法和用途
