一种天然产物微量活性成分筛选系统及其使用方法与应用
文献发布时间:2024-01-17 01:26:37
技术领域
本发明属于天然药物筛选技术领域,特别涉及一种天然产物微量活性成分筛选系统及其使用方法与应用。
背景技术
中药等天然产物是药物先导化合物的重要来源,如何高通量、高效率地从复杂天然产物中发现有效成分是当前亟待解决的技术问题。
传统的活性追踪分离(Activity-guided fractionation,AGF)是目前业内普遍采用的先导化合物筛选方法,该方法以天然产物(例如中药提取液)经过反复的分离纯化以后,得到分离状态的单体化合物,再经过质谱确定单体化合物结构,积累足够量的单体化合物后,再测试单体化合物的生物活性,直至获得具有生物活性的单体化合物。因此,该方法是一种低效、盲目的方法。该方法使用的样品用量大(提纯粗品需1g以上),增加了药物开发的成本;此外,该方法还存在活性评价与化学分离不同步、分离通量低、单次信息分析量有限、耗时费力等不足,极大地制约了新药开发的效率。
随着生物监测技术以及科学仪器的发展,近年来中药等天然产物中先导化合物的快速筛选方法获得了一些进展。在AGF模式的指导下发展起来的Off-line(离线)筛选模式(例如Off-line post-column assay,离线柱后检测),通过引入高效液相及高分辨率质谱构建的分析系统,实现了筛选流程的半自动化,但仍存在样品消耗量大、活性测试和结构鉴定实时数据不匹配等缺陷,因而导致活性先导化合物的检出效率低。On-line(在线)筛选模式(例如On-line post-column assay,在线柱后检测)在Off-line筛选模式的基础上,通过引入在线活性评测模块,将先导化合物分离分析-结构鉴定-活性评价一体化,提高分析通量的同时,实现了色谱、质谱以及活性谱图数据的实时同步匹配,提高了先导化合物的检出效率。然而,为了确保在线活性检测的灵敏度,On-line模式对样品的需求量仍然较大;此外高比例有机溶剂的存在以及有限的在线孵育时间使得活性评测数据存在极大的不确定性,限制药物靶标的同时也极易造成有效成分的漏检“,且检测灵敏度仍然较低,分辨率不佳。
因此,提供一种化学分离与活性评价互为匹配,且检测快速、样品需求量低、检测灵敏度高、分辨率高的新型高通量药物筛选系统,对天然产物中药物先导化合物发现具有重要意义。
发明内容
本发明旨在至少解决上述现有技术中存在的技术问题之一。为此,本发明的首要目的在于提供一种天然产物微量活性成分筛选系统,所述天然产物微量活性成分筛选系统能检测μM、nM、pM(即μmol/L、nmol/L、pmol/L)的活性成分,灵敏度高。本发明所述天然产物微量活性成分筛选系统所需要使用的待测样品的量极小,可达到nL级别,这大大降低了药物筛选成本,本发明所述天然产物微量活性成分筛选系统的分辨率可达到5-40点/峰水平,大大提高了检测效率。
本发明的第二目的在于提供一种天然产物微量活性成分筛选系统的使用方法。该使用方法操作简单,待检测样品经该筛选系统分析后,可获得实时匹配的色谱图、质谱图以及活性图谱,经各个谱图的对比、信息提取,可直观反应出样品中各成分的活性情况、分子结构情况以及光学谱图情况。
本发明的第三目的在于提供一种天然产物微量活性成分筛选系统在药物筛选领域中的应用。
本发明的首要目的通过下述技术方案实现:
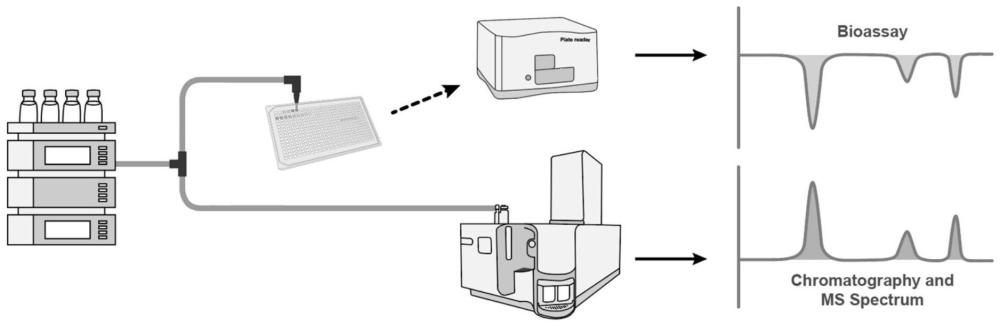
一种天然产物微量活性成分筛选系统,依次包括液相色谱系统、分流装置、质谱系统、微流分自动收集系统以及活性成分检测系统,所述液相色谱系统与分流装置连接,所述分流装置分别连接质谱系统与微流分自动收集系统,所述微流分自动收集系统连接活性成分检测系统。
优选地,所述微流分自动收集系统由精密机械臂系统或改装的CTC PAL系统、微流分收集装置及相应的控制软件组成,所述控制软件通过精密机械臂系统或改装的CTC PAL系统将微流分收集到微流分收集装置。
优选地,当所述微流分自动收集系统包括精密机械臂系统时,所述精密机械臂系统包括龙门架,Z轴位移平台,第一点样针,第一载物支架,Y轴位移平台,X轴位移平台;根据控制软件的设置,所述第一点样针将所需收集的成分从第一载物支架运送到微流分收集装置,完成微流分的自动收集;
或,当所述微流分自动收集系统包括改装的CTC PAL系统时,所述改装的CTC PAL系统包括X,Z轴机械臂,Y轴机械臂,第二点样针,第二载物支架,支撑架;根据控制软件的设置,所述第二点样针将所需收集的成分从第二载物支架运送到微流分收集装置,完成微流分的自动收集。
优选地,所述微流分收集装置为孔板或微阵列芯片。
优选地,当微流分收集装置为孔板时,所述孔板为96孔板、384孔板或1536孔板中的一种;或,当微流分收集装置为微阵列芯片(Micro-array)时,所述微阵列芯片为具有成千上万相互独立反应区域的微型芯片。
在选择微流分收集装置中,所述微阵列芯片相比较于孔板,虽然同样具有样品消耗低和分析通量高等优点,但是由于微阵列芯片形成液滴体积小,相对浓度高,微尺寸效应明显,检测灵敏度相较于384孔板或1536孔板有进一步的提高。
优选地,所述分流装置为多通路分流装置,例如三通分流装置、四通分流装置等。所述分流装置起到串联分流的作用,将液相色谱系统中出来的物质同时分流到质谱系统和微流分自动收集系统中;其中,液相色谱系统中出来的物质大部分分流到微流分自动收集系统中,进一步进入活性成分检测系统检测,少部分分流到质谱系统进一步分析,所述分流装置可接入多个微流分自动收集系统,同时进行多次流分收集。
优选地,所述液相色谱系统包括高效液相色谱系统或纳升液相色谱系统。
优选地,使用软件用来控制液相色谱系统和微流分自动收集系统,使得两个系统之间信号传递与液相色谱系统中的进样器同步,并控制微流分收集装置(孔板或微阵列芯片),实现按单个色谱峰分别进行收集。
优选地,所述液相色谱系统中使用的检测器为光学检测器(如紫外、荧光检测器等)或通用性检测器(点喷雾检测器、蒸发光散热检测器等)。
优选地,所述活性成分检测系统为多功能酶标仪、激光共聚焦显微镜或高内涵筛选仪。
优选地,所述活性成分检测系统检测方法为常规的高通量活性检测方法,不限于酶体系、细胞体系、活体体系的活性评估模型,进一步地,所述检测方法不限于紫外、荧光、生物成像技术、PCR测序技术等。
本发明的第二目的通过下述技术方案实现:
一种天然产物微量活性成分筛选系统的使用方法,包括以下步骤:
(1)取待测样品,加入液相色谱系统进行分离,分离得到的成分通过分流装置分别进入质谱系统和微流分自动收集系统,微流分自动收集系统的微流分收集装置收集到成分;所述质谱系统对获得的成分进行分析,得到质谱信息;
(2)将步骤(1)中微流分收集装置收集到的成分进行干燥,然后通过活性成分检测系统进行检测,获得成分的生物活性图谱,将步骤(1)通过质谱系统获得的质谱信息与生物活性图谱进行对照,从而筛选出活性成分。
优选地,步骤(1)中,所述待测样品为天然物质,例如为各种中药的提取液(例如黄栌提取液),植物提取液或动物提取液。
优选地,步骤(1)中,所述液相色谱系统以Diamonsil C18 column(250mm×4.6mm,5μm)色谱柱为固定相;以甲酸水溶液和甲醇为流动相。
优选地,所述液相色谱系统进行分离的过程中流动相为0.1%-0.2%质量分数的甲酸水溶液(标记为A)-甲醇(标记为B)进行线性梯度洗脱,梯度为:
0-10分钟,10%-30%甲醇,90-70%甲酸水溶液(即在流动相中,甲醇的体积为10%,质量分数为0.1%-0.2%的甲酸水溶液的体积为90%,甲醇的体积上升至30%,0.1%-0.2%质量分数的甲酸水溶液的体积为70%);
10-20分钟,30%甲醇,70%甲酸水溶液;
20-30分钟,30%-40%甲醇,70%-60%甲酸水溶液;
30-40分钟,40%-45%甲醇,60%-55%甲酸水溶液;
40-60分钟,45%-50%甲醇,55%-50%甲酸水溶液;
60-70分钟,50%-60%甲醇,50%-40%甲酸水溶液;
70-85分钟,60%-90%甲醇,40%-10%甲酸水溶液。
优选地,步骤(1)中,所述液相色谱系统的检测波长为250-254nm,流速为0.30-0.50mL/min。
优选地,步骤(2)中,在通过活性成分检测系统进行检测的过程中,加入靶蛋白和底物溶液来与待测样品所述成分混合,靶蛋白和底物溶液根据待检测的目标活性成分进行调整。
例如,筛选黄栌中胰蛋白酶抑制剂时,优选地,所述靶蛋白为酶溶液(trypsin溶液,胰蛋白酶溶液),所述底物溶液包括Na-苯甲酰-DL-精氨酸-对硝基酰胺盐酸盐。
本发明的第三目的通过下述技术方案实现:
一种天然产物微量活性成分筛选系统在药物筛选领域中的应用。
本发明相对于现有技术的优点以及有益效果如下:
本发明所述天然产物微量活性成分筛选系统依次包括液相色谱系统、分流装置、质谱系统/微流分自动收集系统、活性成分检测系统,各系统相互协调发挥作用,使得检测灵敏度高,需要使用的待测样品的量极小,且检测效率高。所述天然产物微量活性成分筛选系统能检测μM、nM、pM(即μmol/L、nmol/L、pmol/L)的活性成分,灵敏度高。本发明所述天然产物微量活性成分筛选系统需要使用的待测样品的量极小,可达到nL、pL、fL级别,这大大降低了药物筛选成本,分辨率可达到5-40点/峰水平。
所述微流分自动收集系统的功能为将液相的流分精准、有序、自动化收集在载体上,载体不限于微孔板(96、384、1536)以及自定义高通量孔板或阵列芯片。
附图说明
图1为本发明实施例1天然产物微量活性成分筛选系统示意图;
图2为本发明实施例1天然产物微量活性成分筛选系统流程框图;
图3为本发明实施例3微阵列芯片的结构示意图;
其中,100-液相色谱系统,200-分流装置,300-质谱系统,400-微流分自动收集系统,500-活性成分检测系统。
图4为改装的CTC PAL系统的结构示意图;
图5为精密机械臂系统的结构示意图。
其中,1-龙门架,2-Z轴位移平台,3-第一点样针,4-第一载物支架,5-Y轴位移平台,6-X轴位移平台;7-X、Z轴机械臂,8-Y轴机械臂,9-第二点样针,10-第二载物支架,11-支撑架。
具体实施方式
为了让本领域技术人员更加清楚明白本发明所述技术方案,现列举以下实施例进行说明。需要指出的是,以下实施例对本发明要求的保护范围不构成限制作用。
以下实施例中所用的原料、试剂或装置如无特殊说明,均可从常规商业途径得到,或者可以通过现有已知方法得到。
以下实施例中使用的纳升液相色谱系统的型号为Thermo U3000RSLC nano,高效液相色谱系统的型号为Agilent 1100,微流分自动收集系统的型号为改装的CTC PAL机械臂系统或自组装机械臂系统、活性成分检测系统的型号为Synergy
实施例1:基于384孔板的微流分自动收集系统的黄栌中活性成分(胰蛋白酶抑制剂)的筛选
一种天然产物微量活性成分筛选系统,依次包括高效液相色谱系统、三通分流装置、质谱系统/微流分自动收集系统、活性成分检测系统(Synergy
使用Cycle Composer(Cycle Composer是一种软件名称)软件控制微流分自动收集系统并与高效液相色谱系统软件连接,使得两个系统之间信号传递与高效液相色谱系统中的进样器同步,并控制孔板,实现按单个色谱峰分别进行收集。高效液相色谱系统中使用的检测器为紫外检测器。
微流分自动收集系统由Cycle Composer软件、改装的CTC PAL机械臂系统以及微流分收集装置(流分收集器)组成,通过三通分流装置与高效液相色谱系统串联后,实现微流分的自动收集。所述微流分收集装置为384孔板。
图1为本发明实施例1天然产物微量活性成分筛选系统结构示意图。图1中的100表示高效液相色谱系统,200表示三通分流装置,300表示质谱系统,400微流分自动收集系统,500表示活性成分检测系统。
图4为改装的CTC PAL系统的结构示意图,所述改装的CTC PAL系统包括X、Z轴机械臂,Y轴机械臂,第二点样针,第二载物支架,支撑架;根据控制软件的设置,所述第二点样针将所需收集的成分从第二载物支架运送到微流分收集装置,完成微流分的自动收集。
上述天然产物微量活性成分筛选系统的使用方法,包括以下步骤:(1)取待测样品,加入高效液相色谱系统进行分离,液相色谱系统以Diamonsil C18 column(250mm×4.6mm,5μm)色谱柱为固定相,以0.1%质量分数的甲酸水溶液(标记为A)和甲醇(标记为B)为流动相进行线性梯度洗脱,梯度为:
0-10分钟,洗脱溶液的组成为体积占比为10%-30%甲醇和体积占比为90-70%甲酸水溶液(即在流动相中,甲醇的体积为10%,甲酸水溶液的体积为90%,甲醇的体积上升至30%,甲酸水溶液的体积为70%,其中甲酸水溶液的质量分数为0.1%-0.2%);
10-20分钟,洗脱溶液的组成为体积占比为30%甲醇和体积占比为70%甲酸水溶液;
20-30分钟,30%-40%甲醇,70%-60%甲酸水溶液;
30-40分钟,40%-45%甲醇,60%-55%甲酸水溶液;
40-60分钟,45%-50%甲醇,55%-50%甲酸水溶液;
60-70分钟,50%-60%甲醇,50%-40%甲酸水溶液;
70-85分钟,60%-90%甲醇,40%-10%甲酸水溶液;检测波长为254nm,流速0.50mL/min;
分离得到的成分通过三通分流装置分别进入质谱系统和微流分自动收集系统(产物占总量的2/3),微流分自动收集系统的384孔板收集到成分;
(2)将步骤(1)收集到的成分进行干燥(35℃真空干燥,溶剂挥发),取出干燥后的384孔板,使用Thermo Multidrop 384分液器将等量待测酶溶液(trypsin溶液,胰蛋白酶溶液)和底物溶液(Na-苯甲酰-DL-精氨酸-对硝基酰胺盐酸盐)加入384孔板,再将384孔板送入Synergy
步骤(1)中,待测样品为黄栌提取液,黄栌提取液的制备过程为:取x g黄栌粉碎成粉末状,乙醇溶解,100℃加热回流90分钟,提取两次,提取液旋转蒸发,干燥称重,然后与xmL甲醇混合,经过0.22微米孔径的滤膜过滤,制得黄栌提取液。
本实施例1获得黄栌提取液中的活性成分包括Methyl gallate(没食子酸甲酯)、Eriodictyol(圣草素)、Fustin(黄栌色素)、Butein(紫铆花素)、Taxifolin(紫杉叶素)、Fisetin(漆黄素)、Sulfuretin(硫黄菊素)、Quercetin(槲皮素)。
其中,Methyl gallate(没食子酸甲酯)在本实施例1中的分辨率分别为:6点/峰,灵敏度为:12μM;Butein(紫铆花素)在本实施例1中的分辨率分别为:7点/峰,灵敏度为7μM。
实施例2:基于1536孔板的微流分自动收集系统的黄栌中活性成分(胰蛋白酶抑制剂)的筛选
与实施例1相比,实施例2的区别仅在于,实施例2中使用1536孔板代替实施例1中的384孔板,实例2中使用自组装精密机械臂系统代替实例1中的改装的CTC PAL机械臂系统。本实施例2获得黄栌提取液中的活性成分包括Methyl gallate(没食子酸甲酯)、Eriodictyol(圣草素)、Fustin(黄栌色素)、Butein(紫铆花素)、Taxifolin(紫杉叶素)、Fisetin(漆黄素)、Sulfuretin(硫黄菊素)、Quercetin(槲皮素)。
其中,Methyl gallate(没食子酸甲酯)在本实施例2中的分辨率分别为:17点/峰,灵敏度为:200nM;Butein(紫铆花素)在本实施例2中的分辨率分别为:17点/峰,灵敏度为765nM。
图5为精密机械臂系统结构示意图,所述精密机械臂系统包括龙门架,Z轴位移平台,第一点样针,第一载物支架,Y轴位移平台,X轴位移平台;根据控制软件的设置,所述第一点样针将所需收集的成分从第一载物支架运送到微流分收集装置,完成微流分的自动收集。
实施例3:基于微阵列芯片的黄栌中胰蛋白酶抑制剂的筛选
与实施例1相比,实施例3的区别仅在于,实施例3中使用型号为Thermo U3000的纳升液相色谱系统(流动相的流速为1000nL/min)代替实施例1中的高效液相色谱系统,且用微阵列芯片代替实施例1中的384孔板。实例3中使用自组装精密机械臂系统代替实例1中的改装的CTC PAL机械臂系统。
本实施例3获得黄栌提取液中的活性成分包括Methyl gallate(没食子酸甲酯)、Eriodictyol(圣草素)、Fustin(黄栌色素)、Butein(紫铆花素)、Taxifolin(紫杉叶素)、Fisetin(漆黄素)、Sulfuretin(硫黄菊素)、Quercetin(槲皮素)。
其中,Methyl gallate(没食子酸甲酯)在本实施例3中的分辨率分别为:35点/峰,灵敏度为:100pM;Butein(紫铆花素)在本实施例3中的分辨率分别为:32点/峰,灵敏度为75pM。
另外,也分别用上述实施例1-3记载的天然产物微量活性成分筛选系统来检测神经氨酸酶抑制剂奥司他韦,实施例1可实现1μM奥司他韦的检出,单峰分辨率约为8点/峰;实施例2可实现1nM奥司他韦的检出,单峰分辨率约为25点/峰;实施例3可实现1pM奥司他韦的检出,单峰分辨率约为30点/峰。
从上述实验结果可以看出,本发明天然产物微量活性成分筛选系统中采用384孔板、1536孔板、微阵列芯片对待测样品的检测灵敏度和分辨率依次提升。
上述实施例为本发明较佳的实施方式,但本发明的实施方式并不受上述实施例的限制,其他的任何未背离本发明的精神实质与原理下所作的改变、修饰、替代、组合、简化,均应为等效的置换方式,都包含在本发明的保护范围之内。
- 一种快速筛选天然产物活性成分的细胞膜磁性微球制备及其应用
- 复杂天然产物中活性成分筛选方法及应用
