一种桔梗细胞外囊泡复合微针贴片的制备方法
文献发布时间:2024-04-18 19:58:30
技术领域
本发明涉及中医药领域,具体是一种桔梗细胞外囊泡复合微针贴片的制备方法。
背景技术
自古以来,中医药是世界上最古老的草药之一,被人们广泛使用。中医药在人类疾病的预防和治疗中发挥着不可或缺的作用,特别是在类风湿性关节炎等慢性疾病中。近年来,随着提取分离技术的迅速发展,越来越多的天然植物活性成分逐步走入人们的视野,与化学合成药物相比,其具有低毒性、多靶点、协同作用更强的优点,因此被人们广为接受。然而活性成分因其自身水溶性差、生物利用度低、半衰期短的弊端限制了其临床应用。
随着纳米医学的快速发展,植物细胞外囊泡也逐渐进入人们视野,将天然植物的活性成分与纳米技术的结合成为一个新的发展趋势。越来越多的研究表明,将聚合物胶束、脂质体、纳米晶、微囊微球等纳米技术与中药活性成分结合可以改善其本身弊端,并且具有更好的靶向性、协同作用等优势,并且可以降低毒副作用,提高生物利用度。
细胞外囊泡(EV)是一种磷脂双分子层包裹的微纳米级生物颗粒,通过传递各种生物分子进而调节细胞通讯。几乎所有的活细胞都可以分泌EV,包括植物细胞。植物来源外泌体样纳米囊泡(Plant-derived exosomes-like nanovesicles,PDENs)已被发现在疾病治疗和药物递送方面具有显著优势,被认为具有广阔的药学应用前景。由于植物的天然来源和人们长期的饮食习惯,植物源性的PDVLNs作为治疗药物有几个明显的优势。首先,植物细胞外囊泡来自大多数可食用植物,且PDVLNs已被证明没有可检测到的毒性或免疫原性。其次,PDVLNs由于其绿色和可持续的植物来源而保证其环保性,植物也可以相对容易地获取,并且可以实现产业化生产。最后,植物没有人类致病病原体,相较于动物源性外泌体安全性可能更高。
桔梗,为桔梗科植物桔梗的干燥根已有相关文献表明桔梗有排脓消痈、宣肺利咽、止咳化痰的功效,具有宣肺、祛痰、利咽、排脓的药理作用,现代药理研究表明桔梗还有解热镇痛、抗炎、抗溃疡、免疫调节、保肝、抗肿瘤、抗高血糖、调血脂等多种药理作用。目前从中药桔梗中得到多种化学物质,主要活性成分主要为三萜皂苷类以及多糖类。基于以上优势,本研究首次分离获得了桔梗细胞外囊泡。基于外泌体囊泡的药物递送纳米平台在靶向性、生物相容性以及稳定性方面具有独特的优势。综上鉴于桔梗具有镇痛、抗炎、调节免疫等药理活性,本研究将从桔梗中分离出的细胞外囊泡与ROS响应性聚合物及可溶性微针结合,用于类风湿性关节炎的治疗。
木犀草素是一种天然黄酮类化合物,存在于菊花、金银花等多种中药中,具有多种药理活性。木犀草素通过抑制白细胞介素-2、γ干扰素的表达来抑制T细胞的增殖和活化,抑制小鼠NF-κB、p65蛋白入核和NF-κB抑制蛋白α的磷酸化,通过NF-κB信号通路抑制T细胞的功能,从而产生抑制免疫的作用;木犀草素能够减少CIA小鼠MMP-1、MMP-3的分泌和IL-6、IL-8、IL-15、TGF-β的表达,从而抑制RASF增殖,并部分阻碍其致病作用。
国内外有大量的研究人员在研究使用微针递送药物来治疗各种疾病,结果显示具有良好的治疗效果,溶解性微针具有各种物理化学特性的分子可以通过角质层迁移,从而促进患者的依从性。微针侵入表皮,在真皮中诱导微通道,使药物能够进一步融入全身循环。此外,通过设计微针聚合物含量,或通过改变工艺,可以实现所需的药物分布。因此将纳米制剂与微针结合可以实现药物的靶向蓄积和响应性释放,并通过绕过皮肤屏障层来增强药物直接进入皮肤的运输,解决了与传统透皮递送系统有关的问题。
基于此我们将桔梗细胞外囊泡与岩藻多糖、硫缩酮、木犀草素构建的ROS响应性纳米载体共孵育,获得一种新型智能工程化桔梗细胞外囊泡,并将其负载到可溶性微针中,用于类风湿性关节炎的治疗。
发明内容
针对上述技术问题,本发明提供了一种桔梗细胞外囊泡复合微针贴片的制备方法。
本发明为实现上述目的,通过以下技术方案实现:
一种桔梗细胞外囊泡复合微针贴片的制备方法,包括以下步骤:
S1.按照桔梗:PBS为1:3的比例将PBS加到桔梗中,榨取桔梗汁,经纱网过滤得滤液;
S2.将所述步骤S1中得到的滤液转移到离心管中,采用差速离心法在4℃下离心,弃去底部沉淀,取上清液;
S3.对所述步骤S2得到的上清液再离心2h,取沉淀,用PBS重悬;采用蔗糖密度梯度离心法分离不同粒径的囊泡混合物,随后用PBS重悬,即得桔梗细胞外囊泡溶液;
S4.将适量的硫缩酮溶于适量有机溶剂中,获得硫缩酮溶液;称取适量催化剂EDC和DMAP溶于适量有机溶剂中,待完全溶解,将其与硫缩酮溶液混合,在38-41℃的温度下反应2.5-3.5h得到活化的硫缩酮溶液;
S5.称取适量的木犀草素,取适量有机溶剂其溶解,待完全溶解后将混合溶液加入到所述步骤S4中得到的活化的硫缩酮溶液中,25℃室温反应24h后得到硫缩酮-木犀草素(TK-Lut)产物,用于后续实验;
S6.将一定量EDC和DMAP溶于适量有机溶剂,加入到所述步骤S5反应中,一定温度下活化硫缩酮另一端羧基;称取一定量岩藻多糖,用适量溶剂将其溶解,加入到活化的TK-Lut溶液中,25℃室温反应24h后,透析、冻干即得到纯化的Fuc-TK-Lut,即两亲性载体材料;
S7.将所述步骤S6获得的两亲性载体材料溶解,获得空白载体溶液;配制一定量的姜黄素(Cur)溶液,将所述空白载体溶液与姜黄素溶液混合,超声、透析后即得到具有ROS敏感的纳米制剂FTL@Cur,离心取上清液进行冻干保存,用于后续实验;
S8.将所述步骤S3获得的桔梗细胞外囊泡与所述步骤S7制得的FTL@Cur室温下共孵育6h即得一种具有活性氧(ROS)响应性纳米修饰桔梗细胞外囊泡;
S9.称取适量的透明质酸和岩藻多糖按一定比例混合,加入8-11ml的所述步骤S8得到的共孵育后的桔梗细胞外囊泡与FTL@Cur溶液,搅拌溶解,制得基质溶液;
S10.将0.8-1.2ml的所述步骤S9得到的基质放入微针模具中,真空干燥箱抽真空、晾干,即得到溶解性微针。
进一步的,所述步骤S4中硫缩酮与EDC和DMAP混合物的摩尔比为1:1.5。
进一步的,所述步骤S5中硫缩酮与木犀草素的摩尔比为1:1。
进一步的,所述步骤S6中岩藻多糖与TK-Lut的摩尔比为1.5:1。
进一步的,所述步骤S7中两亲性载体材料与姜黄素的摩尔比为10:1。
进一步的,所述步骤S9中透明质酸与岩藻多糖的质量比为3:2。
进一步的,所述步骤S3中蔗糖梯度分别为8%、30%、45%、60%。
进一步的,溶解所述硫缩酮溶液、EDC溶液和DMAP溶液的有机溶剂与溶解所述木犀草素溶液的有机溶剂、溶解姜黄素的溶剂均为无水级DMSO,溶解所述岩藻多糖溶液的溶剂为无水级甲酰胺。
对比现有技术,本发明的有益效果在于:
1、本发明通过将桔梗细胞外囊泡与ROS响应性纳米制剂共孵育制得一种具有活性氧(ROS)响应性纳米修饰桔梗细胞外囊泡,能够负载药物成分,避免胃酸作用下降解,保证药效;
2、通过将岩藻多糖与木犀草素制成纳米制剂,并将姜黄素负载其中,使得药物可以特异性集聚在炎症病灶部位,改善药物水溶性,提高生物利用度,更高效的治疗类风湿性关节炎;
3、利用活性氧的特点,结合炎症部位微环境特征,引用二硫键在高ROS的炎症部位特异性断裂,达到在炎症部位特异性释药的效果;
4、制备FTL空白载体,负载姜黄素,解决天然中药材溶解度差,生物利用度不高等关键性问题;
5、将共孵育后的桔梗细胞外囊泡与FTL@Cur溶液负载到可溶性微针中,利用微针递送药物能够提高经皮给药效率,从而使得类风湿性关节炎的治疗效果更好。
附图说明
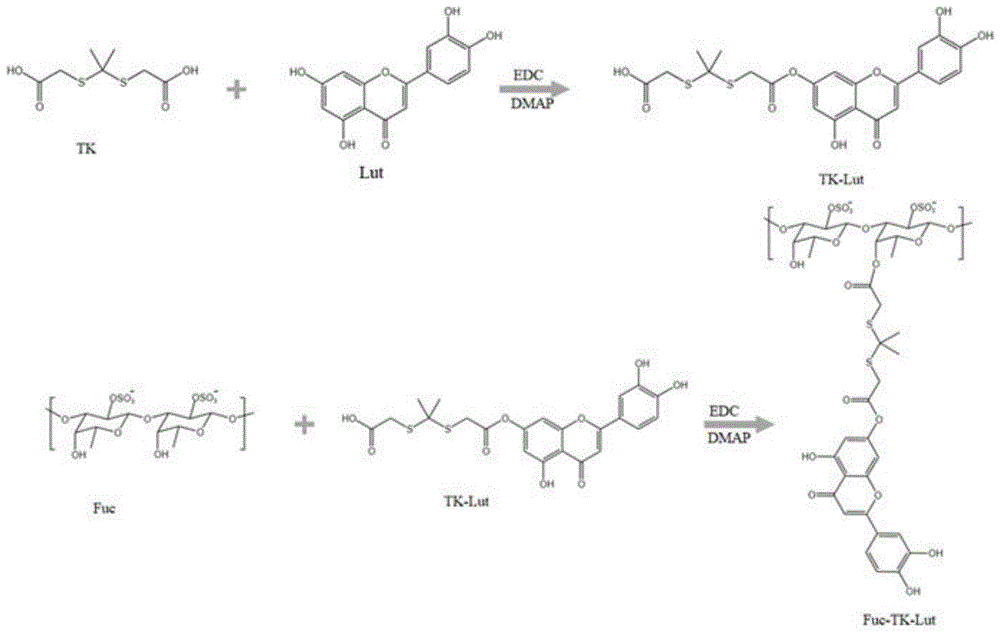
附图1是本发明的两亲性载体材料合成路线图。
附图2是本发明的两亲性载体材料的
附图3是本发明的纳米制剂图。
附图4是本发明的纳米制剂粒径图。
附图5是本发明的纳米制剂电位图。
附图6是本发明的纳米制剂透射电镜图。
附图7是本发明的负载ROS响应性纳米制剂的桔梗细胞外囊泡的透射电镜图。
附图8是本发明的空白载体(FTL)24h和48h细胞毒性实验对比。
附图9是本发明的负载药物载体与游离药24h的细胞毒性试验对比。
附图10是本发明的负载药物载体与游离药48h的细胞毒性试验对比。
附图11是本发明的RAW264.7浓度依赖摄取实验。
附图12是本发明的微针在扫描电镜下的形态。
附图13是本发明的微针在光学显微镜下的形态。
附图14是本发明的微针不同时间下在皮肤中的溶解性。
附图15是本发明的微针刺皮恢复实验。
附图16是本发明的不同制剂组对类风湿性关节炎的治疗效果。
具体实施方式
下面结合具体实施例,进一步阐述本发明。应理解,这些实施例仅用于说明本发明而不用于限制本发明的范围。此外应理解,在阅读了本发明讲授的内容之后,本领域技术人员可以对本发明作各种改动或修改,这些等价形式同样落于本申请所限定的范围。
实施例1:一种桔梗细胞外囊泡复合微针贴片的制备方法,包括以下步骤:
1、桔梗细胞外囊泡的制备:
(1)按照桔梗根:PBS=1:3(g/mL)的比例将PBS加到桔梗中,榨取桔梗汁,经纱网过滤得滤液;
(2)将滤液转移到50mL离心管中,采用差速离心法在4℃下依次经400g离心20min、800g离心20min、10000g离心20min后,弃去底部沉淀,取上清液;
(3)将步骤(2)中得到的上清液再经150000g离心2h,取沉淀,用PBS重悬。采用蔗糖密度梯度离心法分离不同粒径的囊泡混合物。分别配制8%、30%、45%、60%的蔗糖PBS溶液,先在超速离心管中加入2mL重悬液,用细长针头在底部加入2.5mL8%的蔗糖溶液,后用相同方法依次加入相同量30%、45%、60%的蔗糖PBS溶液,最后在最上层补加重悬液至离心管管口2mm处。经150000g离心2h后,收集蔗糖密度30%和45%之间的混合物条带,加入等量PBS重悬,在100000g离心条件下离心1h,洗去蔗糖,收集沉淀。用PBS重悬,即得桔梗细胞外囊泡溶液,并用BCA蛋白测定试剂盒测定膜蛋白含量。
2.ROS响应性纳米载体的制备:
选用硫缩酮作为高ROS敏感键,将其溶解,溶剂为无水级二甲基亚砜,获得硫缩酮溶液,EDC和DMAP分别溶于无水级二甲基亚砜,并将其溶液与硫缩酮溶液混合,40℃搅拌反应3h,反应完成后得到活化的硫缩酮溶液,以备后续反应使用,其中硫缩酮与EDC和DMAP的摩尔比为1:1.5;将木犀草素溶于适量的无水级二甲基亚砜,得到木犀草素溶液,将其加入到上述反应,室温搅拌24h即得到初步产物硫缩酮-木犀草素(TK-Lut)溶液用于后续实验,其中硫缩酮与木犀草素的摩尔比为1:1;称取适量EDC和DMAP溶于无水级二甲基亚砜,加入TK-Lut溶液中,40℃搅拌反应3h,活化硫缩酮另一端羧基;称取一定量的岩藻多糖溶于甲酰胺,得到岩藻多糖溶液加入到上述反应中室温搅拌24h后,用截留分子量2000Da的透析袋透析36h;透析完成后离心取出上清液进行冻干保存,得到FTR,即两亲性载体材料,其结构式如式1所示,用
3、基于ROS敏感的纳米制剂(FTL@Cur)的制备:
将上述获得的两亲性载体材料溶于无水级二甲基亚砜,浓度为5mg/mL;获得空白载体溶液;配置姜黄素溶液,溶剂为无水级二甲基亚砜,浓度为1mg/mL,将所述空白载体溶液与姜黄素溶液混合,超声十分钟后(载体材料与姜黄素的摩尔比为10:1)使用截留分子量为2000Da的透析袋进行透析反应24h,透析完成后,离心取上清液,用0.8μm微孔滤膜过滤,冻干保存,获得所述基于ROS敏感的纳米制剂。
4、将上述获得的桔梗细胞外囊泡与上述制得的FTL@Cur在室温下共孵育6h即得一种具有活性氧(ROS)响应性桔梗细胞外囊泡。
5、称取300mg的透明质酸与200mg的岩藻多糖按3:2的比例混合,加入10ml的所述步骤S8得到的共孵育后的桔梗细胞外囊泡与FTL@Cur溶液,搅拌溶解,制得基质溶液;将1ml的基质放入微针模具中,真空干燥箱抽真空、晾干,即得到溶解性微针。
实施例2:ROS敏感的纳米制剂的表征及性能实验:
1、纳米制剂的载药量、包封率测定:
实施例1制得的纳米制剂如图3所示,通过高效液相色谱法测定FTL@Cur的包封率和载药量。将1mL制备好的纳米制剂用甲醇破乳稀释成所需浓度,并过0.22μm的微孔滤膜,通过紫外分光光度法测定在波长为425nm处的吸光度,并按照公式计算纳米制剂的载药量和包封率。
载药量(%)=(制剂中所包载药物的含量/制剂总质量)×100%;
包封率(%)=(制剂中所包载药物含量/药物的初始加入量)×100%。
计算后得知本发明实施例1中载有姜黄素胶束的载药量为6.41%,包封率为76.73%。
本发明中聚合物胶束载体材料和姜黄素的重量比为10:1,对本发明来说是重要的。
3、FTL@Cur粒径和电位:
将制备好的FTL@Cur过0.80μm的微孔滤膜,然后用粒度仪进行检测FTL@Cur的粒径以及电位,实验结果如图4、5所示。
过0.8μm微孔滤膜后,粒径为146.9nm±1.23,粒径均匀电位为-22.2±0.49。
4、电镜检测:
将制备好的FTL@Cur采用铜网固定并且染色,用透射电镜拍摄FTL@Cur的外观形态如图6所示。负载ROS响应性纳米颗粒的桔梗细胞外囊泡的透射电镜如图7所示。
5、空白载体和游离药的细胞毒性评价:
采用MTT法,测定空白载体的培养基溶液,评价纳米制剂的细胞毒性,结果表明FTL空白胶束对RAW264.7细胞的损伤较小,在培养24h后,FTL空白胶束浓度为200μg/mL时,细胞存活率依然大于70%,在培养48h后,细胞存活率依然大于60%。因此证明FTL空白纳米胶束具有很低细胞毒性,对神经细胞几乎没有毒性,实验结果如图8所示。
同时本发明验证了游离姜黄素对RAW264.7细胞的毒性,通过MTT实验表明,当游离的姜黄素浓度达到20μg/mL时,处理RAW264.7细胞24h,发现细胞的存活率为75%以上,实验结果如图9所示;处理RAW264.7细胞48h,细胞的存活率为65%以上。实验结果如图10所示。上述两个实验充分的证明了本发明制备的纳米载体的安全性。
6、纳米制剂细胞摄取及分布研究:
利用激光共聚焦显微镜观察纳米制剂被RAW264.7细胞细胞内吞后在细胞内的分布情况,本发明以姜黄素(Cur)作为荧光染料,用我们制备的纳米胶束包裹姜黄素,随着浓度的增加,RAW264.7细胞的吞噬情况,并与游离姜黄素进行比较,实验结果表明:随着不同制剂摄取浓度的增加,细胞荧光强度会随之增加,这说明RAW264.7细胞对Free Cur和FTL@Cur的细胞摄取行为具有浓度依赖性,并且细胞对于FTL@Cur具有更高的摄取量,证明了纳米载体胶束具有更好的生物利用度,可以达到更好的治疗目的。实验结果如图11所示。
7、用具有微环境响应性的桔梗细胞外囊泡溶液溶解透明质酸和岩藻多糖制备成具有负载药物的微针基质,放入模具中制备成可溶性微针,自然晾干后扫描电镜如图12所示;光学显微镜下微针形态如图13所示;将制备好的微针刺入皮肤分别在0、30、60、120、180s取出,放在光学显微镜下观察,微针溶解情况如图14所示;微针刺入皮肤后,皮肤针孔可在十分钟内恢复,结果如图15所示。
综上所述,本发明针对天然产物活性成分不能有效的聚集在炎症部位,且不能特异性释放药物,将其活性成分制备成纳米制剂材料,负载天然药物活性成分,通过共孵育包裹于桔梗细胞外囊泡内,改善了其溶解度差,生物利用度低的缺点,并且提高了药物的稳定性。本发明构建的具有微环境响应性的桔梗细胞外囊泡,达到在炎症部位特异性释药的效果;提高药物的生物利用度的同时避免全身不良反应,更高效的治疗类风湿性关节炎。
- 一种高生物活性细胞膜仿生微囊泡及其制备方法与应用
- 一种治疗类风湿性关节炎的微针透皮给药贴片及其制备方法
- 一种微针减肥贴片及其制备方法
- 一种基于LBL法修饰肝素分离细胞外囊泡的方法
- 一种细胞外囊泡中RNA的提取方法
- 一种细胞外囊泡捕获或细胞外囊泡定量分析或细胞外囊泡内含物定量分析的试剂盒及方法
- 基于天然细胞外囊泡的球形核酸及其制备方法、向细胞递送细胞外囊泡的方法
