一种新型冠状病毒抗体检测试纸及其制备方法
文献发布时间:2024-04-18 20:00:50
技术领域
本发明涉及体生物医学检测技术领域,尤其涉及一种新型冠状病毒抗体检测试纸及其制备方法。
背景技术
新冠病毒是一种典型的β冠状病毒,国际病毒分类委员会将其命名为严重急性呼吸综合征冠状病毒2(SARS-CoV-2),其四种结构蛋白包括刺突蛋白(Spike,S)、包膜蛋白(Envelope,E)、膜蛋白(Membrane M)和核衣壳蛋白(Nucle ocapsil,N),是病毒组装和生成结构完整的病毒颗粒所必需的。新冠病毒感染靶细胞是通过其表面的刺突蛋白S与细胞受体血管紧张素转化酶2(Angiotensin-Converting Enzyme2,ACE2)特异性结合而完成的。刺突蛋白(S)是SARS-CoV-2的主要靶点,S1亚基中的RBD(receptor binding domain,RBD)结构域负责与ACE2受体结合,S2亚基负责将S蛋白固定在宿主细胞膜上,以促进病毒进入宿主细胞。ACE2作为受体介导SARS-CoV-2侵入宿主细胞。因此,阻断新冠病毒S蛋白与ACE2特异性结合是一个重要的抗病毒干预手段,在对抗各类病毒性感染疾病时发挥重要作用。
新型冠状病毒中和抗体,可与S蛋白的RBD结合从而阻断病毒与人体ACE2结合,表现出直接中和活性。目前在中和抗体检测中,主要通过真病毒或假病毒进行体外中和实验,检测技术水平要求高,且检测时间长,检测效率低。
为了提高检测效率,现有技术如CN 114594256 A公开的一种新型冠状病毒抗体检测方法及其试剂盒,利用胶体金免疫层析竞争法,将ACE2蛋白标记上胶体金,中和抗体可与ACE2蛋白竞争结合COVID-19病毒上的RBD蛋白,若检测样品中含有COVID-19中和抗体会阻断ACE2蛋白与RBD蛋白结合,显色结果较浅甚至无,便可实现对COVID-19中和抗体的快速检测,提高了检测效率。然而,该方法在中和抗体的浓度较小的情况下,显色结果较浅甚至无,灵敏度较低,不便于对感染情况或疫苗接种情况的判断,容易产生假阴性结果。
发明内容
本发明针对现有技术灵敏度和准确度不高的问题,提出一种新型冠状病毒抗体检测试纸及其制备方法,提高了检测灵敏度和准确度,同时实现了半定量。
第一方面,本发明首先提供一种新型冠状病毒抗体检测试纸,由样品垫、胶体金垫、硝酸纤维素膜和吸水纸组成,其中,所述胶体金垫包被有胶体金标记的COVID-19重组RBD蛋白;所述硝酸纤维素膜上依次设置有检测线T1、检测线T2和质控线C,其中,所述检测线T1上包被有ACE2蛋白,所述检测线T2上包被有COVID-19重组RBD蛋白,所述质控线C上包被有兔抗COVID-19重组RBD的单克隆抗体。
进一步地,所述ACE2蛋白的基因序列如SEQ ID NO.1所示。
进一步地,所述COVID-19重组RBD蛋白的基因序列如SEQ ID NO.2所示。
进一步地,所述胶体金标记的COVID-19重组RBD蛋白的制备方法如下:
步骤1:将胶体金溶液进行搅拌,用0.2mol/L碳酸钾调节pH值至8.5,逐滴缓慢加入COVID-19重组RBD蛋白,使蛋白的终浓度为10μg/ml,室温静置60分钟;
步骤2:将加入蛋白的胶体金溶液中加入10%的BSA溶液使其终浓度为1%,混匀后封闭30分钟或4℃过夜,7500r/min离心20分钟,弃上清,用金标缓冲液将离心的沉淀重悬,使其体积为原体积1/10,获得金标结合物,即胶体金标记的COVID-19重组RBD蛋白。
进一步地,步骤1中胶体金溶液的制备方法为:0.01%氯金酸溶液加入经硅化处理过的玻璃容器中,置于磁力加热搅拌器上,煮沸3分钟后,在搅拌状态下迅速一次性加入1%柠檬酸三钠水溶液,继续加热6~8分钟,冷却至室温后用纯化水恢复到100ml,用0.22μm滤膜过滤后装入洁净的玻璃瓶中,置于磁力搅拌器上,300g/min搅拌,用0.2mol/L碳酸钾溶液调节pH值至8.5,得到胶体金溶液。
进一步地,步骤2中所述金标缓冲液是由以下成分组成:0.02mol/LpH7.2的PBS、终浓度1%的牛血白蛋白、终浓度0.5%的蔗糖和终浓度0.01%的叠氮钠。
进一步地,所述COVID-19重组RBD蛋白,按照每1ml胶体金离心得到的金标结合物加入300μl金标抗原重悬液,混匀后喷涂在玻璃纤维膜上,喷涂量为25μl/cm
进一步地,所述ACE2蛋白用膜包被液稀释后,按照1.0μg/cm
第二方面,本发明还提供了上述的新型冠状病毒抗体检测试纸的制备方法,包括以下步骤:
S1、胶体金溶液的制备:0.01%氯金酸溶液加入经硅化处理过的玻璃容器中,置于磁力加热搅拌器上,煮沸3分钟后,在搅拌状态下迅速一次性加入1%柠檬酸三钠水溶液,继续加热6~8分钟,冷却至室温后用纯化水恢复到100ml,用0.22μm滤膜过滤后装入洁净的玻璃瓶中,置于磁力搅拌器上,300g/min搅拌,用0.2mol/L碳酸钾溶液调节pH值至8.5,得到胶体金溶液;
S2、胶体金标记的COVID-19重组RBD蛋白的制备:将胶体金溶液进行搅拌,用0.2mol/L碳酸钾调节pH值至8.5,逐滴缓慢加入COVID-19重组RBD蛋白,使蛋白的终浓度为10μg/ml,室温静置60分钟;将加入蛋白的胶体金溶液中加入10%的BSA溶液使其终浓度为1%,混匀后封闭30分钟或4℃过夜,7500r/min离心20分钟,弃上清,用金标缓冲液将离心的沉淀重悬,使其体积为原体积1/10,获得金标结合物,即胶体金标记的COVID-19重组RBD蛋白;
S3、胶体金垫的制备:每1ml胶体金离心得到的金标结合物加入300μl金标抗原重悬液,混匀后喷涂在玻璃纤维膜上,喷涂量为25μl/cm
S4、硝酸纤维素膜的制备:将ACE2蛋白用膜包被液稀释后,按照1.0μg/cm
S5、试纸的制备:将样品垫、胶体金垫、硝酸纤维素膜膜、吸水纸依次粘贴在洁净的PVC底板上,即得新型冠状病毒抗体检测试纸。
第三方面,本发明还提供了一种新型冠状病毒抗体检测试剂盒,包含上述任一项所述的新型冠状病毒抗体检测试纸以及比色卡,所述比色卡的颜色按照由深至浅依次包括四个等级,分别对应新型冠状病毒中和抗体标准品的浓度为15ng/ml、30ng/ml、50ng/ml和100ng/ml。
与现有技术相比,本发明的技术效果:
1、本发明提供的新型冠状病毒抗体检测试纸及试剂盒,在检测过程中,将样品滴入样品孔中,新型冠状病毒的中和抗体与胶体金标记的新型冠状病毒的重组RBD蛋白结合,从而阻止了胶体金标记的重组RBD蛋白与T1线上的ACE2蛋白结合,提高了检测的灵敏度,最低检出限为15ng/ml,同时中和抗体含量越低,T1显色越深,避免了假阴性的出现。
2、本发明通过设置包被重组RBD蛋白的T2线,可以阻断样本中ACE2和结合垫的新型冠状病毒RBD抗原标记物反应,消除不同个人体内不同ACE2含量引起的测试结果不一致情况,即通过T2线判断样本中ACE2和RBD反应,判断是否为非特异性结合,进一步确保测试结果的准确性。
3、本发明提供的新型冠状病毒抗体检测试纸,检测方便快捷,适用于血清/血浆/全血等血液样品,检测后,可根据预设的比色卡,实现对血液(血清/血浆/全血)样品中新型冠状病毒中和抗体的半定量检测。
附图说明
为了更清楚地说明本申请实施例或现有技术中的技术方案,下面将对实施例中所需要使用的附图作简单地介绍,显而易见地,下面描述中的附图仅仅是本发明中记载的一些实施例,对于本领域普通技术人员来讲,还可以根据这些附图获得其他的附图。
图1为本发明实施例1提供的ACE2的电泳纯度检测。
图2为本发明实施例2提供的重组RBD优化序列说明。
图3为本发明实施例2提供的重组RBD蛋白的电泳纯度检测。
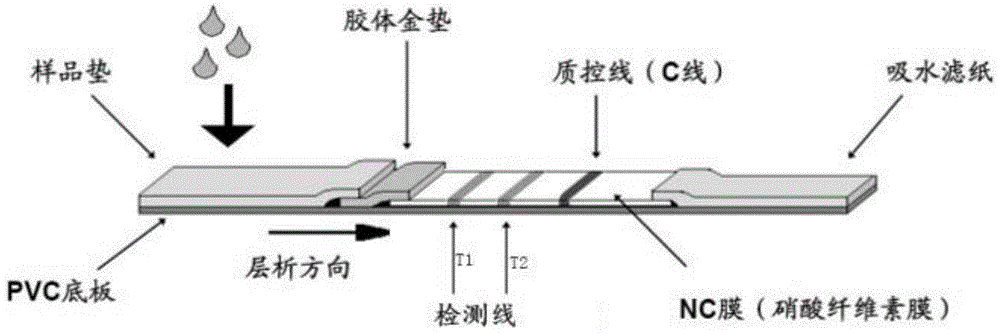
图4为本发明实施例3提供的检测试纸条的结构示意图。
图5为本发明实施例4提供的中和抗体标准溶液跑条结果。
图6为本发明实施例4提供的标准比色卡示意图。
图7为本发明实施例5提供的临床确诊2019-nCoV病人的血清样本试纸条检测结果。
图8为本发明实施例5提供的接种新冠疫苗1-2个月的样本试纸条检测结果。
具体实施方式
为了使本领域的技术人员更好地理解本发明的技术方案,下面将结合实施例和附图对本发明作进一步的详细介绍。显然,所描述的实施例仅仅是本发明一部分实施例,而不是全部的实施例。基于本发明中的实施例,本领域普通技术人员在没有做出创造性劳动前提下所获得的所有其他实施例,都属于本发明保护的范围。
下述实施例中的实验方法,如无特殊说明,均为常规方法。
下述实施例中所用的试验材料,如无特殊说明,均为自常规生化试剂商店购买得到的。
实施例1ACE2蛋白的表达与纯化
1实验材料
E.coil BL21(DE3)、IPTG、卡那霉素来自北京索莱宝公司;Ni-NTA蛋白纯化树脂来自全式金公司;SDS-PAGE凝胶快速配制试剂盒来自北京阳光英锐生物科技有限公司。
2实验方法
2.1基因合成
根据NCBI中Human ACE2蛋白基因序列(序列号为NM_021804.3),截取ACE2胞外区序列(如SEQ ID NO.1所示),将序列通过XhoⅠ和KpnⅠ合成至pET30a(+)载体中。
2.2转化
取合成后的重组质粒加入100μl刚刚融化的BL21(DE3)感受态中,经热激法转化后,将菌液涂于卡那霉素抗性平板中,37℃培养12h。挑取单菌落置于4ml卡那霉素抗性的LB培养基中进行培养,培养12h后进行鉴定,将鉴定正确的菌液进行保菌,置于-80℃保存。
2.3纯化
将-80℃保存的菌液取50μl加入卡那霉素抗性培养基中,37℃、200rpm培养12h。再按照1:100的比例将试管中的菌液接种至摇瓶中培养。当菌液OD600值为0.6~0.8时,加入0.6mmol/L的IPTG,37℃、200rpm诱导6h。
将诱导后的菌液4℃、8000rpm离心10min,用含8mol/L尿素,10mmol/L咪唑的PBS缓冲液重悬菌体,体积为菌液体积的1/15~1/20,重悬后置于冰上进行超声破碎,当液体变澄清后停止。4℃、12000rpm离心5min后收集上清,将上清与Ni-NTA蛋白纯化树脂充分混匀,放置4℃缓慢结合过夜。按照Ni-NTA蛋白纯化树脂说明书所述步骤配制相关试剂并进行纯化。
将纯化后的蛋白转移至10KD超滤离心管内,4℃、3500rpm离心15min,离心后再加入PBS缓冲液使尿素浓度降低至2.5mol/L,并继续离心将蛋白进行浓缩。浓缩后蛋白通过SDS-PAGE进行鉴定及纯度分析,结果如图1所示。
实施例2COVID-19重组RBD蛋白的表达与纯化
1实验材料
OPM-293 CD05培养基、OPM-293 ProFeed无蛋白质补料来自奥蒲迈公司;PEI来自Polysciences公司;葡萄糖来自天津市永大化学试剂有限公司;Ni-NTA蛋白纯化树脂来自全式金公司;SDS-PAGE凝胶快速配制试剂盒来自北京阳光英锐生物科技有限公司。
2实验方法
2.1基因优化与合成
根据NCBI中SARS-Cov-2019-Delta全长序列(序列号OM108132.1)(或SARS-Cov-2019-Omicron全长序列,序列号OM095411.1)中RBD蛋白序列,在不改变氨基酸序列的前提下,再根据HEK 293细胞密码子偏爱性采用GenSmart
2.2转染
转染提前1天按0.8×10
2.3纯化
将细胞上清与含10mmol/L咪唑的PBS缓冲液等体积混合,再与Ni-NTA蛋白纯化树脂充分混匀,按照Ni-NTA蛋白纯化树脂说明书所述步骤配制相关试剂并进行纯化。将纯化后的目的蛋白转移至10KD超滤离心管内进行浓缩。浓缩后蛋白通过SDS-PAGE进行鉴定及纯度分析,结果如图3所示。
实施例3新型冠状病毒抗体检测试纸的制备
1胶体金的制备:
取氯金酸1g,加纯化水定容至100ml,用0.22μm滤膜过滤后装入洁净的玻璃容器中,冷藏避光保存。取1%氯金酸溶液加入到适量的纯化水中,使氯金酸溶液的浓度为0.01%。取0.01%氯金酸溶液加入经硅化处理过的玻璃容器中,置于磁力加热搅拌器上,煮沸3分钟后,在搅拌状态下迅速一次性加入1%柠檬酸三钠水溶液1.3ml,继续加热6~8分钟,冷却至室温后用纯化水恢复到100ml,用0.22μm滤膜过滤后装入洁净的玻璃瓶中,胶体金溶液置于2~8℃保存,在使用前目视胶体金外观,应呈酒红色,液面无油状漂浮物,容器底部无黑色颗粒物凝集。
2金标结合物的制备:
(1)最佳pH值:取1ml胶体金溶液于1.5ml离心管中,用0.2mol/L的K
表1不同pH值下用胶体金标记的重组RBD蛋白的吸光度
从表1中可以看出,当pH值为8.5时,制备得到的胶体金标记重组RBD蛋白的吸光度值最大,说明在该pH值下制备的胶体金标记重组RBD蛋白溶液最稳定,即最佳pH值为8.5。
(2)最佳蛋白量:取1ml胶体金溶液于1.5ml离心管中,用0.2mol/L的K
表2不同蛋白量下用胶体金标记的重组RBD蛋白的吸光度
从表2中可以看出,当pH值为8.5时,重组RBD蛋白的加入量为10μg时,制备得到的胶体金标记重组RBD蛋白的吸光度值最大,即最佳蛋白量为10μg/ml。
(3)封闭、重悬:将加入蛋白的胶体金溶液中加入10%的BSA溶液使其终浓度为1%,混匀后封闭30分钟或4℃过夜,7500r/min离心20分钟,弃上清,用金标缓冲液(0.02mol/L PBS pH7.2、牛血白蛋白终浓度1%(m/V)、蔗糖终浓度0.5%(m/V)和叠氮钠终浓度0.01%(m/V))将离心的沉淀重悬,使其体积为原体积1/10,即为金标结合物,冷藏保存备用。
3金标结合垫的制备:每1ml胶体金离心得到的金标结合物加入300μl金标抗原重悬液(0.02mol/L PBS pH7.2、牛血白蛋白终浓度1%(m/V)、蔗糖终浓度0.5%(m/V),混匀,喷涂在玻璃纤维膜上(金标结合物喷涂量为25μl/cm
4硝酸纤维素膜(NC膜)的包被:将ACE2蛋白用包被液(0.02mol/L PBS,1.5%蔗糖)稀释,按照1.0μg/cm喷于硝酸纤维素膜上,作为检测线T1;将RBD蛋白用包被液(0.02mol/LPBS,1.5%蔗糖)稀释,按照1.0μg/cm喷于硝酸纤维素膜上,作为检测线T2。将兔抗RBD的单克隆抗体用膜包被液(0.02mol/L PBS,1.5%蔗糖)稀释,按照1.0μg/cm喷于硝酸纤维素膜上检测线下5mm处,作为质控线C线。将包被好的硝酸纤维素膜37℃干燥3小时后,密封保存。
5大板的制备:按图4所示,将各组件(样品垫、胶体金垫、NC膜、吸水纸等)按次序粘贴在洁净的PVC底板上,粘贴完毕后加干燥剂,密封保存。
6成品组装
切条取大板,将其切割成宽为4mm的试纸单条。
组装把切好的试纸单条装配到塑料卡的底座凹槽,盖上塑料卡的上盖,压紧,再用压壳机进行压卡,形成试纸条。
包装单个试纸条、干燥剂及塑料滴管等一起放入铝箔袋中,用封口机密封。
实施例4检出限的检验
新型冠状病毒抗体检测试纸条检出限的检测:配制一系列浓度的新型冠状病毒中和抗体标准品溶液(15ng/ml、30ng/ml、50ng/ml、100ng/ml、200ng/ml),使用实施例3制备的试纸进行跑条检测。图5为跑条结果,从图6中可以看出,随着中和抗体浓度的升高,检测线T1上的颜色逐渐变浅直至消线。当标准品中新型冠状病毒中和抗体为15ng/ml时,检测线T1线比样本稀释液的T1线浅,说明中和抗体阻断了胶体金标记的重组RBD蛋白与T1线的ACE2蛋白结合,使T1线变浅;分别检测新冠中和抗体标准品浓度30ng/ml、50ng/ml和100ng/ml,T1线如图5所示,随着中和抗体浓度的增加,T1线逐渐变浅,当标准品中新型冠状病毒中和抗体为200ng/ml时,检测线T1线出现消线。因此将15ng/ml作为新冠中和抗体的最低检出限。同时中和抗体含量越低,T1显色越深,便于比对和判断,避免了假阴性的出现,提高了检测的灵敏度。
根据上述新型冠状病毒中和抗体标准品溶液T1线的颜色固定比色卡的颜色等级,如图6所示,检测样品时,可将样品的T1线颜色与比色卡相比较。当颜色比15ng/ml深且比样本稀释液浅时,说明样本中中和抗体浓度在0-15ng/ml之间;当T1线颜色比30ng/ml深且比15ng/ml浅时,说明样本中中和抗体浓度在15-30ng/ml之间;当T1线颜色比50ng/ml深且比30ng/ml浅时,说明样本中中和抗体浓度在30-50ng/ml之间;当T1线颜色比100ng/ml深且比50ng/ml浅时,说明样本中中和抗体浓度在50-100ng/ml之间;当T1线颜色比100ng/ml浅且T1线未出现消线现象,说明样本中中和抗体浓度在100-200ng/ml之间;当T1线颜色出现消线现象,说明样本中中和抗体浓度在大于200ng/ml。
实施例5样本检测
参照实施例3制备试纸,测试接种新型冠状疫苗1-2个月的样本5例(全血,已灭活)、临床确诊2019-nCoV病人的血清样本5例(已灭活)。分别于加样孔处滴加100μl血液样本,室温反应15min后判定结果。
如图7所示,1~5号试纸条检测样本为临床确诊2019-nCoV病人的样本(全血,已灭活),T2线均显色,说明均有新冠病毒抗体;1号、2号和3号的T1线颜色相近,根据比色卡得知,当T1线颜色比100ng/ml深且比50ng/ml浅时,说明样本中中和抗体浓度在50-100ng/ml之间;4号和5号的T1线颜色相近,根据比色卡得知,当T1线颜色比30ng/ml深且比15ng/ml浅时,说明样本中中和抗体浓度在15-30ng/ml之间。
如图8所示,6~10号试纸条为接种新型冠状疫苗1-2个月的样本(血清或血浆,已灭活),6号样本T1和T2均显色,T2显色,说明体内有新型冠状病毒抗体,T1显色,根据比色卡得知,当T1线颜色比15ng/ml深且比样本稀释液浅时,说明样本中中和抗体浓度在0-15ng/ml之间;7号样本T1和T2均显色,T2显色,说明体内有新型冠状病毒抗体,T1显色,根据比色卡得知,当T1线颜色比100ng/ml深且比50ng/ml浅时,说明样本中中和抗体浓度在50-100ng/ml之间;8号样本T1和T2均显色,T2显色,说明体内有新型冠状病毒抗体,T1显色,根据比色卡得知,当T1线颜色比50ng/ml深且比30ng/ml浅时,说明样本中中和抗体浓度在30-50ng/ml之间;9号样本T1和T2均显色,T2显色,说明体内有新型冠状病毒抗体,T1显色,根据比色卡得知,当T1线颜色比100ng/ml深且比50ng/ml浅时,说明样本中中和抗体浓度在50-100ng/ml之间;10号样本T1和T2显色较弱,T2显色,说明体内有新型冠状病毒抗体,T1显色,根据比色卡得知,当T1线颜色比100ng/ml深且T1线未出现消线现象,说明样本中中和抗体浓度在100-200ng/ml之间。
- 近距离煤层群老空区注氮-抽放分阶瓦斯稀释与置换方法
- 一种协同抽采刀柱式老空区及下煤层煤层气的方法
