一种高通量淋巴肿瘤细胞微流控检测芯片及其检测方法
文献发布时间:2023-06-19 11:40:48
技术领域
本发明属于微流控技术领域,特别涉及一种高通量淋巴肿瘤细胞微流控检测芯片。
背景技术
微流控技术又称芯片实验室,它可以以宏观上进行的生物化学反应整合到一个几平方厘米的芯片内。考虑到细胞的尺寸在微米级别,这与微流控芯片中的通道尺寸相当,所以微流控芯片在单细胞的研究中越来越受到关注。
最早用于单细胞研究的微流控芯片是Quake芯片,该芯片集成有复杂的泵阀系统,可以对单细胞进行操控。之后随着液滴技术的发展,出现了drop-seq技术,该技术极大的提高了单细胞测序的通量。另外还有一些通过微结构进行单细胞捕获及分析的微流控芯片相继出现。但是,现有高通量单细胞测序中,由于在液滴形成过程中单细胞和单个微珠的包被都服从泊松分布,细胞的利用率极低(1%左右),而淋巴肿瘤细胞的在血液中流动性强,难以捕获。
发明内容
本发明的目的在于,克服现有技术中的不足之处,提供一种高通量淋巴肿瘤细胞微流控检测芯片,解决了现有技术中淋巴肿瘤细胞难以捕获的技术难题,使用本发明可实现对流动性强的单个细胞的捕获和操控,操作方便,灵活性高。
本发明的目的是这样实现的:一种高通量淋巴肿瘤细胞微流控检测芯片,包括上层芯片本体、中层芯片本体和下层芯片本体,所述中层芯片本体在上层芯片本体和下层芯片本体之间,中层芯片本体固定在上层芯片本体的下侧,所述上层芯片本体朝上的一端排布有至少一个进液池,上层芯片本体朝下的一端设有若干反应通道,所述反应通道包括若干连接在一起的细胞捕获通道本体,首端的细胞捕获通道本体与进液池连通,相邻细胞捕获通道本体之间相互连通,所述下层芯片本体上排布有至少一组检测单元,所述检测单元包括排布在下层芯片本体上的若干与细胞捕获通道本体一一对应的检测槽,所述检测槽覆盖对应的细胞捕获通道本体所在区域,所述细胞捕获通道本体和中层芯片本体均为可溶解材料。
为了进一步实现反应通道对细胞的捕获,所述反应通道还包括主通道本体,所述主通道本体的一端与进液池连通,细胞捕获通道本体在长度方向上的两端分别连接有主进液通道本体一和主进液通道本体二,主通道本体的另一端至少与一个首端的主进液通道本体一连接,所述主进液通道本体一和主进液通道本体二之间还连接有次进液通道本体,所述细胞捕获通道本体的一端开有足够让细胞穿过的进液孔,细胞捕获通道本体的另一端开有出液孔,所述出液孔比进液孔小,细胞无法穿过出液孔,主通道本体、主进液通道本体一、主进液通道本体二和次进液通道本体足以让细胞穿过,相邻两个细胞捕获通道本体之间,前面的主进液通道本体二远离细胞捕获通道本体的一端与后面的主进液通道本体一的一端连接,所述检测槽内设有包被有细胞抗体的磁珠,所述下层芯片本体的两端排布有若干组与检测单元一一对应的入液口和排液口,入液口贯穿对应的检测单元与排液口连通,所述下层芯片本体的底部排布有若干偏离检测单元设置的感应磁铁。
使用微流控检测芯片检测淋巴肿瘤细胞的方法,包括以下步骤,
(1)使用上固定板和下固定板将检测芯片固定住,将用于往进液池内通入液体的接头插装在上固定板上,接头的出液孔与进液池连通;
(2)将固定好的芯片放置在磁铁上,使检测单元中的所有磁珠固定在芯片上;
(3)通过接头上的注射器往对应的进液池内输入稀释过后的人体血液,待所有细胞被捕获在细胞捕获通道本体内,转至步骤(4);
(4)通过注射器往进液池内通入PBS缓冲液,洗去反应通道内多余的细胞;
(5)通过注射器往进液池内通入牛血清白蛋白,使牛血清白蛋白与反应通道内所有可能与淋巴肿瘤细胞抗体相结合的位点结合;
(6)通过注射器往进液池内通入PBS缓冲液,使PBS缓冲液流进整条反应通道;
(7)通过注射器经进液池往反应通道内通入带有酶标二抗的水相,待酶标二抗完成对细胞的特异性捕获后转至步骤(8);
(8)通过注射器经进液池往反应通道内通入醋酸,溶解细胞捕获通道本体和中层芯片本体,被酶标二抗捕获的位于细胞捕获通道本体内的细胞落入对应的检测槽内;
(9)经各个入液口往对应的检测单元的各个检测槽内通入PBS缓冲液,从排液口排出的废液排进废液池,撤去磁铁;
(10)经各个入液口往对应的检测单元的各个检测槽内通入化学发光试剂,使得化学发光试剂与HRP酶结合;
(11)抽出下层芯片本体,将其放置在检测箱内,检测箱的底部设有给芯片提供光源的发光灯,打开灯和相机,检测结束,导出相机的图像,发光的单元对应需要进行分析的淋巴肿瘤细胞,未发光的检测单元表明未捕获到细胞或者淋巴肿瘤细胞抗体捕获细胞错误。
为了进一步实现芯片的发光检测,还包括检测壳体,所述检测箱设置在检测壳体内,检测箱正上方的检测壳体内固定有成像镜,所述成像镜从下往上倾斜,成像镜覆盖检测箱朝上的开口所在区域,所述检测箱的底板上侧连接有检测底座,所述检测底座上侧排布有若干发光灯,检测底座上侧还排布有若干电磁铁,所述相机的镜头相对成像镜设置,检测壳体上连接有用于调节电磁铁的磁感应强度的旋钮,芯片可刚好放置在检测箱内。
作为本发明的进一步改进,检测箱的下部开有抽气口,所述抽气口在电磁铁的上方,抽气口上方的检测箱上排布有至少两个可滑动地连接在检测箱上且用于支撑芯片的支撑杆,所述支撑杆可伸进检测箱内。
为了进一步提高成像的清晰度,所述步骤(11)中,在放置芯片前,推动支撑杆,使支撑杆推进检测箱内,将芯片放置在支撑杆上;打开电磁铁后,将支撑杆收回,使支撑杆远离检测箱的腔体,粗调旋钮,调节芯片的浮空高度,使芯片稳定浮空在检测箱内,微调旋钮,使成像清晰,停止调节,根据各个检测槽内的发光情况,选择发光的检测槽,抽取样液得到需要的单个细胞。
本发明与现有技术相比,能自动完成对淋巴肿瘤细胞的分选,减少常规分选过程中过多的人为操作,降低细胞损伤甚至死亡的概率;芯片结构简单,引入二抗进行检测,被限制在下层芯片的磁珠具有灵活性,撤去磁铁即可完成对特定细胞的最终捕获;本申请中先在上层芯片本体注入酶标二抗,完成对单个细胞的负极,再溶解中层芯片本体,使细胞进入下层芯片本体的检测槽内,再次被磁珠上包被的特异性抗体捕获,两侧特异性识别大大减少了抗体由于捕获错误细胞而出现的假阳性现象的概率,提高检测的准确性和纯度;检测过程中,检测壳体上设有控制板,旋钮与控制板电连接,旋钮将电流调节信号发送给控制板,控制板根据接收到的调节信号调节电磁铁的线圈的供电电流,采用电磁铁、感应磁铁及对电磁铁通入电流大小的控制,能将芯片在任意高度架住,减小空间占用,提高空间利用率。
附图说明
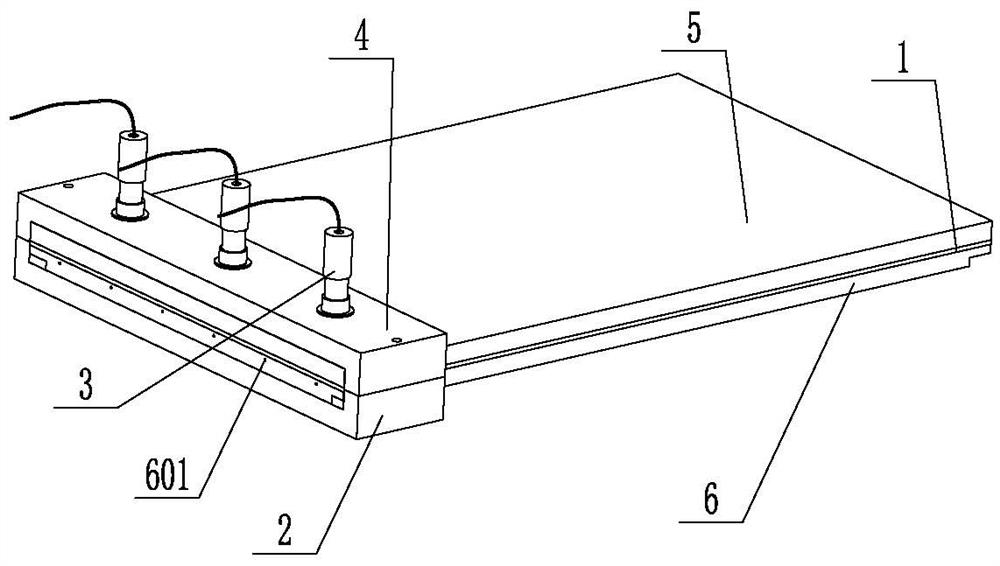
图1为本发明中高通量淋巴肿瘤细胞微流控检测芯片的立体结构图。
图2为本发明中高通量淋巴肿瘤细胞微流控检测芯片的爆炸结构图。
图3为本发明中上层芯片本体的立体结构图一。
图4为本发明中上层芯片本体的立体结构图二。
图5为本发明中细胞通道本体、主进液通道本体一、主进液通道本体二和次进液通道本体连接在一起时的局部结构放大图。
图6为本发明中下层芯片本体的立体结构图一。
图7为本发明中下层芯片本体的立体结构图二。
图8为本发明中接头的立体结构图。
图9为本发明中检测设备的立体结构图。
图10为本发明中检测设备的内部结构图。
图11为本发明中检测箱体和支撑杆连接的结构图。
图12为本发明中实现芯片浮空的结构图。
其中,1中层芯片本体,2下固定座,3接头,301导头,302注射器,303导管,304注射孔,305卡扣,4上固定座,5上层芯片本体,501进液池,502反应通道,502a细胞捕获通道本体,502b主通道本体,502c主进液通道本体一,502d次进液通道本体,502e主进液通道本体二,502f进液孔,502g出液孔,502h分进液通道本体,503出液口,6下层芯片本体,601入液口,602排液口,603检测单元,603a检测槽,604缺口,7活动门,8旋钮,9检测壳体,10相机,11控制板,12成像镜,13镜框,14抽气口,15支撑杆,1501推拉手柄,16发光灯,17检测底座,18电磁铁。
具体实施方式
下面结合附图对本发明进行进一步说明。
在阐述本发明的具体实施方案之前,定义本文使用的术语如下:
术语“PDMS”是指:聚二甲基硅氧烷。
术语“HRP”是指:辣根过氧化物。
如图1~8所示的一种高通量淋巴肿瘤细胞微流控检测芯片,包括上层芯片本体、中层芯片本体和下层芯片本体,中层芯片本体在上层芯片本体和下层芯片本体之间,中层芯片本体固定在上层芯片本体的下侧,上层芯片本体朝上的一端排布有至少一个进液池,上层芯片本体朝下的一端设有若干反应通道,反应通道包括若干连接在一起的细胞捕获通道本体,首端的细胞捕获通道本体与进液池连通,相邻细胞捕获通道本体之间相互连通,下层芯片本体上排布有至少一组检测单元,检测单元包括排布在下层芯片本体上的若干与细胞捕获通道本体一一对应的检测槽,检测槽覆盖对应的细胞捕获通道本体所在区域,细胞捕获通道本体和中层芯片本体均为可溶解材料,优选为壳聚糖薄膜,上层芯片本体上排布有与进液池数量相同的出液口,出液口与对应的最末端的主进液通道本体二的内腔连通。
为了进一步实现反应通道对细胞的捕获,反应通道还包括主通道本体,主通道本体的一端与进液池连通,细胞捕获通道本体在长度方向上的两端分别连接有主进液通道本体一和主进液通道本体二,主通道本体的另一端至少与一个首端的主进液通道本体一连接,本实施例中,主通道本体的另一端连接有两个分进液通道本体,分进液通道本体远离主通道本体的一端与首端的主进液通道本体一连接,主进液通道本体一主进液通道本体一和主进液通道本体二之间还连接有次进液通道本体,细胞捕获通道本体的一端开有足够让细胞穿过的进液孔,细胞捕获通道本体的另一端开有出液孔,出液孔比进液孔小,细胞无法穿过出液孔,主通道本体、分进液通道本体、主进液通道本体一、主进液通道本体二和次进液通道本体足以让细胞穿过,相邻两个细胞捕获通道本体之间,前面的主进液通道本体二远离细胞捕获通道本体的一端与后面的主进液通道本体一的一端连接,检测槽内设有包被有细胞抗体的磁珠,下层芯片本体的两端排布有若干组与检测单元一一对应的入液口和排液口,入液口贯穿对应的检测单元与排液口连通,下层芯片本体的底部排布有若干偏离检测单元设置的缺口,可在缺口内安装感应磁铁。
对三层芯片本体进行装配时,装配时使用到的机构包括下固定座、上固定座和接头,下固定座和上固定座可经连接销固定在一起,上固定座上排布有若干与进液池一一对应的进液口,接头包括导头,导头上螺纹连接有注射器,注射器的上侧接有PE导管,注射器上开有注射孔,注射孔与导管的官腔连通,导头的下侧设有至少两个卡扣,导头经卡扣插入上固定座的三个进液口,进液池覆盖对应的进液口所在区域,具体装配步骤为,
(1)将1-2wt%的壳聚糖涂抹在玻璃基底表面,放置于加热板上形成壳聚糖薄膜;
(2)往下层芯片本体的各个入液口注入牛血清白蛋白,在每一个检测槽内放有磁珠,检测槽的数量与细胞捕获通道本体的数量相等;
(3)将包被好的磁珠逐一加入下层芯片本体的每一个检测槽内;
(4)将上层芯片本体蘸取5-10微米厚的预聚合PDMS,将其放置在壳聚糖薄膜上,置于80℃烘箱中使PDMS固化一个小时;
(5)将0.5-5%的NaOH溶液注入到上层芯片本体的三个进液池中,将含有壳聚糖薄膜的基底以及与壳聚糖薄膜结合在一起的上层芯片本体、下层芯片本体一起浸入到0.5-5%的NaOH溶液当中;
(6)48-72小时后,利用等离子水洗去残余的NaOH溶液,置于室温下干燥;
(7)干燥结束,将上层、中层、下层芯片本体的对应通道对准,使用等离子清洗仪对上层和中层芯片本体进行封接;
(8)将对准的三层芯片本体一起放置在下固定座上,再将上固定座压紧在上层芯片本体上,使用连接销将上固定座和下固定座固定在一起,将各个导头的卡扣插入上固定座的进液口内,完成整个芯片的装配。
本发明中,利用可溶解的壳聚糖将上层和下层芯片本体分隔,在下层芯片本体下侧放置磁铁,细胞经进液池进入主通道本体内后,细胞由于自身大小的原因会单个地卡在细胞捕获通道本体的出液孔处,此时未进入细胞捕获通道本体的其它细胞会由于流阻的原因,进入主进液通道本体一以上的次进液通道本体内,当细胞来到下一个细胞捕获通道本体时,再次由于细胞捕获通道本体出口的原因,卡在细胞捕获通道本体的出液孔处,剩下的细胞以此类推,待所有细胞捕获通道本体完成对细胞的分离后,加入PBS缓冲液,洗去多余细胞,再进行后续的检验,在上层芯片本体的三个进液池通入牛血清蛋白,使得PDMS材料上所有的结合位点预先被牛血清白蛋白结合,避免后序抗体进入时造成二者的结合问题而造成堵塞,待牛血清白蛋白与通道本体内壁充分结合后,再加入PBS缓冲液,洗去未与通道本体内壁结合的牛血清白蛋白,再通过三个进液池注入酶标二抗,抗体上所携带的酶为HRP酶,会与化学发光剂结合后发光,使得酶标二抗与淋巴肿瘤细胞进行特异性结合,待所有细胞被富集后,溶解中层的壳聚糖薄膜,使上下层芯片的对应捕获腔室和检测槽连通,让特定细胞被带有特异性淋巴肿瘤细胞抗体的酶标二抗捕获,等待捕获完成后,溶解中层的壳聚糖薄膜,使待测细胞进入对应的检测槽内,此时,淋巴肿瘤细胞的第二结合位点会与连接在底面的磁珠包被的抗体特异性结合,从而形成捕获,向下层芯片本体的各个入液口通入PBS缓冲液,将多余的酶标二抗带走,进行磁分离,待芯片内免疫反应进行完毕后,撤去磁铁,取出下层芯片本体,在芯片背面的四个缺口处加入四个磁铁,再进行细胞检测;本发明中能与磁珠表面淋巴肿瘤细胞抗体特异性结合的细胞,由于磁珠受磁场的作用从而使得细胞与磁珠这一系统在磁场中受力平衡,滞留在磁场中,不能与磁珠上的特异性淋巴肿瘤细胞抗体结合的细胞,由于没有磁性,无法在磁场中形成受力平衡,受流体的作用,不在磁场中停留,被流体带走,能够很好地实现细胞的特异性分选,筛选效果好,无论需要筛选什么细胞,只需要更换磁珠上的特异性淋巴肿瘤细胞抗体即可达到筛选的目的,这样的结构不仅实现了单个细胞的分选,而且具有一般性,能对大部分细胞进行筛选。
实施例2
对实施例1中的芯片进行检测淋巴肿瘤细胞的方法,包括以下步骤,
(1)使用上固定板和下固定板将检测芯片固定住,将用于往进液池内通入液体的接头插装在上固定板上,接头的出液孔与进液池连通;
(2)将固定好的芯片放置在磁铁上,使检测单元中的所有磁珠固定在芯片上;
(3)通过接头上的注射器往对应的进液池内输入稀释过后的人体血液,待所有细胞被捕获在细胞捕获通道本体内,转至步骤(4);
(4)通过导管往进液池内通入PBS缓冲液,洗去反应通道内多余的细胞;
(5)通过导管往进液池内通入牛血清白蛋白,使牛血清白蛋白与反应通道内所有可能与淋巴肿瘤细胞抗体相结合的位点结合;
(6)通过导管往进液池内通入PBS缓冲液,使PBS缓冲液流进整条反应通道;
(7)通过导管往进液池内通入带有酶标二抗的水相,完成对细胞的特异性捕获后转至步骤(8);
(8)通过导管经进液池往反应通道内通入醋酸,溶解细胞捕获通道本体和中层芯片本体,被酶标二抗捕获的位于细胞捕获通道本体内的细胞落入对应的检测槽内;
(9)经各个入液口往对应的检测单元的各个检测槽内通入PBS缓冲液,从排液口排出的废液排进废液池,撤去磁铁;
(10)经各个入液口往对应的检测单元的各个检测槽内通入化学发光试剂,使得化学发光试剂与HRP酶结合;
(11)抽出下层芯片本体,将其放置在检测箱内,检测箱的底部设有给芯片提供光源的发光灯,打开灯和相机,检测结束,导出相机的图像,发光的单元对应需要进行分析的淋巴肿瘤细胞,未发光的检测单元表明未捕获到细胞或者淋巴肿瘤细胞抗体捕获细胞错误。
为了进一步实现芯片的发光检测,如图9~12所示,还包括检测壳体,检测壳体的侧端可活动地连接有活动门,检测箱设置在检测壳体内,活动门相对检测箱设置,检测箱正上方的检测壳体内固定有镜框,镜框上安装有成像镜,成像镜从下往上倾斜,成像镜覆盖检测箱朝上的开口所在区域,检测箱的底板上侧连接有检测底座,检测底座上侧排布有若干发光灯,检测底座上侧还排布有若干电磁铁,相机的镜头相对成像镜设置,检测壳体上连接有用于调节电磁铁的磁感应强度的旋钮,芯片可刚好放置在检测箱内;检测箱的下部开有抽气口,抽气口在电磁铁的上方,抽气口上方的检测箱上排布有至少两个可滑动地连接在检测箱上且用于支撑芯片的支撑杆,支撑杆可伸进检测箱内,支撑杆朝外的一端设有推拉手柄。
为了进一步提高成像的清晰度,步骤(11)中,在放置芯片前,推动支撑杆,使支撑杆推进检测箱内,将芯片放置在支撑杆上;打开电磁铁后,将支撑杆收回,使支撑杆远离检测箱的腔体,粗调旋钮,调节芯片的浮空高度,使芯片稳定浮空在检测箱内,微调旋钮,使成像清晰,停止调节,根据各个检测槽内的发光情况,选择发光的检测槽,抽取样液得到需要的单个细胞。
本发明中,使用蠕动泵与导管连接,蠕动泵将液体抽出经导管注入注射器内,进入注射器内的测试液进入进液池内;本发明能自动完成对淋巴肿瘤细胞的分选,减少常规分选过程中过多的人为操作,降低细胞损伤甚至死亡的概率;芯片结构简单,引入二抗进行检测,被限制在下层芯片的磁珠具有灵活性,撤去磁铁即可完成对特定细胞的最终捕获;本申请中先在上层芯片本体注入酶标二抗,完成对单个细胞的负极,再溶解中层芯片本体,使细胞进入下层芯片本体的检测槽内,再次被磁珠上包被的特异性抗体捕获,两侧特异性识别大大减少了抗体由于捕获错误细胞而出现的假阳性现象的概率,提高检测的准确性和纯度;检测过程中,检测壳体上设有控制板,旋钮与控制板电连接,旋钮将电流调节信号发送给控制板,控制板根据接收到的调节信号调节电磁铁的线圈的供电电流,采用电磁铁、感应磁铁及对电磁铁通入电流大小的控制,能将芯片在任意高度架住,减小空间占用,提高空间利用率。
本发明并不局限于上述实施例,在本发明公开的技术方案的基础上,本领域的技术人员根据所公开的技术内容,不需要创造性的劳动就可以对其中的一些技术特征作出一些替换和变形,这些替换和变形均在本发明的保护范围内。
- 一种高通量淋巴肿瘤细胞微流控检测芯片及其检测方法
- 一种检测猪呼吸道疫病病原的高通量微流控芯片及检测方法
