一种抗生素抗性基因的污染风险评估方法
文献发布时间:2024-04-18 19:58:30
技术领域
本发明涉及生物技术领域,尤其是涉及一种抗生素抗性基因的污染风险评估方法。
背景技术
抗生素的使用会诱导产生抗生素抗性基因(Antibiotic Resistance Genes,ARGs),ARGs已被定义为新型环境污染物,对公共卫生构成重大威胁。ARGs会持久存在,而且会通过垂直传播和水平转移等方式在动物和环境之间传播,最终通过食物链影响人类健康;还会导致出现能够抗多种抗生素的致病菌。
生态风险评估用于评价生态系统暴露于一种或多种胁迫因子时不利效应发生的可能性。目前对于ARGs的风险评估已开展了较多的研究,方法上主要分为定量和定性评估两个方面。但是,相关技术中,定量评估的方法只能对所有关键危害评估点不为0的ARGs进行风险评估,一旦有关键危害评估点为0,会导致出现假阴性结果,不利于对ARGs的风险进行全面评估。定性评估的方法不能对同一等级的ARGs进行风险评估,不利于对ARGs的风险进行准确评估。
因此,需要提供一种能够准确、全面的对抗生素抗性基因进行风险评估的方法。
发明内容
本发明旨在至少解决现有技术中存在的技术问题之一。为此,本发明提出一种抗生素抗性基因的污染风险评估方法,能够准确、全面的对抗生素抗性基因进行风险评估。
本发明还提供一种抗生素抗性基因的风险评估系统。
根据本发明的第一方面实施例的一种抗生素抗性基因的污染风险评估方法,包括以下步骤:
S1、对待分析样本的宏基因数据进行分析,获得与所述抗生素抗性基因相关的参数;
S2、采用层次分析法建立抗生素抗性基因的风险评估模型,计算风险评价指标的权重系数;
S3、基于步骤S1得到的所述参数和步骤S2得到的所述权重系数,计算最终风险得分,分析得到所述抗生素抗性基因的风险评估结果。
根据本发明实施例的污染风险评估方法,至少具有如下有益效果:
本发明通过对猪粪源的宏基因组数据进行生物信息学分析,以宿主致病性、可移动性、抗生素抗性和基因相对丰度作为危害评估的关键点,采用定量评估与定性评估相结合的风险表征方式,结合层次分析法建立ARGs的风险评估框架,为进一步针对性消减高风险的猪粪源典型ARGs提供理论参考。实施例提供的抗生素抗性基因的污染风险评估方法在不同来源的样本分析中均具有很好的应用前景。
根据本发明的一些实施例,所述待分析样本的来源包括粪源、土壤、水体中的至少一种。例如:所述粪源可以为猪粪源。
根据本发明的一些实施例,所述参数包括ARGs在所述待分析样本的基因集中的相对丰度、与ARGs关联的潜在致病菌的种类、与ARGs关联的潜在致病菌的丰度、与ARGs关联的可移动遗传元件的种类数量、与ARGs关联的可移动遗传元件的相对丰度、ARGs抗抗生素的数量。
根据本发明的一些实施例,所述潜在致病菌包括人畜共患病原、动物病原微生物和人类病原微生物中的至少一种。所述潜在致病菌为潜在致病细菌。
根据本发明的一些实施例,可以根据危险性和致病性对所述潜在致病菌进行分类,基于此进一步分析ARGs风险。
根据本发明的一些实施例,可以为根据危险性和致病性对所述人畜共患病原、动物病原微生物和人类病原微生物进行分类,基于此进一步分析ARGs风险。例如:所述人畜共患病原可以包括一级人畜共患病原、二级人畜共患病原、三级人畜共患病原和四级人畜共患病原;所述动物病原微生物可以包括一级动物病原微生物、二级动物病原微生物、三级动物病原微生物和四级动物病原微生物;所述人类病原微生物可以包括一级人类病原微生物、二级人类病原微生物、三级人类病原微生物和四级人类病原微生物。
根据本发明的一些实施例,所述可移动遗传元件包括整合/切除、噬菌体、复制/重组/修复、稳定性/转移/防御、转移。
根据本发明的一些实施例,所述ARGs抗抗生素的数量中的所述抗生素包括人兽共用抗生素、人用抗生素、兽用抗生素和非人用/兽用抗生素。
根据本发明的一些实施例,步骤S1中,对待分析样本的宏基因数据进行分析包括:数据质控;Metagenome组装,获得contigs;基于所述contigs进行基因预测及过滤去冗余,获得gene catalogue;基于gene catalogue和抗生素抗性基因数据库进行ARGs与可移动遗传元件注释,获得MGEs合集mges catalogue;提取gene catalogue中只含抗性基因的序列文件,获得ARGs基因集;对ARGs基因集进行物种注释;对MGEs合集mges catalogue和ARGs基因集进行丰度注释。
根据本发明的一些实施例,所述风险评价指标包括准则层和指标层;
所述准则层包括相对丰度、宿主致病性、可移动性和抗生素抗性;
所述宿主致病性的指标层因素包括人畜共患病原、动物病原微生物和人类病原微生物;
所述可移动性的指标层因素包括噬菌体、稳定性/转移/防御、整合/切除、复制/重组/修复、转移;
所述抗生素抗性的指标层因素包括抗人兽共用抗生素、抗人用抗生素、抗兽用抗生素、抗非人/兽用抗生素;
所述相对丰度准则层因素包括ARGs在样本基因集中的相对丰度。
根据本发明的一些实施例,所述宿主致病性的指标层各因素下设置一级、二级、三级和四级四个因子;
根据本发明的一些实施例,步骤S2具体可以包括以下步骤:
S21、获取专家对所述风险评价指标间的标度;
所述风险评价指标包括准则层和指标层;
S22、构建ARGs风险的准则层和指标层的判断矩阵,并计算标度初始权重系数及其最大特征根;
S23、对准则层和指标层的判断矩阵进行第一次一致性检验;通过后,计算归一化权重系数以及归一化最大特征根,进行第二次一致性检验;通过后,经过计算后的归一化权重系数的判断矩阵的值即为ARGs风险指标间的权重系数。
根据本发明的一些实施例,步骤S22中,标度初始权重系数w
式中,m指矩阵的维度值;
式中,A为对应指标层的判断矩阵,w为经过计算后的标度初始权重系数的判断矩阵,w
根据本发明的一些实施例,步骤S23中,进行第一次一致性检验具体包括以下步骤:
CI=(λ
CR=CI/RI,
式中,CI为一致性指标;m为判断矩阵的维度值,λ
当m大于或等于2时,CR小于或等于0.10,即认为判断矩阵具有满意的一致性;否则需要调整判断矩阵,并使之具有满意的一致性。
根据本发明的一些实施例,步骤S23中,归一化权重系数w以及归一化最大特征根λ
式中,w
式中,A为指标层的判断矩阵,w
根据本发明的一些实施例,步骤S23中,进行第二次一致性检验具体包括以下步骤:
CI=(λ
CR=CI/RI,
式中,CI为一致性指标;m为判断矩阵的维度值;λ
当m大于或等于2时,CR小于或等于0.10,即认为判断矩阵具有满意的一致性;否则需要调整判断矩阵,并使之具有满意的一致性。
根据本发明的一些实施例,步骤S3中,最终风险得分(AI)的计算公式如下:
式中,w
宿主致病性、可移动性和抗生素抗性对应的AI
式中,x
相对丰度对应的AI
AI
式中,x
根据本发明的一些实施例,分析得到所述抗生素抗性基因的风险评估结果包括:
所述最终风险得分越高,ARGs的污染风险越大,对人类健康产生的威胁越大。
根据本发明的一些实施例,还可以包括:依据所述最终风险得分进行排名。
根据本发明的第二方面实施例的一种抗生素抗性基因的风险评估系统,用于实现上述抗生素抗性基因的污染风险评估方法;包括:
基础信息获取单元,用于对待分析样本的宏基因数据进行分析,获得与所述抗生素抗性基因相关的参数;
风险评价指标权重系数获取单元,用于采用层次分析法建立抗生素抗性基因的风险评估模型,计算风险评价指标的权重系数;
风险评估单元,用于计算最终风险得分,分析得到所述抗生素抗性基因的风险评估结果。
本发明的其它特征和优点将在随后的说明书中阐述,并且,部分地从说明书中变得显而易见,或者通过实施本发明而了解。
附图说明
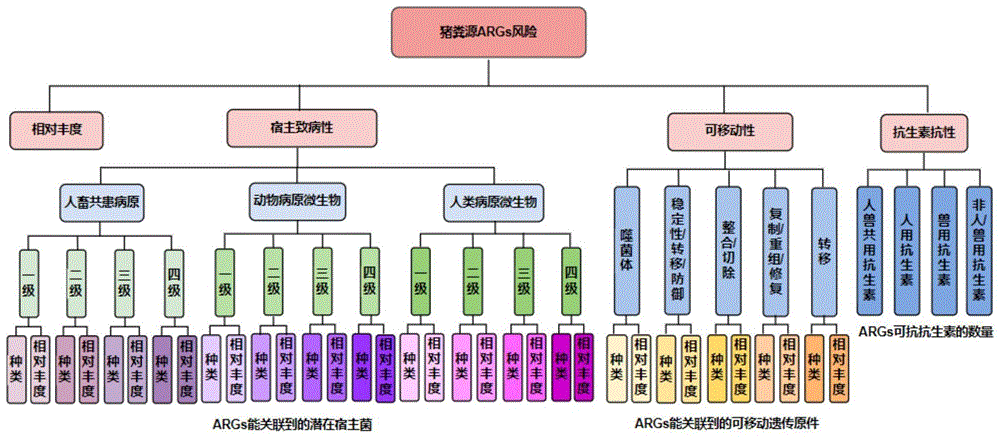
图1是本发明的猪粪源ARGs风险层次分析指标体系递阶层次结构示意图;
图2是本发明的宏基因数据分析流程图;
图3是宏基因样本AO4-44中41类ARGs的种类和相对丰度分析结果;其中,F-R:氟喹诺酮类抗生素-利福霉素抗生素;C-P:头孢菌素-青酶烷;C-C-P:头孢菌素-头霉素类抗生素-青酶烷;M-S:大环内酯类抗生素-链阳霉素类抗生素;M-F:大环内酯类抗生素-氟喹诺酮类抗生素;M-F-R:大环内酯类抗生素-氟喹诺酮类抗生素-利福霉素抗生素;F-A:氟喹诺酮类抗生素-氨基糖苷类抗生素;F-D-P:氟喹诺酮类抗生素-二氨基嘧啶消炎药-苯尼考尔抗生素;M-F-P:大环内酯类抗生素-氟喹诺酮类抗生素-青酶烷;O-P:恶唑烷酮类抗生素-苯尼考尔抗生素;M-D:核苷类抗生素-消毒剂和防腐剂;T-D:四环素类抗生素-消毒剂和防腐剂;D:消毒剂和防腐剂;L-S-P:林可胺类抗生素-链阳霉素类抗生素-胸膜茉利抗生素;T-O-P:四环素类抗生素-恶唑烷酮类抗生素-苯尼考尔抗生素;L-S-P:林可胺类抗生素-链阳霉素类抗生素-胸膜茉利抗生素;M-L-S:大环内酯类抗生素-林可胺类抗生素-链阳霉素类抗生素;A-A:氨基糖苷类抗生素-氨基香豆素抗生素;S-S:链阳霉素类抗生素-链阳霉素A类抗生素;G-T:甘油环素-四环素类抗生素;F-T:氟喹诺酮类抗生素;四环素类抗生素;multildrge:所耐抗生素的数量大于三种的ARGs类别;
图4为宏基因样本AO4-44在属水平可比对到各类各级致病性宿主的种类;其中,百分数为各类各级致病性宿主的种类占总种类数的百分比,数字为各类各级致病性宿主的种类数量;
图5为宏基因样本AO4-44的可移动遗传元件集中各类MGEs的相对丰度及数量;
图6为宏基因样本AO4-44的281种ARGs中,ARGs在同一个contigs上与MGEs比对的结果;
图7为宏基因样本AO4-44的281种ARGs所耐抗生素数量统计结果;
图8为宏基因样本AO4-44中ARGs耐人兽共用抗生素(a)、耐人用抗生素(b)、耐兽用抗生素(c)和耐非人用/兽用抗生素(d)的数量统计结果。
具体实施方式
以下将结合实施例对本发明的构思及产生的技术效果进行清楚、完整地描述,以充分地理解本发明的目的、特征和效果。显然,所描述的实施例只是本发明的一部分实施例,而不是全部实施例,基于本发明的实施例,本领域的技术人员在不付出创造性劳动的前提下所获得的其他实施例,均属于本发明保护的范围。
在本发明的描述中,如果有描述到第一、第二等只是用于区分技术特征为目的,而不能理解为指示或暗示相对重要性或者隐含指明所指示的技术特征的数量或者隐含指明所指示的技术特征的先后关系。
在本发明的描述中,术语“包括”和“具有”以及他们的任何变形,意图在于覆盖不排他的包含,例如,包含了一系列步骤或单元的过程、方法、系统、产品或设备不必限于清楚地列出的那些步骤或单元,而是可包括没有清楚地列出的或对于这些过程、方法、产品或设备固有的其它步骤或单元。
当本文中公开一个数值范围时,上述范围视为连续,且包括该范围的最小值及最大值,以及这种最小值与最大值之间的每一个值。进一步地,当范围是指整数时,包括该范围的最小值与最大值之间的每一个整数。此外,当提供多个范围描述特征或特性时,可以合并该范围。换言之,除非另有指明,否则本文中所公开之所有范围应理解为包括其中所归入的任何及所有的子范围。
如无特殊说明,本发明中的“致病菌”、“潜在宿主菌”均指细菌。
本发明提供一种抗生素抗性基因的污染风险评估方法,基于四个关键风险评价指标进行,获取四个关键风险评价指标的量化参数,并通过层次分析法确定关键风险评价指标间的权重系数后,计算不同ARGs的最终风险得分并对其进行风险分级。
以系统调研筛选到的猪粪源宏基因数据样本进行抗生素抗性基因风险评估。系统调研筛选并获取猪粪源宏基因数据样本的方法如下:
(1)以检索关键词“(pig manure OR pig feces OR pig faeces OR pigexcrement OR swine manure)AND(metagenomics OR metagenome)AND English”和“TS=((pig manure OR pig feces OR pig faeces OR pig excrement OR effluent pig ORswine manure)AND(metagenomics OR metagenome))AND language(English)AND(Article))”分别在Pubmed和Web of Science筛选符合要求的文献;
(2)利用Zotero软件对步骤(1)筛选到的文献进行汇总整理,并进一步筛选文献,具体要求如下:
1)排除重复的文献;
2)排除标题和摘要与关键词无关的文献;
3)排除猪粪样本数据格式不是FASTQ的文献。
(3)对经过步骤(2)筛选获得的文献和猪粪源宏基因样本进行归纳整理,进行二轮筛选,以保证所选择的样本具有普适性;由此获得待分析的猪粪源宏基因数据样本,用于构建不同生猪阶段猪粪源宏基因原始数据目录。样本要求如下:
1)筛选样本来源于中国的猪粪样本;
2)排除非常见的猪种(包括仅为试验用猪和野猪)的猪粪样本;
2)排除日龄信息缺失且不健康的猪粪样本。
(4)依据猪粪源宏基因原始数据目录,通过欧洲核苷酸序列数据库(https://www.ebi.ac.uk/ena)、美国国家生物技术信息中心公共数据库(https://www.ncbi.nlm.nih.gov)和国家基因库生命大数据平台(https://db.cngb.org/)下载猪粪源鸟枪法宏基因序列原始数据,构建猪粪源宏基因原始数据库。
确定用于后续分析的猪粪源宏基因原始数据下载文献目录如表1所示。猪粪源宏基因原始数据样本相关信息如表2所示。
表1
表2
注:表2中来源的序号对应表1中文献的序号。
其中,由于AO1和AO2样本无法找到原始数据下载路径故不纳入后续分析。
本发明提供一种抗生素抗性基因的污染风险评估方法,以猪粪源宏基因数据样本(AO3-44)进行抗生素抗性基因风险评估。共包括三个步骤。
S1、采用宏基因数据分析的方法分析样本(AO3-44),获取四个关键风险评价指标的量化参数。
四个关键风险评价指标(准则层因子)分别为相对丰度(TPM)、宿主致病性(humanpathogenicity,HP)、可移动性(Mobility,MO)和抗生素抗性(Drug Class nameber,DC)。猪粪源ARGs风险层次分析指标体系递阶层次结构如图1所示。
宏基因数据分析流程如图2所示。对猪粪源宏基因数据样本(AO3-44)进行数据质控、Metagenome组装、基因预测及过滤去冗余、ARGs与MGEs注释、提取只含抗性基因的序列文件、物种注释、丰度注释。具体如下:
S11、数据质控:下载得到每个样本的原始数据(Raw Data)会存在一定比例的低质量数据,为了保证后续信息分析结果的准确可靠,用kneaddata对每个样本的原始数据进行质控和宿主过滤,得到有效数据(Clean Data)。
共下载得到42个仔猪猪粪便样本的宏基因组测序数据用于分析,每个样品数据在2.2G~4.4G之间,共得到253.7GB的原始数据。在使用kneaddata对每个样本的原始数据进行质控和宿主过滤处理后,发现AO3在质控关键指标Per base sequence quality中显示“FALL”,不符合质控要求,故AO3将不纳入后续的研究。其余样本(AO4-44)均符合质控要求,可用于后续抗生素抗性基因的风险评估分析。
S12、Metagenome组装、获得contigs:从步骤S11得到的有效数据出发,选用meghit对每个样本进行Metagenome组装;为了使组装结果更具完整性和连续性,此处k-mer选用默认的长度值(21,29,39,59,79,99,119,141);随后用seqtk对小于500bp的contigs进行过滤,获得每个样本的contigs合集;
S13、基因预测及过滤去冗余:从单样本组装过滤后获得的contigs出发,采用prodigal进行基因预测,完成基因预测后,将分析样本中所有分析获得的基因文件进行合并,获得基因集(nuc),用seqtk对合并样本小于100bp的基因进行过滤,并用mmseqs2对合并样本预测产生的protien.faa文件去冗余,构建合并样本的gene catalogue;
S14、ARGs与MGEs注释:利用rgi5.2.0对每个样本的gene catalogue与抗生素抗性基因数据库CARD(The Comprehensive Antibiotic Resistance Database)进行注释,获得包含每个样本ARGs种类、不同contigs可比对到同一种ARGs的数量、同一ARGs抗不同抗生素的种类和抗性机制等信息;利用diamond2.0.1对每个样本的gene catalogue与可移动遗传元件数据库mibioeOG进行注释,获得包含每个样本MGEs种类、不同contigs可比对到同一种MGEs的数量以及这些MGEs在contigs上的位置等信息,构建出所有猪粪源样本的MGEs合集mges catalogue;
S15、提取只含抗性基因的序列文件:利用seqtk将所有样本经过基因预测获得的基因文件与经过ARGs注释的文件进行比对,从通过基因预测获得的基因文件中提取出只含ARGs的序列文件(card gene catalogue),构建出所有猪粪源样本的ARGs基因集(all cardgene catalogue);
S16、物种注释:利用kaiju将all card gene catalogue与MicroNR数据库进行比对,获得all card gene catalogue中所有可比对到ARGs的物种注释信息;
S17、丰度注释:从all card gene catalogue和mges catalogue出发,利用metawrap1.3.1综合其对应样本的Clean Data,获得每个样本中ARGs和MGEs的丰度信息。
针对猪粪源宏基因数据样本(AO3-44)进行分析,共计含41类,281种ARGs。分析得到相对丰度、宿主致病性、可移动性和抗生素抗性的相关参数如下:
(1)相对丰度:指ARGs在基因集中的相对丰度。通过宏基因数据分析方法获得ARGs在样本基因集中相对丰度参数值,并以该值作为ARGs基因相对丰度(TPM)的量化指标。
猪粪源宏基因数据样本(AO3-44)中,每类ARGs的相对丰度和数量情况如图3所示。以畜禽源ARGs在仔猪猪粪样本中的相对丰度大小作为不同ARGs相对丰度的评估参数。
(2)宿主致病性:指ARGs与致病菌的关联性,包括与ARGs关联的潜在宿主菌是致病菌的种类及其丰度大小。通过宏基因数据分析方法获得ARGs潜在宿主菌的种类和丰度参数值,并以此作为ARGs宿主致病性的量化指标。
人畜共患病原指会同时使人类和动物患病的病原微生物;动物病原微生物指不会使人类患病,但会使多种动物(本示例分析包括猪)共患病的病原微生物;人类病原微生物指不会使动物(本示例分析包括猪)患病,但会使人类患病的病原微生物。
在人畜共患病原、动物病原微生物和人类病原微生物的四个等级中,依据相关分类标准,根据危险性和致病性进行分类,“一级”、“二级”、“三级”和“四级”的危险性和致病性逐渐下降。其中,“一级”为最高级别,即危险性最大和致病性最高的一类病原微生物。
例如:可以依据中华人民共和国农业农村部于2022年8月19日发布的人畜共患传染病名录(2022年修订版)(中华人民共和国农业农村部公告第571号)、中华人民共和国农业农村部于2005年7月20日发布的《动物病原微生物分类名录》(中华人民共和国农业部令第53号)和国家卫生健康委办公厅于2006年1月11日发布的关于《人间传染的病原微生物目录》对人畜共患病原、动物病原微生物和人类病原微生物进行分类,每个类别下设四个等级。ARGs的潜在宿主可依据此分类标准统计各类别中各级致病性宿主菌的数量。
以下示例性地给出与细菌相关的人畜共患传染病等级分类情况和动物病原微生物分类等级分类情况。如表3和表4所示。
表3.与细菌相关的人畜共患传染病等级分类
表4.动物病原微生物分类等级
种类指ARGs关联的潜在宿主菌是致病菌的种类数量;相对丰度指ARGs关联的潜在宿主菌是致病菌的相对丰度大小。
根据宿主致病性的分类标准,进一步分析了细菌在猪粪源宏基因样品(AO3-44)在属水平上各类各级致病性宿主的数量和种类。结果如图4所示。
(3)可移动性:指ARGs与可移动遗传元件(Mobile Genetic Elements,MGEs)的相关性;包括与猪粪源ARGs关联的可移动遗传元件的种类和相对丰度。通过宏基因数据分析方法获得在各分类类别中,同一个contigs上ARGs与MGEs比对上的种类及其在MGEs集的相对丰度信息,以此作为MO的量化指标。其中,MGEs的分类类别以mobileOG数据库的功能分类为标准(网址:mobileOG-db(vt.edu)),包括整合/切除、噬菌体、复制/重组/修复、稳定性/转移/防御和转移五个类别。
种类指ARGs关联到的可移动遗传元件的种类数量;相对丰度指ARGs关联到的可移动遗传元件的相对丰度大小。
猪粪源宏基因数据样本(AO3-44)中,可移动遗传元件集中各类MGEs的相对丰度及数量如图5所示;在281种ARGs中,ARGs在同一个contigs上与MGEs比对的结果如图6所示。
(4)抗生素抗性:指ARGs与人用和兽用抗生素的相关性。将经过宏基因数据分析方法获得ARGs注释抗生素的信息与人用和兽用抗生素的相关性进行比对,获得ARGs分别抗人兽共用、人用、兽用和非人用/兽用抗生素的数量,并将此作为ARGs抗生素抗性的量化指标。
例如:可以依据中华人民共和国农业农村部于2021年11月4日发布的《2020年中国兽用抗菌药使用情况报告》及国家药品监督管理局于2003年1月30日发布的《化学药品地方标准升为国家标准品种目录》对抗生素进行划分。
猪粪源宏基因数据样本(AO3-44)中,ARGs共耐32类抗生素。根据ARGs抗生素抗性的分类标准,对32类抗生素进行分类。分类结果如表5所示。
表5.宏基因样本AO4-44 ARGs所抗抗生素的分类情况
进而依据表5所示的分类标准,对ARGs所耐不同抗生素类别的数量进行分类统计,并以此作为不同ARGs抗生素抗性的评估参数。
统计结果如图7和图8所示。
S2、采用层次分析法计算出每个准则层和指标层指标间的权重系数,确定关键风险评价指标间的权重系数。
S21、通过制定“关于抗生素抗性基因风险指标间重要程度的专家咨询调查问卷”,结合ARGs研究领域专家依据标度及其判断依据(表6),获得ARGs风险指标间的标度。
表6.标度及其判断依据
注:a
如下给出示例性的部分“关于抗生素抗性基因风险指标间重要程度的专家咨询调查问卷”。如表7所示。
表7
注:两个指标间的重要性比较是用“行”的指标与“列”的指标进行比较。
S22、构建ARGs风险的准则层和指标层的判断矩阵,并计算其初始权重系数和最大特征根。
准则层包括相对丰度、宿主致病性、可移动性和抗生素抗性四个因素。
指标层为反映准则层的具体评价指标体系。如图1所示。
宿主致病性的指标层包括人畜共患病原、动物病原微生物和人类病原微生物三个因素;各因素下设置一级、二级、三级和四级四个因子;各因子基于种类、相对丰度两个参数进行评分。
可移动性的指标层包括噬菌体、稳定性/转移/防御、整合/切除、复制/重组/修复、转移五个因素;各因素基于种类、相对丰度两个参数进行评分。
抗生素抗性的指标层包括抗人兽共用抗生素、抗人用抗生素、抗兽用抗生素、抗非人/兽用抗生素四个因素。各因素基于数量进行评分。
依据步骤S21获取的调查问卷专家的填写意见,利用获得的各指标间的标度构建准则层和指标层的判断矩阵A(如表8所示),计算专家们在各指标给出的标度初始权重系数w
表8
注:a
w
式中,m指该矩阵的维度值;
式中,A为对应指标层的判断矩阵,w为经过计算后的标度初始权重系数的判断矩阵,w
S23、对准则层和指标层的判断矩阵进行一致性检验,并对权重系数归一化处理,确定ARGs风险指标间的权重系数。
只有当判断矩阵满足一致性的条件,才能应用层次分析法得出基本合理的结论。因此必须对利用各专家给出的标度所构造的判断矩阵进行一致性检验。剔除不符合一致性检验的判断矩阵,保留符合一致性检验的判断矩阵。
在一致性检验中,如果判断矩阵各行成比例且各列成比例,那么该矩阵就是一致矩阵。如果判断矩阵各行各列不成比例,则需要采用如下的公式进行一致性检验:
CI=(λ
CR=CI/RI,
式中,CI为一致性指标,m为判断矩阵的维度值,λ
采用1~9阶判断矩阵,其RI值见表9。
表9
当m大于或等于2时,CR小于或等于0.10,即认为判断矩阵具有满意的一致性;否则需要调整判断矩阵,并使之具有满意的一致性。
通过对计算获得专家们在各指标给出的判断矩阵进行一致性检验,将通过一致检验的标度初始权重系数进行归一化计算,获得归一化权重系数w
式中,w
式中,A为指标层的判断矩阵,w
如果没有通过一致性检验,则需要依据层次分析法对各指标间的平均值进行微调,直到通过一致性检验为止。经归一化后通过一致性检验的特征向量w的值,即为同一层次相应因素对于上一层次某一因素相对重要性的权重系数向量。并以通过一致性检验的特征向量w(即经过计算后的归一化权重系数的判断矩阵)的值作为ARGs风险指标间的最终权重系数。
S3、计算不同ARGs的最终风险得分(AI),并依据最终风险得分进行不同ARGs的最终风险排名,结合风险级别划分规则将待分析样品中的ARGs划分为Ⅰ-Ⅳ个级别。ARGs风险级别划分规则见表10。
表10
注:最终风险得分越高,风险等级越高,ARGs危害越大。
通过如下公式计算不同层级ARGs的最终风险得分AI。
式中,w
宿主致病性、可移动性和抗生素抗性对应的AI
式中,x
相对丰度对应的AI
AI
式中,x
上面结合实施例对本发明实施例作了详细说明,但本发明不限于上述实施例,在所属技术领域普通技术人员所具备的知识范围内,还可以在不脱离本发明宗旨的前提下作出各种变化。
