一种应用于新型冠状病毒灭活疫苗的裂解液及抗原解离的方法
文献发布时间:2023-06-19 09:55:50
技术领域
本发明涉及一种应用于新型冠状病毒灭活疫苗的裂解液及抗原解离的方法,属于疫苗检测、评价技术领域。
背景技术
随着新型冠状病毒肺炎在全球爆发,全世界都进入紧急状态。到目前为止,全球感染新冠肺炎的病人已经突破千万大关,这给我国乃至全球造成了巨大影响,严重阻碍了全球经济、社会的发展。
研究表明新冠肺炎是由一种新型冠状病毒引起(severe acute respiratorysyndrome coronavirus 2,SARS-Cov-2),该病毒是一种直径约为80-120nm的正链RNA病毒,属于冠状病毒科(Coronaviridae)正冠状病毒亚科(Orthocoronavirinae),该亚科包括4个属(α、β、γ和δ),其中β属正是引起新冠肺炎的病原体。病毒基因组由29891个核苷酸组成,可编码9860个氨基酸。整个病毒主要由4种蛋白构成,分别为S蛋白(Spike protein)、E蛋白(Envelope protein)、M蛋白(Membrane protein)和N蛋白(Nucleocapsid protein)。目前大多研究主要针对S抗原和N抗原,研究表明S蛋白有丰富的B细胞和T细胞表位,能诱导产生有效的中和抗体中和病毒,在动物实验中证实具有保护作用。此外N抗原也具有较强的抗原原性,也能诱导产生中和抗体。
氢氧化铝佐剂在灭活疫苗中的使用已有多年的历史,以氢氧化铝作为佐剂的疫苗能有效的增强疫苗的免疫效果,研究表明,氢氧化铝能在注射部位保留抗原,将抗原呈递给APC细胞,诱发炎症反应,促进激活树突状细胞的细胞因子及其他介质的释放,从而增强免疫应答,并且安全可靠,因此SARS-Cov-2灭活疫苗也是采用氢氧化铝作为佐剂,动物实验表明SARS-Cov-2病毒经灭活处理,S、N抗原经铝吸附后能在恒河猴中诱导高水平的中和抗体,并且抗体滴度与S、N抗原的含量呈正相关,因此如何准确的评价疫苗中吸附到铝上的S抗原和N抗原的含量尤为重要,是保证疫苗安全有效的重要指标,但吸附到铝上的S抗原和N抗原无法直接用ELISA的方法检测,需要预先用裂解剂将抗原从铝上裂解下来再用ELISA检测定量。氢氧化铝吸附抗原的原理很复杂,目前的理论认为氢氧化铝是通过静电作用、疏水作用、表面羟基与抗原上的磷酸基团等物理或化学的作用对抗原进行吸附。
传统的裂解液大多使用一些表面活性剂,比如二乙醇胺、Triton X-100等配制而成,2010版《中华人民共和国药典》就公布一种由二乙醇胺、Triton X-100配制的裂解液,用于铝吸附甲型肝炎灭活疫苗和EV71灭活疫苗的抗原含量检测,效果都很好,但该裂解液却不适用于铝吸附SARS-Cov-2灭活疫苗,裂解效果不佳,抗原回收率较低,只有46%,因此目前急需寻找一种针对铝吸附SARS-Cov-2灭活疫苗的裂解液。
发明内容
为了克服现有技术的问题,本发明提出了一种应用于新型冠状病毒灭活疫苗的裂解液及抗原解离的方法,利用本发明所述裂解液并配合适当的裂解条件,可高效回收新型冠状病毒灭活疫苗抗原,从而实现对疫苗中吸附到铝上的S抗原和N抗原含量的精准测定。
本发明的目的是这样实现的:
一种应用于新型冠状病毒灭活疫苗的裂解液,其原料包括二乙醇胺、Triton X-100、柠檬酸钠、尿素和EDTA,利用PBS缓冲液配置该裂解液,各原料的浓度分别为:
进一步的,所述PBS缓冲液的浓度为0.01mol/L~0.1mol/L,优选浓度为0.01mol/L。
本发明的另一方面:
一种铝吸附新型冠状病毒灭活疫苗抗原解离的方法,其中,利用了上述裂解液对新型冠状病毒灭活疫苗的抗原进行解离,具体包括以下步骤:
步骤1,裂解液的配置:用PBS缓冲液配置含二乙醇胺、Triton X-100、柠檬酸钠、尿素和EDTA的混合液,即为所述裂解液;
步骤2,抗原裂解:将步骤1制备得到的裂解液加至新型冠状病毒灭活疫苗中,在4℃~37℃条件下裂解30min~90min,获得抗原解离液;
步骤3,抗原含量测定:利用ELISA测定所述抗原解离液中新型冠状病毒灭活疫苗抗原的含量。
进一步的,步骤2中所述裂解液的添加量为:以裂解液与疫苗1:1的体积比添加。
进一步的,步骤2中抗原裂解的优选条件为4℃裂解90min。
进一步的,步骤3中ELISA的具体测定步骤为:
步骤301,ELISA检测板的制备:将人抗S抗原的单克隆抗体用包被液稀释后包被到96孔板中,每孔100μl,置4℃过夜,然后丢弃孔中溶液并拍干,每孔中加入1%的BSA、放置4℃封闭过夜,丢弃封闭液拍干板子并抽真空密封包装,保存于-20℃备用;
步骤302,抗原测定:将ELISA检测板取出后室温平衡30min,将步骤2获得的抗原解离液和标准品做2倍系列稀释后加入板中,每孔100μl,并置37℃孵育2h,用0.05%Tween20洗板4次,拍干,加入兔抗SARS-Cov-2抗体,每孔100μl,置37℃孵育1h,用0.05%Tween20洗板4次、拍干,加入羊抗兔HRP,每孔100μl,置37℃孵育0.5h,用0.05%Tween20洗板4次,拍干,加入TMB显色液,室温显色8min,显色完成后每孔中加入50μl硫酸终止,以450nm为检测波长,630nm为参比波长读取每孔的OD值,根据标准的含量利用双平行线法计算每个抗原解离液的抗原含量。
本发明相比现有技术的优点和有益效果是:
1、本发明所述的裂解液是在现有用于甲型肝炎灭活疫苗的裂解液基础上,加入了一定浓度的尿素和EDTA,配制成了以二乙醇胺、Triton X-100、柠檬酸钠、尿素和EDTA组成的新裂解液,二乙醇胺和Triton X-100等表面活性剂破坏了抗原与氢氧化铝之间的非共价键结合,柠檬酸根对氢氧化铝的溶解共同使抗原释放,尿素导致抗原的构象改变、作为金属离子螯合剂的EDTA使铝离子溶解不容易沉淀,减少了ELISA的干扰,能够高效回收新型冠状病毒灭活疫苗抗原,从而实现对疫苗中吸附到铝上的S抗原和N抗原含量的精准测定;
2、本发明所述铝吸附新型冠状病毒灭活疫苗抗原解离的方法,通过对本发明所述裂解液在不同裂解温度和时间的研究,确定了该裂解液对SARS-Cov-2灭活疫苗的最佳裂解条件为裂解温度:4℃,裂解时间:90min,此条件下裂解液对新冠灭活疫苗的裂解效果较好,回收率、线性(R
附图说明
下面结合附图和实施例对本发明作进一步说明。
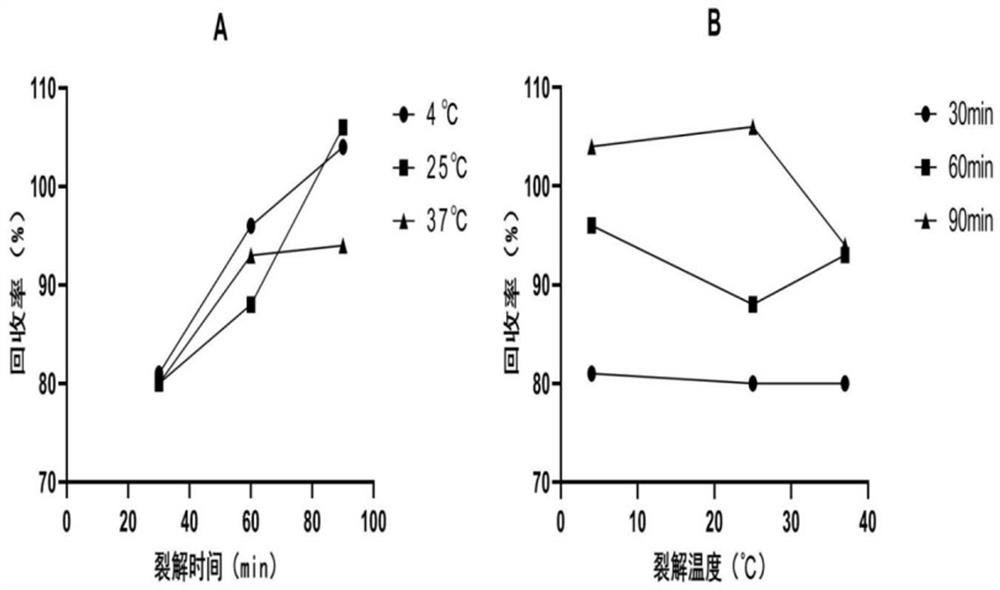
图1是本发明实施例3所述抗原解离方法中在不同裂解时间(A)和裂解温度(B)条件下回收率结果图。
具体实施方式
实施例1:
本实施例提供了一种应用于新型冠状病毒灭活疫苗的裂解液,其原料包括二乙醇胺、Triton X-100、柠檬酸钠、尿素和EDTA,利用0.01mol/L的PBS缓冲液配置该裂解液,各原料的浓度分别为:
实施例2:
本实施例提供了一种铝吸附新型冠状病毒灭活疫苗抗原解离的方法,其中,利用了实施例1所述裂解液对新型冠状病毒灭活疫苗的抗原进行解离。
所述SARS-Cov-2灭活疫苗的配制方法为:SARS-Cov-2毒种(由申请人自行制备)经细胞培养后,收集培养液并灭活,后续纯化后加入氢氧化铝吸附,配制成S抗原含量分别为150U/ml、202U/ml和250U/ml的灭活疫苗备用。
所述灭活疫苗的抗原解离具体包括以下步骤:
步骤1,裂解液的配置:如实施例1所述用0.01mol/L的PBS缓冲液配置含二乙醇胺、Triton X-100、柠檬酸钠、尿素和EDTA的混合液,二乙醇胺、TritonX-100、柠檬酸钠、尿素和EDTA的浓度分别为0.3%(v/V)、1%(v/V)、10%(w/V)、1mol/L、0.05mol/L,即为所述裂解液;
步骤2,抗原裂解:1.5ml的EP管中加入0.2ml抗原浓度为202U/ml的疫苗,再加入0.2ml步骤1制备得到的裂解液,在4℃条件下裂解90min,获得抗原解离液;
步骤3,抗原含量测定:利用ELISA测定所述抗原解离液中新型冠状病毒灭活疫苗抗原的含量,具体操作为:
步骤301,ELISA检测板的制备:将人抗S抗原的单克隆抗体用包被液稀释后包被到96孔板中,每孔100μl,置4℃过夜,然后丢弃孔中溶液并拍干,每孔中加入1%的BSA、放置4℃封闭过夜,丢弃封闭液拍干板子并抽真空密封包装,保存于-20℃备用;
步骤302,抗原测定:将ELISA检测板取出后室温平衡30min,将步骤2获得的抗原解离液和标准品做2倍系列稀释后加入板中,每孔100μl,并置37℃孵育2h,用0.05%Tween20洗板4次,拍干,加入兔抗SARS-Cov-2抗体,每孔100μl,置37℃孵育1h,用0.05%Tween20洗板4次、拍干,加入羊抗兔HRP,每孔100μl,置37℃孵育0.5h,用0.05%Tween20洗板4次,拍干,加入TMB显色液,室温显色8min,显色完成后每孔中加入50μl硫酸终止,以450nm为检测波长,630nm为参比波长读取每孔的OD值,根据标准的含量利用双平行线法计算每个抗原解离液的抗原含量。
本实施例使用的试剂:兔抗SRAS-Cov-2抗体、羊抗兔HRP、2mol/L硫酸和S抗原标准品均由申请人自行制备;单组份TMB显色液购自Sollarbio。
实施例3:
为探索不同裂解条件对新冠灭活疫苗的裂解效果,本实施例进行了不同时间和温度裂解疫苗的试验。
取6支1.5ml的EP管,毎管中加入0.2ml抗原浓度为202U/ml的SARS-Cov-2灭活疫苗,再加入0.2ml的实施例1所述裂解液,随机抽取两支分别置于4℃、25℃和37℃裂解30min;重复以上操作分别裂解60min和90min。
样品回收率通过裂解后抗原含量除以理论抗原含量计算,用SPSS17.0对回收率进行t检验,以P<0.05为具有统计学差异,对回收率与裂解温度、裂解时间之间进行相关性分析。
实施例1所述裂解液对铝吸附SARS-Cov-2灭活疫苗在不同温度和时间条件下进行裂解,裂解温度为37℃,裂解时间为30min、60min和90min时,平均回收率、平均R
表1.裂解液在不同条件下对SARS-Cov-2灭活疫苗的裂解效果
实施例4:
为探索不同抗原含量疫苗的裂解效果,本实施例进行了以下试验:
取6支1.5mlEP管,毎管中加入抗原含量为250U/ml的疫苗0.2ml,再加入0.2ml的裂解液,并置4℃裂解90min;另取6支1.5mlEP管,毎管中加入抗原含量为150U/ml的疫苗0.2ml,再加入0.2ml的裂解液,并置4℃裂解90min。
实施例1所述裂解液对不同抗原含量疫苗的裂解效果如下:
在4℃条件,对高、低含量的疫苗裂解60min,平均回收率分别为100%和104%,统计分析显示,无统计学差异(t=1.363,P=0.203),平均R
表2.裂解液在4℃条件下对不同抗原含量疫苗的裂解效果
实施例5:
本实施例评价了实施例1所述裂解液的重复性和精密性,具体方法为:在不同天进行裂解实验,每天取6支1.5mlEP管,毎管中加入抗原含量为250U/ml的疫苗0.2ml,再加入0.2ml的实施例1所述裂解液,并置4℃裂解90min。以上操作重复3次,每天重复1次。
实施例1所述裂解液对S抗原含量为250U/ml的疫苗在3天内重复多次进行裂解,每天重复试验的平均回收率分别99%、95%和108%,平均R
表3.裂解液的重复性和精密性结果
对比例:
本对比例提供了一种甲型肝炎灭活疫苗裂解液,其原料为二乙醇胺和TritonX-100,利用0.01mol/L的PBS缓冲液配置该裂解液,各原料的浓度分别为:
二乙醇胺 2.5%(v/V)
TritonX-100 0.2%(v/V)。
比较实施例1所述应用于新型冠状病毒灭活疫苗的裂解液与本对比例所述甲型肝炎灭活疫苗裂解液的裂解效果,具体操作为:
取12支1.5mlEP管,每管中加入抗原含量为250U/ml的SARS-Cov-2灭活疫苗0.2ml,随机分成两组、每组6只,其中一组每管中加入实施例1所述裂解液0.2ml,另一组每管中加入本对比例所述甲型肝炎灭活疫苗裂解液0.2ml,将所有样品置4℃裂解90min。
参照实施例2步骤3所述抗原含量测定方法,测定每个样品的S抗原含量。实施例1所述裂解液(1)与用于甲型肝炎灭活疫苗裂解的裂解液(2)对同一新冠灭活疫苗进行裂解,两种裂解液的回收率分别为86%和46%,实施例1所述裂解液的裂解效果(回收率)明显高于用于甲型肝炎灭活疫苗裂解的裂解液,具有明显的统计学差异(t=-9.312,P=0.000),两种裂解液的平均R
表4.两种裂解液对新冠灭活疫苗的裂解效果比较
经过上述研究可以确定,实施例1所述裂解液在“4℃-90min”条件下能有效的将S抗原从氢氧化铝上裂解下来,回收率在80-120%内,线性较好,变异系数都小于15%,可以用于新冠灭活疫苗的裂解。
最后应说明的是,以上仅用以说明本发明的技术方案而非限制,尽管参照较佳布置方案对本发明进行了详细说明,本领域的普通技术人员应当理解,可以对本发明的技术方案进行修改或者等同替换,而不脱离本发明技术方案的精神和范围。
- 一种应用于新型冠状病毒灭活疫苗的裂解液及抗原解离的方法
- 一种应用于新型冠状病毒灭活疫苗的裂解液及抗原解离的方法
