条形码化肽-MHC复合物及其用途
文献发布时间:2023-06-19 10:46:31
相关申请的交叉引用
本申请要求2018年9月24日提交的美国临时申请号62/735,803的权益,将所述临时申请通过引用以其整体并入本文。
技术领域
本发明涉及T细胞表位组作图和转录组分析。
背景技术
T细胞在对抗病毒感染和肿瘤中起着至关重要的作用。T细胞通过T细胞受体(TCR)与肽主要组织相容性复合物(pMHC)之间的相互作用被激活。TCR与pMHC之间的相互作用可诱导增殖、效应物表型的发展(包括细胞因子释放)。因此,鉴定由单独T细胞识别的肽(抗原)和表征肽特异性T细胞对于理解和治疗免疫相关疾病至关重要。
目前,基于质谱流式细胞技术(Newell等人(2013)Nature Biotechnology,623-629)、基于荧光(Altman(1996)Science,94-96)或基于双链DNA条形码的方法(Bentzen等人(2016)Nature Biotechnology,1037-1045)限于通过抗原特异性T细胞的有限的基于流的表征来鉴定由单独T细胞识别的抗原。类似地,DNA条形码抗体标记策略(Stoeckius等人(2017)Nature Methods,865-868;Peterson等人(2017)Nature Biotechnology,936-939)限于同时测量基因表达和细胞表面表位表达。
发明内容
本公开文本提供了在包含T细胞的样品中以单细胞分辨率同时进行T细胞表位作图和/或转录组表征的方法,所述方法包括:(a)用独特的条形码标记每个独特的肽-主要组织相容性复合物(pMHC),从而产生条形码化pMHC构建体群体;(b)使所述包含T细胞的样品与所述条形码化pMHC构建体群体接触,其中T细胞上的至少一种T细胞受体与所述条形码化pMHC构建体(“T细胞受体表位”)中的至少一种结合;并且(c)使用单细胞测序对所述T细胞进行测序,其中所述单细胞测序同时鉴定每个T细胞中的T细胞受体表位和转录组基因。
本公开文本还提供了在从样品获得的单个T细胞中同时进行T细胞表位作图和/或转录组表征的方法,所述方法包括:(a)用独特的条形码标记每个独特的肽-主要组织相容性复合物(pMHC),从而产生条形码化pMHC构建体群体;(b)使T细胞与所述条形码化pMHC构建体群体接触,其中所述T细胞上的T细胞受体与所述条形码化pMHC构建体(“T细胞受体表位”)中的至少一种结合;并且(c)使用单细胞测序对所述T细胞进行测序,其中所述单细胞测序同时鉴定所述T细胞中的T细胞受体表位和转录组基因。
在一些方面,所述单细胞测序是基于液滴的单细胞测序。在一些方面,所述测序的每个液滴包含(i)由(b)中的至少一种条形码化pMHC构建体标记的T细胞;以及(ii)包含用于转录组测量的引物的引物珠。
在一些方面,每个条形码是单链核酸。在一些方面,所述单链核酸就是DNA。在一些方面,每个条形码包含独特的样品标识序列。在一些方面,基于汉明码设计所述样品标识序列。在一些方面,所述样品标识区的长度为至少10bp、至少11bp、至少12bp、至少13bp、至少14bp、至少15bp、至少16bp、至少17bp、至少18bp、至少19bp、至少20bp、至少21bp、至少22bp、至少23bp、至少24bp、至少25bp、至少26bp、至少27bp、至少28bp、至少29bp或至少30bp。在一些方面,所述样品标识区在10bp与30bp之间、11bp与29bp之间、12bp与28bp之间、13与27bp之间、14bp与26bp之间、15bp与25bp之间、16bp与24bp之间、17bp与23bp之间、或18bp与22bp之间。
在一些方面,所述样品标识区侧接两个恒定区(5'恒定区和3'恒定区)。在一些方面,所述5'恒定区用于PCR扩增和退火到索引引物。在一些方面,所述索引引物包含独特的分子索引(UMI)。在一些方面,所述UMI包括Illumina i7 UMI。在一些方面,所述3'恒定区退火到在基于液滴的单细胞测序平台中的模板转换寡聚物。
在一些方面,所述模板转换寡聚物包含10X细胞条形码或Dropseq细胞条形码。在一些方面,每个条形码化pMHC构建体包含支架。在一些方面,所述支架包含中性抗生物素蛋白。在一些方面,所述支架包含右旋糖酐。在一些方面,每个条形码化pMHC构建体包含4个相同的附接至中性抗生物素蛋白支架上的pMHC单体。在一些方面,每个条形码化pMHC构建体包含5个相同的附接至右旋糖酐支架上的pMHC单体。
在一些方面,所述包含T淋巴细胞的样品是外周血、脐带血、组织活检物或液体活检物。在一些方面,所述5'恒定区包含如SEQ ID NO:1中所示的核酸序列(ACCTTAAGAGCCCACGGTTCC)。在一些方面,所述3'恒定区包含如SEQ ID NO:2中所示的核酸序列(AAAGAATATACCC)。
本公开文本还提供了通过本文公开的任何一种方法鉴定的T细胞表位。还提供了通过本文公开的任何方法鉴定的T细胞转录组。
本公开文本还提供了一种DNA条形码化pMHC构建体,其包含共价或非共价附接至支架分子的至少一个pMHC肽、以及共价或非共价附接至所述支架的至少一个条形码。在一些方面,所述支架分子是中性抗生物素蛋白或右旋糖酐。在一些方面,所述DNA条形码包含SEQ ID NO:3。
还提供了一种制造本公开文本的DNA条形码化pMHC构建体的方法,其包括(1)将4或5个pMHC肽附接至支架上,其中所述支架是右旋糖酐或中性抗生物素蛋白;并且(2)将至少一个DNA条形码附接至所述支架上,其中所述DNA条形码包含SEQ ID NO:3。
附图说明
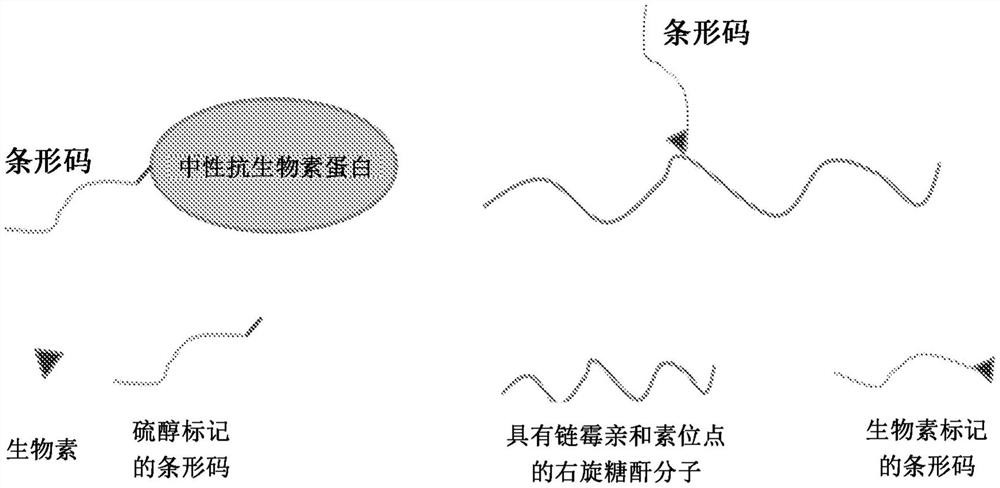
图1示出了两种可供选择的DNA条形码标记策略。这些包含pMHC的DNA条形码化构建体可用于在单细胞测序方案中鉴定抗原特异性T细胞。在一种策略中,DNA条形码化pMHC构建体是包含中性抗生物素蛋白支架的pMHC四聚体构建体。在替代策略中,DNA条形码化pMHC构建体是包含右旋糖酐支架的pMHC多聚体构建体(例如五聚体)。
图2示出了生成pMHC多聚体的DNA条形码化文库的策略,使得每个DNA条形码对应于独特的pMHC多聚体。
图3是示出用于测序的液滴的示意图,所述液滴包含T细胞、DNA条形码化pMHC构建体(特别是中性抗生物素蛋白复合物)和用于转录组分析的测序引物珠,所述测序引物珠将含有与作为转录组分析的一部分的每个待扩增基因对应的一系列引物。
具体实施方式
本公开文本提供了允许在单细胞水平上同时检测抗原特异性T细胞和测量其转录组的方法。所公开的方法使用肽-主要组织相容性复合物(pMHC)构建体,所述构建体包含支架以及DNA条形码,所述支架包含附接至所述支架上的若干pMHC单体。每个独特的条形码都与独特的pMHC一对一地相关。
这些方法通过将单细胞测序与用特定单链DNA条形码化的pMHC相组合,从而能够快速、同时地鉴定和定量细胞表面上的特定T细胞受体,并对T淋巴细胞进行转录组学表征。这些方法可用于例如筛选肽特异性、同时表征在单细胞水平上不同抗原特异性T细胞的转录组、验证来自T细胞受体(TCR)测序的结果、诊断测试、预测免疫疗法的功效、或测量在疫苗接种或免疫疗法后的免疫反应性。
此外,本文公开的方法还可用于基于稀有细胞类型对配体的亲和力来鉴定和表征稀有细胞类型。
因此,本公开文本提供了在包含T细胞的样品中以单细胞分辨率同时进行T细胞表位作图和/或转录组表征的方法,所述方法包括:(a)用独特的条形码标记每个独特的肽-主要组织相容性复合物(pMHC),从而产生条形码化pMHC构建体群体;(b)使所述包含T细胞的样品与所述条形码化pMHC构建体群体接触,其中T细胞上的至少一种T细胞受体与所述条形码化pMHC构建体(“T细胞受体表位”)中的至少一种结合;并且(c)使用单细胞测序对所述T细胞进行测序,其中所述单细胞测序同时鉴定每个T细胞中的T细胞受体表位和转录组基因。
如本文所用,术语“独特”是指DNA条形码与缀合至所述条形码或缀合至包含所述条形码的构建体的pMHC之间的一对一关系。因此,术语独特意指特定DNA条形码对应于特定pMHC且仅对应于该特定pMHC,并且该特定pMHC对应于特定DNA条形码且仅对应于该特定DNA条形码。
如本文所用,术语“以单细胞分辨率”或“在单细胞水平”意指样品包括T细胞群体,但在每个单细胞测序反应中获得的每组T表位作图数据和转录组数据对应于单细胞。
在一些方面,所述单细胞测序是基于液滴的单细胞测序。然而,允许对另一隔室(例如珠、阵列孔等)中的单细胞进行测序的其他测序方法也可用于实践本文公开的方法。本文公开的方法还可以通过使用测序方法来实践,尽管测序方法不对单细胞进行测序,但允许对多个细胞进行多重测序,其中每个细胞是独特标识的(例如通过条形码化)。
在一些方面,测序的每个液滴包含(i)由(b)中的至少一种条形码化pMHC构建体标记的T细胞;以及(ii)包含用于转录组测量的引物的引物珠。如上所讨论,测序反应可以使用替代系统进行,在所述替代系统中将反应物限制在例如微流体系统中的阵列孔、毛细管或隔室中、珠、脂质体等中。此外,用于转录组测量的引物可以结合至替代支架或容器,例如树状聚合物、线性或支化聚合物、孔、液滴等。
在一些方面,每个条形码是单链核酸。在本公开文本的其他方面,所述核酸可以是例如双链或支化的。在一些方面,所述核酸(例如单链核酸)是DNA或RNA。在一些方面,所述核酸可包含例如非天然核碱基(例如LNA)和/或非天然主链连接(例如硫代磷酸酯)。在一些方面,所述条形码可以包含通用基底。在一些方面,每个条形码包含独特的样品标识序列。
在一些方面,基于汉明码设计所述样品标识序列。在一些方面,可在所述样品标识序列中使用替代代码。在一些方面,所述代码是纠错码,例如包含哈希函数的代码。在一些方面,所述哈希函数是例如重复码、奇偶检验位或校验和。
在一些方面,所述样品标识区的长度为至少10bp、至少11bp、至少12bp、至少13bp、至少14bp、至少15bp、至少16bp、至少17bp、至少18bp、至少19bp、至少20bp、至少21bp、至少22bp、至少23bp、至少24bp、至少25bp、至少26bp、至少27bp、至少28bp、至少29bp或至少30bp。在一些方面,所述样品标识区在10bp与30bp之间、11bp与29bp之间、12bp与28bp之间、13与27bp之间、14bp与26bp之间、15bp与25bp之间、16bp与24bp之间、17bp与23bp之间或18bp与22bp之间。
在一些方面,所述样品标识区侧接两个恒定区(5'恒定区和3'恒定区)。在一些方面,所述5'恒定区用于PCR扩增和退火到索引引物。在一些方面,所述3'恒定区退火到在单细胞测序平台例如基于液滴的单细胞测序平台中的模板转换寡聚物。在一些方面,侧翼恒定区被转置,即3'恒定区用于PCR扩增和退火到索引引物,而5'恒定区退火到在单细胞测序平台例如基于液滴的单细胞测序平台中的模板转换寡聚物。
在一些方面,所述索引引物包含独特的分子索引(UMI)。在一些下一代测序方案中,独特的分子标识符(UMI)是添加至每个读段的短序列或“条形码”。它们的作用是减少cDNA扩增引入的定量偏差,所述cDNA扩增是获得足够的读段以便检测所必需的。在一些具体方面,UMI包括Illumina i7UMI。
在一些方面,模板转换寡聚物包含10X细胞条形码或Drop-Seq细胞条形码。模板转换聚合酶链反应(TS-PCR)是一种通过鼠白血病病毒逆转录酶活性进行的依靠在聚腺苷酸化位点处的天然PCR引物序列并添加第二引物的逆转录聚合酶链反应(PCR)扩增的方法。例如,在Drop-Seq中,通过使用注射器泵传输稳定速率的分离的细胞和独特条形码化珠,可以将单独的细胞和珠一起分离在裂解缓冲液的液滴中,其中聚腺苷酸化位点结合至含有独特标识序列的珠特异性引物。此引物还含有标识符上游的一个共同序列,使得在通过逆转录延伸后,随后的几轮PCR将掺入标签,这允许每个分离的测序cDNA被追踪回到特定的起始珠。这允许同时分析许多单独细胞中转录物的相对水平,从而例如为将这些细胞分类为特定的细胞类型创建合理的基础。
在一些方面,每个条形码化pMHC构建体包含支架。本领域技术人员将理解,除了本文公开的支架之外,还有许多本领域已知的支架分子可用于实践要求保护的本发明(例如可使用其他聚合物代替右旋糖酐)。
在一些具体方面,所述支架包含中性抗生物素蛋白。中性抗生物素蛋白是抗生物素蛋白的去糖基化形式,其质量约为60,000道尔顿。由于碳水化合物的去除,凝集素结合得以降低至无法检测的水平,然而生物素结合亲和力得以保留,因为碳水化合物不是这种活性所必需的。抗生物素蛋白具有高pI,但中性抗生物素蛋白具有近中性的pI(pH 6.3),从而使得与带负电荷的细胞表面或与DNA/RNA的非特异性相互作用最小化。中性抗生物素蛋白仍具有赖氨酸残基,所述赖氨酸残基可用于衍生化或缀合。类似于抗生物素蛋白本身,中性抗生物素蛋白是一种四聚体,对生物素有很强的亲和力(Kd=10-15M)。
在一些具体方面,所述支架包含右旋糖酐。右旋糖酐是一种复杂的支化葡聚糖(由葡萄糖缩合而来的多糖)。IUPAC将右旋糖酐定义为“微生物来源的具有主要为C-1→C-6的糖苷键的支化聚-α-d-葡糖苷”。[1]右旋糖酐链的长度不等(从3至2000kDa)。聚合物主链由在葡萄糖单体之间的α-1,6糖苷键和从α-1,3键的分支组成。
在一些方面,每个条形码化pMHC构建体包含4个相同的附接至中性抗生物素蛋白支架上的pMHC单体。在其他方面,条形码化pMHC包含1、2、3、4个附接至中性抗生物素蛋白支架上的pMHC单体。
在一些方面,每个条形码化pMHC构建体包含1、2、3、4、5、6、7、8、9或10个附接至右旋糖酐支架上的pMHC单体。在一些方面,每个条形码化pMHC构建体包含5个相同的附接至右旋糖酐支架上的pMHC单体。
在一些方面,所述包含T淋巴细胞的样品为例如外周血样品、脐带血样品、组织活检样品、液体活检样品或其组合。在一些方面,所述样品包括纯化或部分纯化的T淋巴细胞。在一些方面,所述样品是汇集的样品。在一些方面,所述汇集的样品包括来自同一个体的多个样品。在一些方面,所述汇集的样品包括来自多个个体的多个样品。在一些方面,从多个个体汇集的所有样品都是同一类型的样品。
在一些方面,所述一个样品或多个样品是从人类受试者获得的。在其他方面,所述一个样品或多个样品是从动物获得的。在一些方面,所述一个样品或多个样品是从动物模型例如小鼠、大鼠或非人灵长类动物获得的。在一些方面,所述一个样品或多个样品是从细胞系获得的。
在一些方面,用于PCR扩增和退火到索引引物的5'恒定区序列包含如SEQ ID NO:1中所示的核酸序列(ACCTTAAGAGCCCACGGTTCC)。在一些方面,退火到在单细胞测序平台中的模板转换寡聚物的3'恒定区序列包含如SEQ ID NO:2中所示的核酸序列(AAAGAATATACCC)。
本公开文本还提供了通过本文公开的任何方法鉴定的T细胞表位。还提供了通过本文公开的任何方法鉴定的T细胞转录组。
在本公开文本的一些方面,T细胞表位的鉴定可以是定性的。在其他方面,T细胞表位的鉴定可以是定量的。在一些方面,在转录组分析中鉴定的基因是定性确定的。在一些方面,在转录组分析中鉴定的基因是定量确定的。
在一些方面,在应用本文公开的方法时获得的T细胞表位数据和/或转录组数据可用作生物标记物。生物标记物的存在或不存在、生物标记物相对于一个或多个阈值的量、生物标记物相对于一个或多个对照的增加或减少、或这些的组合可用于例如,
(i)对受试者群体进行分层,
(ii)确定受试者的预后,
(iii)用某种治疗剂治疗受试者,
(iv)中止用某种治疗剂对受试者的治疗,
(v)改变用某种治疗剂对受试者的治疗,
(vi)确定受试者对治疗剂或缺乏治疗剂的反应,
(vii)选择患者进行采用治疗剂的治疗,
(viii)确定治疗剂的功效,
(ix)筛选治疗剂以确定其治疗疾病或病症的功效,或
(x)其任何组合。
本公开文本还提供了可用于实践以上公开的方法的条形码化肽构建体。这些条形码化肽构建体包含(a)支架(例如中性抗生物素蛋白或右旋糖酐支架),(b)共价或非共价附接至支架上的肽群体(例如pMHC),和(c)至少一种共价或非共价附接至所述支架上的核酸条形码(例如DNA条形码)。在一些方面,本文公开的条形码化肽构建体包含至少一种pMHC和至少一种DNA条形码,所述DNA条形码包含至少一种样品标识序列和至少一种PCR扩增引物。
在一些方面,本公开文本的条形码化肽构建体可以包含pMHC以外的肽,例如结合T淋巴细胞中的表面受体(不是TCR)的非pMHC肽。此外,在一些方面,本公开文本的条形码化肽构建体可以靶向T淋巴细胞以外的淋巴细胞,或者甚至不是淋巴细胞的细胞。因此,通常,本文公开的条形码化肽构建体可用于产生条形码化文库,所述条形码化文库包含与某种细胞表面上的一种或多种受体结合的肽,其中特定条形码化肽构建体与细胞表面上的特定受体分子的结合可用于鉴定某种类型的受体的存在或者鉴定或表征受体对某种配体或配体变体的特异性。如上文所公开的,通过使用本公开文本的条形码化肽构建体对某种表面受体的鉴定和表征可以是定量和/或定性的。
本公开文本还提供了制造本文公开的条形码化肽构建体的方法。在一些方面。所述制造方法包括将至少一种肽(例如pMHC)共价或非共价附接至支架分子(例如中性抗生物素蛋白)上,并且将至少一种条形码(例如本文公开的DNA条形码)共价或非共价附接至所述支架上。
在具体方面,所述制造方法包括将SEQ ID NO:3的DNA条形码共价附接至中性抗生物素蛋白支架上,并且将4个相同的pMHC单体非共价附接至所述中性抗生物素蛋白支架上。
在另一个具体方面,所述制造方法包括将SEQ ID NO:3的DNA条形码非共价附接至右旋糖酐支架上,并且将5个相同的pMHC单体非共价附接至所述右旋糖酐支架上。
通过以下实施例进一步说明本发明,不应将所述实施例视为进一步限制。本申请中引用的所有附图和所有参考文献、专利和公开的专利申请的内容通过引用明确地并入本文。
实施例1
DNA条形码与中性抗生物素蛋白或右旋糖酐缀合物的产生
本文公开的方法使用特定DNA条形码,其允许使用基于液滴的测序方法在单细胞水平上同时鉴定抗原特异性T淋巴细胞和表征其转录组。
DNA条形码可以用5'生物素标签或5'硫醇修饰物合成,并分别附接至链霉亲和素-右旋糖酐或中性抗生物素蛋白的表面(图1)。对于与链霉亲和素-右旋糖酐的缀合,5'修饰的DNA条形码的滴定量允许估计每个右旋糖酐主链有一个DNA条形码。DNA条形码由基于汉明码设计的12bp样品标识序列组成,所述样品标识序列侧接两个恒定区:
5’ACCTTAAGAGCCCACGGTTCC 3’(SEQ ID NO:1)(DNA条形码的5'端,用于PCR扩增和退火到Illumina i7索引引物)。
5’AAAGAATATA CCC 3’(SEQ ID NO:2)(DNA条形码的3'端,用于退火到在10X单细胞或其他基于液滴的单细胞平台中的模板转换寡聚物)。
条形码的中间12个核苷酸(标记为“nnnnnnnnnnnn”)指定对每个表位具有特异性的四聚体DNA条形码。此序列可用于在测序后对读段进行解卷积。为了鉴定多个表位,人们可以为每个目的表位设计特定的条形码,可以合并条形码,因此使得能够在与单细胞悬浮液孵育期间进行多路复用。因此完整的DNA条形码将是
5'-生物素/5'-硫醇-ACCTTAAGAGCCCACGGTTCCnnnnnnnnnnnnAAAGAATATACCC-3’(SEQ ID NO:3)。
实施例2
DNA条形码化pMHC多聚体文库的构建。
化学合成的或可商购的肽用于合成生物素化MHC/肽复合物,如Garboczi等人(1992)PNAS,3429-3433所述。四个或五个生物素化pMHC单体与DNA条形码化右旋糖酐或DNA条形码化中性抗生物素蛋白上未占据的SA结合位点缀合。将DNA条形码化pMHC多聚体(“pMHC构建体”)汇集,使得每个DNA条形码编码不同的pMHC多聚体。图2示意性地描述了该过程。
在已知的生物素结合蛋白中,pMHC四聚体使用DNA条形码标记的中性抗生物素蛋白为核心而不是使用链霉亲和素为核心的策略提供了非特异性结合最低的优点。
最终的文库由不同的pMHC多聚体(“pMHC构建体”)组成,它们中的每一个由独特的DNA条形码编码。在此方法中利用DNA条形码作为标识对特定pMHC多聚体具有特异性的T淋巴细胞的信标。每种特异性四聚体读段将指示细胞表面上特异性表位的表达。
实施例3
利用以DNA条形码化的pMHC多聚体对抗原特异性T细胞进行染色
利用以DNA条形码化的pMHC多聚体对抗原特异性T细胞进行染色,以便使用基于液滴的测序技术同时检测和表征抗原特异性T细胞。
可收集来自外周血、脐带血、组织活检物、液体活检物、或由T淋巴细胞组成的任何其他细胞的单细胞悬浮液,并在磷酸盐缓冲盐水中洗涤两次。然后,将细胞用冰冷却的封闭缓冲液(2%BSA,0.01%吐温-20或其他低离子试剂,和10%FBS)洗涤。通过将细胞与可商购的Fc受体封闭缓冲液在冰上孵育10分钟来阻断非特异性相互作用。在阻断后,将细胞通过与用DNA条形码编码的pMHC多聚体文库在冰上孵育30分钟进行染色。
染色后,通过在冰冷却的封闭缓冲液中洗涤细胞5次来去除T细胞受体与MHC多聚体之间的非特异性相互作用,以及自由漂浮的MHC多聚体。将适当数量的细胞重悬浮于磷酸盐缓冲盐水中,以装载在10X genomics单细胞平台或其他基于液滴的系统上。在合成cDNA的同时,还添加了独特的细胞条形码,所述独特的细胞条形码编码每个被包封在油滴中的细胞。
在cDNA合成之后,使用10X引物扩增产物,或者在基于液滴的定制测序的情况下使用定制引物扩增产物。为确保与pMHC多聚体连接的条形码有足够的扩增,我们还添加了定制引物(ACCTTAAGAGCCCACGGTTCC)。基因表达cDNA文库和pMHC多聚体DNA条形码文库二者均被扩增和索引,以用于下一代测序技术的测序。
测序的读段将被解复用以获得fastq文件。
将从中提取以下特征:
1.10X或Dropseq细胞条形码-用于鉴定产生读段的细胞
2.独特的分子索引(UMI)-用于鉴定来自PCR扩增的读段。
3.测序读段-来自基因的读段。
4.来自pMHC多聚体的DNA条形码-以鉴定来自pMHC多聚体的读段。
从fastq文件中提取的信息用于构造矩阵,其中行对应于与pMHC多聚体连接的基因或条形码。这些矩阵中的列对应于细胞条形码。这里提出的策略不仅允许筛选大的抗原池,鉴定T淋巴细胞表面上的受体,鉴定抗原特异性T淋巴细胞,并且允许在单细胞水平上研究所述抗原特异性T淋巴细胞的转录组。
***
应理解,具体实施方式部分(而不是发明内容和摘要部分)旨在用于解释权利要求。发明内容和摘要部分可以阐述如本发明人所设想的本发明的一个或多个但不是所有示例性实施方案,并且因此,并非旨在以任何方式限制本发明和所附权利要求。
以上已经借助于功能构造模块(展示特定功能的实施及其关系)描述了本发明。为了描述方便,本文已经任意定义了这些功能构造模块的边界。只要适当执行特定功能及其关系,就可以定义替代的边界。
具体实施方案的前面描述将充分揭示本发明的总体性质,使得其他人可以通过应用本领域技术内的知识,在无需过度实验并且不偏离本发明总体概念的情况下容易地修改和/或改编此类具体实施方案的各种应用。因此,基于本文提出的传授内容和指导,此类改编和修改旨在处于所公开的实施方案的等效物的含义和范围内。应理解,本文中的措辞或术语是出于描述而非限制的目的,因此本说明书的术语或措辞将由熟练技术人员根据传授内容和指导来解释。
本发明的宽度和范围应当不限于以上描述的示例性实施方案中的任一个,而应当仅根据以下权利要求和它们的等效物来限定。
本申请中的权利要求与母案申请或其他相关申请的权利要求不同。因此,申请人撤销在与本申请有关的母案申请或任何先前申请中对权利要求范围所作的任何免责声明。因此,应告知审查员,可能需要重新查看任何此类先前免责声明以及应规避的引用参考文献。此外,还应提醒审查员,在本申请中所作的任何免责声明不应被读入母案申请中或抵抗母案申请。
序列表
<110> 百时美施贵宝公司
<120> 条形码化肽-MHC复合物及其用途
<130> 13205-WO-PCT
<150> 62/735803
<151> 2018-09-24
<160> 3
<170> PatentIn 3.5版
<210> 1
<211> 21
<212> DNA
<213> 人工序列
<220>
<223> 寡核苷酸
<400> 1
accttaagag cccacggttc c 21
<210> 2
<211> 13
<212> DNA
<213> 人工序列
<220>
<223> 寡核苷酸
<400> 2
aaagaatata ccc 13
<210> 3
<211> 46
<212> DNA
<213> 人工序列
<220>
<223> 寡核苷酸
<220>
<221> 尚未归类的特征
<222> (22)..(33)
<223> n是a、c、g或t
<400> 3
accttaagag cccacggttc cnnnnnnnnn nnnaaagaat ataccc 46
- 条形码化肽-MHC复合物及其用途
- 靶向NY‑ESO‑1肽/MHC复合物的构建体及其用途
