比格犬血浆中达拉他韦的定量检测方法
文献发布时间:2023-06-19 09:43:16
技术领域
本发明涉及一种药物浓度的检测,属于药物检测技术领域,具体地涉及一种比格犬血浆中达拉他韦的定量检测方法。
背景技术
丙型肝炎是临床常见的传染性疾病之一,丙肝已被公认为是造成全球慢性肝脏疾病的主要原因,约有27%肝硬化、25%肝细胞癌是由丙肝引起的。丙肝已成为一种不容忽视的公共卫生问题,引起了全社会的广泛关注。
达拉他韦是一种选择性HCV非结构蛋白5a复制体抑制剂,对多个慢性丙型肝炎(HCV)基因型/亚型具有高度特异性,对宿主细胞的毒性较低。其由百时美施贵宝公司研发,2014年底获欧盟批准上市,联合其他药物,用于1、2、3、4基因型慢性丙型肝炎(HCV)成人感染者的治疗。并于2017年4月,中国国家食品药品监督管理总局批准盐酸达拉他韦片和阿舒瑞韦胶囊进口上市,用于成人慢性丙型肝炎的联合治疗,这是国内首次获批全口服抗丙型肝炎病毒的药物(DAA)。直接抗病毒药物(DAAs)的问世开创了丙型肝炎治疗新时代,使丙型肝炎的临床治愈成为可能。
盐酸达拉他韦(Daclatasvir Dihydrochloride),化学名为((1S)-1-(((2S)-2-(5-(4’-(2-((2S)-1-((2S)-2-((甲氧羰基)氨基)-3-甲基丁酰基)-2-吡咯烷基)-1H-咪唑-5-基)-4-联苯基)-1H-咪唑-2-基)-1-吡咯烷基)羰基)-2-甲基丙基)氨基甲酸甲酯二盐酸盐,其结构如下所示:
百时美施贵宝公司在专利CN101778841A中公开了一种盐酸达拉他韦的合成方法,并提到了其精制方法,中国专利CN109305962A公开了一种盐酸达拉他韦的精制方法。然而现有技术并未公开关于其在动物体内的药物检测方法,因此需要开发一种快速、灵敏、准确的分析方法来定量血浆中达拉他韦的浓度。
发明内容
为解决上述技术问题,本发明公开了一种比格犬血浆中达拉他韦的定量检测方法。该检测方法不仅具备操作简便、灵敏度高、重现性好、选择性高、检测限低、分析时间短等优点,同时还适合对比格犬血浆样本的高通量定量测定。
为实现上述技术目的,本发明公开了一种比格犬血浆中达拉他韦的定量检测方法,它包括如下步骤:
1)配制达拉他韦系列工作溶液和达拉他韦-d6内标工作溶液;
2)待测比格犬血浆的预处理:向待测比格犬血浆中加入步骤1)所述达拉他韦-d6内标工作溶液及乙腈沉淀剂后,经过首次涡旋混合、离心分离、上清液加纯化水和二次涡旋混合后得处理后待测比格犬血浆;
3)配制系列校正标样及随行质控样品:将步骤1)所述达拉他韦系列工作溶液分为两份,分别加入比格犬空白血浆后,制备得到系列校正标样及随行质控样品;
4)测定待测比格犬血浆中达拉他韦浓度:取待测比格犬血浆、步骤3)的系列校正标样、随行质控样品按步骤2)的方式预处理后分别送入LC-MS/MS中进行测定,以达拉他韦和内标达拉他韦-d6的色谱峰面积比为纵坐标,以比格犬空白血浆中达拉他韦的浓度为横坐标制作标准曲线,根据所述标准曲线计算出待测比格犬血浆中达拉他韦浓度。
进一步地,步骤2)和3)中,所述乙腈沉淀剂体积为待测比格犬血浆或比格犬空白血浆体积的4~8倍。
进一步地,步骤2)和3)中,所述离心分离温度为2~8℃。
进一步地,步骤3)中,所述系列校正标样的个数为6~10个,所述系列校正标样中达拉他韦的浓度为5.00~2000ng·mL
所述随行质控样品包括DQC、HQC、MQC、GMQC、LQC和LLOQ QC;所述DQC中达拉他韦的浓度为4000ng·mL
进一步地,步骤4)中,所述色谱条件:色谱柱为ACE Excel 5C18-AR,2.1×50mm;流动相A:100%的水含0.1%甲酸和2mM乙酸铵;流动相B:100%的乙腈;流速:0.2~0.8mL/min;洗脱方式为梯度洗脱,且柱温箱温度:30~50℃。
进一步地,所述色谱条件还包括采用自动进样器进样,所述自动进样器进样体积为5.00μL,自动进样器温度为8.0℃;
且所述自动进样器清洗溶液为甲醇,自动进样器洗针体积为1000μL;自动进样器进样针清洗时浸泡时间为1s,自动进样器清洗模式为进样前清洗和进样后清洗。
进一步地,步骤4)中,所述质谱条件包括,离子源为ESI源,采用正离子模式、多反应监测模式;电喷雾电压:5000~6000V;涡旋离子喷雾温度:400~600℃;气帘气:35psi;碰撞池气体:中级;离子源气体Gas1:50psi;辅助气Gas2:50psi;数据收集时间:1~4min。
进一步地,所述质谱条件还包括达拉他韦的监测离子对为739.5/565.4,每次扫描一个离子对时所停留的时间150msec,去簇电压40V,碰撞能量60V;
内标达拉他韦-d6的监测离子对为745.5/568.4,每次扫描一个离子对时所停留的时间150msec,去簇电压40V,碰撞能量60V。
进一步地,步骤1)中,所述达拉他韦系列工作溶液中达拉他韦浓度为100~40000ng·mL
进一步地,步骤1)中,
所述达拉他韦系列工作溶液的配置过程如下:
取达拉他韦用甲醇溶解后,继续用甲醇水溶液稀释成达拉他韦浓度为100~40000ng·mL
所述内标工作溶液的配置过程如下:
取达拉他韦-d6用甲醇溶解后,继续用甲醇水溶液稀释成达拉他韦-d6浓度为100~300ng·mL
所述甲醇水溶液中甲醇与水的体积比为1:1。
有益效果:
1、本发明提供的比格犬血浆中达拉他韦的定量检测方法,采用多反应监测模式和氘代内标达拉他韦-d6进行定性和定量,能够有效提高定性准确度和方法的灵敏度,最低检测限可达到5ng·mL
2、本发明提供的比格犬血浆中达拉他韦的定量检测方法,利用校正标样及随行质控样品确定标准曲线,提高了检测的精密度和准确度,确保定性定量分析结果可靠。
附图说明
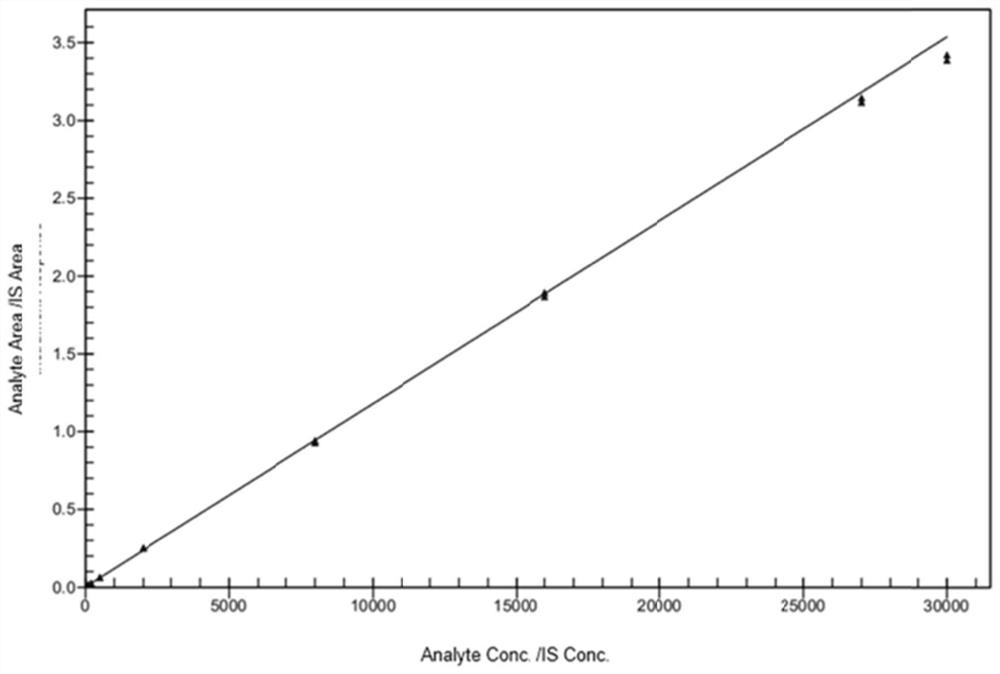
图1为本发明设计的待测比格犬血浆中达拉他韦浓度测定的代表性标准曲线;
图2为实施例中空白血浆样品中达拉他韦和达拉他韦-d6的MRM色谱图;
图3为实施例中LLOQ血浆样品中达拉他韦和达拉他韦-d6的MRM色谱图;
图4为实施例中待测比格犬血浆样品中达拉他韦和达拉他韦-d6的MRM色谱图;
图5为本发明设计的待测比格犬血浆中达拉他韦浓度测定的代表性内标散点图。
具体实施方式
本发明为解决现有技术并未公开关于达拉他韦在动物体内及人体内的药物检测方法,公开了一种比格犬血浆中达拉他韦的定量检测方法。该检测方法主要包括如下步骤:
1)配制达拉他韦系列工作溶液和达拉他韦-d6内标工作溶液;
2)待测比格犬血浆的预处理:向待测比格犬血浆中加入步骤1)所述达拉他韦-d6内标工作溶液及乙腈沉淀剂后,经过首次涡旋混合、离心分离、上清液加纯化水和二次涡旋混合后得处理后待测比格犬血浆;
3)配制系列校正标样及随行质控样品:将步骤1)所述达拉他韦系列工作溶液分为两份,分别加入比格犬空白血浆后,制备得到系列校正标样及随行质控样品;
4)测定待测比格犬血浆中达拉他韦浓度:取待测比格犬血浆、步骤3)的系列校正标样、随行质控样品按步骤2)的方式预处理后分别送入LC-MS/MS中进行测定,以达拉他韦和内标达拉他韦-d6的色谱峰面积比为纵坐标,以比格犬空白血浆中达拉他韦的浓度为横坐标制作标准曲线,根据所述标准曲线计算出待测比格犬血浆中达拉他韦浓度。
1、本发明设计的检测方法涉及使用的的检测仪器及相关型号如下:
分析天平:XP6百万分之一电子天平,METTLER TOLEDO;
离心机:5810R离心机,Eppendorf;
超声清洗器:KQ-400DE超声波清洗器,昆山市超声仪器有限公司;
移液器:0.5~10μL,2~20μL,20~200μL,100~1000μL,Eppendorf;
玻璃样品瓶及螺旋盖:包含1.5mL,4mL,10mL,100mL,500mL,1000mL及2000mL等不同规格,武汉宝因生物科技有限公司;
96孔深孔板:DW-96-22-C,2.2mL,上海百赛生物技术股份有限公司;
聚丙烯离心管:1.5mL,武汉宝因生物科技有限公司;
高效液相色谱泵:LC-30AD,Shimadzu公司;
自动进样器:SIL-30AC
柱温箱:CTO-20AC,Shimadzu公司;
质谱仪:QTRAP5500,ABSciex公司;
2、具体检测过程如下:
(1)储备液和标准工作溶液的配制:
储备液的配制:精密称取两份一定量的达拉他韦对照品至玻璃瓶中,精密加入一定体积的甲醇,配制成浓度为1.00mg·mL-1的达拉他韦储备液,标记为S1-1与S1-2;称取一定量的达拉他韦-d6作为内标至玻璃瓶中,精密加入一定体积的甲醇,配制成达拉他韦-d6的浓度为1.00mg·mL
将配制好的达拉他韦储备液用体积比为1:1的甲醇水溶液逐级稀释成浓度为40000ng·mL
(2)血浆样品的预处理:
(2.1)待测比格犬血浆样品的预处理:
取20.0~60.0μL的待测比格犬血浆样品进行预处理,本发明优选取50.0μL待测比格犬血浆样品,加入50.0μL上述步骤(1)配制的内标工作溶液,然后加入300μL乙腈沉淀剂,涡旋混合至少10分钟,继续置于2~8℃的离心机中以4000rpm的离心速度离心处理8~12分钟,之后静置,取部分上部清液至干净的96孔板中,加入纯化水,继续振荡混匀至少3分钟,进行LC-MS/MS分析。其中,本发明优选置于4℃的离心机中以4000rpm的离心速度离心处理10分钟,效果最好。其中,上述待测比格犬血浆样品是通过临床试验得到。
(2.2)空白比格犬血浆样品的预处理:
分别取20μL步骤(1)配制的达拉他韦工作溶液,加入到380μL空白人血浆中,经过如步骤(2.1)的预处理过程,配制成5.00ng·mL
(3)LC-MS/MS测定过程工作条件为:
(3.1)色谱条件:
色谱柱:ACE Excel 5C18-AR,2.1×50mm;
流动相A:100%的水含0.1%甲酸和2mM乙酸铵;
流动相B:100%的乙腈;梯度洗脱;
0~1.30分钟:25%→38%B、75%→62%A;
1.30~1.31分钟:38%→95%B、62%→5%A;
1.31~1.80分钟:95%B、5%A;
1.80~1.81分钟:95%→25%B、5%→75%A;
1.81~3.00分钟:25%B、75%A;
其中,以乙腈作为流动相中有机相可使待测物质谱图响应峰值更高,加入0.1%甲酸有利于提高后续质谱分析的离子化效率,而选择加入2mM乙酸铵和0.1%甲酸两种添加剂是为了得到尖锐的峰型和更高的检测灵敏度,保证分析物和内标的保留时间重现性。
自动进样器清洗溶液:甲醇;
柱温箱温度:40℃;
流速:0.45mL/min;
自动进样器温度:8.0℃;
自动进样器清洗模式:进样前清洗和进样后清洗;
自动进样器洗针体积:1000μL;
自动进样器进样针清洗时浸泡时间:1s;
自动进样器进样体积:5.00μL;
洗脱梯度:洗脱梯度如表1所示。
表1洗脱梯度列表
(3.2)质谱条件:
离子化模式:正离子模式,电喷雾离子源(ESI);
扫描模式:多反应监测(MRM);
电喷雾电压:5500V;
涡旋离子喷雾温度:500℃;
气帘气种类:氮气,设置为35psi;
碰撞池气体种类:氮气,设置为中级;
雾化气种类:氮气,设置为50psi;
辅助气种类:氮气,设置为50psi;
数据收集时间:约1.2min;
分析物和内标的监测离子对、停留时间、去簇电压和碰撞能量参数见表2。
表2质谱部分条件列表
其中,表2中,停留时间,此处指的是在监测离子对时,每次扫描一个离子对时所停留的时间。
(4)分析结果:进样原始结果见表3,以达拉他韦和达拉他韦-d6的峰面积比(Analyte Area/IS Area)为纵坐标,比格犬血浆中达拉他韦的浓度(ng·mL
同时结合图2、图3及图4可知,本发明选择的内标物达拉他韦-d6和待测物达拉他韦在本发明设计的测量方法中所表现出的峰形及保留时间一致性较高,这一方面说明了本发明选择的内标物稳定性好,另一方面也间接的体现了检测方法的重现性高。其中,图2至图4中,图a表示待测物达拉他韦峰形,图b表示内标物达拉他韦-d6峰形,由图5说明同一分析批当中,内标响应波动很小,基本上是一条直线,方法重复性好。
表3图1中八个坐标点对应数据
其中,表3中每个标曲样品浓度设置两个2个平行样品;
(5)准确度及精密度评价:
为对上述实施例中LC-MS/MS方法测定比格犬血浆中达拉他韦浓度的准确度、精密度进行评价,本发明设计具体的取50.0μL上述由高到低的HQC、MQC、GMQC、LQC、LLOQ QC五个浓度的质控样品各6份,按上述方法操作,于1日内进行LC-MS/MS测定,计算准确度和精密度,结果如下表所示:
表4准确度及精密度评价表
由上述表4可知,本发明设计的检测方法日内和日间的准确度高,精密度也好。
由上述描述可知,本发明提供的是一种首次公开的比格犬血浆中达拉他韦的LC-MS/MS定量检测方法,并且各项验证指标均符合ICH指导原则,采用本发明提供的方法能够高效、便捷、准确的进行样品分析,可应用于临床前比格犬血浆中达拉他韦的药代动力学特征的研究,缩短达拉他韦一致性评价的研究周期,提高达拉他韦制剂一致性评价的通过率,利于制药企业成功仿制达拉他韦,使老百姓吃到安全、有效又便宜的药。
本发明不局限于上述可选的实施方式,任何人在本发明的启示下都可得出其他各种形式的产品。上述具体实施方式不应理解成对本发明的保护范围的限制,本发明的保护范围应当以权利要求书中界定的为准,并且说明书可以用于解释权利要求书。
- 比格犬血浆中达拉他韦的定量检测方法
- 一种血浆中沃诺拉赞的定量检测方法
