一种N1,N5-二戊基-1,5-萘二胺的合成方法
文献发布时间:2024-04-18 19:58:21
技术领域
本发明涉及一种N1,N5-二戊基-1,5-萘二胺的合成方法,属于有机电致发光材料领域。
背景技术
有机电致发光器件(OELD)在大容量信息传输、超高密度信息存储、现代平板显示技术、静电复印、全息照相、激光打印、轻印刷制版、计算机终端仪器等领域具有广泛的应用。其中1,5-萘二胺类衍生物N1,N5-二戊基-1,5-萘二胺(DAN)由于氨基距离较近,结构紧凑,有利于增加相邻分子间的接触机会,造成多感性,具有较大的空穴迁移率,较优的光物理及光化学性能,以及良好的热稳定性,广泛应用于有机电致发光器件的研究中。因此,N1,N5-二戊基-1,5-萘二胺的合成工艺研究具有重要意义。
目前,N1,N5-二戊基-1,5-萘二胺的合成路线主要有以下几种:
第一种是类似的1,5-萘二胺与1-溴己烷反应制备N1,N5-二己基-1,5-萘二胺,收率30%。该方法存在的问题是收率低,反应选择性差,容易产生多取代副产物,后处理复杂,不利于放大生产。所述反应式如式1所示:
第二种是1,5-萘二胺与正戊酰氯在碱性试剂作用下,反应4h,制备N,N’-(萘-1,5-二酰基)双戊酰胺,收率为88.37%~92.68%;然后被3.0~4.5当量的硼氢化钠还原,并且在三氟化硼乙醚催化下保温过夜反应,得到N1,N5-二戊基-1,5-萘二胺,收率72.85%~89.32%。该反应硼氢化钠用量较大,反应时间较长,不适合放大生产。所述反应式如式2所示:
第三种是在80℃下,±BINAP溶解在无水甲苯中,再降温至30℃,加入醋酸钯,然后在室温下加入1,5-二碘萘、碳酸铯和甲胺四氢呋喃溶液,在80℃反应48h,得到N1,N5-二甲基-1,5-萘二胺,收率89%。该方法可用于类似的N1,N5-二戊基-1,5-萘二胺的制备,但存在钯盐催化剂和消旋化的配体±BINAP价格昂贵的问题,难以回收利用,也不适合工业化生产。所述反应式如式3所示:
第四种是1,5-萘二胺与2当量的醛,在二氯乙烷与乙酸混合溶液中,在3当量三乙酰氧基硼氢化钠还原下,从室温升温至50℃后加热反应21h,得到N1,N5-二取代基-1,5-萘二胺,收率为82.2%~91.9%。由于三乙酰氧基硼氢化钠的价格昂贵,反应时间较长,也不适合工业化生产。所述反应式如式4所示:
发明内容
本发明的目的在于提供一种N1,N5-二戊基-1,5-萘二胺的合成方法,不仅收率较高,而且产品质量也好。为达到上述目的,主要采用以下技术方案:
(1)环化反应:1,5-萘二胺、2-甲基四氢呋喃在三氯氧磷与有机碱作用下,在80~120℃下反应5~8h,后处理得到1,1’-(1,5-萘二基)双[2-甲基吡咯];
(2)开环反应:在有机溶剂中,1,1’-(1,5-萘二基)双[2-甲基吡咯]与N-卤代丁二酰亚胺、过氧化二苯甲酰,加热回流1~2h,减压蒸馏回收有机溶剂,残留物用氢氧化钠水溶液洗涤,再用水洗,干燥浓缩得到1,1’-(1,5-萘二基)双[5-(2-戊酮)];(3)还原反应:在贵金属催化剂作用下,1,1’-(1,5-萘二基)双[5-(2-戊酮)]与供氢体在溶剂中反应2~4h,得到N1,N5-二戊基-1,5-萘二胺。
本发明的合成路线如式5:
所述的反应步骤(1)环化反应中的有机碱为三乙胺、吡啶、N,N-二甲基甲酰胺、1,8-二氮杂双环[5.4.0]十一碳-7-烯中的一种。
所述的反应步骤(1)环化反应中的1,5-萘二胺、2-甲基四氢呋喃、三氯氧磷、有机碱物质的量之比为:1.0:2.0~3.0:2.0~3.0:2.0~3.5。
所述的反应步骤(2)开环反应中的有机溶剂为二氯甲烷、三氯甲烷、二氯乙烷、氯苯中的一种。
所述的反应步骤(2)开环反应中的N-卤代丁二酰亚胺为N-氯代丁二酰亚胺、N-溴代丁二酰亚胺、N-碘代丁二酰亚胺中的一种。
所述的反应步骤(2)开环反应中的1,1’-(1,5-萘二基)双[2-甲基吡咯]、N-卤代丁二酰亚胺、过氧化二苯甲酰的物质的量之比为:1.0:2.0~3.5:0.01~0.1。
所述的反应步骤(2)开环反应中的有机溶剂与1,1’-(1,5-萘二基)双[2-甲基吡咯]质量比为15~25:1。
所述的反应步骤(3)还原反应中的贵金属催化剂为5%钯碳、钯黑、雷尼镍、氧化铂中的一种。
所述的反应步骤(3)还原反应中的供氢体为甲酸铵、40%水合肼、80%水合肼、次磷酸钠中的一种。
所述的反应步骤(3)还原反应中的溶剂为甲醇、乙醇、异丙醇、水中的一种或两种。
所述的反应步骤(3)还原反应中的1,1’-(1,5-萘二基)双[5-(2-戊酮)]、供氢体物质的量之比为:1.0:2.0~4.0。
所述的反应步骤(3)还原反应中的贵金属催化剂与1,1’-(1,5-萘二基)双[5-(2-戊酮)]的质量比为0.001~0.01:1。
所述的反应步骤(3)还原反应中的溶剂与1,1’-(1,5-萘二基)双[5-(2-戊酮)]的质量比为5~25:1。
与现有技术相比,本发明的有益效果是:一方面,本发明使用的反应原料都为常见的市售试剂,活性较高,无需另行制备,成本低廉;本发明还具有合成工艺简便、环境友好、安全性较好、产品收率及纯度较高、易于工业化生产等优点。
附图说明
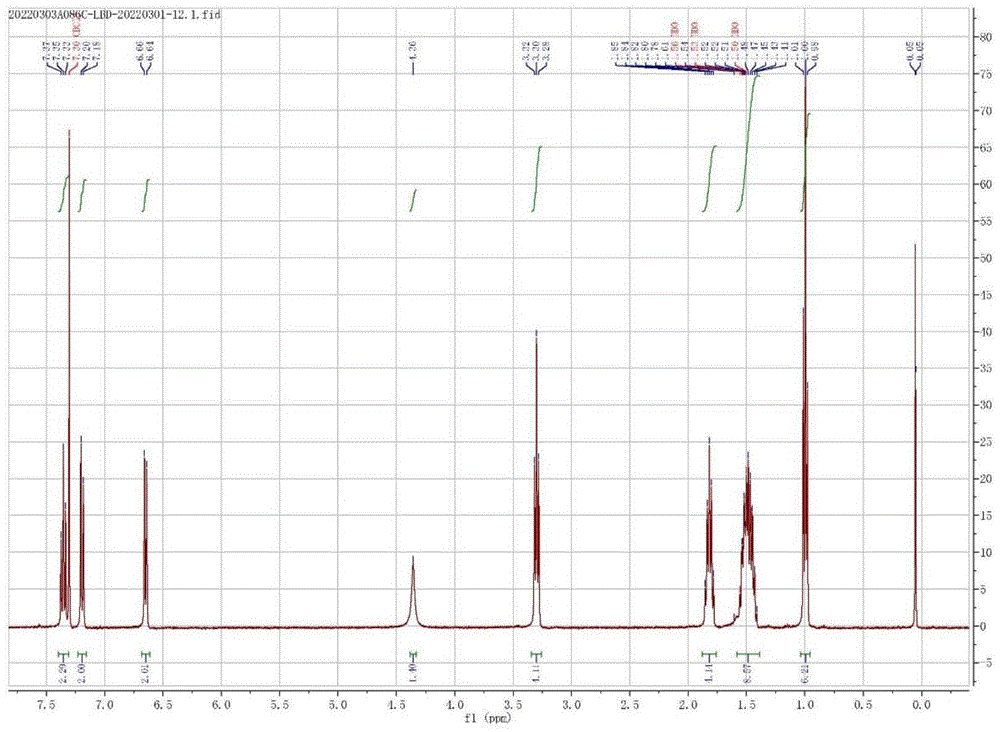
图1是本发明的N1,N5-二戊基-1,5-萘二胺的核磁氢谱图
具体实施方式
下面结合具体实施例对本发明进行进一步描述,但本发明的保护范围并不仅限于此:
实施例1
(1)环化反应:在250mL的三口烧瓶中,加入1,5-萘二胺(7.91g,0.05mol)、2-甲基四氢呋喃(10.0mL,0.1mol)、三乙胺(20.8mL,0.15mol),冷却至0~5℃,缓慢滴加三氯氧磷(11.4mL,0.125mol),滴毕,升温至90℃,反应6h,冷却至室温,然后在冰浴冷却下,缓慢滴加100mL水,再用30%NaOH溶液调节pH=8~9,然后回流1h,冷却至室温,过滤,水洗至中性;滤饼用乙醇重结晶得到1,1’-(1,5-萘二基)双[2-甲基吡咯]14.15g,收率为96.1%。
(2)开环反应:在500mL的三口烧瓶中,加入1,1’-(1,5-萘二基)双[2-甲基吡咯](11.78g,0.04mol)、二氯甲烷(220mL)、N-氯代丁二酰亚胺(13.35g,0.1mol)、过氧化二苯甲酰(0.48g,0.002mol),加热回流1.5h,减压蒸馏回收有机溶剂,残留物用100mL10%NaOH溶液洗涤,然后用水洗涤至中性,真空干燥后得到1,1’-(1,5-萘二基)双[5-(2-戊酮)]12.31g,收率为94.3%。
(3)还原反应:在250mL三口烧瓶中,加入1,1’-(1,5-萘二基)双[5-(2-戊酮)](9.79g,0.03mol)和62mL甲醇,室温下搅拌至溶解,再依次加入甲酸铵(3.78g,0.06mol)、5%钯碳催化剂0.027g,回流反应2h,趁热抽滤,用热甲醇洗涤滤饼;滤液减压浓缩,回收甲醇;残留物水洗,并用甲苯重结晶,得到N1,N5-二戊基-1,5-萘二胺8.38g,收率为93.6%,HPLC纯度为98.4%。
实施例2
(1)环化反应:在250mL三口烧瓶中,加入1,5-萘二胺(7.91g,0.05mol)、2-甲基四氢呋喃(12.5mL,0.125mol)、吡啶(14.1mL,0.175mol),冷却至0~5℃,缓慢滴加三氯氧磷(13.7mL,0.15mol),滴毕,升温至110℃,反应8h,冷却至室温,然后在冰浴冷却下,缓慢滴加100mL水,再用30%NaOH溶液调节pH=8~9,然后回流1h,冷却至室温,过滤,水洗至中性;滤饼用乙醇重结晶得到1,1’-(1,5-萘二基)双[2-甲基吡咯]14.19g,收率为96.4%。
(2)开环反应:在500mL的三口烧瓶中,加入1,1’-(1,5-萘二基)双[2-甲基吡咯](11.78g,0.04mol)、三氯甲烷(160mL)、N-溴代丁二酰亚胺(24.92g,0.14mol)、过氧化二苯甲酰(0.97g,0.004mol),加热回流1h,减压蒸馏回收有机溶剂,残留物用100mL10%NaOH溶液洗涤,然后用水洗涤至中性,真空干燥后得到1,1’-(1,5-萘二基)双[5-(2-戊酮)]12.63g,收率为96.7%。
(3)还原反应:在250mL三口烧瓶中,加入1,1’-(1,5-萘二基)双[5-(2-戊酮)](9.79g,0.03mol)和100mL乙醇,室温下搅拌至溶解,再依次加入80%水合肼(4.6mL,0.075mol)、钯黑催化剂0.013g,回流反应2.5h,趁热抽滤,用热乙醇洗涤滤饼;滤液减压浓缩,回收乙醇;残留物水洗,并用甲苯重结晶,得到N1,N5-二戊基-1,5-萘二胺8.44g,收率为94.3%,HPLC纯度为98.6%。
实施例3
(1)环化反应:在250mL三口烧瓶中,加入1,5-萘二胺(7.91g,0.05mol)、2-甲基四氢呋喃(10.0mL,0.1mol)、N,N-二甲基甲酰胺(9.6mL,0.125mol),冷却至0~5℃,缓慢滴加三氯氧磷(9.2mL,0.1mol),滴毕,升温至80℃,反应5h,冷却至室温,然后在冰浴冷却下,缓慢滴加100mL水,再用30%NaOH溶液调节pH=8~9,然后回流1h,冷却至室温,过滤,水洗至中性;滤饼用乙醇重结晶得到1,1’-(1,5-萘二基)双[2-甲基吡咯]13.97g,收率为94.9%。
(2)开环反应:在500mL的三口烧瓶中,加入1,1’-(1,5-萘二基)双[2-甲基吡咯](11.78g,0.04mol)、二氯乙烷(180mL)、N-碘代丁二酰亚胺(27.0g,0.12mol)、过氧化二苯甲酰(0.10g,0.0004mol),加热回流2h,减压蒸馏回收有机溶剂,残留物用100mL10%NaOH溶液洗涤,然后用水洗涤至中性,真空干燥后得到1,1’-(1,5-萘二基)双[5-(2-戊酮)]12.48g,收率为95.6%。
(3)还原反应:在500mL三口烧瓶中,加入1,1’-(1,5-萘二基)双[5-(2-戊酮)](9.79g,0.03mol)和150mL异丙醇,室温下搅拌至溶解,再依次加入次磷酸钠(7.92g,0.09mol)、雷尼镍催化剂0.024g,回流反应3.5h,趁热抽滤,用热异丙醇洗涤滤饼;滤液减压浓缩,回收异丙醇;残留物水洗,并用甲苯重结晶,得到N1,N5-二戊基-1,5-萘二胺8.70g,收率为97.2%,HPLC纯度为98.3%。
实施例4
(1)环化反应:在250mL三口烧瓶中,加入1,5-萘二胺(7.91g,0.05mol)、2-甲基四氢呋喃(15.0mL,0.15mol)、1,8-二氮杂双环[5.4.0]十一碳-7-烯(14.9mL,0.1mol),冷却至0~5℃,缓慢滴加三氯氧磷(9.2mL,0.1mol),滴毕,升温至120℃,反应7h,冷却至室温,然后在冰浴冷却下,缓慢滴加100mL水,再用30%NaOH溶液调节pH=8~9,然后回流1h,冷却至室温,过滤,水洗至中性;滤饼用乙醇重结晶得到1,1’-(1,5-萘二基)双[2-甲基吡咯]13.76g,收率为93.5%。
(2)开环反应:在500mL的三口烧瓶中,加入1,1’-(1,5-萘二基)双[2-甲基吡咯](11.78g,0.04mol)、氯苯(160mL)、N-氯代丁二酰亚胺(10.68g,0.08mol)、过氧化二苯甲酰(0.29g,0.0012mol),加热回流1.5h,减压蒸馏回收有机溶剂,残留物用100mL10%NaOH溶液洗涤,然后用水洗涤至中性,真空干燥后得到1,1’-(1,5-萘二基)双[5-(2-戊酮)]12.12g,收率为92.8%。
(3)还原反应:在500mL三口烧瓶中,加入1,1’-(1,5-萘二基)双[5-(2-戊酮)](9.79g,0.03mol)和190mL水,室温下搅拌至溶解,再依次加入甲酸铵(6.62g,0.105mol)、氧化铂催化剂0.067g,回流反应4h,趁热抽滤,用热甲醇洗涤滤饼;滤液减压浓缩,回收甲醇;残留物水洗,并用甲苯重结晶,得到N1,N5-二戊基-1,5-萘二胺8.69g,收率为97.0%,HPLC纯度为98.1%。
实施例5
(1)环化反应:在250mL三口烧瓶中,加入1,5-萘二胺(7.91g,0.05mol)、2-甲基四氢呋喃(12.5mL,0.125mol)、三乙胺(24.3mL,0.175mol),冷却至0~5℃,缓慢滴加三氯氧磷(13.7mL,0.15mol),滴毕,升温至100℃,反应8h,冷却至室温,然后在冰浴冷却下,缓慢滴加100mL水,再用30%NaOH溶液调节pH=8~9,然后回流1h,冷却至室温,过滤,水洗至中性;滤饼用乙醇重结晶得到1,1’-(1,5-萘二基)双[2-甲基吡咯]13.93g,收率为94.6%。
(2)开环反应:在500mL的三口烧瓶中,加入1,1’-(1,5-萘二基)双[2-甲基吡咯](11.78g,0.04mol)、二氯甲烷(180mL)、N-溴代丁二酰亚胺(21.36g,0.12mol)、过氧化二苯甲酰(0.78g,0.0032mol),加热回流2h,减压蒸馏回收有机溶剂,残留物用100mL10%NaOH溶液洗涤,然后用水洗涤至中性,真空干燥后得到1,1’-(1,5-萘二基)双[5-(2-戊酮)]11.95g,收率为91.5%。
(3)还原反应:在500mL三口烧瓶中,加入1,1’-(1,5-萘二基)双[5-(2-戊酮)](9.79g,0.03mol)和240mL乙醇-水(1:1,V/V),室温下搅拌至溶解,再依次加入40%水合肼(14.6mL,0.12mol)、5%钯碳催化剂0.098g,回流反应3h,趁热抽滤,用热乙醇洗涤滤饼;滤液减压浓缩,回收乙醇;残留物水洗,并用甲苯重结晶,得到N1,N5-二戊基-1,5-萘二胺8.22g,收率为91.8%,HPLC纯度为98.8%。
N1,N5-二戊基-1,5-萘二胺的HPLC分析条件为:高效液相色谱仪(Agilent1200Series);色谱柱型号为LlChrospher 60RP-select B(5μL);流动相为碳酸氢铵缓冲液(称取3.79g碳酸氢铵于1000mL水中溶解,用磷酸调节pH=6.0):乙腈(体积比为30:70);流速为1.0mL/min,柱温:30℃,进样量为10μL;检测器为紫外光度检测器,波长为240nm;样品用乙腈溶解稀释后(0.01mg/mL)进样。
本发明中所描述的具体实施例仅是对本发明精神作举例说明。本发明所属技术领域的技术人员可以对所描述的具体实施例作各种各样的修改或补充或采用类似的方式替代,但并不会偏离本发明的精神或者超越所附权利要求书所定义的范围。
尽管对本发明已作了详细的说明并引证了一些具体实施例,但是对本领域熟练的技术人员来说,只要不离开本发明的精神和范围可作各种变化或修正是显然的。
- 一种N1,N5-二戊基萘-1,5-二胺制备方法
- 一种RuO2负载聚1,5-萘二胺纳米管的合成方法
