一种医用聚醚醚酮复合材料及其制备方法和应用
文献发布时间:2024-04-18 20:00:50
技术领域
本发明属于生物医用高分子材料技术领域,具体涉及一种医用聚醚醚酮复合材料及其制备方法和应用。
背景技术
聚醚醚酮(PEEK)作为一种医用高分子,已经广泛应用于脊柱类椎间融合器等脊柱固定系统,运动医学类界面螺钉、锚钉等关节固定系统,颅骨修复系统等骨科植入类医疗器械。其主要优势体现在:首先,PEEK的弹性模量接近皮质骨,并且弹性优于金属,这能避免对骨骼的应力遮蔽效应,从而延长骨骼寿命,使骨骼更健康;其次,PEEK在使用X射线、CT扫描、MRI和其他成像方法时可提供出色的种植体可视化效果,可以规避金属材料吸收X射线并在X-光图像上产生伪影的缺陷。然而,PEEK医疗器械的劣势也不能忽略,PEEK由于其相对疏水的表面而具有较低的表面能,从而限制了细胞的黏附,PEEK的这种生物惰性使得PEEK植入体与宿主骨组织之间的骨整合能力较差,在临床上经常会碰到许多并发症,如种植体移位、笼陷或假性关节,这在体外和临床应用研究中都导致了令人不满意的结果。因此,解决PEEK表面的生物惰性,促进骨细胞的黏附和增殖,诱导PEEK植入物所接触的骨组织生长愈合,以增强PEEK植入物与宿主骨组织之间的骨整合能力,是行业内亟需解决的技术难题。
磷酸钙作为骨组织的主要无机成分,具有优良的骨传导性和骨诱导性,因此,含磷酸钙的PEEK复合材料的开发是解决PEEK表面的生物惰性,提高其生物活性和生物相容性的一大研究热点。一般来说,随着磷酸钙化合物含量升高,复合材料的生物活性相应升高,但因磷酸钙含量仍偏低,升高程度有限;当磷酸钙化合物含量低于某一浓度阈值时,力学性能随之升高,但当磷酸钙化合物含量达到一定浓度阈值,并逐渐成为连续相后,会发生团聚且加工效果较差,导致材料脆性加大。
CN110152068A采用通过球磨预混结合双螺杆挤出的复合改性工艺,制备出分散均匀的聚醚醚酮/磷酸钙复合材料。该方法的不足之处在于未对聚醚醚酮或磷酸钙进行表面改性,只是采用球磨这种机械混合的方法将聚醚醚酮和磷酸钙化合物混合均匀,虽然一定程度上得到了机械强度和生物活性改进的复合材料,但是聚醚醚酮与磷酸钙颗粒的复合会带来界面分层,且磷酸钙颗粒易发生团聚,造成形状不规则,也使得该复合材料在临床长期应用于人体时,存在磷酸钙颗粒析出的风险,从而造成复合材料生物活性的下降。此外,该方法采用机械混合后再挤出造粒的方法,聚醚醚酮与磷酸钙颗粒之间的物理混合会导致该混合料在挤出机熔融后流动性变差,磷酸钙颗粒易发生团聚,形状不规则,加工性能不佳。
CN112587732A公开了一种磷酸钙化合物与磺化聚醚醚酮复合材料的制备方法,该方法将磺化聚醚醚酮基体浸入到磷酸钙的凝胶中,浸涂满凝胶后进行煅烧,煅烧温度为600-800℃,得到复合材料。一般来说,作为线性热塑性塑料,聚醚醚酮在330-420°C的温度范围内进行熔融加工。因此,该方法的不足之处在于涂覆磷酸钙凝胶的聚醚醚酮在600-800℃范围内煅烧,600℃以上的高温极易破坏聚醚醚酮的化学或物理结构,容易导致聚醚醚酮的部分链锻重排甚至降解,损害聚醚醚酮的使用性能。该方法获得的聚醚醚酮复合材料应用于长期植入体内的器械,会有降解以及产生毒副作用的风险。此外,磷酸钙的加入容易损害聚醚醚酮的机械性能,煅烧后的聚醚醚酮/磷酸钙复合材料较难保持优异的柔韧性能。
CN106421922A公布了一种改性羟基磷灰石/碳纳米管/聚醚醚酮复合材料及其制备方法。该方法的不足之处在于仅对羟基磷灰石进行了改性,而未对碳纳米管和聚醚醚酮进行改性,聚醚醚酮和碳纳米管的生物惰性会使得羟基磷灰石与聚醚醚酮和碳纳米管三者的复合效果不好,特别是作为骨植入材料,在植入体内后,该复合材料有析出碳纳米管的风险。
除此之外,在聚醚醚酮基体上修饰磷酸钙涂层也是研究的重点,比如CN114805888A,虽然给聚醚醚酮带来一定的生物活性和骨整合性能,但是磷酸钙涂层的附着力仍然有限,磷酸钙化合物涂层短时间能发挥一定的诱导骨组织细胞贴附的作用,但较难保证长期(超过3个月甚至1年以上)有效。因为PEEK表面的惰性,短期附着在磷酸钙涂层上的骨组织会随着涂层的脱落而与PEEK形成生物惰性界面,导致脱落磷酸钙后的PEEK惰性表面与骨组织存在的生物相容性差的问题不能有效解决,其在骨科长期植入类的医疗器械上的使用仍然会受到限制。
一般来说,复合材料含有芯部或基材、以及复合层(添加剂等),其植入体内的表面与机体接触,生物活性要求高;芯部则主要承载机体负荷,力学性能要求高。因此,在制作PEEK/磷酸钙复合材料时,制备磷酸钙浓度梯度分布的复合材料,即芯部为PEEK,芯部到表面,磷酸钙化合物浓度逐渐增大,磷酸钙化合物在复合材料中的含量从表面到芯部径向降低,这可以提升骨科植入物的生物活性。因此,CN115737933A公开了一种采用等离子体烧结的径向梯度磷酸钙/聚醚醚酮复合材料及其制备方法与应用。该方法通过放电等离子烧结,结合焦耳热,快速均匀加热粉末使其表面熔融烧结,并在高压下致密化。此法不足之处是无法规避放电等离子体烧结工艺的缺点:只能烧结形状简单的样品,同时需要真空或气氛保护条件,导致其难以实现批量化生产;另外,等离子体烧结的设备贵,工业化生产的成本较高,目前应用不广;此外,如果要制造大尺寸产品,还需要增加设备模具的多功能性和脉冲电流的容量,而且烧结过程中,磷酸钙与聚醚醚酮界面融合的情况取决于烧结前原料的混合均一性,但因为是机械混合,很难控制磷酸钙在聚醚醚酮的内部呈现纳米颗粒的均匀分布,烧结的磷酸钙易发生团聚,且烧结工艺要花精力建立模具温度和工件实际温度的温差关系,以便调控产品质量,产品合格率不好控制。
为了解决磷酸钙与聚醚醚酮的界面分层、磷酸钙易析出和团聚、磷酸钙层易脱落以及聚醚醚酮的生物惰性等问题,开发一种新的聚醚醚酮复合材料的制备方法刻不容缓。
发明内容
针对现有技术的不足,本发明的目的在于提供一种医用聚醚醚酮复合材料及其制备方法和应用,通过原料和工艺步骤的设计,使得到的医用聚醚醚酮复合材料具有较高的力学模量和机械强度,具有较强的生物活性,可以促进成骨细胞的粘附和增殖,提升骨诱导能力,同时磷酸钙层不容易脱落,磷酸钙不易析出且分布均匀。
为达此目的,本发明采用以下技术方案:
第一方面,本发明提供一种医用聚醚醚酮复合材料的制备方法,所述制备方法包括如下步骤:
(1)制备n个含磷酸钙的聚乙二醇衍生物前驱体溶液;所述含磷酸钙的聚乙二醇衍生物前驱体溶液包括磷酸钙、聚乙二醇衍生物和水的组合;
所述n个含磷酸钙的聚乙二醇衍生物前驱体溶液中所述磷酸钙的质量浓度互不相同;
对聚醚醚酮颗粒和聚醚醚酮基材分别进行改性处理,得到改性聚醚醚酮颗粒和改性聚醚醚酮基材;
(2)将步骤(1)得到的任意一个所述含磷酸钙的聚乙二醇衍生物前驱体溶液、所述改性聚醚醚酮颗粒和交联剂混合后进行第一反应,得到含磷酸钙的聚乙二醇水凝胶/聚醚醚酮颗粒复合体系;将步骤(1)得到的剩余含磷酸钙的聚乙二醇衍生物前驱体溶液,按照前述步骤,依次制备所述磷酸钙的质量浓度互不相同的含磷酸钙的聚乙二醇水凝胶/聚醚醚酮颗粒复合体系;
当n=1时,步骤(2)完成后进行步骤(3),得到所述医用聚醚醚酮复合材料;
当n=2时,步骤(2)完成后依次进行步骤(3)和步骤(4),得到所述医用聚醚醚酮复合材料;
当n>2时,步骤(2)完成后依次进行步骤(3)、步骤(4)和步骤(5),得到所述医用聚醚醚酮复合材料;
(3)将步骤(2)得到的任意一个含磷酸钙的聚乙二醇水凝胶/聚醚醚酮颗粒复合体系设置于所述改性聚醚醚酮基材的至少一面,经成型工艺在所述改性聚醚醚酮基材的至少一面设置一层磷酸钙层;
(4)对所述磷酸钙层进行改性处理,将步骤(2)得到的剩余含磷酸钙的聚乙二醇水凝胶/聚醚醚酮颗粒复合体系中的任意一个设置于所述磷酸钙层上,经成型工艺在所述改性聚醚醚酮基材的至少一面设置两层磷酸钙层;
(5)重复步骤(4),将步骤(2)得到的其余含磷酸钙的聚乙二醇水凝胶/聚醚醚酮颗粒复合体系,依次层叠设置于所述改性聚醚醚酮基材上,在所述改性聚醚醚酮基材的至少一面设置至少三层磷酸钙层。
以下作为本发明的优选技术方案,但不作为对本发明提供的技术方案的限制,通过以下优选的技术方案,可以更好的达到和实现本发明的目的和有益效果。
作为一个优选的技术方案,所述n选自1-10的整数,例如可以为1、2、3、4、5、6、7、8、9或10等。
优选地,所述含磷酸钙的聚乙二醇衍生物前驱体溶液中,所述聚乙二醇衍生物与所述磷酸钙的质量比为(0.1-8):1,例如可以为0.1:1、0.5:1、1:1、2:1、3:1、4:1、5:1、6:1、7:1或8:1等。
优选地,所述聚醚醚酮颗粒的粒径为2-100μm,例如可以为2μm、10μm、20μm、30μm、40μm、50μm、60μm、70μm、80μm、90μm或100μm,以及上述点值之间的具体点值,限于篇幅及出于简明的考虑,本发明不再穷尽列举所述范围包括的具体点值。
优选地,所述聚醚醚酮颗粒在温度为380℃,载荷为5kg的条件下的熔融指数≥50g/10min,聚醚醚酮颗粒的粒径越小越容易与聚乙二醇水凝胶复合;熔融指数控制在限定范围内,可以保证热压成型工艺的进行。
优选地,所述聚醚醚酮基材的厚度为0.001-0.2m,例如可以为0.001m、0.002m、0.004m、0.006m、0.008m、0.01m、0.012m、0.014m、0.016m、0.018m或0.2m,以及上述点值之间的具体点值,限于篇幅及出于简明的考虑,本发明不再穷尽列举所述范围包括的具体点值。
经过所述改性处理后,所述改性聚醚醚酮颗粒、所述改性聚醚醚酮基材或各层所述磷酸钙层的表面同时且各自独立地含有氨基、巯基、乙烯基或异氰酸酯基,进一步优选氨基。
通过所述改性处理得到表面含有氨基的改性聚醚醚酮基材、表面含有氨基的改性聚醚醚酮颗粒或表面含有氨基的磷酸钙层的方法可参考CN110003412A,所述改性处理的方法包括如下步骤:
(S1)使用浓硫酸对待改性物料进行磺化处理,得到磺化后的物料;所述浓硫酸的质量浓度为95-98wt%;所述磺化处理的时间为32-40h;所述浓硫酸与待改性物料的质量比为(0.1-20):1;
(S2)将所述磺化后的物料、氯化亚砜和N-N二甲基甲酰胺混合后,在油浴条件下进行酰氯化反应,得到芳香磺酰氯,并将所述芳香磺酰氯进行真空旋蒸;所述酰氯化反应的温度为60-80℃;所述酰氯化反应的时间为10-14h;所述真空旋蒸的温度为50-70℃;所述氯化亚砜与待改性物料的质量比为(14-18):1;所述N-N二甲基甲酰胺的加入量是所述待改性物料的30-40wt%;
(S3)冰浴下,所述芳香磺酰氯、含氨基的物质、三乙胺溶液和乙醇水溶液混合后进行酰化反应,得到表面含有氨基的聚醚醚酮基材、表面含有氨基的聚醚醚酮颗粒或表面含有氨基的磷酸钙层;所述酰化反应的时间为20-30h;所述含氨基的物质与待改性物料的质量比为(0.03-3.6):1;所述三乙胺溶液的加入量是所述待改性物料的30-40wt%;所述含氨基的物质包括乙二胺、精胺或甘氨酸-精氨酸-甘氨酸-天冬氨酸多肽中的任意一种或至少两种的组合;所述三乙胺溶液中三乙胺的质量浓度为5-30%;所述乙醇水溶液的加入量是所述待改性物料的(1-50):1;所述乙醇水溶液中乙醇的质量百分含量为20-90%。
通过所述改性处理得到表面含有乙烯基的改性聚醚醚酮基材、表面含有乙烯基的改性聚醚醚酮颗粒或表面含有乙烯基的磷酸钙层的方法包括:将2-100g所述表面含有氨基的改性聚醚醚酮基材、表面含有氨基的改性聚醚醚酮颗粒或表面含有氨基的磷酸钙层与2-500g聚(乙二醇)二丙烯酸酯混合后反应,得到所述表面含有乙烯基的改性聚醚醚酮基材、表面含有乙烯基的改性聚醚醚酮颗粒或表面含有乙烯基的磷酸钙层;所述反应的温度为20-60℃;所述反应的时间为0.5-6h。
所述聚乙二醇衍生物包括端基为活性官能团的多臂聚乙二醇中的任意一种或至少两种的组合。
所述活性官能团包括乙烯基、氨基、异氰酸酯基或巯基中的至少一种,进一步优选乙烯基。由于合成端基为乙烯基的多臂聚乙二醇比端基为氨基的多臂聚乙二醇容易,且价格更便宜,同时表面含有氨基的改性PEEK与表面含有乙烯基的改性PEEK相比工艺简便,因此,优选选择端基为乙烯基的多臂聚乙二醇与表面含有氨基的改性PEEK基材、表面含有氨基的改性PEEK颗粒或表面含有氨基的磷酸钙层进行反应。
所述端基为活性官能团的多臂聚乙二醇包括八臂聚乙二醇、六臂聚乙二醇、四臂聚乙二醇或三臂聚乙二醇中的任意一种或至少两种的组合。
优选地,所述聚乙二醇衍生物为端基为乙烯基的八臂聚乙二醇;所述端基为乙烯基的八臂聚乙二醇具有如式Ⅰ所示结构:
式Ⅰ。
其中,n选自1-140的整数,例如可以为1、10、20、30、40、50、60、70、80、90、100、110、120、130或140,以及上述点值之间的具体点值,限于篇幅及出于简明的考虑,本发明不再穷尽列举所述范围包括的具体点值。
优选地,所述聚乙二醇衍生物的分子量为1-50kDa,例如可以为1 kDa、2 kDa、4kDa、6 kDa、8 kDa、10 kDa、15 kDa、20 kDa、25 kDa、30 kDa、35 kDa、40 kDa、45 kDa或50kDa,以及上述点值之间的具体点值,限于篇幅及出于简明的考虑,本发明不再穷尽列举所述范围包括的具体点值。
本发明中,所述聚乙二醇衍生物的臂数越多同时聚乙二醇衍生物的分子量越大,越能增强聚乙二醇网络结构中磷酸钙的含量及其均匀性分布。所述聚乙二醇衍生物的端基的选择需与所述改性聚醚醚酮基材、改性聚醚醚酮颗粒的表面含有的基团匹配,以使所述聚乙二醇衍生物与所述改性聚醚醚酮基材和所述改性聚醚醚酮颗粒之间可以形成化学键,从而增强层与层之间的结合力,以及复合体系各组分的相容性。所述改性聚醚醚酮基材也包含了富含有所述磷酸钙层的聚醚醚酮基材。
本发明中所述聚乙二醇衍生物均为市售产品,示例性地,端基为乙烯基的八臂聚乙二醇可购自Sigma-Aldrich公司。
优选地,所述端基为活性官能团的多臂聚乙二醇与所述改性聚醚醚酮颗粒或所述改性聚醚醚酮基材的表面含有的基团可以发生键合反应。
优选地,所述端基为活性官能团的多臂聚乙二醇以乙烯基或异氰酸酯基的至少一种作为端基时,所述改性聚醚醚酮颗粒或所述改性聚醚醚酮基材的表面含有的基团为氨基或巯基中的至少一种;所述端基为活性官能团的多臂聚乙二醇以氨基或巯基的至少一种作为端基时,所述改性聚醚醚酮颗粒或所述改性聚醚醚酮基材的表面含有的基团为乙烯基或异氰酸酯基中的至少一种。
优选地,所述含磷酸钙的聚乙二醇衍生物前驱体溶液的制备方法包括第一方法或第二方法。
优选地,所述第一方法包括:将钙盐溶液、磷酸铵类盐溶液、所述聚乙二醇衍生物和pH调节剂混合后进行第二反应,得到所述含磷酸钙的聚乙二醇衍生物前驱体溶液。
优选地,所述钙盐溶液包括钙盐和水的组合。
优选地,所述钙盐包括硝酸钙、硫酸钙、氯化钙或氢氧化钙中的任意一种或至少两种的组合。
优选地,所述钙盐溶液的浓度为0.01-5mol/L,例如可以为0.01 mol/L、0.5 mol/L、1 mol/L、1.5 mol/L、2 mol/L、2.5 mol/L、3 mol/L、3.5 mol/L、4 mol/L、4.5 mol/L或5mol/L,以及上述点值之间的具体点值,限于篇幅及出于简明的考虑,本发明不再穷尽列举所述范围包括的具体点值。
优选地,所述磷酸铵类盐溶液包括磷酸铵类盐和水的组合。
优选地,所述磷酸铵类盐包括磷酸铵、磷酸氢二铵或磷酸二氢铵中的任意一种或至少两种的组合。
优选地,所述磷酸铵类盐溶液的浓度为0.01-5mol/L,例如可以为0.01 mol/L、0.5mol/L、1 mol/L、1.5 mol/L、2 mol/L、2.5 mol/L、3 mol/L、3.5 mol/L、4 mol/L、4.5 mol/L或5 mol/L,以及上述点值之间的具体点值,限于篇幅及出于简明的考虑,本发明不再穷尽列举所述范围包括的具体点值。
优选地,所述pH调节剂包括氨水。
优选地,所述氨水的浓度为0.1-10mol/L,例如可以为0.1mol/L、1mol/L、2mol/L、3mol/L、4mol/L、5mol/L、6mol/L、7mol/L、8mol/L、9mol/L或10mol/L,以及上述点值之间的具体点值,限于篇幅及出于简明的考虑,本发明不再穷尽列举所述范围包括的具体点值。
优选地,所述第二方法包括:将所述钙盐溶液、所述磷酸铵类盐溶液和所述pH调节剂混合后进行第三反应,得到所述磷酸钙,将所述磷酸钙与聚乙二醇衍生物溶液混合,得到所述含磷酸钙的聚乙二醇衍生物前驱体溶液。
优选地,所述聚乙二醇衍生物溶液包括所述聚乙二醇衍生物和水的组合。
优选地,所述聚乙二醇衍生物溶液中聚乙二醇衍生物的质量百分含量为1-80%,例如可以为1%、2%、5%、10%、20%、30%、40%、50%、60%、70%或80%以及上述点值之间的具体点值,限于篇幅及出于简明的考虑,本发明不再穷尽列举所述范围包括的具体点值。
优选地,所述第一方法和第二方法中,所述钙盐与所述磷酸铵类盐的摩尔比各自独立地为(0.1-10):1,例如可以为0.1:1、1:1、2:1、3:1、4:1、5:1、6:1、7:1、8:1、9:1或10:1等。
优选地,所述第二反应和第三反应各自独立地在pH值为9.5-12.5的条件下进行,例如可以为9.5、10、10.5、11、11.5、12或12.5等。
优选地,所述第二反应和第三反应的温度各自独立地为30-55℃,例如可以为30℃、32℃、35℃、38℃、40℃、42℃、45℃、48℃、50℃、52℃或55℃,以及上述点值之间的具体点值,限于篇幅及出于简明的考虑,本发明不再穷尽列举所述范围包括的具体点值。
优选地,所述第二反应和第三反应的时间各自独立地为0.5-5h,例如可以为0.5h、1h、1.5h、2h、2.2h、2.5h、2.8h、3h、3.2h、3.8h、4h、4.2h、4.5h、4.8h或5h,以及上述点值之间的具体点值,限于篇幅及出于简明的考虑,本发明不再穷尽列举所述范围包括的具体点值。
采用在聚乙二醇衍生物溶液中原位反应生成磷酸钙(第一方法),得到的磷酸钙尺寸分布均一,且可保持在纳米级别,微纳尺寸的磷酸钙对PEEK基材的力学性能增强效果更显著;而如果将聚乙二醇衍生物与磷酸钙直接混合(第二方法),磷酸钙的尺寸不易控制,且磷酸钙本身具备一定尺寸,与聚乙二醇衍生物混合后,容易团聚,团聚后对PEEK基材的力学性能增强效果不明显。
优选地,所述聚乙二醇衍生物与所述交联剂的摩尔比为(0.1-10):1,例如可以为0.1:1、1:1、2:1、3:1、4:1、5:1、6:1、7:1、8:1、9:1或10:1等。
优选地,所述聚乙二醇衍生物与所述改性聚醚醚酮颗粒的质量比为(0.1-10):1,例如可以为0.1:1、1:1、2:1、3:1、4:1、5:1、6:1、7:1、8:1、9:1或10:1等。
优选地,所述第一反应的温度为25-60℃,例如可以为25℃、28℃、30℃、32℃、35℃、38℃、40℃、45℃、50℃、55℃或60℃,以及上述点值之间的具体点值,限于篇幅及出于简明的考虑,本发明不再穷尽列举所述范围包括的具体点值。
优选地,所述第一反应的时间为0.5-6h,例如可以为0.5h、1 h、1.5 h、2 h、2.5 h、3 h、3.5 h、4 h、4.5 h、5 h、5.5 h或6 h,以及上述点值之间的具体点值,限于篇幅及出于简明的考虑,本发明不再穷尽列举所述范围包括的具体点值。
所述端基为乙烯基的聚乙二醇水凝胶的制备可参考如下文献:
①Micro-Patterning of PEG-Based Hydrogels With Gold NanoparticlesUsing a Reactive Micro-Contact-Printing Approach. C Yesildag, Z. Ouyang, ZZhang and M. Lensen. Front. Chem., 2019.
②Synthesis of Poly(ethylene glycol)-based Hydrogels via Amine-Michael Type Addition with Tunable Stiffness and Postgelation ChemicalFunctionality. Z Zhang, A Loebus, G Vicente, F Ren, M Arafeh, Z Ouyang, MLensen. Chem. Mater.2014, 26, 3624.
优选地,所述改性聚醚醚酮基材上每层所述磷酸钙层的厚度各自独立地为0.01-50mm,例如可以是0.01 mm、1 mm、2 mm、4 mm、6 mm、8 mm、10 mm、12 mm、14 mm、16 mm、18mm、20 mm、30 mm、40 mm或50 mm,以及上述点值之间的具体点值,限于篇幅及出于简明的考虑,本发明不再穷尽列举所述范围包括的具体点值。
优选地,以所述改性聚醚醚酮基材指向所述磷酸钙层的方向为第一方向,各层所述磷酸钙层中所述磷酸钙的质量百分含量沿所述第一方向梯度增加。
优选地,以所述改性聚醚醚酮颗粒和所述磷酸钙的总质量为100%计,各层所述磷酸钙层中磷酸钙的质量百分含量各自独立地为2-70%,例如可以为2%、4%、5%、10%、15%、20%、25%、30%、35%、40%、45%、50%、55%、60%、65%或70%,以及上述点值之间的具体点值,限于篇幅及出于简明的考虑,本发明不再穷尽列举所述范围包括的具体点值。
优选地,任意相邻两个磷酸钙层中所述磷酸钙的质量百分含量相差2-50%,例如可以为2%、3%、4%、5%、6%、7%、8%、9%、10%、15%、20%、25%、30%、35%、40%、45%或50%,以及上述点值之间的具体点值,限于篇幅及出于简明的考虑,本发明不再穷尽列举所述范围包括的具体点值。
采用本发明提供的医用聚醚醚酮复合材料的制备方法,使制备得到的医用聚醚醚酮复合材料具有磷酸钙的质量百分含量径向梯度增加的特点,即磷酸钙在聚醚醚酮复合材料的表面具有最高质量百分含量,从聚醚醚酮复合材料的表面到芯部,磷酸钙的质量百分含量逐渐降低,直至芯部全部为聚醚醚酮。这既能保持聚醚醚酮(PEEK)基材的高模量,又可通过表面构建的磷酸钙微纳颗粒层,促进成骨细胞的增殖,提升骨诱导能力,更重要的是,可以通过调控磷酸钙层的数量和各层中磷酸钙的质量百分含量,调控聚醚醚酮复合材料的骨整合能力,以匹配植入物所在部位所需要的骨愈合速率。本发明提供的医用聚醚醚酮复合材料的制备方法中,聚醚醚酮基材上的磷酸钙层的具体的层数可以根据植入部位进行调整,以满足应用需求。
优选地,所述交联剂包括氨基酸、氨基酸盐、端基为乙烯基的聚乙二醇衍生物或端基为氨基的聚乙二醇衍生物中的任意一种或至少两种的组合。
优选地,所述氨基酸包括赖氨酸、精氨酸或天门冬酰胺中的任意一种或至少两种的组合。
优选地,所述氨基酸盐包括
优选地,所述端基为氨基的聚乙二醇衍生物包括如下化合物中的至少一种:
、/>
优选地,所述端基为乙烯基的聚乙二醇衍生物包括如下化合物中的至少一种:
、
;其中m、p、k、x、y、z各自独立地选自1-100的整数,例如可以为1、5、10、20、30、40、50、60、70、80、90或100等。
优选地,在进行所述改性处理前先对所述聚醚醚酮基材的至少一面和各层磷酸钙层进行图案化处理。
优选地,经过所述图案化处理后,所述聚醚醚酮基材和各层所述磷酸钙层的表面各自独立地形成多个凹凸结构。
优选地,所述凹凸结构的凸起的宽度为5-500μm,例如可以是5μm、50μm、100μm、150μm、200μm、250μm、300μm、350μm、400μm、450μm或500μm,以及上述点值之间的具体点值,限于篇幅及出于简明的考虑,本发明不再穷尽列举所述范围包括的具体点值。
优选地,所述凸起的高度为5-100μm,例如可以是5μm、10μm、20μm、30μm、40μm、50μm、60μm、70μm、80μm、90μm或100μm,以及上述点值之间的具体点值,限于篇幅及出于简明的考虑,本发明不再穷尽列举所述范围包括的具体点值。
优选地,相邻两个所述凸起的间距为5-500μm,例如可以是5μm、50μm、100μm、150μm、200μm、250μm、300μm、350μm、400μm、450μm或500μm,以及上述点值之间的具体点值,限于篇幅及出于简明的考虑,本发明不再穷尽列举所述范围包括的具体点值。
本发明所述图案化处理的方法包括飞秒激光切割或机械刀具切割,经过所述图案化处理,使得所述PEEK基材和各层所述磷酸钙层的表面具有一定尺寸的凹凸不平的图案化形貌结构,可以增强各层之间的结合力。通过控制所述凹凸结构的相邻两个所述凸起的间距和凸起的高度,使聚醚醚酮颗粒可以填充到沟壑中。
所述飞秒激光切割可参考CN112625397A,可选择下述两种方式中的任意一种:
方式I:对所述PEEK基材或磷酸钙层的表面进行周期性扫描;
方式II:对所述PEEK基材或磷酸钙层的表面先进行平面扫描后,再进行周期性扫描。
其中,方式I或方式II中,经所述周期性扫描后使材料表面形成凹凸结构。本发明采用方式II,具体操作为:使用飞秒激光仪器对PEEK基材的表面实行平面扫描和周期性扫描。所述飞秒激光切割的工艺参数可按本领域常规操作进行设置,其中:所述飞秒激光切割的输出波长优选为500-1100nm;所述飞秒激光切割的脉冲宽度优选50-200fs;所述飞秒激光切割的频率优选为800-1200Hz;所述飞秒激光切割的光功率优选为20-40mW(例如30mW);所述飞秒激光切割的扫描速度优选为400-1000μm/s(例如600μm/s)。
本发明中所述改性聚醚醚酮基材上,沿所述第一方向,最后一层磷酸钙层不用进行所述图案化处理和改性处理。
优选地,所述成型工艺包括热压成型工艺。
优选地,所述热压成型工艺的温度为330-410℃,例如可以为330℃、340℃、350℃、360℃、370℃、380℃、390℃、400℃或410℃,以及上述点值之间的具体点值,限于篇幅及出于简明的考虑,本发明不再穷尽列举所述范围包括的具体点值。
优选地,所述热压成型工艺的压力为0.5-5MPa,例如可以为0.5MPa、1MPa、2MPa、3MPa、4MPa或5MPa,以及上述点值之间的具体点值,限于篇幅及出于简明的考虑,本发明不再穷尽列举所述范围包括的具体点值。
优选地,所述热压成型工艺的加热时间为0.5-5h,例如可以为0.5h、1h、1.5h、2h、2.5h、3h、3.5h、4h、4.5h或5h,以及上述点值之间的具体点值,限于篇幅及出于简明的考虑,本发明不再穷尽列举所述范围包括的具体点值。
第二方面,本发明提供一种医用聚醚醚酮复合材料,所述医用聚醚醚酮复合材料采用如第一方面所述的制备方法制备得到。
第三方面,本发明提供一种如第二方面所述的医用聚醚醚酮复合材料的应用,所述医用聚醚醚酮复合材料在3D打印医用料、人工假体、医疗导管、口腔种植体、颌面骨、心脏瓣膜、输液港、心脏起搏器外壳、医用瞄准杆、医用瞄准架、人体骨锁定系统、医用扳手、医用连接件、医用定位架、手术头架与牵开系统、医疗手柄、医用穿刺针、医用接头、医用缝合线、人工骨头、人工关节、股骨髁、骨钉、螺钉、锚钉、铆钉、髓内针、接骨板、胫骨托、颅骨修复系统或脊柱椎间融合器中的应用。
与现有技术相比,本发明具有以下有益效果:
(1)本发明提供的医用聚醚醚酮复合材料的制备方法,在PEEK基材的表面构建磷酸钙的质量百分含量梯度分布的磷酸钙层,既能保持PEEK基材的高模量,又可通过表面构建的磷酸钙层,促进成骨细胞的增殖,提升骨诱导能力,更重要的是,可以通过调控各层磷酸钙层中的磷酸钙的浓度,来调控复合材料的骨整合能力,以匹配植入物所在部位所需要的骨愈合速率;
(2)磷酸钙层是通过水凝胶体系整合到PEEK基材的表面,且该水凝胶体系为生物可降解的聚乙二醇水凝胶,可保证体系的无细胞毒性,同时采用的聚乙二醇衍生物可以使磷酸钙的分布更均匀,更难析出;
(3)PEEK基材以及PEEK颗粒都进行了改性处理,同时采用端基为活性官能团的聚乙二醇衍生物,端基为活性官能团的聚乙二醇衍生物与交联剂进行交联反应生成水凝胶后,端基为活性官能团的聚乙二醇衍生物未进行反应的端基与PEEK基材以及PEEK颗粒之间形成化学键,可以增强层与层之间的结合力;同时将PEEK基材和磷酸钙层进行图案化处理,可通过物理作用加强层与层之间的结合程度,保证整体材料具有一定的力学模量。
附图说明
图1是实施例1中经过图案化处理后的聚醚醚酮基材的剖面微观图;
图2是实施例1中聚醚醚酮基材、磷酸钙A层、磷酸钙B层和磷酸钙C层的SEM扫描测试图;
图3是实施例1中聚醚醚酮基材、磷酸钙A层、磷酸钙B层和磷酸钙C层的细胞毒性测试图;
图4是实施例1中聚醚醚酮基材、磷酸钙A层、磷酸钙B层和磷酸钙C层的成骨细胞增殖测试图;
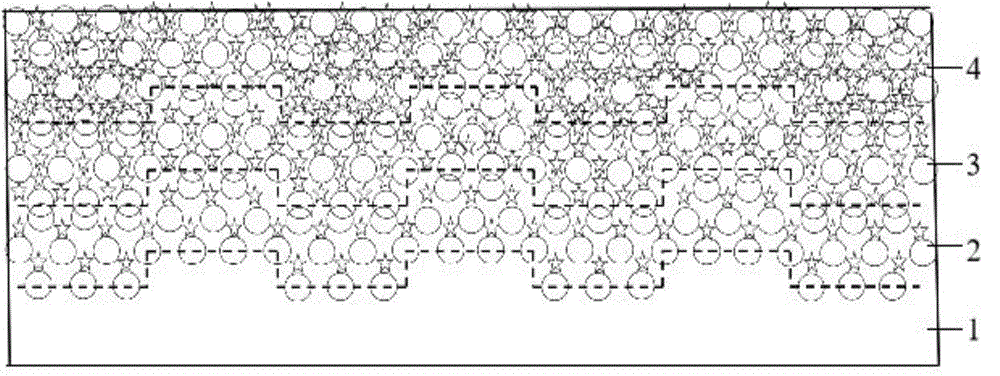
图5是实施例1提供的聚醚醚酮复合材料的结构示意图;
其中,五角星为磷酸钙,圆形为聚醚醚酮颗粒,1-聚醚醚酮基材,2-磷酸钙A层,3-磷酸钙B层,4-磷酸钙C层。
具体实施方式
下面结合附图并通过具体实施方式来进一步说明本发明的技术方案。本领域技术人员应该明了,所述实施例仅仅是帮助理解本发明,不应视为对本发明的具体限制。
下述实施例和对比例中部分组分来源如下所述:
(1)端基为乙烯基的八臂聚乙二醇:8臂-PEG-丙烯酸酯,购自Sigma-Aldrich公司,分子量为20kDa;
分子式为:
(2)端基为氨基的八臂聚乙二醇:8臂-PEG-NH
分子式为:
(3)赖氨酸:分子量为146.19,购自Sigma-Aldrich;
(4)聚(乙二醇)二丙烯酸酯:
(5)聚醚醚酮颗粒:购自吉林中研330UPF,950目,粒径为18μm,在温度为380℃,载荷为5kg的条件下的熔融指数为65 g/10min;
(6)聚醚醚酮基材:购自德国赢创公司,牌号VESTAKEEP® i4 PL,长、宽和高的尺寸为20mm×20mm×10mm;
(7)浓硫酸:购自国药集团化学试剂有限公司,质量浓度为96%;
(8)氯化亚砜:购自国药集团化学试剂有限公司;
(9)N-N二甲基甲酰胺:购自国药集团化学试剂有限公司;
(10)三乙胺溶液:购自国药集团化学试剂有限公司,浓度配置为1mol/L。
实施例1
一种医用聚醚醚酮复合材料及其制备方法,所述制备方法包括如下步骤:
(1)将硝酸钙3.3g溶于一定量去离子水中,配成0.1mol/L的硝酸钙溶液200mL,向硝酸钙溶液中加入5g 8臂-PEG-丙烯酸酯。将称量好的磷酸氢二铵1.8g溶于一定量去离子水中,配成0.17mol/L磷酸氢二铵溶液80mL。将配好的磷酸氢二铵溶液在不断搅拌下以0.5mL/min的速率滴入30℃的硝酸钙溶液中,滴加完毕后,再滴加些许氨水(0.1mol/L)以调整混合溶液的pH值为9.5,之后,将混合溶液继续搅拌4h后,得到第一含磷酸钙的聚乙二醇衍生物前驱体水溶液,所述第一含磷酸钙的聚乙二醇衍生物前驱体水溶液中磷酸钙为2g;
将硝酸钙9.9g溶于一定量去离子水中,配成0.3mol/L的硝酸钙溶液200mL,向硝酸钙溶液中加入5g 8臂-PEG-丙烯酸酯。将称量好的磷酸氢二铵5.4g溶于一定量去离子水中,配成0.51mol/L磷酸氢二铵溶液80mL。将配好的磷酸氢二铵溶液在不断搅拌下以0.5mL/min的速率滴入30℃的硝酸钙溶液中,滴加完毕后,再滴加些许氨水(0.1mol/L)以调整混合溶液的pH值为9.5,之后,将混合溶液继续搅拌4h后,得到第二含磷酸钙的聚乙二醇衍生物前驱体水溶液,所述第二含磷酸钙的聚乙二醇衍生物前驱体水溶液中磷酸钙为6g;
将硝酸钙13.2g溶于一定量去离子水中,配成0.4mol/L的硝酸钙溶液200mL,向硝酸钙溶液中加入5g 8臂-PEG-丙烯酸酯。将称量好的磷酸氢二铵7.2g溶于一定量去离子水中,配成0.68mol/L磷酸氢二铵溶液80mL。将配好的磷酸氢二铵溶液在不断搅拌下以0.5mL/min的速率滴入30℃的硝酸钙溶液中,滴加完毕后,再滴加些许氨水(0.1mol/L)以调整混合溶液的pH值为9.5,之后,将混合溶液继续搅拌4h后,得到第三含磷酸钙的聚乙二醇衍生物前驱体水溶液,所述第三含磷酸钙的聚乙二醇衍生物前驱体水溶液中磷酸钙为8g;
对聚醚醚酮基材的一面进行图案化处理,得到图案化处理后的聚醚醚酮基材,对所述图案化处理后的聚醚醚酮基材和聚醚醚酮颗粒分别进行改性处理,得到表面含有氨基的聚醚醚酮颗粒和表面含有氨基的聚醚醚酮基材;
(2)将所述表面含有氨基的聚醚醚酮颗粒5g与步骤(1)制备得到的第一含磷酸钙的聚乙二醇衍生物前驱体水溶液在搅拌下充分混合均匀,然后在搅拌下加入2g赖氨酸。在30℃下搅拌2小时后,静置1小时,得到第一含磷酸钙的聚乙二醇水凝胶/聚醚醚酮颗粒复合体系;将步骤(1)得到的第二含磷酸钙的聚乙二醇衍生物前驱体溶液和第三含磷酸钙的聚乙二醇衍生物前驱体溶液按照前述步骤,依次制备第二含磷酸钙的聚乙二醇水凝胶/聚醚醚酮颗粒复合体系和第三含磷酸钙的聚乙二醇水凝胶/聚醚醚酮颗粒复合体系;
(3)将所述第一含磷酸钙的聚乙二醇水凝胶/聚醚醚酮颗粒复合体系涂覆于所述表面含有氨基的聚醚醚酮基材上,经热压成型工艺在表面含有氨基的聚醚醚酮基材的一面(经过图案化处理的一面)形成第一层磷酸钙层(磷酸钙A层),磷酸钙A层中磷酸钙的质量百分含量为28.5%,磷酸钙A层的厚度为5mm;
(4)对所述磷酸钙A层进行图案化处理,然后进行改性处理,将所述第二含磷酸钙的聚乙二醇水凝胶/聚醚醚酮颗粒复合体系涂覆于经过所述改性处理后的磷酸钙A层上,经热压成型工艺,在表面含有氨基的聚醚醚酮基材上形成第二层磷酸钙层(磷酸钙B层),磷酸钙B层中磷酸钙的质量百分含量为54.5%,磷酸钙B层的厚度为5mm;
(5)对所述磷酸钙B层进行图案化处理,然后进行改性处理,将所述第三含磷酸钙的聚乙二醇水凝胶/聚醚醚酮颗粒复合体系涂覆于经过所述改性处理后的磷酸钙B层上,经热压成型工艺,在表面含有氨基的聚醚醚酮基材上形成第三层磷酸钙层(磷酸钙C层),得到所述医用聚醚醚酮复合材料,磷酸钙C层中磷酸钙的质量百分含量为61.5%,磷酸钙C层的厚度为5mm;
所述热压成型工艺的具体操作为:将物料放入模具中,将模具放到160℃的干燥箱中,预热1h;同时,将平板硫化机预热到380℃,将模具放到平板硫化机中进行合模,压力设置为3MPa,加热1.5h,保温保压30min,然后停止加热,保压冷却1.5h;
所述图案化处理的具体操作为:采用飞秒激光仪器(GLX-200HP-1053,TimeBandwidth Products AG,瑞士)对聚醚醚酮基材、磷酸钙A层和磷酸钙B层进行平面扫描,之后再进行周期性扫描,从而在其表面形成多个凹凸结构,所述凹凸结构的凸起的宽度为100μm,所述凸起的高度为80μm,相邻两个所述凸起的间距为100μm;飞秒激光仪器的参数设置如下:功率30mW,脉冲宽度100fs,中心波长800nm,重复频率1KHz,扫描速度600μm/s;
所述改性处理的方法包括如下步骤:
(S1)用质量浓度为96wt%的浓硫酸25g将待改性物料(所述聚醚醚酮基材、所述磷酸钙A层或所述磷酸钙B层)5g进行磺化处理35h,得到磺化后的物料;
(S2)将所述磺化后的物料、78g氯化亚砜和1.56g N-N二甲基甲酰胺混合后,在油浴70℃条件下进行酰氯化反应12h,得到芳香磺酰氯,并将所述芳香磺酰氯进行60℃真空旋蒸;
(S3)冰浴下,将得到的芳香磺酰氯、5.2g乙二胺和1.56g三乙胺溶液在50mL水/乙醇(25mL:25mL)共混体系混合后进行酰化反应30h,得到表面含有氨基的聚醚醚酮基材、表面含有氨基的聚醚醚酮颗粒、表面含有氨基的磷酸钙A层或表面含有氨基的磷酸钙B层。
实施例2
一种医用聚醚醚酮复合材料及其制备方法,所述制备方法包括如下步骤:
(1)将硝酸钙3.3g溶于一定量去离子水中,配成0.1mol/L的硝酸钙溶液200mL,向硝酸钙溶液中加入5g 8臂-PEG-NH
将硝酸钙9.9g溶于一定量去离子水中,配成0.3mol/L的硝酸钙溶液200mL,向硝酸钙溶液中加入5g 8臂-PEG-NH
将硝酸钙13.2g溶于一定量去离子水中,配成0.4mol/L的硝酸钙溶液200mL,向硝酸钙溶液中加入5g 8臂-PEG-NH
对聚醚醚酮基材的一面进行图案化处理,得到图案化处理后的聚醚醚酮基材,对所述图案化处理后的聚醚醚酮基材和聚醚醚酮颗粒分别进行改性处理,得到表面含有乙烯基的聚醚醚酮颗粒和表面含有乙烯基的聚醚醚酮基材;
(2)将所述表面含有乙烯基的聚醚醚酮颗粒5g与步骤(1)制备得到的第一含磷酸钙的聚乙二醇衍生物前驱体水溶液在搅拌下充分混合均匀,然后在搅拌下加入2g聚(乙二醇)二丙烯酸酯。在30℃下搅拌2小时后,静置1小时,得到第一含磷酸钙的聚乙二醇水凝胶/聚醚醚酮颗粒复合体系;将步骤(1)得到的第二含磷酸钙的聚乙二醇衍生物前驱体溶液和第三含磷酸钙的聚乙二醇衍生物前驱体溶液按照前述步骤,依次制备第二含磷酸钙的聚乙二醇水凝胶/聚醚醚酮颗粒复合体系和第三含磷酸钙的聚乙二醇水凝胶/聚醚醚酮颗粒复合体系;
(3)将所述第一含磷酸钙的聚乙二醇水凝胶/聚醚醚酮颗粒复合体系涂覆于所述表面含有乙烯基的聚醚醚酮基材上(经过图案化处理的一面),经热压成型工艺在表面含有乙烯基的聚醚醚酮基材上形成第一层磷酸钙层(磷酸钙A层),磷酸钙A层中磷酸钙的质量百分含量为28.5%,磷酸钙A层的厚度为5mm;
(4)对所述磷酸钙A层进行图案化处理,然后进行改性处理,将所述第二含磷酸钙的聚乙二醇水凝胶/聚醚醚酮颗粒复合体系涂覆于经过所述改性处理后的磷酸钙A层上,经热压成型工艺,在表面含有乙烯基的聚醚醚酮基材上形成第二层磷酸钙层(磷酸钙B层),磷酸钙B层中磷酸钙的质量百分含量为54.5%,磷酸钙B层的厚度为5mm;
(5)对所述磷酸钙B层进行图案化处理,然后进行改性处理,将所述第三含磷酸钙的聚乙二醇水凝胶/聚醚醚酮颗粒复合体系涂覆于经过所述改性处理后的磷酸钙B层上,经热压成型工艺,在表面含有乙烯基的聚醚醚酮基材上形成第三层磷酸钙层(磷酸钙C层),得到所述医用聚醚醚酮复合材料,磷酸钙C层中磷酸钙的质量百分含量为61.5%,磷酸钙C层的厚度为5mm;
所述热压成型工艺的具体操作和所述图案化处理的具体操作同实施例1;
所述改性处理的方法包括如下步骤:
(Z1)用质量浓度为96wt%的浓硫酸25g对待改性物料(所述聚醚醚酮基材、所述磷酸钙A层或所述磷酸钙B层)5g进行磺化处理35h,得到磺化后的物料;
(Z2)将所述磺化后的物料、78g氯化亚砜和1.56g N-N二甲基甲酰胺混合后,在油浴70℃条件下进行酰氯化反应12h,得到芳香磺酰氯,并将所述芳香磺酰氯进行60℃真空旋蒸;
(Z3)冰浴下,将得到的芳香磺酰氯、5.2g乙二胺和1.56g三乙胺溶液在50mL水/乙醇(25mL:25mL)共混体系混合后进行酰化反应30h,得到表面含有氨基的聚醚醚酮基材、表面含有氨基的聚醚醚酮颗粒、表面含有氨基的磷酸钙A层或表面含有氨基的磷酸钙B层;
(Z4)将5g所述表面含有氨基的聚醚醚酮基材、表面含有氨基的聚醚醚酮颗粒、表面含有氨基的磷酸钙A层或表面含有氨基的磷酸钙B层,浸入到含有5g聚(乙二醇)二丙烯酸酯的50mL水溶液中,反应6h。之后将其移出并干燥,得到表面含有乙烯基的聚醚醚酮颗粒、表面含有乙烯基的聚醚醚酮基材、表面含有乙烯基的磷酸钙A层或表面含有乙烯基的磷酸钙B层。
实施例3
一种医用聚醚醚酮复合材料及其制备方法,其与实施例1的区别仅在于不对聚醚醚酮基材、磷酸钙A层和磷酸钙B层进行图案化处理,其余原料、工艺参数和步骤均与实施例1相同。
实施例4
一种医用聚醚醚酮复合材料及其制备方法,其与实施1的区别仅在于步骤(1)如下,其他原料、工艺参数和步骤均与实施例1相同;
(1)将称量好的硝酸钙3.3g溶于一定量去离子水中,配成0.1mol/L硝酸钙溶液200mL。将称量好的磷酸氢二铵1.8g溶于一定量去离子水中,配成0.17mol/L磷酸氢二溶液80mL。将配好的磷酸氢二铵溶液在不断搅拌下缓慢(0.5mL/min)滴入30℃的硝酸钙溶液中,滴加完毕后,滴加些许氨水(0.1mol/L)以调整溶液的pH值为9.5,待反应完毕后,将产物继续搅拌4小时后,之后将产物过滤,洗涤,干燥后,得到磷酸钙2g。将制备得到的2g磷酸钙与250g 8臂-PEG-丙烯酸酯的质量百分含量为2%的8臂-PEG-丙烯酸酯水溶液直接共混,并搅拌均匀,得到第一含磷酸钙的聚乙二醇衍生物前驱体水溶液;
同理,制备第二含磷酸钙的聚乙二醇衍生物前驱体水溶液:将上述制备得到的6g磷酸钙与250g 8臂-PEG-丙烯酸酯的质量百分含量为2%的8臂-PEG-丙烯酸酯水溶液直接共混,并搅拌均匀,得到第二含磷酸钙的聚乙二醇衍生物前驱体水溶液;
同理,制备第三含磷酸钙的聚乙二醇衍生物前驱体水溶液:将上述制备得到的8g磷酸钙与250g 8臂-PEG-丙烯酸酯的质量百分含量为2%的8臂-PEG-丙烯酸酯水溶液直接共混,并搅拌均匀,得到第三含磷酸钙的聚乙二醇衍生物前驱体水溶液。
对比例1
一种医用聚醚醚酮复合材料及其制备方法,所述制备方法包括如下步骤:
(1)将称量好的硝酸钙3.3g溶于一定量去离子水中,配成0.1mol/L硝酸钙溶液200mL。将称量好的磷酸氢二铵1.8g溶于一定量去离子水中,配成0.17mol/L磷酸氢二溶液80mL。将配好的磷酸氢二铵溶液在不断搅拌下缓慢(0.5mL/min)滴入30℃的硝酸钙溶液中,滴加完毕后,滴加些许氨水以调整溶液的pH值为在9.5。待反应完毕后,将产物继续搅拌4小时后,之后将产物过滤,洗涤,干燥后,得到磷酸钙2g;
对聚醚醚酮基材的一面进行图案化处理,得到图案化处理后的聚醚醚酮基材,对所述图案化处理后的聚醚醚酮基材和聚醚醚酮颗粒分别进行改性处理,得到表面含有氨基的聚醚醚酮颗粒和表面含有氨基的聚醚醚酮基材;
(2)将所述表面含有氨基的聚醚醚酮颗粒5g依次与2g、6g、8g步骤(1)制备得到的磷酸钙混合均匀,依次得到第一含磷酸钙的聚醚醚酮颗粒复合体系、第二含磷酸钙的聚醚醚酮颗粒复合体系和第三含磷酸钙的聚醚醚酮颗粒复合体系;
(3)将所述第一含磷酸钙的聚醚醚酮颗粒复合体系涂覆于所述表面含有氨基的聚醚醚酮基材上,经热压成型工艺,在表面含有氨基的聚醚醚酮基材上形成第一层磷酸钙层(磷酸钙A层),磷酸钙A层中磷酸钙的质量百分含量为28.5%,磷酸钙A层的厚度为5mm;
(4)对所述磷酸钙A层进行图案化处理,然后进行改性处理,将所述第二含磷酸钙的聚醚醚酮颗粒复合体系涂覆于经过所述改性处理后的磷酸钙A层上,经热压成型工艺,在表面含有氨基的聚醚醚酮基材上形成第二层磷酸钙层(磷酸钙B层),磷酸钙B层中磷酸钙的质量百分含量为54.5%,磷酸钙B层的厚度为5mm;
(5)对所述磷酸钙B层进行图案化处理,然后进行改性处理,将所述第三含磷酸钙的聚醚醚酮颗粒复合体系涂覆于经过所述改性处理后的磷酸钙B层上,经热压成型工艺,在表面含有氨基的聚醚醚酮基材上形成第三层磷酸钙层(磷酸钙C层),得到所述医用聚醚醚酮复合材料,磷酸钙C层中磷酸钙的质量百分含量为61.5%,磷酸钙C层的厚度为5mm;
所述热压成型工艺的具体操作、所述图案化处理的具体操作、所述改性处理的方法与实施例1相同。
对比例2
一种医用聚醚醚酮复合材料及其制备方法,其与实施例1的区别仅在于步骤(2)中不加入赖氨酸,其余原料、工艺参数和步骤均与实施例1相同。
性能测试:
(1)力学性能测试:
弯曲模量和弯曲强度:采用弯曲试验机(济南辰鑫试验机制造有限公司),按照ISO178-2010标准进行测试,其中试验加载速度0.2mm/min。每组测试5个样品,结果取其平均值;
拉伸强度:在岛津AGS-X型万能试验机上进行测试,根据GB/T 1040.1-2018《塑料拉伸性能的测定》制备测试拉伸强度的试样,试样加载速度为0.2mm/min,每组测试5个样品,结果取其平均值。
实施例1-4与对比例1-2实验结果如下:
表1
对上述实验数据分析可知:实施例1相对于对比例1,其弯曲模量、弯曲强度和拉伸强度都提升了20%以上,这是因为聚乙二醇水凝胶的三维网状结构可将磷酸钙与PEEK颗粒、PEEK基材进行较好的分散和复合,可有效促进磷酸钙与PEEK的界面融合作用;其次,形成的聚乙二醇水凝胶有剩余的乙烯基残留,残留的乙烯基可以与PEEK颗粒和PEEK基材表面的氨基发生迈克尔加成反应,生成化学键,进一步加强PEEK颗粒与PEEK基材的融合;再者,改性后的PEEK基材的表面含有的氨基可与聚乙二醇衍生物形成大量氢键,也可以促进体系的物理融合;此外,实施例1所形成的磷酸钙为原位反应生成,得到的磷酸钙尺寸分布均一,且可保持在纳米级别,微纳尺寸的磷酸钙对PEEK基材的增强效果更加显著;而对比例1中磷酸钙直接与聚醚醚酮颗粒共混,由于磷酸钙本身具备一定的尺寸,直接与聚醚醚酮颗粒共混容易团聚,力学性能增强效果差。
实施例1相比于对比例2,对比例2未加交联剂,虽然通过原位反应生成磷酸钙,但是因为未加交联剂,导致具有聚乙二醇水凝胶的三维网状结构的复合体系不能形成,导致其力学性能下降。但对比例2相比于对比例1来说,力学性能有所提升,这是因为对比例2的磷酸钙尺寸较均一,能更好地分散PEEK颗粒产生更有效的增强作用。
实施例1相比于实施例2,通过采用不同的聚乙二醇衍生物单体和不同的交联剂,但是磷酸钙均为原位反应生成,故而两者的力学性能接近。
实施例1相比于实施例3,实施例3的力学性能有所下降,这是因为实施例3未对聚醚醚酮基材、磷酸钙A层和磷酸钙B层的表面进行图案化处理,使得各层之间的嵌合作用力有所减弱导致。
实施例1相比于实施例4,实施例4的力学性能较低,这是因为实施例4是将制备得到的磷酸钙与8臂-PEG-丙烯酸酯水溶液直接共混,得到含磷酸钙的聚乙二醇衍生物前驱体水溶液,磷酸钙本身具备一定的尺寸,其相比于实施例1原位反应生成的磷酸钙的尺寸均一性差些,较容易团聚,导致直接共混后的磷酸钙对PEEK基材的增强效果差些。
(2)形貌和生物学性能测试:
1)SEM表征:使用超高分辨场发射扫描电镜(SEM,Thermo Scientific Apreo 2SEM)测试实施例1中进行图案化处理后的聚醚醚酮基材、磷酸钙A层、磷酸钙B层和磷酸钙C层,所得结果如图1实施例1中经过图案化处理后的聚醚醚酮基材的剖面微观图和图2实施例1中聚醚醚酮基材、磷酸钙A层、磷酸钙B层和磷酸钙C层的SEM扫描测试图所示。由图1可以看出,聚醚醚酮基材的表面经过图案化处理后,形成凹凸结构;由图2可以看出,聚醚醚酮基材、磷酸钙A层、磷酸钙B层和磷酸钙C层的表面,磷酸钙明显呈现梯度增加的趋势,实现了磷酸钙的质量百分含量梯度分布的医用PEEK复合材料的合成;磷酸钙的尺寸在微纳级别,粒径分布主要在50nm-10μm之间;
2)细胞培养研究:MC3T3-E1成骨细胞对实施例1中聚醚醚酮基材、磷酸钙A层、磷酸钙B层、磷酸钙C层分别进行体外细胞培养研究。具体方法为:将试验样品用70%乙醇洗涤,用磷酸盐缓冲盐水(PBS)漂洗,并分别放置在8孔聚苯乙烯(TCPs)板的孔中,然后分别接种0.5mL的5×10
(a)成骨细胞毒性研究:
用1000μL溶液接种细胞,所述溶液含有10μL二乙酸荧光素(fluoresceindiacetate,其在丙酮中的浓度为0.5mg/mg)、20μL碘化丙啶(propidium iodide,其在PBS中的浓度为0.5mg/mL)和970μL PBS。代谢活性细胞可以在细胞内酯酶的帮助下将二乙酸荧光素水解为绿色荧光素。同时,碘化丙啶可以穿过受损的细胞质膜,与细胞核的核酸结合,使细胞核产生荧光红101。去除所述溶液并用PBS洗涤之后,通过荧光显微镜(Carl Zeiss公司,型号Axio Observer)测试待测细胞。为了细胞的可视化,二乙酸荧光素和碘化丙啶分别在496nm和561nm处被激发;并且分别在504nm-559nm和569nm-663nm的释放范围内检测。
测试结果如图3实施例1中聚醚醚酮基材、磷酸钙A层、磷酸钙B层和磷酸钙C层的细胞毒性测试图所示,聚醚醚酮基材、磷酸钙A层、磷酸钙B层、磷酸钙C层所培养的细胞在荧光显微镜下都显示绿色,说明细胞都存活,无细胞毒副作用;
(b)成骨细胞增殖的研究:
首先用PBS洗涤甲醛固定的细胞,并用在Dulbecco磷酸盐缓冲盐水(DPBS)中的0.1%聚乙二醇辛基苯基醚(Triton X-100)溶液渗透5分钟,之后再次用PBS洗涤细胞。随后,将样品与PBS中的1%牛血清白蛋白(BSA)溶液孵育30分钟,以重悬非特异性结合位点。对于丝状肌动蛋白位点,将细胞与四甲基异硫氰酸罗丹明(TRITC)缀合的鬼笔肽溶液(在1%BSA-PBS溶液中的浓度为2μg/ml)孵育45分钟。用PBS洗涤几次后,用色霉素A3(CMA3)(在1%BSA-PBS溶液中的浓度为50μg/ml)对细胞核染色15分钟。最后,用PBS培养基保存样品,并在4℃无光条件下保存,直到荧光显微镜检查。为了观察细胞核和肌动蛋白细胞骨架,CMA3和TRITC鬼笔肽的激发分别发生在458nm和561nm,发射波长分别为495nm~525nm和567nm~642nm。通过荧光显微镜分别观察培养了24小时和72小时的细胞增殖情况。
所述结果如图4实施例1中聚醚醚酮基材、磷酸钙A层、磷酸钙B层和磷酸钙C层的成骨细胞增殖测试图所示,可以看出,聚醚醚酮基材上,无细胞贴附,说明其生物惰性。培养24h,磷酸钙A层有细胞贴附,但细胞呈现圆形并堆叠,说明贴附效果不好;磷酸钙B层的细胞,相比磷酸钙A层,其细胞呈现长条形,说明细胞的贴附效果较好;磷酸钙C层表面的细胞的触角伸展,说明贴附效果最佳,这是因为磷酸钙C层中的磷酸钙的含量最多,促进了成骨细胞的贴附。培养72小时,磷酸钙C层样品的细胞增殖最多,几乎铺满,而且细胞触角打开;磷酸钙C层优于磷酸钙B层,磷酸钙B层优于磷酸钙A层;这说明,随着磷酸钙微纳颗粒浓度的梯度增长,成骨细胞的贴附能力增加,增殖情况显著,显示了样品具有潜在的骨诱导和骨整合能力。
申请人声明,本发明通过上述实施例来说明本发明的详细工艺流程,但本发明并不局限于上述详细工艺流程,即不意味着本发明必须依赖上述详细工艺流程才能实施。所属技术领域的技术人员应该明了,对本发明的任何改进,对本发明产品各原料的等效替换及辅助成分的添加、具体方式的选择等,均落在本发明的保护范围和公开范围之内。
- 聚氨酯模具发泡成型预制直埋保温管发泡模具及发泡方法
- 一种聚氨酯发泡模具自动温控系统
- 一种半自动化聚氨酯发泡保温层成型模具
