一种基于特征性肽段同位素稀释质谱法的胰岛素定量方法
文献发布时间:2023-06-19 19:28:50
技术领域
本发明涉及蛋白质定量检测领域,特别是涉及一种基于特征性肽段同位素稀释质谱法的胰岛素定量方法。
背景技术
胰岛素是胰岛分泌的一种激素成分。它的主要作用就是促进周围组织对葡萄糖的利用,促进葡萄糖转变为肝糖原,储存在肝脏内,从而达到降低血糖的目的。所以胰岛素的主要作用是参与调节糖代谢,控制糖平衡。但是过多地使用胰岛素,血糖含量可下降到危险的低水平,这种情况称为低血糖,也称为胰岛素休克或胰岛素反应,是胰岛素治疗可能引致的一种极端严重的并发症。因此胰岛素的准确定量尤为重要。
胰岛素的定量方法有酶联免疫法、氨基酸同位素稀释质谱法等,但这些方法均只能特定测量某一种类的胰岛素。
CN104458890A中公开了一种同位素稀释质谱法测定胰岛素含量的方法,包括如下步骤:
(1)合成同位素标记的胰岛素β链并配制成溶液作为内标;(2)制备胰岛素标准和胰岛素样品溶液;(3)取胰岛素标准溶液和样品溶液并分别加入同位素标记的胰岛素β链;(4)将所述预处理后的胰岛素标准溶液和胰岛素样品进行质谱分析;(5)计算所述胰岛素样品溶液中胰岛素含量。该方法虽然可以采用MALDI-TOF质谱对样品中的胰岛素含量直接进行测定,但是因为该方法内标选择为β链,含有30个氨基酸,内标肽段过长,对于基于液相色谱-串联质谱的同位素稀释质谱法测定并不适用。
目前,因为蛋白样品成分复杂、实验条件要求较高、实验难度大,所以国内尚未见有关肽段同位素稀释质谱法定量胰岛素的研究报道。
而国外报道的肽段同位素稀释质谱法定量胰岛素是采用C端衍生的方法(YoheiSakaguchi,Tomoya Kinumi,Akiko Takatsu,Isotope-dilution liquid chromatography-tandem mass spectrometry for sensitive quantification of human insulin inserum using derivatization-technique,Anal Biochem.2017Nov 15;537:26-32),该方法定量时需要采用衍生试剂进行衍生,操作较为复杂、难度高。
发明内容
本发明的目的是提供一种基于特征性肽段同位素稀释质谱法的胰岛素定量方法。该方法的优点是高灵敏度、高精确性、高度特征性,其测量结果可直接溯源至国际基本单位制。
为实现上述目的,本发明采用的技术方案具体如下:
一种基于特征性肽段同位素稀释质谱法的胰岛素定量方法,包括以下步骤:
(1)特征肽段选择:确定特征肽段序列为GFFYTPK,如SEQ ID No:3所示;
(2)合成用于胰岛素定量的标记肽段;
(3)特征肽段纯度的测定;
(4)特征肽段质谱分析离子对的确定:合成特征肽段标准和标记,进行质谱分析特征肽段的母离子和子离子,调节碰撞能量选择信号强的四对离子,其中信号最强的为定量离子对,其余为定性离子对;
(5)液相分离及质谱条件优化;
(6)样本分析前处理:酶解、浓缩样品;
(7)肽标准曲线制备:标准肽用氨基酸同位素稀释质谱法溯源SI单位,将其用三级水配制标准肽/标记肽比例为0.01、0.05、0.1、0.5、1.0、1.5、2的曲线;分析标准肽、同位素内标肽峰面积并制作标准曲线,根据标准曲线计算标准肽浓度;
检出限及定量限、回收率及精密度:计算标准肽段的检出限、定量限;计算测量值与理论值之比为方法回收率,在一天内连续测量同一样品计算重复性,在不同天数测量同一样品计算批间精密度;
(8)计算胰岛素样品中特征肽段含量,特征肽段含量乘以系数即得胰岛素浓度;其中,所述系数为胰岛素分子量除以特征肽段分子量。
其中,所述步骤(1)具体为,根据胰岛素氨基酸序列,用Peptide mass软件设计,Trypsin酶切,选择特征肽段GFFYTPK,理论分子量为858.98Da;合成肽分子量为859Da,在溶液中主要为二价电荷,分子量为430Da。
其中,所述步骤(2)具体为,在特征肽段第三个位点苯丙氨酸(F)位点标记同位素
其中,所述步骤(3)具体为,将合成的肽段水解成氨基酸,定量添加同位素标记氨基酸,以国家氨基酸标准物质为标准建立高效液相色谱-同位素稀释质谱方法测定水解液中稳定氨基酸含量,并据此计算特征肽段纯度。
其中,所述步骤(4)中,三重四级杆质谱仪鉴定特征性肽段离子对为430/655、430/508、430/328、430/120;同位素标记肽段离子对为435/665、435/508、435/333、435/120,其中430/655与435/665和430/120、435/120为定量离子对。
其中,所述步骤(5)中液相分离及质谱条件优化具体为,高效液相色谱参数液相色谱仪:Agilent 1260液相色谱;色谱柱:AERIS TM PEPTIDE XB-C18 150×2.1mm,3.6μm;柱温40℃,流动相A:0.1%甲酸水溶液,流动相B:0.1%甲酸乙腈溶液,流速0.2mL/min,流动相梯度:(0~3)min 5%,18min 65%,21min 90%,24min 90%,25min 5%;
质谱分离条件:三重四级杆质谱仪,离子喷射电压5500V;温度350℃;气帘气体为28L/min,喷雾气38L/min;正离子方式检测;扫描方式为多反应监测。
其中,所述的步骤(6)中,样本分析前处理的具体步骤为:
a.配制样品:配制1mg/mL胰岛素样品;
b.酶解:加入胰酶,胰酶与样品质量比为1:16,放入37℃恒温烘箱18h,加10%甲酸2μL终止反应;
c.加标记:按照标记:样品的摩尔比1:1加入标记,震荡摇匀;
d.浓缩样品,在氮吹仪上浓缩洗脱液,温度45℃,待有机溶剂挥发后,用0.1%甲酸溶解,0.22μm滤膜过滤,上机进行液相质谱检测,进样量7μL。
其中,所述步骤(8)中,根据下述公式计算酶切溶液中特征肽段的含量,
式中:c为样品中GFFYTPK的含量(mg/g);
m
R
I
I
R
R
M:样品质量(mg);
P:GFFYTPK的纯度。
同现有技术相比,本发明的突出效果在于:
(1)本发明的基于特征性肽段同位素稀释质谱法的胰岛素定量方法可用于定量不同来源的胰岛素和胰岛素类似物,包括猪胰岛素、牛胰岛素、人胰岛素及其他具有GFFYTPK特征性肽段的胰岛素类似物。本发明的定量方法无需进行高温水解,安全性较高。
(2)本发明选择的GFFYTPK肽段具有代表性,是胰岛素特征肽段。该肽段为首次用于胰岛素定值。
(3)本发明方法操作简便,准确度好,速度快,出峰时间短。
(4)本方法在标准品、同位素内标等方面明显不同于氨基酸同位素稀释质谱法定量胰岛素,定量检测结果同样可溯源至SI。
下面结合附图说明和具体实施例对本发明所述的基于特征性肽段同位素稀释质谱法的胰岛素定量方法作进一步说明。
附图说明
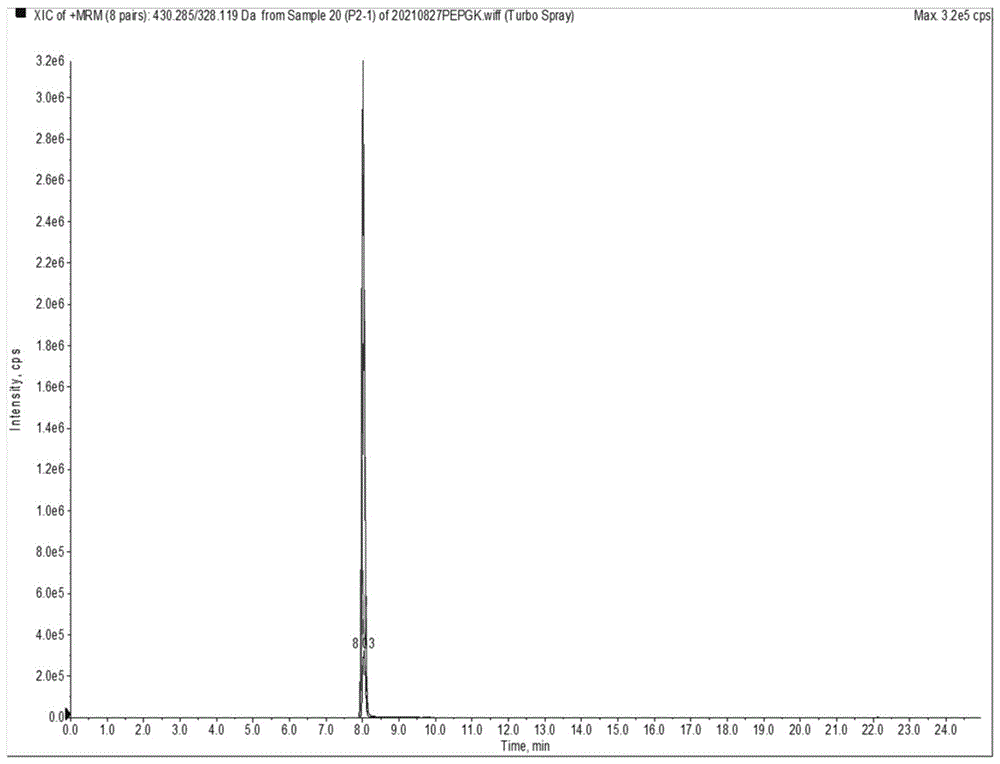
图1为实施例1的不同离子对测量结果图。
图2为实施例2的不同离子对测量结果图。
具体实施方式
实施例1
基于特征性肽段同位素稀释质谱法的胰岛素定量方法对猪胰岛素溶液标准物质的含量进行了测定,包括以下步骤:
(1)特征肽段选择
以猪胰岛素为例,分子式为C
α链:GIVEQCCTSICSLYQLENYCN;
β链:FVNQHLCGSHLVEALYLVCGERGFFYTPKA。
用Peptide mass软件设计,Trypsin酶切,GFFYTPK为最终选择肽段(如SEQ ID No:3所示),见表1,理论分子量为858.98Da。合成肽分子量为859Da,在溶液中主要为二价电荷,分子量为430Da。
表1Peptide mass软件设计
(2)合成用于猪胰岛素定量的标记肽段
在特征肽段第三个氨基酸F位点标记同位素(13C9 15N),GFF*(13C9 15N)YTPK,标记同位素分子量为10Da,同位素标记肽段分子量为869Da,在溶液中主要为二价电荷,分子量为435Da。
(3)特征肽段纯度的准确测定
将合成的肽段水解成氨基酸,定量添加同位素标记氨基酸,以国家氨基酸标准物质为标准建立高效液相色谱-同位素稀释质谱方法测定水解液中稳定氨基酸含量,并据此计算特征肽段纯度。特征肽段GFFYTPK,用于定量的氨基酸为苯丙氨酸(F)。
(4)特征肽段质谱参数的优化
三重四级杆质谱仪鉴定特征性肽段离子对为430/655、430/508、430/328、430/120,同位素标记肽段离子对为435/665、435/508、435/333、435/120,如表2所示。
结合图1结果确定430/120、435/120和430/655与435/665为定量离子对。
表2猪胰岛素检测离子对及测量条件
(5)液相分离及质谱优化条件:
高效液相色谱参数液相色谱仪:Agilent 1260液相色谱;
色谱柱:AERIS TM PEPTIDE XB-C18 150×2.1mm,3.6μm;
柱温40℃;
流动相A:0.1%甲酸水溶液;
流动相B:0.1%甲酸乙腈溶液,流速0.2mL/min,流动相B梯度为:(0~3)min 5%,18min 65%,21min 90%,24min 90%;25min 5%;
质谱分离条件:三重四级杆质谱仪,离子喷射电压5500V;温度350℃;气帘气体为28L/min,喷雾气38L/min;正离子方式检测;扫描方式为多反应监测。
质谱优化条件见表2所示。
(6)样本分析前处理:
主要步骤有:酶解、浓缩样品。
a.配制样品:先用50mM碳酸氢胺溶液将猪胰岛素样品稀释到1mg/mL;
b.酶解:加入胰酶,胰酶与样品质量比为1:16,放入37℃恒温烘箱18h,加10%甲酸2μL终止反应;
c.加标记:按照摩尔比1:1(标记:样品)加入标记,震荡摇匀;
d.浓缩样品,在氮吹仪上浓缩洗脱液,温度45℃,待有机溶剂挥发后,用0.1%甲酸溶解,0.22μm滤膜过滤,上机进行液相质谱检测,进样量7μL。
(7)肽标准曲线制备
检出限及定量限:将其用三级水配制标准肽/标记肽比例为0.01、0.05、0.1、0.5、1.0、1.5、2的曲线;计算标准肽段的检出限、定量限。
标准蛋白肽、标记蛋白肽出峰时间8min,用软件Analyst分析标准肽/同位素内标肽峰面积并制作标准曲线,线性回归方程:y=1.1858x+0.0037,r
计算获得标准肽段的检出限为0.2ng/mL,定量限为0.7ng/mL。不同加标量下,标准肽的回收率为98.9%~102.5%。胰岛素样品测量重复性为0.8%~2.9%,批间精密度为1.5%~3.4%。回收率及精密度符合规定要求。
(8)猪胰岛素样品中特征肽段含量的计算
根据下述公式,计算酶切溶液中GFFYTPK的含量,
式中:c为样品中GFFYTPK的含量(mg/g);
m
R
I
I
R
R
M:样品质量(mg);
P:GFFYTPK的纯度。
根据猪胰岛素分子量5778Da和特征肽段的分子量计算溶液中猪胰岛素的浓度作为猪胰岛素标准物质的定值结果。胰岛素浓度为特征肽段浓度乘以系数(系数为胰岛素分子量除以标准肽分子量)。
基于肽段分析的IDMS法对猪胰岛素的定值结果如下表3所示。
表3基于特征性肽段的IDMS法对猪胰岛素溶液的含量测定结果(mg/g)
(9)将基于特征性肽段同位素稀释质谱法的胰岛素定量方法对猪胰岛素溶液标准物质的含量的测定结果与基于氨基酸同位素稀释质谱法的含量测定结果(表4)进行了比较,结果一致,证明基于特征性肽段同位素稀释质谱法的胰岛素定量方法可以实现对猪胰岛素溶液的准确定量。
表4基于氨基酸分析的IDMS法对猪胰岛素溶液的含量测定结果(mg/g)
/>
实施例2
基于特征性肽段同位素稀释质谱法的胰岛素定量方法对国家标准物质GBW09292人胰岛素纯度标准物质的含量进行了测定,包括以下步骤:
(1)特征肽段选择:
以人胰岛素为例,分子式为C
α链:GIVEQCCTSICSLYQLENYCN;
β链:FVNQHLCGSHLVEALYLVCGERGFFYTPKT。
用Peptide mass软件设计,Trypsin酶切,GFFYTPK为最终选择肽段(如SEQ ID No:3所示),见表5,理论分子量为858.98Da。合成肽分子量为859Da,在溶液中主要为二价电荷,分子量为430Da。
表5Peptide mass软件设计
(2)合成用于人胰岛素定量的标记肽段
在特征肽段第三个氨基酸F位点标记同位素(13C9 15N),标记同位素分子量为10Da,同位素标记肽段分子量为869Da,在溶液中主要为二价电荷,分子量为435Da。
(3)特征肽段纯度的准确测定
将合成的肽段水解成氨基酸,定量添加同位素标记氨基酸,以国家氨基酸标准物质为标准建立高效液相色谱-同位素稀释质谱方法测定水解液中稳定氨基酸含量,并据此计算特征肽段纯度。特征肽段GFFYTPK,用于定量的氨基酸为苯丙氨酸(F)。
(4)特征肽段质谱参数的优化
三重四级杆质谱仪鉴定特征性肽段离子对为430/655、430/508、430/328、430/120,同位素标记肽段离子对为435/665、435/508、435/333、435/120,如表6所示。
结合图2结果确定430/120、435/120和430/655与435/665为定量离子对。
表6人胰岛素检测离子对及测量条件
(5)液相分离及质谱优化条件
高效液相色谱参数液相色谱仪:Agilent 1260液相色谱;
色谱柱:AERIS TM PEPTIDE XB-C18 150×2.1mm,3.6μm;
柱温40℃;
流动相A:0.1%甲酸水溶液;流动相B:0.1%甲酸乙腈溶液,流速0.2mL/min,流动相B梯度为:(0~3)min 5%,18min 65%,21min 90%,24min 90%;25min 5%;
质谱分离条件:三重四级杆质谱仪,离子喷射电压5500V;温度350℃;气帘气体为28L/min,喷雾气38L/min;正离子方式检测;扫描方式为多反应监测。
质谱优化条件见表6所示。
(6)样本分析前处理:
主要步骤有:酶解、浓缩样品。
a.配制样品:配制1mg/mL胰岛素样品;
b.酶解:加入胰酶,胰酶与样品质量比为1:16,放入37℃恒温烘箱18h,加10%甲酸2μL终止反应;
c.加标记:按照摩尔比1:1(标记:样品)加入标记,震荡摇匀;
d.浓缩样品,在氮吹仪上浓缩洗脱液,温度45℃,待有机溶剂挥发后,用0.1%甲酸溶解,0.22μm滤膜过滤,上机进行液相质谱检测,进样量7μL。
(7)人胰岛素样品中特征肽段含量的计算
根据下述公式,计算酶切溶液中GFFYTPK的含量,
式中:c为样品中GFFYTPK的含量(mg/g);
m
R
I
I
R
R
M:样品质量(mg);
P:GFFYTPK的纯度。
根据人胰岛素分子量5807Da和特征肽段的分子量计算溶液中人胰岛素的浓度。胰岛素浓度为特征肽段浓度乘以系数(系数为胰岛素分子量除以标准肽分子量)。
基于特征性肽段的IDMS法对人胰岛素的含量测定结果如下表7所示。
表7基于特征性肽段的IDMS法对人胰岛素的含量测定结果(g/g)
(8)所使用的人胰岛素为国家标准物质GBW09292,标准值0.857g/g,扩展不确定(k=2)为0.024g/g。基于特征性肽段的IDMS法对人胰岛素的含量测定结果在该标准物质的不确定范围内,证明基于特征性肽段同位素稀释质谱法的胰岛素定量方法可以实现对人胰岛素溶液的准确定量。
以上所述的实施例仅仅是对本发明的优选实施方式进行描述,并非对本发明的范围进行限定,在不脱离本发明设计精神的前提下,本领域普通技术人员对本发明的技术方案作出的各种变形和改进,均应落入本发明权利要求书确定的保护范围内。
- 肽段同位素稀释质谱法定量重组肌钙蛋白I含量的方法
- 肽段同位素稀释质谱法定量重组肌钙蛋白I含量的方法
