一种包被重组PEDV S1蛋白的免疫磁珠及其应用
文献发布时间:2024-04-18 19:59:31
技术领域
本发明属于兽医生物技术领域,具体涉及一种包被重组PEDV S1蛋白的免疫磁珠及其应用。
背景技术
猪流行性腹泻(Porcine epidemic diarrhea,PED)是由猪流行性腹泻病毒(Porcine epidemic diarrhea virus,PEDV)感染引起的以水样腹泻、呕吐和脱水为特征的高度传染性肠道疾病。哺乳仔猪感染PEDV后死亡率高达90%~100%,各年龄段皆可感染。2010年流行的快速传播的新高毒力PEDV毒株造成了大量仔猪死亡,死亡率接近100%,给养猪业造成了巨大的经济损失。
PEDV的血清学检测主要包括中和试验(Neutralization test,SNT)、间接血凝试验(Indiret Hemagglutination Assay,IHA)、间接免疫荧光试验(ImmunofluorescenceAssay,IFA)和酶联免疫吸附试验(Enzyme-linked Immunosorbent Assay,ELISA),其中只有ELSIA适合进行高通量检测。但目前临床上针对PEDV抗体,尤其是特异性IgA抗体检测的ELISA方法的灵敏度较低,检测范围较窄,即区分高、中、低抗体水平的能力不够,从而不利于诊断和疫苗免疫效果评估。
磁微粒(Magnetic particle,MP)是一种新型的纳米微粒材料,可以在其表面合成带有如-OH、-COOH和-NH
磁微粒化学发光检测技术在检测时长与价格等方面都优于传统ELISA,目前还没有关于PEDV抗体的磁微粒化学发光检测方法方面的报道。
发明内容
为了解决现有技术中存在的上述技术问题之一,本发明提供一种包被重组PEDVS1蛋白的免疫磁珠及其应用。
第一方面,本发明提供一种包被重组PEDV S1蛋白的免疫磁珠,所述重组PEDV S1蛋白具有SEQ ID NO:1所示的氨基酸序列。
第二方面,本发明提供编码所述重组PEDV S1蛋白的核酸分子,所述核酸分子包括:
(1):SEQ ID NO:2所示的核苷酸序列;或
(2):与(1)的核苷酸序列互补的序列;或
(3):与(1)的核苷酸序列具有95%以上同源性的序列。
在一些实施方案中,编码所述重组PEDV S1蛋白的核苷酸序列具有如SEQ ID NO:2所示的核苷酸序列。
在一些实施方案中,编码所述重组PEDV S1蛋白的核苷酸序列如SEQ ID NO:2所示。
第三方面,本发明提供一种表达系统,所述表达系统为昆虫杆状表达系统。
在一些实施方案中,所述昆虫杆状表达系统为Sf9昆虫细胞。
与大肠杆菌表达相比,本发明的表达系统使重组蛋白翻译后能够进行正确的折叠与修饰,使表达蛋白与天然蛋白更相似,具有更高的活性(包括抗原性、免疫原性、功能)与稳定性。
第四方面,本发明提供所述重组PEDV S1蛋白在制备检测猪流行性腹泻病毒感染的试剂盒中的用途。
在一些实施方案中,所述针对PEDV S1蛋白的抗体或活性片段包括PEDVIgG抗体和PEDVIgA抗体。
第五方面,本发明提供所述重组PEDV S1蛋白在制备检测猪流行性腹泻病毒感染的诊断试剂中的用途。
第六方面,本发明提供一种猪流行性腹泻病毒感染的检测试剂盒,所述试剂盒包括包被重组PEDV S1蛋白的免疫磁珠。
第七方面,本发明提供所述重组PEDV S1蛋白在猪流行性腹泻病毒感染的检测试剂盒的质量控制中的应用。
第八方面,本发明提供所述重组PEDV S1蛋白在制备猪流行性腹泻病毒疫苗中的应用。
第九方面,本发明提供一种试剂盒,所述试剂盒包括特异性结合所述重组PEDV S1蛋白的抗体。
在一些实施方案中,所述试剂盒还包括免疫磁珠、酶标二抗、阳性对照和阴性对照、样品稀释液、显色液、洗涤液以及磁力板。
在一些实施方案中,所述酶标二抗为兔抗猪IgG或IgA抗体。
本发明的有益效果至少包括以下中的一种:
本发明的重组PEDV S1蛋白具有很好的抗原反应活性。
本发明利用昆虫杆状表达系统,获得重组PEDV S1蛋白,以其作为抗原建立检测PEDV抗体(如,PEDVIgG抗体和PEDVIgA抗体)的磁微粒化学发光方法并组装成试剂盒,可对目前流行的PEDV病毒进行有效的血清学诊断和调查,判断猪群中PEDV抗体水平和自然感染的状况,为PEDV病毒的防治提供一种快速、简便的检测方法,还可以用于临床PEDV疫苗的免疫效果分析和评估。
本发明提供了一种快速、准确、简便、适于大批量检测猪流行性腹泻病毒抗体的磁微粒化学发光试剂盒,磁微粒化学发光检测技术具有检测灵敏度高、检测范围广及检测效率高等优点,可用于猪流行性腹泻病毒抗体检测及病毒感染的诊断,以及疫苗免疫效果的评估。
附图说明
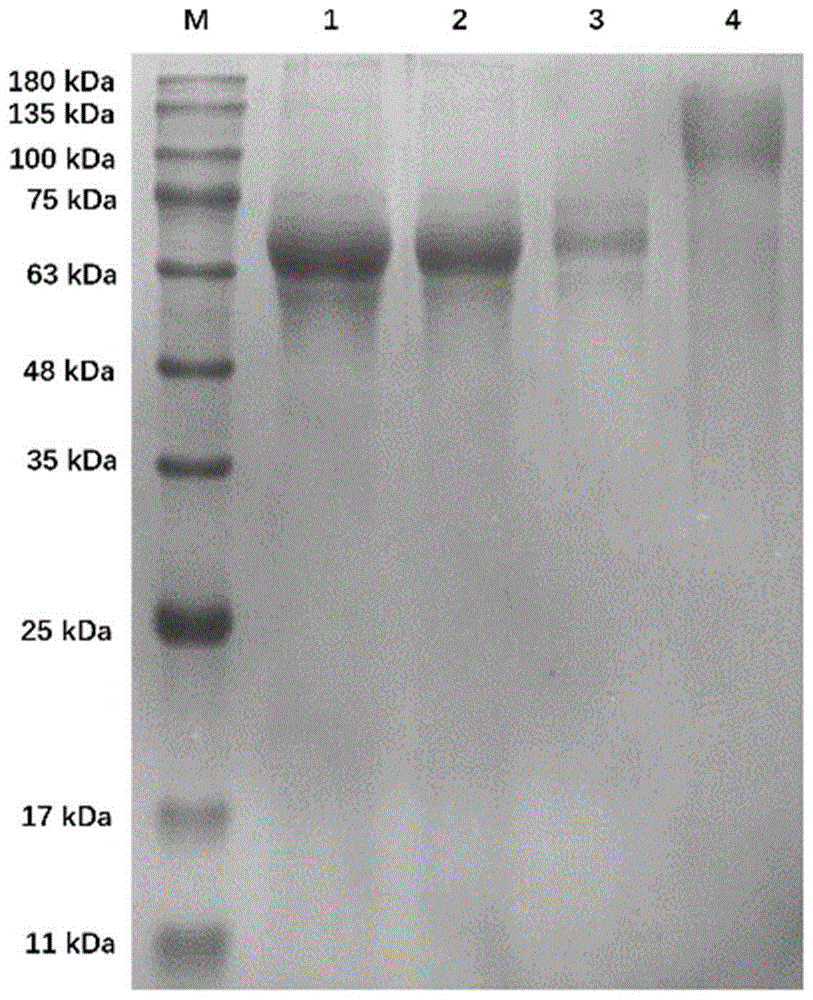
图1示出PEDV S1蛋白的SDS-PAGE分析,其中M:蛋白分子量标准;1:表达产物;2:流穿液;3洗涤液;4:洗脱液。
图2示出PEDV-IgG试剂盒校准曲线。
图3示出PEDV-IgA试剂盒校准曲线。
具体实施方式
为使本发明的目的、技术方案及优点更加清楚明白,以下结合实施例,对本发明进行进一步的详细说明。此处所描述的具体实施例仅用于解释本发明,并不用于构成对本发明的任何限制。此外,在以下说明中,省略了对公知结构和技术的描述,以避免不必要地混淆本公开的概念。这样的结构和技术在许多出版物中也进行了描述。
下面提供实施例和附图以帮助理解本发明。但应理解,这些实施例和附图仅用于说明本发明,但不构成任何限制。本发明的实际保护范围在权利要求书中进行阐述。应理解,在不脱离本发明精神的情况下,可以进行任何修改和改变。
实施例1.重组PEDV S1蛋白的制备与鉴定
1)重组表达质粒的构建:以野生型PEDV S1蛋白为模板,通过PCR扩增,并在基因克隆时在N端添加组氨酸标签(6*His)。人工合成PEDV S1蛋白基因至PfastBac1质粒并命名为pFastBac1-PEDV-S1。重组质粒表达的重组蛋白的氨基酸序列为:
SEQ ID NO:1
本发明的重组PEDV S1蛋白包含病毒的主要中和表位,能刺激机体产生中和抗体,可用作PED血清学诊断的靶抗原。
编码SEQ ID NO:1所示氨基酸序列的核苷酸序列为:
SEQ ID NO:2
2)重组蛋白杆粒的制备:将pFastBac1-PEDV-S1重组质粒转化至MAX
3)重组杆状病毒的构建:将重组杆粒DNA转染至Sf9昆虫细胞系中,生成重组杆状病毒。
4)重组蛋白的表达:参照
5)重组蛋白的纯化:将重组蛋白PEDV-S1用Ni
6)重组蛋白的鉴定:
将纯化后的PEDV S1蛋白进行SDS-PAGE电泳,结果表明,在约110kDa处出现特异性蛋白条带。结果如图1所示。
实施例2.检测PEDV抗体的磁微粒化学发光试剂盒的制备
1)辣根过氧化物酶标记的兔抗猪IgG或IgA抗体:购自Seracare(KPL)公司。
2)免疫磁珠制备:利用混匀器将磁珠进行充分混匀后,移液枪移取2mg磁珠于离心管,将离心管静置于磁力架上固液彻底分离,除去上清液。用偶联缓冲液(15mM MES PH=5.5)将磁珠混匀洗涤2-3遍。磁珠加入50μL活化缓冲液(10mg/mL EDC),充分混匀后,在室温下旋转混合器上反应30min。利用磁力架将固液彻底分离,用偶联缓冲液将磁珠混匀洗涤2-3遍。加入4ug PEDV S1蛋白,充分混匀后,室温旋转反应3h。利用磁力架将固液彻底分离,利用洗涤液将磁珠洗涤2-3遍,将偶联后的磁珠分散到600μL的封闭缓冲液(2% BSA水溶液(质量体积比))中,充分混匀后,室温旋转反应1h,进行免疫磁珠封闭。利用磁力架将固液彻底分离,利用洗涤液将磁珠洗涤2-3遍,将洗涤后的磁珠分散到400μL储存缓冲液(0.1%BSA)中,置于4℃保存。
3)样品稀释液:1% BSA,10g牛血清白蛋白BSA加800mL PBST溶解,加灭菌水至1000mL。
4)辣根过氧化物酶标记二抗:用含1%牛血清白蛋白(BSA)的PBS稀释“1)”中辣根过氧化物酶标记的兔抗猪IgG或IgA抗体100000倍即为辣根过氧化物酶标记二抗。
5)洗涤液:NaCl 80g,KCl 2g,KH
6)底物显色液:包含A液和B液,使用时1:1混合,现配现用。A液为鲁米诺(Luminol)及发光增强剂,B液主要成分为过氧化物及增强剂。
7)阴性对照血清和阳性对照血清制备:
a.阴性对照血清:未经过疫苗免疫且荧光PCR和ELISA检测均为PEDV阴性的健康仔猪血清;
b.阳性对照血清:用稀释液将PEDV抗体强阳血清(灭活)按照比例稀释至工作浓度。
8)校准曲线的绘制:利用校准品浓度和对应的发光值做Logistic曲线拟合,获得一条拟合曲线,即校准曲线,见图2和图3,其中图2示出PEDV-IgG试剂盒校准曲线,图3示出PEDV-IgA试剂盒校准曲线。
9)PEDV-IgG或PEDV-IgA试剂盒的组成:
a.免疫磁珠:4mL;
b.洗涤液:10倍浓缩的含0.5%吐温-20的1M PBS(pH7.4)75mL;
c.样品稀释液:30mL;
d.酶标二抗:30mL;
e.底物显色液A液:15mL;
f.底物显色液B液:15mL;
g.PEDV阴性、阳性对照血清:各1.5mL;
h.磁力板;
i.样品管。
实施例3.PEDV抗体检测试剂盒的使用
a.将待检血清样品用样品稀释液稀释20倍,100μL稀释血清和20μL免疫磁珠一起加入样品管,室温反应15min,使用磁力板分离免疫磁珠与反应体系,250μL~300μL洗涤液洗涤3次;
b.加入100μL的酶标二抗,室温反应15min,250μL~300μL洗涤液洗涤3次;
c.将A液与B液按照1:1混合制成底物显色液,加入100μL的底物显色液,室温避光反应2min;
d.微孔板化学发光检测仪器检测发光值,根据判定标准确定待检样品的阴性、阳性结果。
实施例4.PEDV磁微粒化学发光抗体检测试剂盒判定标准的确定
用PEDV-IgG或PEDV-IgA磁微粒化学发光抗体检测试剂盒分别检测20份SPF猪血清(表1,表2),将检测数据代入标准曲线,得出20次重复测定的阴性血清效价。计算得出两种方法阴性血清测量的平均值分别为0.48RU/mL和0.69RU/mL,标准差SD分别为0.38RU/mL和0.43RU/mL。根据统计学原理,确定PEDV-IgG试剂盒临界值=X+3SD≈1.6RU/mL,同理,确定PEDV-IgA试剂盒阴性、阳性结果的临界值=X+3SD≈2.0RU/mL。
表1.PEDV-IgG试剂盒检测20份SPF猪血清发光值
表2.PEDV-IgA试剂盒检测20份SPF猪血清发光值
由表1和表2的数据可知:PEDV-IgG和PEDV-IgA检测20份SPF猪血清发光值范围分别为324.44~9164.343和393.63~8162.176,两种方法均有较低的发光背景值。其中PEDV-IgG发光值可低至324.44,PEDV-IgA发光值可低至393.63。本发明的方法检测灵敏度高、检测范围广。
实施例5.PEDV磁微粒化学发光抗体检测试剂盒特异性鉴定
采用建立的PEDV-IgG或PEDV-IgA磁微粒化学发光方法分别检测PCV2、CSFV、PRV、PRRSV的阳性血清,结果显示其检测值均小于临界值1.6RU/mL或2.0RU/mL,表明本发明的重组蛋白与其他常见病毒阳性血清无交叉反应,具有良好的特异性。
实施例6.PEDV磁微粒化学发光抗体检测试剂盒判断猪群中PEDV抗体水平和自然感染的状况
采用建立的PEDV-IgA磁微粒化学发光检测方法检测66份猪血清临床样本,其中包括PEDV阴性猪血清样本、自然感染PEDV的猪血清样本和接种PEDV疫苗但未感染的猪血清样本各22份。对猪群中的PEDV抗体水平进行分析(表3)。当检测值≥2.0RU/mL,样品为PEDV抗体阳性,当检测值<2.0RU/mL,样品为PEDV抗体阴性。检测结果显示,自然感染组阳性率为100%,平均检测浓度为68.77RU/mL。接种疫苗但未感染组阳性率为54.5%,平均检测浓度为2.72RU/mL。自然感染的抗体水平明显高于疫苗接种,自然感染抗体水平最高可达155.69RU/mL,而疫苗免疫最高仅为10.29RU/mL,可由此初步对PEDV在猪群中的感染情况进行评估。
表3.PEDV-IgA试剂盒临床猪血清样品检测结果
由表3的数据可知:PEDV-IgA磁微粒化学发光检测方法可区分自然感染猪群与接种疫苗但未感染猪群。根据结果分析可知自然感染猪群的检测值远高于接种疫苗但未感染猪群。自然感染猪最高检测值可达到137.35RU/mL,而接种疫苗但未感染猪最高检测值仅为10.29RU/mL。
本发明的技术方案不限于上述具体实施例的限制,凡是根据本发明的技术方案做出的技术变形,均落入本发明的保护范围之内。
- 一种高稳定性高色泽保真复合地板及其制造方法
- 一种具有高稳定性的数控机床底座
- 一种高稳定性的数控机床
