一种同时测定人血浆中利多卡因及丁卡因浓度的方法
文献发布时间:2023-06-19 19:28:50
技术领域
本发明属于药物色谱-质谱分析领域,涉及化学药物的检测方法,具体涉及一种同时测定人血浆中利多卡因及丁卡因浓度的方法,特别涉及一种液相色谱-质谱法(LC-MS/MS法)用于测定乙二胺四乙酸抗凝血浆(ETDA-K2人血浆,在全血采集时加入1%全血体积的胆碱酯酶抑制剂,10mg/ml新斯的明)中利多卡因和丁卡因浓度的方法。
背景技术
利多卡因是酰胺类局部麻醉药,丁卡因是酯类局部麻醉药,二者均属于起效快但作用时间短的短效局部麻醉药物,都是通过阻断神经冲动启动和传导所需的钠离子通道,从而产生局部麻醉作用。新型表皮局麻软膏
目前,
基于以上所述,考虑到丁卡因在全血及血浆胆碱酯酶下极易水解转化,不仅需提高方法的灵敏度,更需在全血采集时加入胆碱酯酶抑制剂:新斯的明,因此,需开发高灵敏度、稳定耐用的液相色谱-质谱法(LC-MS/MS法)用于
发明内容
针对现有技术同时检测生物样本中利多卡因和丁卡因浓度检测方法方面的空白和缺陷,本发明的目的在于提供一种同时测定人血浆中利多卡因及丁卡因浓度的方法,该方法操作简单、分析快速、灵敏度高、精确度高,而且能应用于多种不同的生物基质。
本发明的技术方案概述如下:
一种同时测定人血浆中利多卡因及丁卡因浓度的方法,包括以下步骤:
S1:配制混合标曲工作液:
S101:配制200μg/mL利多卡因-甲醇溶液,作为利多卡因储备液;具体为:精密称取适量利多卡因(质量校正系数99.7%),置于100mL容量瓶中,用甲醇溶解并定容,配制成200μg/mL利多卡因-甲醇溶液,作为利多卡因储备液;
S102:配制4μg/mL丁卡因-甲醇溶液,作为丁卡因储备液;具体为:
精密称取适量盐酸丁卡因(质量校正系数87.9%),置于100mL容量瓶中,用甲醇溶解并定容,制成80μg/mL丁卡因-甲醇溶液,用移液管取5mL置于100mL容量瓶中,用甲醇稀释并定容,得浓度为4μg/mL丁卡因-甲醇溶液,作为丁卡因储备液;
S103:将利多卡因储备液与丁卡因储备液按等体积混合后,用50v/v%甲醇水溶液进行稀释,配制成含40~8000ng/mL利多卡因、0.8~160ng/mL丁卡因的混合标曲工作液;具体稀释过程如下表所示:
;
S2:配制标曲样品:将S1所得混合标曲工作液加入空白血浆中,控制混合标曲工作液与空白血浆的体积比为1:19,得含2~400ng/mL利多卡因、0.04~8ng/mL丁卡因的标曲样品;具体配制过程如下表所示:
;
S3:配制质控工作液:将利多卡因储备液与丁卡因储备液按等体积混合后,用50v/v%甲醇水溶液进行稀释,配制成含40~30000ng/mL利多卡因、0.8~600ng/mL丁卡因的混合质控工作液;具体为:
精密称取适量利多卡因(质量校正系数99.7%),置于50mL容量瓶中,用甲醇溶解并定容,制成200μg/mL利多卡因-甲醇溶液,作为利多卡因储备液;
精密称取适量盐酸丁卡因(质量校正系数87.9%),置于50mL容量瓶中,用甲醇溶解并定容,制成80μg/mL丁卡因-甲醇溶液,用移液管取5mL置于100mL容量瓶中,用甲醇稀释并定容,得浓度为4μg/mL丁卡因-甲醇溶液,作为丁卡因储备液;
具体稀释过程如下表所示:
;
S4:配制质控样品:将S3所得质控工作液加入空白血浆中,控制质控工作液与空白血浆的体积比为1:19,得含2~1500ng/mL利多卡因、0.04~30ng/mL丁卡因的质控样品;
S5:配制内标工作液:
S501:配制200μg/mL利多卡因-d
S502:配制200μg/mL丁卡因-d
S503:按5:1的体积比将利多卡因-d
S6:前处理:
S601:标曲、质控样品前处理:各量取不同浓度标曲、质控样品100μL并加入至96孔板中,再加入50μL内标工作液、300μL沉淀剂甲醇,涡旋振荡5min后,在3040±30g、4℃条件下,离心10min,取上清液150μL,加入150μL纯水混匀后,吸取5μL进样分析;
S602:待测血浆样品前处理:量取待测血浆样品100μL并加入至96孔板中,再加入50μL内标工作液、300μL沉淀剂甲醇,涡旋振荡5min后,在3040±30g、4℃条件下,离心10min,取上清液150μL,加入150μL纯水混匀后,吸取5μL进样分析;
S7:LC-MS/MS方法检测:通过LC-MS/MS方法检测,基于待测物中利多卡因、丁卡因与内标的峰面积比,通过归一化法得到标准曲线,定量测出生物样品中利多卡因和丁卡因的浓度。
优选的是,所述混合标曲工作液中的利多卡因浓度为40、80、200、400、1000、2000、6400、8000ng/mL,丁卡因浓度为0.8、1.6、4、8、20、40、128、160ng/mL。
优选的是,所述空白血浆的制备方法为:在全血采集时,加入1%全血体积的10mg/mL新斯的明,离心分离后,得空白血浆。
优选的是,所述标曲样品中的利多卡因浓度为2、4、10、20、50、100、320、400ng/mL,丁卡因浓度为0.04、0.08、0.2、0.4、1、2、6.4、8ng/mL。
优选的是,所述混合质控工作液中的利多卡因浓度为40、120、600、2000、6000、30000ng/mL,丁卡因浓度为0.8、2.4、12、40、120、600ng/mL。
优选的是,所述质控样品中的利多卡因浓度为2、6、30、100、300、1500ng/mL,丁卡因浓度为0.04、0.12、0.6、2、6、30ng/mL。
优选的是,所述LC-MS/MS方法的液相色谱及质谱条件如下:
(1)液相色谱条件:色谱柱:Agilent Eclipse Plus C18,其规格为3.0*100mm、3.5μm;流动相:流动相A为0.1v/v%甲酸水溶液、流动相B为乙腈;流速:0.4mL/min;柱温:40℃;进样量:5.00μL;
(2)质谱条件:电喷雾正离子模式;毛细管电压:3500V;雾化器压力:45psi;干燥气流速:12L/min;干燥气温度:300℃;鞘气温度:350℃;鞘气流速:11L/min;扫描方式:多重反应监测。
优选的是,所述液相色谱的梯度洗脱程序如下表所示:
优选的是,所述多重反应监测参数如下表所示:
优选的是,所述待测血浆样品为涂抹含7wt%利多卡因、7wt%丁卡因的复方乳膏后的受试者血浆样品,且在全血采集时,加入1%全血体积的10mg/mL新斯的明,经离心分离后制得。
本发明的有益效果:
1、本发明方法通过高效、快速、灵敏的液相质谱联用系统(LC-MS/MS)方法对利多卡因和丁卡因进行联合分析,利用简单的有机溶剂蛋白沉淀法对生物样本进行前处理,并基于待测物与内标的峰面积比,通过面积归一化法得到标准曲线,从而定量得到受试者血浆样品中利多卡因和丁卡因的浓度。
2、本发明方法能同时测定出利多卡因和丁卡因在人体内的浓度,为药代动力学的计算提供了简便的分析方法。本检测方法操作简单,分析快速高效,单样品检测时间仅需8min,灵敏度高,丁卡因定量下限为0.04ng/ml,相比于传统局部麻醉药检测方法具有明显优势,而且能应用于多种不同的生物基质。
附图说明
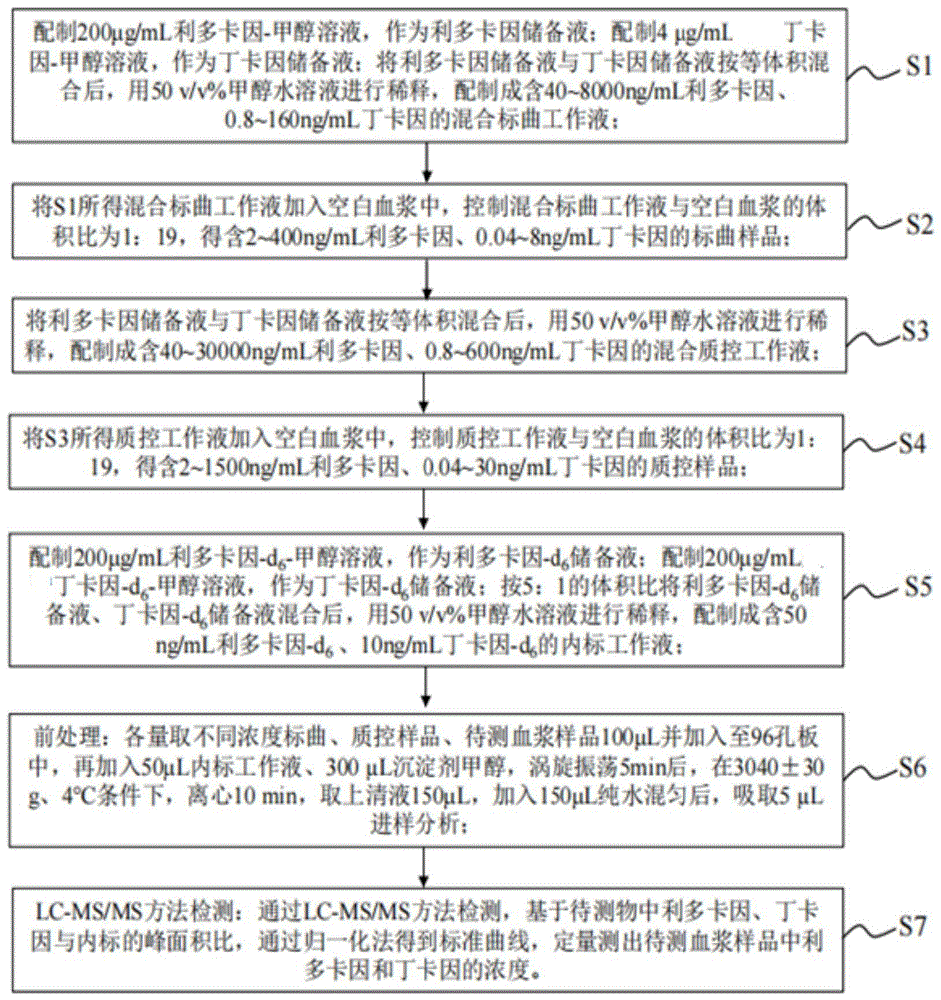
图1为本发明同时测定人血浆中利多卡因及丁卡因浓度的方法流程图;
图2-图5依次为实施例1的标曲、质控样品进样分析测出的利多卡因、内标利多卡因-d
图6-图9依次为实施例1的待测血浆样品进样分析测出的利多卡因、内标利多卡因-d
图10为实施例1的利多卡因面积归一化标准曲线图;
图11为实施例1的丁卡因面积归一化标准曲线图。
具体实施方式
下面结合实施例对本发明做进一步的详细说明,以令本领域技术人员参照说明书文字能够据以实施。
实施例1
一种生物样品中利多卡因和丁卡因的检测方法,包括以下步骤:
(1)准备仪器与试剂:高效液相色谱仪:Agilent 1290HPLC;色谱柱:AgilentEclipse Plus C18,3.0*100mm,3.5μm;利多卡因标准品(中国食品药品检定研究院);盐酸丁卡因标准品(中国食品药品检定研究院);盐酸利多卡因-d
(2)配制混合标曲工作液:
精密称取适量利多卡因(质量校正系数99.7%),置于100mL容量瓶中,用甲醇溶解并定容,配制成200μg/mL利多卡因-甲醇溶液,作为利多卡因储备液;
精密称取适量盐酸丁卡因(质量校正系数87.9%),置于100mL容量瓶中,用甲醇溶解并定容,制成80μg/mL丁卡因-甲醇溶液,用移液管取5mL置于100mL容量瓶中,用甲醇稀释并定容,得浓度为4μg/mL丁卡因-甲醇溶液,作为丁卡因储备液;
将利多卡因储备液与丁卡因储备液按等体积混合后,用50v/v%甲醇水溶液进行稀释,配制成混合标曲工作液,且其中的利多卡因浓度分别为40、80、200、400、1000、2000、6400、8000ng/mL,丁卡因浓度分别为0.8、1.6、4、8、20、40、128、160ng/mL;具体稀释过程如下表所示:
(3)配制标曲样品:
在全血采集时,加入1%全血体积的10mg/mL新斯的明,离心分离后,得空白血浆;
将步骤(2)所得混合标曲工作液加入空白血浆中,控制混合标曲工作液与空白血浆的体积比为1:19,得标曲样品,且其中的利多卡因浓度分别为2、4、10、20、50、100、320、400ng/mL,丁卡因浓度分别为0.04、0.08、0.2、0.4、1、2、6.4、8ng/mL;具体配制过程如下表所示:
(4)配制质控工作液:
精密称取适量利多卡因(质量校正系数99.7%),置于50mL容量瓶中,用甲醇溶解并定容,制成200μg/mL利多卡因-甲醇溶液,作为利多卡因储备液;
精密称取适量盐酸丁卡因(质量校正系数87.9%),置于50mL容量瓶中,用甲醇溶解并定容,制成80μg/mL丁卡因-甲醇溶液,用移液管取5mL置于100mL容量瓶中,用甲醇稀释并定容,得浓度为4μg/mL丁卡因-甲醇溶液,作为丁卡因储备液;
将利多卡因储备液与丁卡因储备液按等体积混合后,用50v/v%甲醇水溶液进行稀释,配制成混合质控工作液,且其中的利多卡因浓度分别为40、120、600、2000、6000、30000ng/mL,丁卡因浓度分别为0.8、2.4、12、40、120、600ng/mL;具体稀释过程如下表所示:
/>
(5)配制质控样品:
在全血采集时,加入1%全血体积的10mg/mL新斯的明,离心分离后,得空白血浆;
将步骤(4)所得质控工作液加入空白血浆中,控制质控工作液与空白血浆的体积比为1:19,得质控样品,且其中的利多卡因浓度分别为2、6、30、100、300、1500ng/mL,丁卡因浓度分别为0.04、0.12、0.6、2、6、30ng/mL;
(6)配制内标工作液:
精密称取适量利多卡因-d
精密称取适量盐酸丁卡因-d
按5:1的体积比将利多卡因-d
(7)前处理:
标曲、质控样品前处理:各量取不同浓度标曲、质控样品100μL并加入至96孔板中,再加入50μL内标工作液、300μL沉淀剂甲醇,涡旋振荡5min后,在3040±30g、4℃条件下,离心10min,取上清液150μL,加入150μL纯水混匀后,吸取5μL进样分析;
空白样品前处理:各量取100μL空白血浆并加入至96孔板中,再加入50μL 50v/v%甲醇水溶液、300μL沉淀剂甲醇,涡旋振荡5min后,在3040±30g、4℃条件下,离心10min,取上清液150μL,加入150μL纯水混匀后,得空白基质处理的双空白样品,并吸取5μL进样分析;
待测血浆样品前处理:
待测血浆样品为受试者涂抹含7wt%利多卡因、7wt%丁卡因的
量取待测血浆样品100μL并加入至96孔板中,再加入50μL内标工作液、300μL沉淀剂甲醇,涡旋振荡5min后,在3040±30g、4℃条件下,离心10min,取上清液150μL,加入150μL纯水混匀后,吸取5μL进样分析;
(8)LC-MS/MS方法检测:通过LC-MS/MS方法检测,基于待测物中利多卡因、丁卡因与内标的峰面积比,通过归一化法得到标准曲线,定量测出生物样品中利多卡因和丁卡因的浓度;具体的检测条件、数据分析结果如下:
(8a)LC-MS/MS方法的液相色谱及质谱条件如下:
液相色谱条件:色谱柱:Agilent Eclipse Plus C18,其规格为3.0*100mm、3.5μm;流动相:流动相A为0.1v/v%甲酸水溶液、流动相B为乙腈;流速:0.4mL/min;柱温:40℃;进样量:5.00μL;梯度洗脱程序如下表所示:
质谱条件:电喷雾正离子模式;毛细管电压:3500V;雾化器压力:45psi;干燥气流速:12L/min;干燥气温度:300℃;鞘气温度:350℃;鞘气流速:11L/min;扫描方式:多重反应监测(MRM)且其参数如下表所示:
(8b)建立标准曲线:
图2-图5依次为实施例1的标曲、质控样品进样分析测出的利多卡因、内标利多卡因-d
根据图2-图9得出,利多卡因基于待测血浆样品与内标的峰面积比,通过归一化法得到标准曲线,如图10所示,标准方程为:y=0.054696x-0.002824(R
标准曲线样品测定结果:利多卡因标准曲线样品测定结果见表1(A)、丁卡因标准曲线样品测定结果见表1(B)。
表1(A)利多卡因标准曲线样品测定结果表
表1(B)丁卡因标准曲线样品测定结果表
/>
(8c)选择性:
6个不同来源空白基质处理的双空白样品结果:利多卡因选择性空白基质样品测定结果见表2(A)、丁卡因选择性空白基质样品测定结果见表2(B);6个不同来源空白基质的处理定量下限(LLOQ)样品结果:利多卡因选择性LLOQ样品测定结果见表2(C)、丁卡因选择性LLOQ样品测定结果见表2(D)。
表2(A)利多卡因选择性空白基质样品测定结果表
表2(B)丁卡因选择性空白基质样品测定结果表
表2(C)利多卡因选择性定量下限(LLOQ)样品测定结果表
表2(D)丁卡因选择性定量下限(LLOQ)样品测定结果表
(8d)准确度与精密度:
准确度与精密度考察结果:利多卡因准确度与精密度测定结果见表3(A)、丁卡因准确度与精密度测定结果见表3(B)。
表3(A)利多卡因准确度与精密度结果表
表3(B)丁卡因准确度与精密度结果表
(8e)稀释因子:
模拟配制高于定量上限(ULOQ)血浆样品,经空白基质5倍稀释后的测定结果:利多卡因稀释因子考察结果见表4(A)、丁卡因稀释因子考察结果见表4(B)
表4(A)利多卡因稀释因子结果表
表4(B)丁卡因稀释因子结果表
(8f)定量结果:通过标准曲线定量得到人血浆中利多卡因和丁卡因的浓度如表5所示:
表5通过标准曲线定量得到人血浆中利多卡因和丁卡因的浓度结果表
综上所述,实施例1能同时测定出利多卡因和丁卡因在人体内的浓度,为药代动力学的计算提供了简便的分析方法,且实施例1测定方法操作简单,分析快速高效,灵敏度高,丁卡因定量下限为0.04ng/ml,相比于传统局部麻醉药检测方法具有明显优势,而且能应用于多种不同的生物基质。
尽管本发明的实施方案已公开如上,但其并不仅仅限于说明书和实施方式中所列运用,它完全可以被适用于各种适合本发明的领域,对于熟悉本领域的人员而言,可容易地实现另外的修改,因此在不背离权利要求及等同范围所限定的一般概念下,本发明并不限于特定的细节。
- 一种测定人血浆中阿帕替尼药物浓度的方法
- 一种测定人血浆中雷替曲塞药物浓度的方法
- 一种测定人血浆中麦考酚酸总浓度和游离浓度的方法
- 一种测定人血浆中麦考酚酸总浓度和游离浓度的方法
