一种检测试剂盒、检测工具及其在预测阿尔兹海默病中的用途
文献发布时间:2023-06-19 18:32:25
技术领域
本发明属于生物技术领域,具体涉及一种阿尔茨海默病预测标志物检测试剂盒与检测工具。
背景技术
阿尔茨海默病(Alzheimer’s disease,AD)是一种起病隐袭、呈进行性发展的神经退行性疾病,临床特征主要为认知障碍、精神行为异常和社会生活功能减退。阿尔茨海默病在65岁以上的人群中发病率最高,随着我国人口老龄化的进展,若没有很好的治疗方法,预计在未来几十年阿尔茨海默病的增加比例将更加迅速,将导致家庭和社会承担巨大的经济负担。目前尚无治愈阿尔茨海默病的有效手段。阿尔茨海默病的症状进展缓慢,并随着时间逐渐恶化。因此,发现经济、方便的阿尔茨海默病预测标志物对于提供更好的阻碍阿尔茨海默病进展的机会是至关重要的。有研究报道β-淀粉样蛋白积聚形成的有毒斑块导致了阿尔茨海默症,且多项证据表明,阿尔茨海默病患者大脑中Aβ和tau蛋白的异常积累早在痴呆症状出现前年即已经开始。
近年来的研究已经证实,人体内共生微生物种类与数量与阿尔茨海默病的发生与发展密切相关,中国专利申请CN201880066002.7公开了一种通过细菌宏基因组分析来诊断阿尔茨海默氏症的方法,其使用人体血液样品,对细菌的细胞外囊泡进行宏基因组分析来预测轻度认知障碍和阿尔茨海默氏症发作的风险,可早期诊断和预测阿尔茨海默氏症风险群体以利用适当的治愈延迟该疾病发作的时间或防止该疾病发作,并且在该疾病发作之后,可进行早期诊断,从而降低阿尔茨海默氏症的发生率并提高治疗效果。然而该技术存在以下的缺陷:一、由于检测样本为血液,必须采用介入式采集方式,无法在短期内进行多次测量,从而增加了单次检测假阳性的风险,提高了误诊的发生率;二、检测对象是人体血液样本的细胞外囊泡,样本处理操作复杂,成本高;三、检测的标志物仅针对各种不同种属细菌的细胞外囊泡,指标相对单一,如果出现菌群失调情况,可能导致检测结果不准确,从而增加误诊的可能。
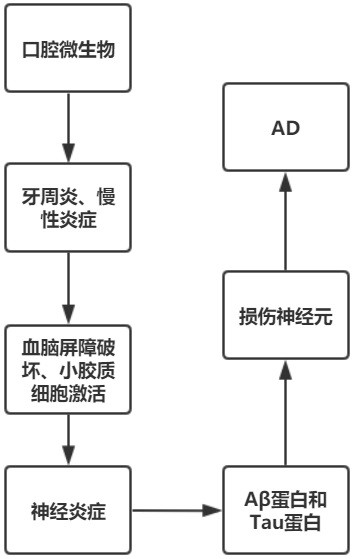
本研究团队发现阿尔茨海默病患者的大脑中存在多种口腔致病微生物种群,如:细菌(牙龈卟啉单胞菌、幽门螺杆菌、福赛坦氏菌、普氏杆菌、具核梭杆菌、螺旋体)、病毒(单纯疱疹病毒1型、巨细胞病毒、人类疱疹病毒6型、EB病毒)和真菌(白色假丝酵母菌、光滑假丝酵母菌),如附图1所示,这些口腔微生物种群可因感染、外伤或医源性因素进入血液,突破血脑屏障直接进入大脑,产生有毒物质引起炎症反应,进一步引起Aβ沉积、tau 蛋白过磷酸化,最终对神经元产生不可逆损伤甚至导致神经元凋亡。口腔样本采集方便,但鉴于口腔微生物种类繁多且口腔微生物种群随环境变化、食品卫生等外界因素波动幅度较大,检测结果偏差较大,易产生假阳性,因此制约着利用口腔微生物检测阿尔茨海默病患病风险的技术发展。
有鉴于此,针对上述技术问题,本发明提出一种设计合理、采样便捷、便于持续动态监测且精确度更高的阿尔茨海默病预测标志物检测试剂盒和检测方法。
发明内容
为了解决上述问题,本发明利用宏基因组测序,可以检测口腔中存在的所有稳定微生物,从而获得测试样本与阿尔茨海默病相关的全面信息。
具体技术方案是:
本发明在第一方面涉及用于选择自口腔稳定微生物中的AD生物标志物的检测工具在制备通过包括以下的方法诊断受试者中的阿尔兹海默症(AD)或确定受试者中发生阿尔兹海默症(AD) 的风险的试剂或试剂盒中的用途:
(1)口腔稳定微生物样本获取
(2)样本基因文库制备与扩增;
(3)宏基因测序;
(4)将宏基因组测序结果与数据库中已知微生物基因组进行比对与分类;
(5)根据比对与分类结果获得口腔稳定微生物种群与丰度。
利用多元回归模型衡量不同微生物群落对AD的影响程度,并将微生物种群丰度与影响程度加权后计算受试者阿尔兹海默症患病风险。优选的,作为所述AD生物标志物的口腔稳定微生物样本取自牙菌斑或舌苔,且包括细菌、病毒、真菌中的至少两种。
进一步的,所述基因文库包括基因组文库和/或cDNA文库。
优选的,所述细菌包括牙龈卟啉单胞菌、幽门螺杆菌、福赛坦氏菌、普氏杆菌、具核梭杆菌、螺旋体中的一种或多种。
优选的,所述病毒包括单纯疱疹病毒1型、巨细胞病毒、人类疱疹病毒6型、EB病毒中的一种或多种。
优选的,所述真菌包括白色假丝酵母菌、光滑假丝酵母菌中的一种或多种。
本发明在另一方面涉及一种用于实现上述用途的试剂盒,所述试剂盒中的试剂至少包括:接头核酸试剂组,所述接头核酸试剂组包括文库接头与若干PCR核酸扩增随机引物组;酶试剂组,所述酶试剂组包括DNA聚合酶、DNA连接酶;基因纯化装置,所述基因纯化装置适于将文库接头连接产物与PCR扩增产物进行纯化;以及缓冲液组,所述缓冲液组包括与所述接头核酸试剂组、所述酶试剂组中各组分一一对应的缓冲液。
进一步的,所述酶试剂组还包括核酸片段化酶和末端修复酶。
优选的,所述基因纯化装置为核酸纯化磁珠。
优选的,所述文库接头的序列选自SEQ ID NO.1和/或SEQ ID NO.2。
本发明在第三方面涉及用于选择自口腔稳定微生物中的AD生物标志物的检测工具在制备通过包括以下的计算机实施的方法诊断受试者中的阿尔兹海默症(AD)或确定受试者中发生阿尔兹海默症(AD)的风险的试剂或试剂盒中的用途:
i)采集宏基因组测序数据;
ii)将宏基因组测序数据与数据库中已知微生物基因组进行比对与分类;
iii)根据比对与分类结果获得受试者口腔稳定微生物种群与丰度;
iv)利用多元回归模型衡量不同微生物群落对AD的影响程度,并将微生物种群丰度与影响程度加权后计算受试者阿尔兹海默症患病风险。;
v)向受试者输出判断结果,输出方式至少包括语音、显示、蜂鸣、打印之一;所述判断结果包括细菌、病毒、真菌中至少两类微生物种群的丰度以及患病风险。
本发明在第四方面涉及一种计算机可读介质,其具有用于执行上述计算机实施的方法的计算机可执行的指令。
本发明的有益效果体现在:本发明将牙龈牙菌斑、舌苔或口腔内其他器官上长期稳定附着的微生物样本作为检测样本得到口腔内稳定微生物种群,并将其作为阿尔茨海默病预测标志物,应用于检测试剂盒的制备中实现阿尔茨海默病预测,一方面便于采样,避免了介入取样对受试者的伤害,可对口腔内稳定微生物种群变化进行长期动态监测,避免了单次监测数据的偶然性与不全面性;另一方面,口腔微生物种群随环境变化波动较大,采集诸如牙龈、舌苔等器官上长期与人体共生的稳定口腔微生物可以极大程度避免因环境变化、食品卫生等外界因素造成的监测结果偏差;本发明是依据国内外对阿尔茨海默病发病相关的口腔微生物的分子机制研究的成果,检测与阿尔兹海默症相关的一系列口腔微生物,包括细菌(牙龈卟啉单胞菌、幽门螺杆菌、福赛坦氏菌、普氏杆菌、具核梭杆菌、螺旋体)、病毒(单纯疱疹病毒1型、巨细胞病毒、人类疱疹病毒6型、EB病毒)和真菌(白色假丝酵母菌、光滑假丝酵母菌),根据宏基因组测序全面的检测出样本所含的微生物种类,具有简便、全面、高效、准确等优点。该方法可运用于出现记忆力衰退、语言障碍等老年痴呆症状或者家里有阿尔茨海默病遗传的患者,有利于对该疾病的早期预防治疗,具有巨大的普及和推广应用价值。
附图说明:
为了更清楚的说明本发明实施例或现有技术中的技术方案,下面将对实施例或现有技术描述中所需要使用的附图作简单地介绍,显而易见地,下面描述中的附图仅仅是本发明的一些实施例,对于本领域普通技术人员来讲,在不付出创造性劳动性的前提下,还可以根据这些附图获得其他的附图。
附图1为口腔微生物引发阿尔兹海默症的原理示意图。
具体实施方式:
为了使本技术领域的人员更好地理解本发明的技术方案,下面将结合各实施方式对本发明实施例中的技术方案进行清楚、完整地描述。但应当说明的是,这些实施方式并非对本发明的限制,本领域普通技术人员根据这些实施方式所作的功能、方法、或者用途上的等效变换或替代,均属于本发明的保护范围之内。以下实施例中所使用的实验方法如无特殊说明,实施例中未注明具体条件的实验方法,通常按照常规条件,下述实施例中所使用的材料、试剂等,如无特殊说明,均可从商业途径得到。
本发明选择细菌、病毒、真菌三类,共计十二种稳定口腔微生物作为阿尔兹海默病风险标记物,分别是:细菌(牙龈卟啉单胞菌、幽门螺杆菌、福赛坦氏菌、普氏杆菌、具核梭杆菌、螺旋体)、病毒(单纯疱疹病毒1型、巨细胞病毒、人类疱疹病毒6型、EB病毒)和真菌(白色假丝酵母菌、光滑假丝酵母菌),提取口腔稳定微生物的基因组DNA和/或总 RNA,构建基因组文库和/或cDNA文库,并利用宏基因组测序得到各风险标记物的种群丰度,利用多元回归模型衡量不同微生物群落对阿尔兹海默病的影响程度,并将微生物种群丰度与影响程度加权后计算受试者阿尔兹海默症患病风险。下文将从基因组文库和cDNA文库宏基因组测序两个实施例阐述本发明的具体构思与实施方式。
总步骤一:提取口腔微生物基因组DNA和总RNA。
a.将获取的牙龈牙菌斑/舌苔样本部分转移至1.5ml离心管中.加入750μl缓冲液RL至样品中,用移液器轻轻吹打混匀转移;
b.把DNA吸附柱装在收集管中,小心将以上所得混合液转移750μl至柱子中,14000xg离心 2min;
c.加入等倍体积70%乙醇至滤液中,用移液枪吸打混匀;
d.把RNA吸附柱装在2ml收集管中。转移750μl混合液至柱子中。12000x g离心1min;e.倒弃收集管中的滤液,转移剩余的混合液至柱子中,12000xg离心1min。弃去废液和收集管;
f.把柱子装在新的收集管中。小心加入500μl洗涤液RW1至柱子中。盖紧离心管盖,12000xg离心1min。倒弃滤液,把柱子装回收集管;
g.加入650μl洗涤液RW2至柱子中。盖紧离心管盖,12000×g离心1min。倒弃滤液,把柱子装回收集管;
h.重复步骤g一次;
i.倒弃滤液,把柱子重新装回收集管中。12000xg离心2min;
j.将柱子装在新的1.5ml离心管中。加入20~100μl预热至70℃无核酸酶水至柱子的膜中央。室温静置分钟,12000xg离心1min。弃去柱子,把RNA保存于-80℃;
k.将b步骤中的DNA吸附柱装进新的收集管中,加入500μl洗涤液GW1至柱子中。盖紧离心管盖,10000xg离心1min。倒弃滤液,把柱子装回收集管;
l.加入500μl洗涤液GW1至柱子中。盖紧离心管盖,10000xg离心1min。倒弃滤液,把柱子装回收集管;
m.小心加入650μl洗涤液GW2至柱子中。盖紧离心管盖,10000×g离心1min。倒弃滤液,把柱子装回收集管;
n.重复步骤m一次;
o.倒弃滤液,把柱子重新装回收集管中。10000xg离心3min;
p.将柱子装在新的1.5ml离心管中。加入20~100μl预热至70℃无核酸酶水至柱子的膜中央。
放置3分钟,10000xg离心1min;
q.丢弃DNA结合柱,把DNA保存于2~8℃,长期保存需保存于-20℃。
总步骤二:基因文库构建。
实施例一:基因组DNA文库构建。
(1)接头退火
文库接头序列如下所示:
SEQ ID NO.1:5-acactctttccctacacgacgctcttccgatctatcacgt-3′
SEQ ID NO.2:5-gatcggaagagcacacgtctgaactccagtc-3′
使用退火缓冲液将SEQ ID NO.1和SEQ ID NO.2的干粉分别稀释成20μM,将两者稀释液等比例混合,得到的混合液置于PCR仪中,运行程序:95℃变性2min;缓慢降温至25℃,降温过程用时至少45min,,制备的产物保存于-20℃。
(2)宏基因组文库制备
片段化和末端修复:取100ng口腔微生物DNA,按照表1配置反应体系:
表1
注:表中X为投入100ngDNA的体积,公式X=100/DNA浓度。
振荡混匀、离心(避免气泡)后在PCR仪上运行表2程序,热盖75℃:
表2
接头连接反应:按照表3配置反应体系,可提前将接头连接预混液和增强剂混合, 接头需要单加;
表3
将上述体系置于PCR仪中,运行程序:20℃,15min,热盖关闭。
连接反应后纯化步骤:
a.提前30min以上取出文库纯化磁珠室温静置,使用前需混匀;
b.将反应物移到新的已编号1.5mL离心管,加入31.5μL无核酸酶水将总体积补至100μL,加入90μL重悬的文库纯化磁珠,使用适当量程的移液器轻轻吹打混匀,室温孵育5min;
c.将离心管置于磁力架上,待溶液澄清后,弃上层清液;
d.向其中加入新鲜配置的200μL 80%的乙醇,静置30s后,弃上层清液;
e.重复步骤d一次;
f.磁力架上取下离心管,瞬时离心3s,离心管放回磁力架上,吸弃掉残留的80%乙醇,注意不要吸到磁珠。打开管盖,室温晾干2-10min;
g.待磁珠成亚光色,离心管中加入17μL无核酸酶水,轻微震荡使磁珠重悬,室温孵育5min;
h.将离心管置于磁力架上,静置2min。待溶液澄清后,取15μL上清至0.2mlPCR管中,留待下一步扩增反应。
PCR扩增:按表4加入相应试剂至PCR管中:
表4
其中,P7端标签引物和P5端标签引物具体序列如表5所示:
表5
将混合好的PCR管放入至PCR仪中,运行表6所示程序,热盖105℃:
表6
PCR产物纯化:
a.提前30min以上取出文库纯化磁珠室温静置,使用前需混匀;
b.将反应物移到新的已编号1.5mL离心管,加入45μL重悬的文库纯化磁珠,使用适当量程的移液器轻轻吹打混匀,室温孵育5min;
c.将离心管置于磁力架上,待溶液澄清后,弃上层清液;
d.向其中加入新鲜配置的200μL 80%的乙醇,静置30s后,弃上层清液;
e.重复步骤d一次;
f.磁力架上取下离心管,瞬时离心3s,离心管放回磁力架上,吸弃掉残留的80%乙醇,注意不要吸到磁珠。打开管盖,室温晾干2-10min;
g.待磁珠成亚光色,离心管中加入42μL无核酸酶水,轻微震荡使磁珠重悬,室温孵育 5min;
h.将离心管置于磁力架上,静置2min;待溶液澄清后,取40μL上清至新的离心管中。
应该理解的是虽然本实施例中选择的基因纯化装置为磁珠,但磁珠不应被理解为对权利要求保护范围的限制,本领域任何能够起到基因纯化作用的装置都应该纳入本发明的权利要求的保护范围。
实施例二.cDNA文库构建
逆转录cDNA:
rRNA的去除:将随机引物及rRNA去除混合液室温解冻后,颠倒混匀,置于冰上备 用。按照下表7配置反应液:
表7
使用移液器轻轻吹打混匀,瞬离将反应液离心至管底。将上述PCR管置于PCR仪中, 按照表8程序进行RNA的预变性:
表8
合成cDNA第一链:将第一链合成试剂从-20℃取出,室温解冻,颠倒混匀后瞬离。按 表9所示,配制第一链cDNA合成的反应液:
表9
使用移液器轻轻吹打混匀,瞬离将反应液离心至管底。将上述PCR管置于PCR仪中, 按照表10所示设置反应程序,进行第一链cDNA的合成,反应结束后立即进行第二链:
表10
合成cDNA第二链:将第二链合成试剂从-20℃取出,室温解冻,颠倒混匀后瞬离。按 表11所示,配制第二链cDNA合成的反应液:
表11
使用移液器轻轻吹打混匀,瞬离将反应液离心至管底。将上述PCR管置于PCR仪中,运行16℃60min,4℃∞程序,进行第二链cDNA的合成。
cDNA产物纯化:
a.提前30min以上取出RNA纯化磁珠室温静置,使用前涡旋重悬磁珠;
b.将反应物移到新的已编号1.5mL离心管,加入21μL重悬的RNA纯化磁珠,使用适当量程的移液器轻轻吹打混匀,室温孵育5min;
c.将离心管置于磁力架上,待溶液澄清后,弃上层清液;
d.向其中加入新鲜配置的200μL80%的乙醇,静置30s后,弃上层清液;
e.重复步骤d一次;
f.磁力架上取下离心管,瞬时离心3s,离心管放回磁力架上,吸弃掉残留的80%乙醇,注意不要吸到磁珠。打开管盖,室温晾干2-10min;
g.待磁珠成亚光色,离心管中加入14μL无核酸酶水,轻微震荡使磁珠重悬,室温孵育 5min;
h.将离心管置于磁力架上,静置3min。待溶液澄清后,取13μL上清至新的PCR中。
(2)cDNA文库制备
将反应缓冲液室温解冻后,颠倒混匀,置于冰上备用,按表12所示配置反应体系:
表12
使用移液器轻轻吹打或低速振荡混匀,并短暂离心将反应液离心至管底。将上述PCR管置于PCR仪,运行:55℃10min,4℃∞(热盖开)程序,进行DNA片段化,末端修复及加dA、接头连接反应。
文库扩增:
按照下表13配置扩增反应体系:
表13
其中,所述P5端标签引物和P7端标签引物具体序列同表5所示一致。
使用移液器轻轻吹打或低速振荡混匀,并短暂离心将反应液离心至管底。将上述PCR管置于PCR仪,按表14所示运行程序:
表14
扩增产物纯化:
a.提前30min以上取出DNA纯化磁珠室温静置,使用前涡旋重悬磁珠;
b.将反应物移到新的已编号1.5mL离心管,加入45μL重悬的DNA纯化磁珠,使用适当量程的移液器轻轻吹打混匀,室温孵育5min;
c.将离心管置于磁力架上,待溶液澄清后,弃上层清液;
d.向其中加入新鲜配置的200μL80%的乙醇,静置30s后,弃上层清液;
e.重复步骤d一次;
f.磁力架上取下离心管,瞬时离心3s,离心管放回磁力架上,吸弃掉残留的80%乙醇,注意不要吸到磁珠。打开管盖,室温晾干2-10min;
g.待磁珠成亚光色,离心管中加入42μL无核酸酶水,轻微震荡使磁珠重悬,室温孵育 5min;
h.将离心管置于磁力架上,静置3min。待溶液澄清后,取40μL上清至新的PCR中。
总步骤三:上机测序及结果分析。
(1)文库定量上机:
上述纯化文库,使用定量试剂盒对文库质量浓度进行测量,Agilent 2100质检文库片段大小,通过质量浓度和片段大小计算文库摩尔浓度,根据测序仪说明书使用MGISEQ-200测序仪进行测序。
测序结果计算机比对分析:
质控下机数据后,将宏基因组测序结果利用MetaPhlAn2软件将测序片段比对到微生物参考数据库,进行微生物物种成分分析,并根据各微生物比对的reads数分析样本中各微生物的相对种群丰度。
(2)计算患AD的概率
将多个确定具有和AD相关的微生物因素用于构建多元回归模型,衡量不同微生物群落对 AD的影响程度,进一步将微生物种群丰度与影响程度加权后计算受试者阿尔兹海默症患病风险,具体公式如下所示:
Y=β0+β1·T1+β2+T2+…βn·Tn+∈
其中:
Y:微生物种群总体事件
T:相应微生物的比例
∈:其他因素,如是否有其他基础病,认识损伤等因素
β:权重
P:患AD的概率。
本发明研究团队对20例临床确诊为AD患者和32例健康人的样本制备文库上机测序,验证以上提及的口腔微生物的相对丰度明显高于健康人,且通过多元回归模型计算公式计算, P<0.3时患AD属于低风险;当0.3
另外,虽然本发明优选的实施例是将微生物种群丰度与影响程度加权后计算受试者阿尔兹海默症患病风险,但同样可以通过其他公式来表征微生物种群丰度与患病风险之间的关系,具体如下所示。
i)定量分析,判断在某种因素下,患AD风险的概率。皮尔逊相关系数计算,衡量单个微生物群落的丰度和AD患者是否存在相关性分析,具体公式为:
其中,
X:微生物丰度比例
Y:患AD的概率
ii)决策树是建立在病原微生物和AD有密切关系的基础上判断的,因个体差异,在测取口腔的微生物组合的比例会有差异,因此通过已有的案例进行数据建模,当有新测取的数据加入时,模型即可给出大概的风险等级,具体公式为:
信息熵:
其中,
D表示数据总体,P
信息增益:
D表示数据总体,D
应该理解的是,上述表达的图形、说明,仅为本发明的几种较佳实施例而已,并非是对本发明的保护范围进行限制,对本领域技术人员而言,在不脱离本发明精神和范围的前提下,凡在本发明的精神和原则之内所作的任何修改、等同替换和改进等,都应落入要求保护的本发明权利要求范围内。
序列表
<110> 苏州熵道生物科技有限公司
<120> 一种检测试剂盒、检测工具及其在预测阿尔兹海默病中的用途
<160> 22
<170> SIPOSequenceListing 1.0
<210> 1
<211> 40
<212> DNA
<213> 人工序列(Artificial Sequence)
<400> 1
acactctttc cctacacgac gctcttccga tctatcacgt 40
<210> 2
<211> 31
<212> DNA
<213> 人工序列(Artificial Sequence)
<400> 2
gatcggaaga gcacacgtct gaactccagt c 31
<210> 3
<211> 8
<212> DNA
<213> 人工序列(Artificial Sequence)
<400> 3
gtactgac 8
<210> 4
<211> 8
<212> DNA
<213> 人工序列(Artificial Sequence)
<400> 4
caggacgt 8
<210> 5
<211> 8
<212> DNA
<213> 人工序列(Artificial Sequence)
<400> 5
taatctta 8
<210> 6
<211> 8
<212> DNA
<213> 人工序列(Artificial Sequence)
<400> 6
aggcgaag 8
<210> 7
<211> 8
<212> DNA
<213> 人工序列(Artificial Sequence)
<400> 7
ggctctga 8
<210> 8
<211> 8
<212> DNA
<213> 人工序列(Artificial Sequence)
<400> 8
cctatcct 8
<210> 9
<211> 8
<212> DNA
<213> 人工序列(Artificial Sequence)
<400> 9
atagaggc 8
<210> 10
<211> 8
<212> DNA
<213> 人工序列(Artificial Sequence)
<400> 10
tatagcct 8
<210> 11
<211> 8
<212> DNA
<213> 人工序列(Artificial Sequence)
<400> 11
agcgatag 8
<210> 12
<211> 8
<212> DNA
<213> 人工序列(Artificial Sequence)
<400> 12
tctcgcgc 8
<210> 13
<211> 8
<212> DNA
<213> 人工序列(Artificial Sequence)
<400> 13
tccgcgaa 8
<210> 14
<211> 8
<212> DNA
<213> 人工序列(Artificial Sequence)
<400> 14
taatgcgc 8
<210> 15
<211> 8
<212> DNA
<213> 人工序列(Artificial Sequence)
<400> 15
cggctatg 8
<210> 16
<211> 8
<212> DNA
<213> 人工序列(Artificial Sequence)
<400> 16
gaattcgt 8
<210> 17
<211> 8
<212> DNA
<213> 人工序列(Artificial Sequence)
<400> 17
ctgaagct 8
<210> 18
<211> 8
<212> DNA
<213> 人工序列(Artificial Sequence)
<400> 18
attactcg 8
<210> 19
<211> 8
<212> DNA
<213> 人工序列(Artificial Sequence)
<400> 19
tccggaga 8
<210> 20
<211> 8
<212> DNA
<213> 人工序列(Artificial Sequence)
<400> 20
cgctcatt 8
<210> 21
<211> 8
<212> DNA
<213> 人工序列(Artificial Sequence)
<400> 21
gagattcc 8
<210> 22
<211> 8
<212> DNA
<213> 人工序列(Artificial Sequence)
<400> 22
attcagaa 8
- 一种阿尔兹海默症检测试剂及其在阿尔兹海默症检测中的应用
- 一种阿尔兹海默症检测试剂及其在阿尔兹海默症检测中的应用
